
қысқа мерзімді сабақ жоспарларын

Радиоактивность. Природа радиоактивных излучений.Опыт Резерфорда, строение атома.
Сатылымнан түскен қаражат авторға автоматты түрде аударылады. Толығырақ
беріледі

Дипломдар мен сертификаттарды алып үлгеріңіз!




1 слайд
Радиоактивность.
Природа радиоактивных излучений.
Опыт Резерфорда, строение атома.
•
"Учитесь так, словно вы постоянно
ощущаете нехватку своих знаний, и
так, словно вы постоянно боитесь
растерять свои знания."
Конфуций

2 слайд
В презентации использованы материалы Единой коллекции
цифровых образовательных ресурсов Мир сложен –
Он полон событий, сомнений
И тайн бесконечных,
И смелых догадок.
Как чудо природы
Является гений
И в хаосе этом
Находит порядок.

3 слайд
https://www.youtube.com/watch?v=czRNJihtf7w&t=326s
ВИЛЬГЕЛЬМ КОНРАД
РЕНТГЕН
В конце XIX века в научном
мире происходили
удивительные и необычайно
интересные события, которые
положили начало новому этапу в
формировании физической
картины мира.
Всемирную славу ученому принесло знаменитое
открытие «нового типа лучей», которые теперь называют
рентгеновскими . Это произошло в ноябре 1895 г . в
Вюрцбургском университете, ректором которого был
Рентген .

4 слайд
•
Антуан Анри Беккерель
•
Антуан Анри Беккерель был третьим в роду
Беккерелей заведующий кафедрой
прикладной физики в учреждении, которое
сейчас носит название Национального музея
естественной истории в Париже. Именно
здесь произошло открытие, перевернувшее
мир ХХ в .
Беккерель хотел установить, испускают ли
фосфоресцирующие вещества (калийуранилсульфат)
рентгеновские лучи. Но наблюдал нечто другое. И, подобно
Рентгену, в одиночку более полутора лет изучал открытое
явление. В частности, установил, что источником нового вида
лучей является элемент уран - последний в периодической
системе.

5 слайд
•
Изучив большое количество
разнообразных минералов, Мария Кюри
обнаружила, что похожие лучи испускает
не только уран, но и другие элементы.
•
В 1898 г. они открыли новые
радиоактивные элементы – полоний ,
радий , торий .
•
Именно Мария Кюри предложила
название «радиоактивность» (англ.слово
radiatin – излучение, лучеиспускание) для
нового вида излучения.

6 слайд
К 20-м годам XX века физики уже не сомневались в том, что атомные ядра,
открытые Э. Резерфордом в 1911 г., также как и сами атомы, имеют сложную
структуру. В этом их убеждали многочисленные экспериментальные факты,
накопленные к этому времени: открытие радиоактивности, экспериментальное
доказательство ядерной модели атома, измерение отношения e / m для
электрона, α-частицы и для так называемой H-частицы – ядра атома водорода,
открытие искусственной радиоактивности и ядерных реакций, измерение зарядов
атомных ядер и т. д.
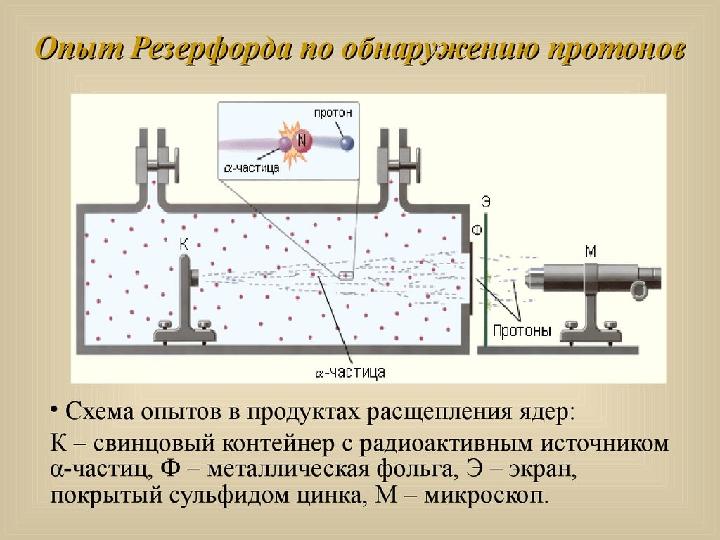
В настоящее время твердо установлено, что атомные ядра различных элементов
состоят из частиц двух видов – протонов и нейтронов .
Первая из этих частиц представляет собой атом водорода, из которого удален
единственный электрон. Эта частица наблюдалась уже в 1907 г. в
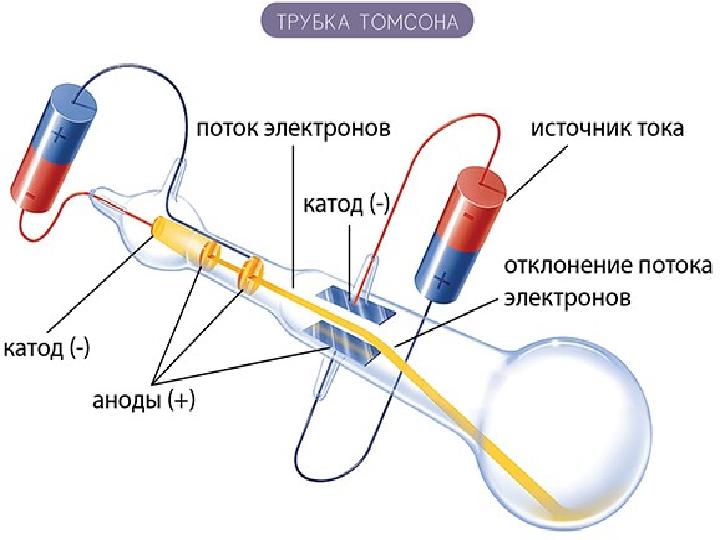
опытах Дж. Томсона , которому удалось измерить у нее отношение e / m . В
1919 году Э. Резерфорд обнаружил ядра атома водорода в продуктах расщепления
ядер атомов многих элементов. Резерфорд назвал эту частицу протоном. Он
высказал предположение, что протоны входят в состав всех атомных ядер. Схема
опытов Резерфорда представлена на рис. 6.5.1.

7 слайд
Открытие электрона. Модель атома Томсона Открытие электрона. Модель атома Томсона
(1903 г.)(1903 г.)
•
Электроны, по
мнению Томсона,
вкраплены в
положительно
заряженную сферу,
«как изюм в кекс».
ОШИБКА!
Дж. Томсон в 1897 г.
открыл электронДолгое время атом считался наименьшей не делимой частицей
вещества. Такое представление об атоме было разрушено в 1897
году. Этот год считается датой открытия элементарной частицы –
электрона .

8 слайд
9 слайд

10 слайд
АтомАтом
– это мельчайшая – это мельчайшая
химическихимически
неделимая частица неделимая частица
вещества.вещества.
Атомы всех химических
элементов сведены в табл.
Д.И. Менделеева

11 слайд
Знание о строении атома позволяет Знание о строении атома позволяет
объяснить многие явленияобъяснить многие явления
Например:Например:
•
Как происходит электризация тел?Как происходит электризация тел?
•
Почему металлы проводят Почему металлы проводят
электрический ток , а неметаллы - нет?электрический ток , а неметаллы - нет?
•
Как создается атомное оружие?Как создается атомное оружие?
12 слайд
АТОМАТОМ
ядро электроны ядро электроны
Что вам известно о строении атома?Что вам известно о строении атома?

13 слайд
Опыты РезерфордаОпыты Резерфорда
(1906 (1906
– 1911гг.)– 1911гг.)
Цель опытов: подтвердить
или опровергнуть модель,
предложенную Томсоном. Эрнст Резерфорд (англ.)
предложил ПЛАНЕТАРНУЮ
модель атома
14 слайд

15 слайд
Планетарная модель атомаПланетарная модель атома
В центре атома, в ядре ,
сосредоточен весь
положительный заряд положительный заряд и
практически вся масса
атома.
Вокруг ядра по орбитам Вокруг ядра по орбитам
вращаются вращаются
отрицательно отрицательно
заряженные заряженные
электроныэлектроны
(подобно планетам в (подобно планетам в
Солнечной системе).Солнечной системе).

16 слайд
Электрон – элементарная частицаЭлектрон – элементарная частица
•
Заряд электрона неделимый
– элементарный
( доказано опытами
А.Ф.Иоффе и Р. Милликена)
•
Обозначается ē
•
Значение заряда
электрона:Кл e
19
10 6, 1
Черта над е указывает на то,
что заряд электрона
отрицательный 1. Заряд электрона
принимают за 1
относительную
единицу заряда!
2. Заряд любого тела
обозначается буквой
q и измеряется в
Кулонах (Кл).
Его можно
вычислить по формуле: Запомните:
e n q
17 слайд
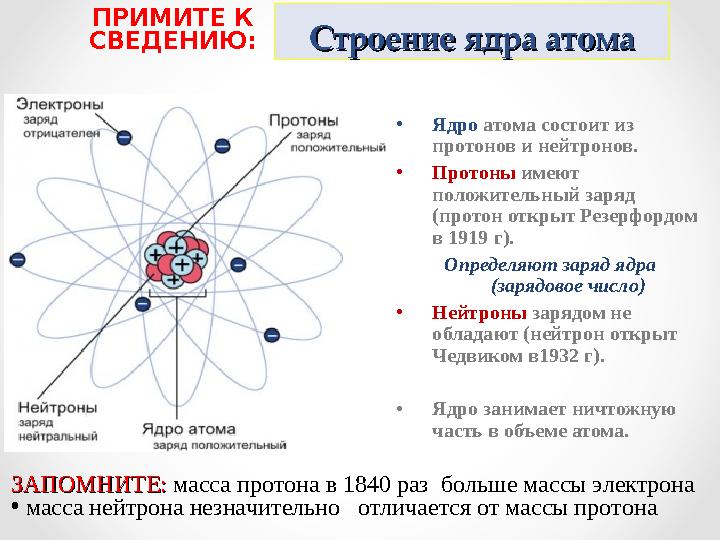
Строение ядра атомаСтроение ядра атома
•
Ядро атома состоит из
протонов и нейтронов.
•
Протоны имеют
положительный заряд
(протон открыт Резерфордом
в 1919 г).
Определяют заряд ядра
(зарядовое число)
•
Нейтроны зарядом не
обладают (нейтрон открыт
Чедвиком в1932 г).
•
Ядро занимает ничтожную
часть в объеме атома.ПРИМИТЕ К
СВЕДЕНИЮ:
ЗАПОМНИТЕ:ЗАПОМНИТЕ: масса протона в 1840 раз больше массы электрона
•
масса нейтрона незначительно отличается от массы протона

18 слайд
Периодическая система элементов Периодическая система элементов
Д.И. МенделееваД.И. Менделеева
•
Порядковый номер
элемента совпадает с
зарядом ядра ( Z) атома, т.е.
определяет число протонов .
•
Порядковый номер
определяет и число
электронов (n) в атоме.
n = Z
•
сумма протонов ( Z) и
нейтронов (N) в ядре
составляет массовое число
(А)
А = Z+N
массовое число приблизительно равно относительной массе
атома, округленной до целого числа

19 слайд
Обычно атом электрически нейтрален. Обычно атом электрически нейтрален.
Что это означает?Что это означает?
Это значит, что
общее число
электронов в
атоме равно
общему числу
протонов.
Попробуйте определить, атом
какого химического элемента
представлен на картинке?

20 слайд
Положительный и отрицательный Положительный и отрицательный
ионыионы
ЗАПОМНИТЕ:ЗАПОМНИТЕ:
ЕСЛИ АТОМ ЗАРЯЖЕН, ЕГО
НАЗЫВАЮТ ИОНОМ.

21 слайд
Положительный ион.Положительный ион.
Атом, потерявший на
внешней орбите
электрон, называется
положительным ионом .

22 слайд
Отрицательный ионОтрицательный ион
Атом, имеющий на
внешней орбите
лишний электрон,
называется
отрицательным ионом.

23 слайд
Вопросы для самоконтроля:Вопросы для самоконтроля:
•
Является ли нейтральным атом лития, вокруг
ядра которого движутся два электрона?
•
Что является главной характеристикой
данного элемента?
•
В ядре атома азота 14 частиц. Из них 7
протонов. Сколько электронов имеет атом в
нейтральном состоянии? Сколько
нейтронов?
•
Атом гелия потерял один электрон. Будет ли
он заряжен?
24 слайд
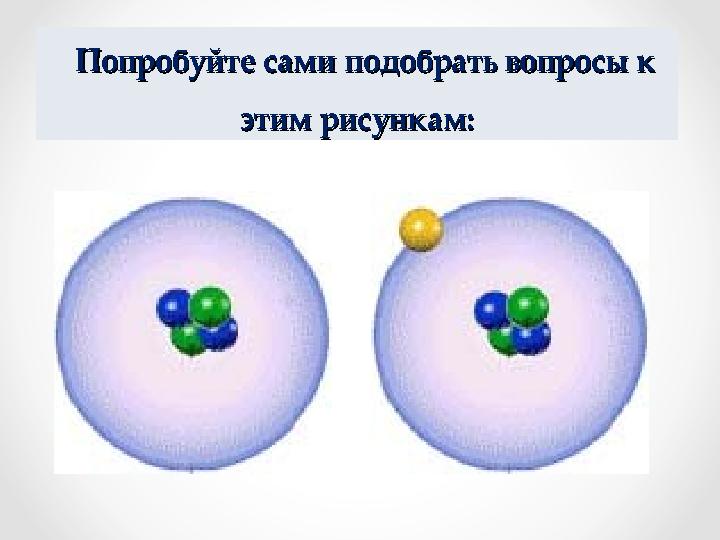
Попробуйте сами подобрать вопросы к Попробуйте сами подобрать вопросы к
этим рисункам:этим рисункам:

25 слайд
Задание для самоподготовки:
1. Прочитайте § 29, 30 в учебнике.
2. Подумайте и объясните, используя
знания о строении атома, когда тело
получает положительный заряд, а
когда – отрицательный.
3. Подготовьте сообщение о научной
деятельности А.Ф. Иоффе
Сіз үшін 400 000 ұстаздардың еңбегі мен тәжірибесін біріктіріп, ең үлкен материалдар базасын жасадық. Төменде пәніңізді белгілеп, керек материалды алып сабағыңызға қолдана аласыз
 Дайын ҚМЖ. Барлық пәндерден 2022-2023 оқу жылына, жаңа бұйрыққа сай жасалған
Дайын ҚМЖ. Барлық пәндерден 2022-2023 оқу жылына, жаңа бұйрыққа сай жасалған