

«СЕМЕЙ ҚАЛАСЫНЫҢ ШӘКӘРІМ
АТЫНДАҒЫ УНИВЕРСИТЕТІ»
КеАҚ

2023

СӨЖ №1. Бір- және екі
компонетті жүйелердің күй диаграммасын
тұрғызу.
Орындаған: Қабылқақов
Әміржан.
Жетекші: Баяхметова
Б.Б.
Жоспар:
-
Негізгі анықтамалар. Гиббстің
фазалар ережесі.
-
Фаза аралық тепе-тендік, күй
диаграммалары.
-
Бір және екі компонентті
гетерогенді жүйелердің күй диаграммалары.
1.Термодинамикалық
жүйелер гомогенді және
гетерогенді болып
бөлінеді. Гомогенді жүйе бір ғана фазадан,
ал гетерогенді жүйе- екі не одан да көп
фазадан тұрады.
Фаза- құрамы, физикалық және
химиялық қасиеттері бірдей, басқа бөліктерден бөлу беті арқылы
бөлінетін жүйенің бөлігін айтамыз.
Жүйе фазаның санына байланысты
бір фазалы, екі фазалы және одан да көп фазалы деп
бөледі.
Компонент- жүйеден тыс жеке өмір сүре
алатын оның негізгі құрамдас бөлігі болып келетін жеке химиялық
зат.
Термодинамикалық жүйенің
барлық фазаларын түзуге және фазаның құрамын математикалық
өрнектеуге қажетті жеке химиялық заттың ең аз
саны компонент
саны деп
атайды.
Жүйе күйі еркіндік дәреже
санымен сипатталады.
Жүйедегі тепе-теңдікті,
фазалар санын бұзбай өзгертуге болатын термодинамикалық параметрлер
санын еркіндік дәреже
саны деп атайды.
Оны С
әрпімен белгілейді. Еркіндік
дәреже саны бойынша жүйе инвариантты (с=0),
моновариантты (с=1),
бивариантты (с=3).
Жүйенің фазалық күйі фазалар
санымен (ф), компонент санымен (к), еркіндік дәреже санымен (с)
және жүйеге әсер етуші сыртқы факторлар санымен (n)
сипатталады. Гиббстің фазалар ережесі:
С=
к-ф+n
Диаграмма- нақты процестер мен
құбылыстардың өзара байланыстарын сипаттайтын сандық көрсеткіштер
сызба түрінде кескінделетін нұсқалар
Гиббстік фазалар ережесі –
термодинамикалық тепе-теңдік жағдайда тұрған гетерогендік
жүйеде, фазалар саны компоненттер санынан екі екіден
артық болмауы керек делінген заң. Мұны американ физигі Джозайя
Гиббс (1839 – 1903) тұжырымдаған.
Кирхгоф ережелері –
күрделі электрлік және магниттік тізбектерді есептеуге арналған
әдістер.
2.
Күйлер
диаграммасы (грекше «диаграмма – кескін,
сызба»), тепетеңдік диаграммасы – термодинамикалық
жүйенің тепе-теңдік күйлерін анықтайтын параметрлердің: температураның
Т, қысымның р, жүйе құрамының [компонеттердің х1 шоғырлануын
(концентрацияларын)], мольдік көлемін
υ, электрлік және магниттік өрістердің т.б. әр
түрлі мәндері кезінде термодинамикалық
жүйенің тепе-теңдік күйлерінің геометриялық
кескіні. Күйлер диаграммасы жүйенің фазалық құрамы туралы Т, р,
х1 және басқа параметрлерге тәуелділігі туралы ақпараттар
береді.
3. Бір компонентті гетерогенді жүйелер.
Су күйінің диаграммасы. Сыртқы
фактордан температура мен қысым әсер ететін
жүйелер үшін
теңдеу келесі түрде болады: С = К – Ф + 2 (4.8). Р және Т
тәуелділіктерінің графикалық бейнеленуі (Р құрамнан және Т
құрамнан) диаграмма күйі деп
аталады. Диаграмма күйін талдау фазалар санын, олардың болу
шегін, олардың компоненттерінің өзара әрекеттесу сипатын, жаңа түзілген
қосылыстардың бар екенін, олардың құрамын анықтауғамүм кіндік
береді.
|
7
|
A-KI
Б-CdI2
|
0
|
658
|
53
|
504
|
|
|
|
10
|
643
|
55
|
515
|
|
|
|
30
|
696
|
60
|
575
|
|
|
|
45
|
520
|
65
|
656
|
|
|
|
47
|
470
|
80
|
833
|
|
|
|
49
|
489
|
100
|
951
|
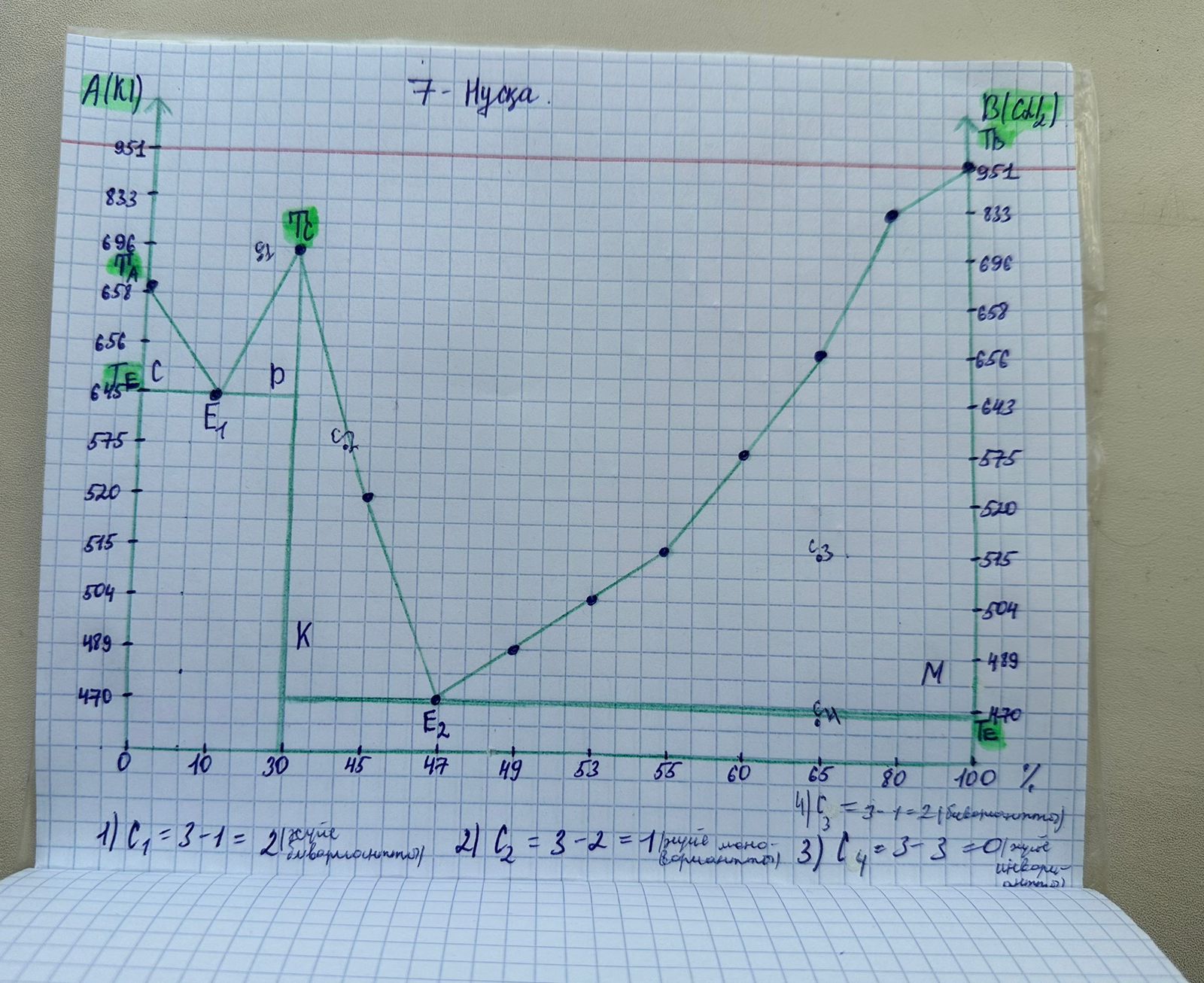
Қорытынды:
Біз конгруэнтті балқитын
химиялық қосылыстар жүйелерінің күй диаграммасын тұрғыздық. Бізде
екі компонетті жүйе үшін температура қатысында болғандытан,
Гиббстің фазалар ережесі келесі теңдеумен
анықтадық: с= 2-ф+1=
3-ф.
Біздің бірінші нүкте солидус
сызығының астында орналасты, яғни оған эвтетикалық кристалдық
қоспасы бар қатты зат аламыз.(суыту процессі). Солидус сөзінің өзі
аударғанда «қату» деген мағына береді. Ал екінші нүкте ол ликвидус
сызығы мен солидус сызығы арасында қатты және сұйық фаза
орналасқан.Ал төттінші нүктеге үш фаза тән.Себебі E нүктесіне
балқыма және А мен В кристалда-рының екі қатты фазалар жүйе құрамы
сәйкес келеді.
С
=2-3+1=0 жүйе
инвариантты.
Қолданылған
дереккөздер:
Физикалық химияның негізгі
тараулары. Баяхметова Б.Б.Семей2023.






 Дайын ҚМЖ. Барлық пәндерден 2022-2023 оқу жылына, жаңа бұйрыққа сай жасалған
Дайын ҚМЖ. Барлық пәндерден 2022-2023 оқу жылына, жаңа бұйрыққа сай жасалған


