Қышқыл және негізгі катализ. Каталитикалық белсенділік және селективтілік


#1 слайд
Қышқыл және негізгі
катализ. Каталитикалық
белсенділік және
селективтілік
1 слайд
Қышқыл және негізгі катализ. Каталитикалық белсенділік және селективтілік

#2 слайд
Катализ (грекше katalysіs – бұзылу) – катализатор әсерінен жылдамдығын
өзгертетін процесс түрі.
Катализатор деп, реакция жылдамдығын өзгертетін және реакция нәтижесінде
өзгеріссіз қалатын заттарды атайды.
● Егер катализатор реакция
жылдамдығын арттыратын болса, оны
оң, ал баяулататын болса теріс
катализатор деп атайды.
●Егер катализатор реакция барысында
түзілсе, оны автокатализ деп атайды.
●Кейбір заттар катализатордың әсер
етуіне кедергі жасайды, ондай заттарды
ингибиторлар немесе катализатор улары
дейді.
●Ал кейбір заттар өздері катализатор
болмаса да, катализатордың активтілігін
арттырады, ондай заттарды
активаторлар дейді
2 слайд
Катализ (грекше katalysіs – бұзылу) – катализатор әсерінен жылдамдығын өзгертетін процесс түрі. Катализатор деп, реакция жылдамдығын өзгертетін және реакция нәтижесінде өзгеріссіз қалатын заттарды атайды. ● Егер катализатор реакция жылдамдығын арттыратын болса, оны оң, ал баяулататын болса теріс катализатор деп атайды. ●Егер катализатор реакция барысында түзілсе, оны автокатализ деп атайды. ●Кейбір заттар катализатордың әсер етуіне кедергі жасайды, ондай заттарды ингибиторлар немесе катализатор улары дейді. ●Ал кейбір заттар өздері катализатор болмаса да, катализатордың активтілігін арттырады, ондай заттарды активаторлар дейді

#3 слайд
⚬Қышқылдық –
негіздік
⚬(Катализатор –
қышқыл немесе
негіз)
⚬Металл кешені
(катализатор – иондар
немесе металл, металл
комплексті қосылыстар)
⚬Ферментативті
(биокатализаторлар
- ферменттер)
Гомогенді катализ түрлері
●Гомогенді катализ әрекеттесуші
заттар және катализатор бірдей
фазада болады.
2SO2+O2[NO]→2SO3
●Гетерогенді катализ әрекеттесуші
заттар және катализатор әртүрлі
фазада болады.
2SO2+O2[V2O5]→2SO3
Катализ 2-ге бөлінеді:
3 слайд
⚬Қышқылдық – негіздік ⚬(Катализатор – қышқыл немесе негіз) ⚬Металл кешені (катализатор – иондар немесе металл, металл комплексті қосылыстар) ⚬Ферментативті (биокатализаторлар - ферменттер) Гомогенді катализ түрлері ●Гомогенді катализ әрекеттесуші заттар және катализатор бірдей фазада болады. 2SO2+O2[NO]→2SO3 ●Гетерогенді катализ әрекеттесуші заттар және катализатор әртүрлі фазада болады. 2SO2+O2[V2O5]→2SO3 Катализ 2-ге бөлінеді:

#4 слайд
Қышқылдық-негіздік
катализ
С.Аррениус (1884) бойынша қышқыл суда
диссоциацияланғанда сутегі иондары Н3О+
түзетін қосылыс, ал негіз суда
диссоциацияланған кезде гидроксид – ОН-
иондары түзетін қосылыс.
Кемшілігі - тек сулы ерітінділер үшін
қолданылады
4 слайд
Қышқылдық-негіздік катализ С.Аррениус (1884) бойынша қышқыл суда диссоциацияланғанда сутегі иондары Н3О+ түзетін қосылыс, ал негіз суда диссоциацияланған кезде гидроксид – ОН- иондары түзетін қосылыс. Кемшілігі - тек сулы ерітінділер үшін қолданылады

#5 слайд
Қышқылдық-негіздік катализ
Г.Льюис бойынша қышқыл –
жалғыз электрон жұбының
акцепторы, ал негіз – электрон
жұбының доноры болып
табылатын зат.
Льюис қышқылдары - FeCl3,
AlCl3, AlBr3, BF3 сияқты
қосылыстар
FeCl3 + :Cl- =
FeCl-4
Негіздер: NH3, N2H4, NO3-,
C6H5N
NH3 + H+ = NH+4
Дж.Брестед пен Т.Лоури
(1923) бойынша қышқыл –
протон доноры болып
табылатын зат, ал негіз –
протонды қабылдаушы зат.
Ерітіндіде қышқыл-негіз тепе-
теңдігі бар:
HA + H2O ↔ H3O+ + A-
Қышқылдық негіз
Қышқылдық негіз
5 слайд
Қышқылдық-негіздік катализ Г.Льюис бойынша қышқыл – жалғыз электрон жұбының акцепторы, ал негіз – электрон жұбының доноры болып табылатын зат. Льюис қышқылдары - FeCl3, AlCl3, AlBr3, BF3 сияқты қосылыстар FeCl3 + :Cl- = FeCl-4 Негіздер: NH3, N2H4, NO3-, C6H5N NH3 + H+ = NH+4 Дж.Брестед пен Т.Лоури (1923) бойынша қышқыл – протон доноры болып табылатын зат, ал негіз – протонды қабылдаушы зат. Ерітіндіде қышқыл-негіз тепе- теңдігі бар: HA + H2O ↔ H3O+ + A- Қышқылдық негіз Қышқылдық негіз
#6 слайд
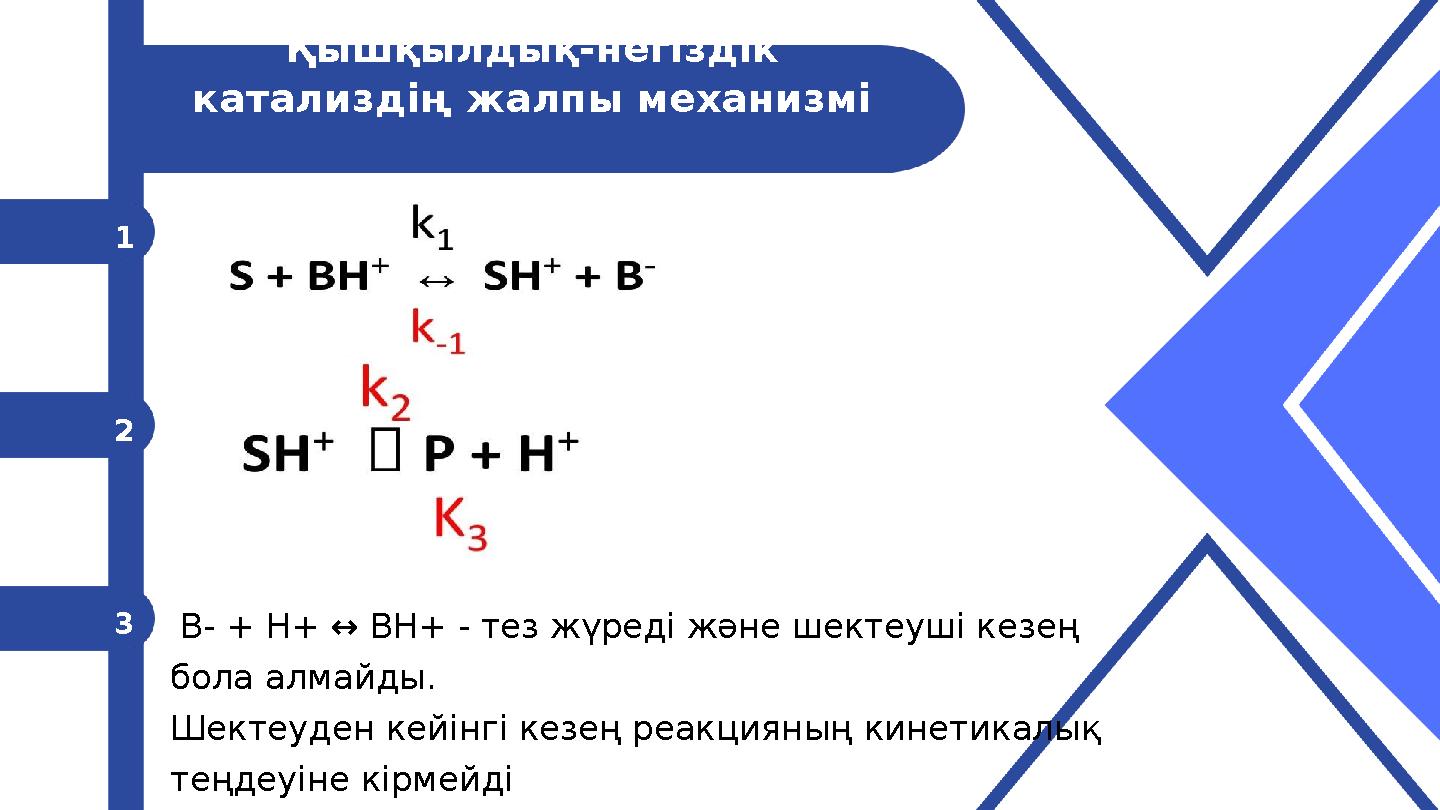
B- + H+ ↔ BH+ - тез жүреді және шектеуші кезең
бола алмайды.
Шектеуден кейінгі кезең реакцияның кинетикалық
теңдеуіне кірмейді
1
2
3
Қышқылдық-негіздік
катализдің жалпы механизмі
6 слайд
B- + H+ ↔ BH+ - тез жүреді және шектеуші кезең бола алмайды. Шектеуден кейінгі кезең реакцияның кинетикалық теңдеуіне кірмейді 1 2 3 Қышқылдық-негіздік катализдің жалпы механизмі

#7 слайд
Жалпы қышқыл-негіз
катализінің қысқаша
мазмұны
⚬Жалпы негізгі катализ . Бұл жағдайда
катализатор Бронстед негіздері болып
табылады, яғни. В:
⚬ S + В↔ВH+ + S-
⚬Шектеу кезеңі SH+ немесе S- түзілудің
бірінші кезеңі.
Жалпы қышқылдық катализ. Бұл
жағдайда катализатор Бронстед
қышқылдары болып табылады, (немесе
BH+):
S + ВН+ ↔ SH+ + В-
7 слайд
Жалпы қышқыл-негіз катализінің қысқаша мазмұны ⚬Жалпы негізгі катализ . Бұл жағдайда катализатор Бронстед негіздері болып табылады, яғни. В: ⚬ S + В↔ВH+ + S- ⚬Шектеу кезеңі SH+ немесе S- түзілудің бірінші кезеңі. Жалпы қышқылдық катализ. Бұл жағдайда катализатор Бронстед қышқылдары болып табылады, (немесе BH+): S + ВН+ ↔ SH+ + В-

#8 слайд
Белсенділік
1
2
Селективтілік
3
Тұрақтылық
Кез-келген катализатор, ең алдымен, үш
негізгі параметрмен сипатталады:
8 слайд
Белсенділік 1 2 Селективтілік 3 Тұрақтылық Кез-келген катализатор, ең алдымен, үш негізгі параметрмен сипатталады:

#9 слайд
Катализатордың активтілігі оның өнімділігі болып
табылады, ол бастапқы реагенттің қанша бөлігі уақыт
бірлігінде катализаторда мақсатты түрленуге
болатындығын сипаттайды.
Каталитикалық реакцияның жылдамдығы әдеттегі
жағдайда каталитикалық емес реакцияға қарағанда
айтарлықтай жоғары, сондықтан реакция келесі
формуламен есептелген нақты жылдамдықпен
сипатталады:
Катализатор
белсенділігі
9 слайд
Катализатордың активтілігі оның өнімділігі болып табылады, ол бастапқы реагенттің қанша бөлігі уақыт бірлігінде катализаторда мақсатты түрленуге болатындығын сипаттайды. Каталитикалық реакцияның жылдамдығы әдеттегі жағдайда каталитикалық емес реакцияға қарағанда айтарлықтай жоғары, сондықтан реакция келесі формуламен есептелген нақты жылдамдықпен сипатталады: Катализатор белсенділігі

#10 слайд
Формальды түрде катализатордың белсенділігін
берілген шарттардағы каталитикалық және
каталитикалық емес реакциялар жылдамдығының
қатынасы арқылы бағалауға болады.
Катализатор тепе-теңдікті ауыстырмай, оған
жеткенше уақытты қысқартады, яғни каталитикалық
белсенділікті ток энергиясының өзгеруі арқылы
бағалауға болады.
Реакциялар бірдей жағдайларда болған жағдайда
активация:
10 слайд
Формальды түрде катализатордың белсенділігін берілген шарттардағы каталитикалық және каталитикалық емес реакциялар жылдамдығының қатынасы арқылы бағалауға болады. Катализатор тепе-теңдікті ауыстырмай, оған жеткенше уақытты қысқартады, яғни каталитикалық белсенділікті ток энергиясының өзгеруі арқылы бағалауға болады. Реакциялар бірдей жағдайларда болған жағдайда активация:

#11 слайд
Катализатордың активтілігі каталитикалық процеске
қатысатын Naц белсенді орталықтарының санымен
және табиғатымен анықталады. Демек, идеалды
жағдайларда катализдегі барлық белсенді
орталықтардың қатысуымен белсенділік t уақыт
бірлігінде 1 белсенді орталықта әрекеттесетін
молекулалардың ең көп саны N моль ретінде
анықталады:
Бұл мән абсолютті белсенділік немесе деп аталадыTOF
(turnover
frequency) – «революция жиілігі».
11 слайд
Катализатордың активтілігі каталитикалық процеске қатысатын Naц белсенді орталықтарының санымен және табиғатымен анықталады. Демек, идеалды жағдайларда катализдегі барлық белсенді орталықтардың қатысуымен белсенділік t уақыт бірлігінде 1 белсенді орталықта әрекеттесетін молекулалардың ең көп саны N моль ретінде анықталады: Бұл мән абсолютті белсенділік немесе деп аталадыTOF (turnover frequency) – «революция жиілігі».

#12 слайд
Селективтілік
Full access to two of
our main services
Routine checks for six
months
Service adjustment in
the sixth month
Pick one of our services
Routine checks for six
months
Service adjustment in the
sixth month
Селективтілік немесе талғамдылылық - бұл катализатордың берілген жағдайда
реакцияның термодинамикалық мүмкін болатын көптеген бағыттардың ішінен бір
бағытқа қарай талғамдылылықпен жүзеге асыру қабілеті.
Селективтілік (S) - бастапқы заттардың мақсатты өнімге айналу үлесін сипаттайды.
Мысалы:
мұндағы, А, В - бастапқы реагенттер; R – мақсатты өнім; D – қосымша өнім.
Сонда:
m R және m D – мақсатты және қосымша өнімдердің массалары.
12 слайд
Селективтілік Full access to two of our main services Routine checks for six months Service adjustment in the sixth month Pick one of our services Routine checks for six months Service adjustment in the sixth month Селективтілік немесе талғамдылылық - бұл катализатордың берілген жағдайда реакцияның термодинамикалық мүмкін болатын көптеген бағыттардың ішінен бір бағытқа қарай талғамдылылықпен жүзеге асыру қабілеті. Селективтілік (S) - бастапқы заттардың мақсатты өнімге айналу үлесін сипаттайды. Мысалы: мұндағы, А, В - бастапқы реагенттер; R – мақсатты өнім; D – қосымша өнім. Сонда: m R және m D – мақсатты және қосымша өнімдердің массалары.

#13 слайд
Тұрақтылық-бұл катализатордың
маңызды сипаттамасы, оның белсенділігі
мен селективтілігінің бастапқы мөлшерін
уақыт өте келе сақтау қабілетімен,
тұрақты белсенділікпен және жалпы
жұмыс ұзақтығымен жеткілікті пайдалану
кезеңіне ие болу.
Тұрақтылық
13 слайд
Тұрақтылық-бұл катализатордың маңызды сипаттамасы, оның белсенділігі мен селективтілігінің бастапқы мөлшерін уақыт өте келе сақтау қабілетімен, тұрақты белсенділікпен және жалпы жұмыс ұзақтығымен жеткілікті пайдалану кезеңіне ие болу. Тұрақтылық

#14 слайд
Назарларыңызға рахмет!
14 слайд
Назарларыңызға рахмет!

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
