

Резерфорд тәжірбиелері, атомның планетарлық моделі
Дипломдар мен сертификаттарды алып үлгеріңіз!


1 слайд
Атомның құрылысы.
Резерфорд тәжірибелері.
1 слайд
Атомның құрылысы. Резерфорд тәжірибелері.

2 слайд
ХІХ ғасырдың аяғына дейін атом
бөлінбейді деген ұғым қалыптасты.
Алайда, ХІХ ғасырдың аяғы ХХ
ғасырдың басында физика
саласында ашылған
радиоактивтілік құбылыс, рентген
сәулелері тәрізді жаңалықтар
атомның өте күрделі бөлшек екенін
дәлелдеді.
2 слайд
ХІХ ғасырдың аяғына дейін атом бөлінбейді деген ұғым қалыптасты. Алайда, ХІХ ғасырдың аяғы ХХ ғасырдың басында физика саласында ашылған радиоактивтілік құбылыс, рентген сәулелері тәрізді жаңалықтар атомның өте күрделі бөлшек екенін дәлелдеді.

3 слайд
Радиоактивті сәулелердің табиғаты 3
түрлі: альфа, бетта және гамма
сәулелері. Альфа – сәулелер гелий
иондарының ағымы, бетта – сәулелер
электрондар ағымы, гамма – сәулелер
толқын ұзындығы 10 -11
– 10 -13
м
шамасындағы электромагниттік
сәулелер кванттарының ағыны.
3 слайд
Радиоактивті сәулелердің табиғаты 3 түрлі: альфа, бетта және гамма сәулелері. Альфа – сәулелер гелий иондарының ағымы, бетта – сәулелер электрондар ағымы, гамма – сәулелер толқын ұзындығы 10 -11 – 10 -13 м шамасындағы электромагниттік сәулелер кванттарының ағыны.
4 слайд
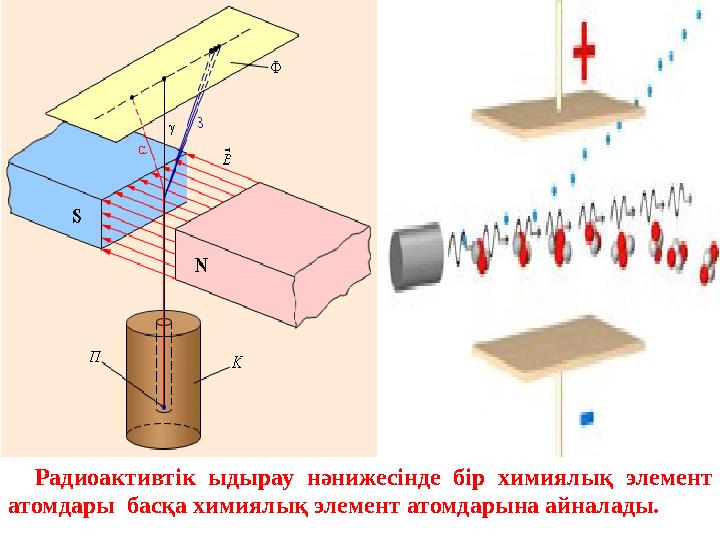
Радиоактивтік ыдырау нәнижесінде бір химиялық элемент
атомдары басқа химиялық элемент атомдарына айналады.
4 слайд
Радиоактивтік ыдырау нәнижесінде бір химиялық элемент атомдары басқа химиялық элемент атомдарына айналады.

5 слайд
5 слайд

6 слайд
Атомның ішінде оң зарядты
және массаның таралуының
зерттеу үшін 1906 жылы
Э.Резерфорд атомды альфа –
бөлшекпен атқылауды ұсынды.
1911 жылы ағылшын физигі
Резерфорд атомның ядролық
моделін ұсынды. Резерфорд
өзінің шәкірттері Г.Гейгер және
Э. Марсденмен бірге альфа-
бөлшектер шоғын өте жұқа
алтын фольгадан өткізіп,
бірнеше тәжірибелер жасады.
Осы тәжірибелерді зерделеу
нәтижесінде атомның ядролық,
басқаша айтсақ, планетарлық
моделі өмірге келді.
6 слайд
Атомның ішінде оң зарядты және массаның таралуының зерттеу үшін 1906 жылы Э.Резерфорд атомды альфа – бөлшекпен атқылауды ұсынды. 1911 жылы ағылшын физигі Резерфорд атомның ядролық моделін ұсынды. Резерфорд өзінің шәкірттері Г.Гейгер және Э. Марсденмен бірге альфа- бөлшектер шоғын өте жұқа алтын фольгадан өткізіп, бірнеше тәжірибелер жасады. Осы тәжірибелерді зерделеу нәтижесінде атомның ядролық, басқаша айтсақ, планетарлық моделі өмірге келді.
7 слайд
7 слайд

8 слайд
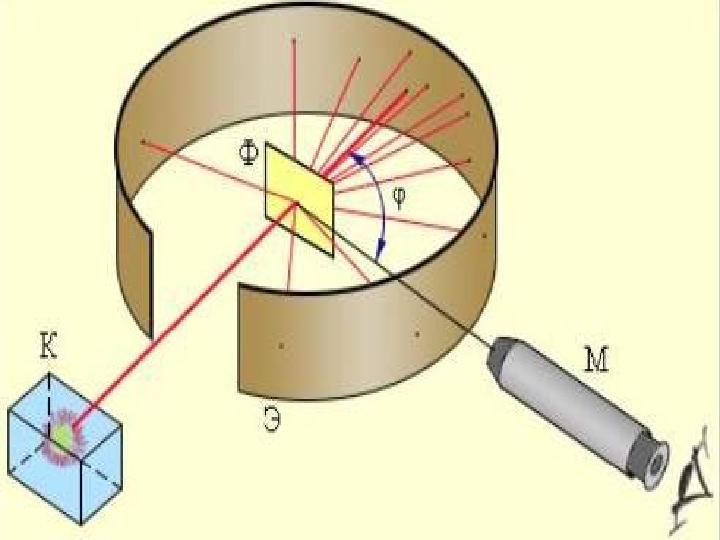
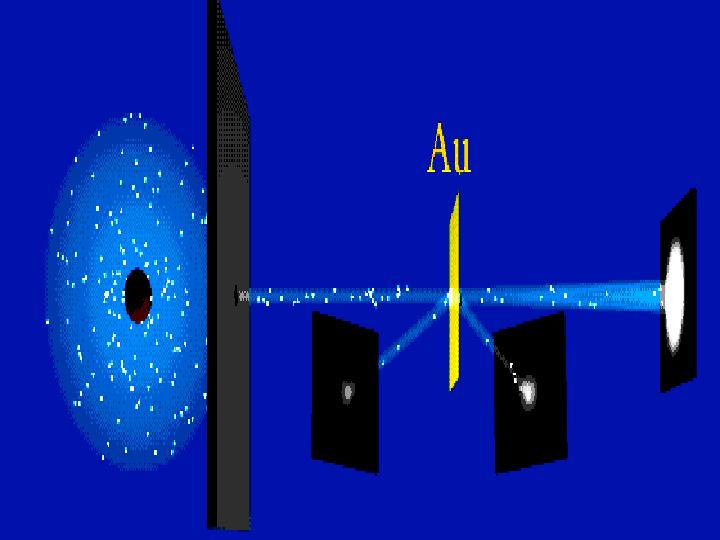
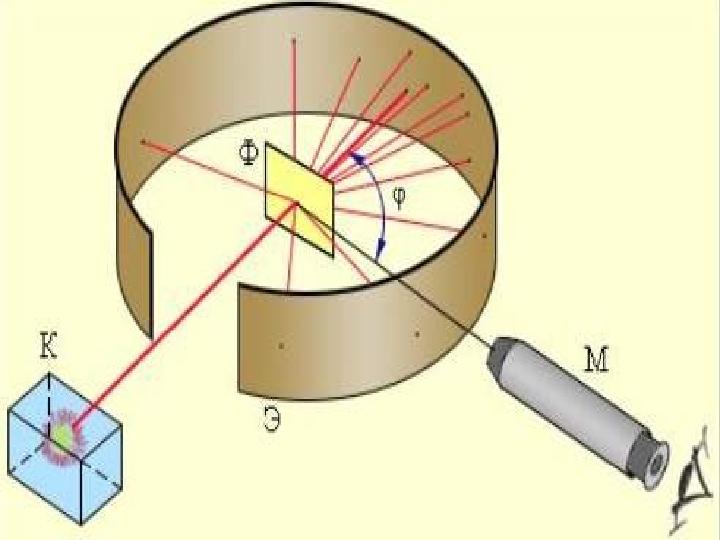
Тәжірибе барысында өте жұқа ( l=6*10-7 м) алтын
фольганы энергиясы 7,68 МэВ жылдам альфа бөлшектермен
атқылаған. Қорғасын контейнердің түбінде орналасқан 21484 Ро
радиоактивті элементтен шыққан альфа-бөлшектердің жіңішке
шоғы алтын фольгадан өткенде шашырайды, яғни алғашқы
бағытынан ауытқиды. Ол кезде альфа-бөлшектердің оң заряды
(2е) гелий иондары екені белгілі болатын. Фольгадан шашыраған
альфа-бөлшектердің қаншасы қандай бұрышқа ауытқығанын
есептей отырып, осы ауытқуларды тудырған нысана-
атомдардың құрылымы анықталады. Фольганың қалыңдығы өте
аз болғандықтан, одан өткенде әрбір альфа-бөлшек тек бір
атоммен ғана әсерлеседі, яғни бір-ақ рет шашырауға ұшырайды
деп есептеуге болады. Шашыраған альфа-бөлшектер күкіртті
цинкпен ( ZnS) қапталған экранға келіп соғылады. Күкіртті цинк
молекулаларының альфа-бөлшекпен соқтығысқанда сәуле
шығаратын қасиеті бар. Сондықтан экранның альфа-бөлшек
соғылған жерлерінде сцинтилляция, яғни өте әлсіз жарқыл
байқалады. Тәжірибенің мақсаты берілген уақыт аралығында
байқалатын жарқылдардың φ ауытқу бұрышына тәуелділігін
анықтау.
8 слайд
Тәжірибе барысында өте жұқа ( l=6*10-7 м) алтын фольганы энергиясы 7,68 МэВ жылдам альфа бөлшектермен атқылаған. Қорғасын контейнердің түбінде орналасқан 21484 Ро радиоактивті элементтен шыққан альфа-бөлшектердің жіңішке шоғы алтын фольгадан өткенде шашырайды, яғни алғашқы бағытынан ауытқиды. Ол кезде альфа-бөлшектердің оң заряды (2е) гелий иондары екені белгілі болатын. Фольгадан шашыраған альфа-бөлшектердің қаншасы қандай бұрышқа ауытқығанын есептей отырып, осы ауытқуларды тудырған нысана- атомдардың құрылымы анықталады. Фольганың қалыңдығы өте аз болғандықтан, одан өткенде әрбір альфа-бөлшек тек бір атоммен ғана әсерлеседі, яғни бір-ақ рет шашырауға ұшырайды деп есептеуге болады. Шашыраған альфа-бөлшектер күкіртті цинкпен ( ZnS) қапталған экранға келіп соғылады. Күкіртті цинк молекулаларының альфа-бөлшекпен соқтығысқанда сәуле шығаратын қасиеті бар. Сондықтан экранның альфа-бөлшек соғылған жерлерінде сцинтилляция, яғни өте әлсіз жарқыл байқалады. Тәжірибенің мақсаты берілген уақыт аралығында байқалатын жарқылдардың φ ауытқу бұрышына тәуелділігін анықтау.

9 слайд
9 слайд
10 слайд
10 слайд
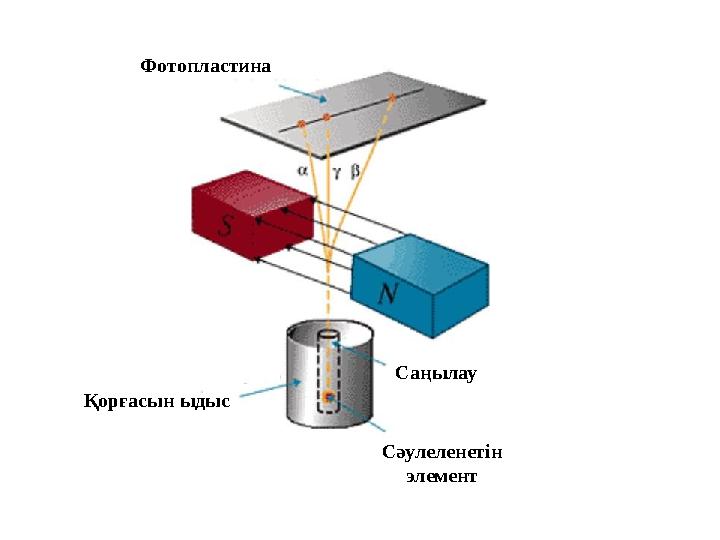
11 слайд
Фотопластина
Қорғасын ыдыс
Сәулеленетін
элементСаңылау
11 слайд
Фотопластина Қорғасын ыдыс Сәулеленетін элементСаңылау

12 слайд
Тәжірибенің нәтижесінде альфа-бөлшектердің
басым көпшілігі фольгадан өткенде алғашқы
бағыттан ауытқымайтыны (φ≈1 – 2°)
анықталды. Бұл нәтиже, негізінен, Томсон
моделіне сүйеніп жасалған есептеулермен дәл
келді. Бірақ, альфа-бөлшектердің мардымсыз аз
бөлігі 90°-тан артық бұрышқа ауытқитыны,
яғни олар фольгаға соғылып, кері бағытта
ұшатыны таңдандырды. Сегіз мыңға жуық
бөлшектердің біреуі ғана осындай үлкен
бұрышқа ауытқиды екен! Мұны Томсон моделі
негізінде түсіндіру тіпті мүмкін болмады.
12 слайд
Тәжірибенің нәтижесінде альфа-бөлшектердің басым көпшілігі фольгадан өткенде алғашқы бағыттан ауытқымайтыны (φ≈1 – 2°) анықталды. Бұл нәтиже, негізінен, Томсон моделіне сүйеніп жасалған есептеулермен дәл келді. Бірақ, альфа-бөлшектердің мардымсыз аз бөлігі 90°-тан артық бұрышқа ауытқитыны, яғни олар фольгаға соғылып, кері бағытта ұшатыны таңдандырды. Сегіз мыңға жуық бөлшектердің біреуі ғана осындай үлкен бұрышқа ауытқиды екен! Мұны Томсон моделі негізінде түсіндіру тіпті мүмкін болмады.

13 слайд
Тәжірибеде алынған нәтижелерді зерделей отырып
Резерфорд өз моделін ұсынды. Ол атомның оң заряды оның
ортасында орналасқан радиусы шамамен 10-15 м өте аз көлемге
жинақталған деген қорытындыға келді. Бірақ орталық бөлшекті
Резерфорд ядро деп атады. Атомның массасын түгел дерлік ядрода
шоғырланған. Ядроны айнала әр түрлі орбиталармен электрондар
қозғалып жүреді. Бұл үлгі Күн жүйесінің құрылымына ұқсайтын
болғандықтан, оны атомның планетарлық моделі деп те атайды.
Модель бойынша атом көлемінің басым көпшілік бөлігі «бос»
болып шығады, ядроның радиусы атомның радиусынан 100000 есе
кіші. Орбиталардағы электрондардың теріс зарядтарының
қосындысы ядроның оң зарядына тең, атом электрлік бейтарап.
13 слайд
Тәжірибеде алынған нәтижелерді зерделей отырып Резерфорд өз моделін ұсынды. Ол атомның оң заряды оның ортасында орналасқан радиусы шамамен 10-15 м өте аз көлемге жинақталған деген қорытындыға келді. Бірақ орталық бөлшекті Резерфорд ядро деп атады. Атомның массасын түгел дерлік ядрода шоғырланған. Ядроны айнала әр түрлі орбиталармен электрондар қозғалып жүреді. Бұл үлгі Күн жүйесінің құрылымына ұқсайтын болғандықтан, оны атомның планетарлық моделі деп те атайды. Модель бойынша атом көлемінің басым көпшілік бөлігі «бос» болып шығады, ядроның радиусы атомның радиусынан 100000 есе кіші. Орбиталардағы электрондардың теріс зарядтарының қосындысы ядроның оң зарядына тең, атом электрлік бейтарап.

14 слайд
Атомның ішіндегі бос кеңістік «өте үлкен». Сондықтан,
фольга арқылы өткенде альфа-бөлшектерінің көбі
ядродан алыс өтеді де, шашырамайды. Электрондар
альфа-бөлшектен 8 мың еседей жеңіл болғандықтан,
оның қозғалыс траекториясын өзгерте алмайды. Тек
ядроға тікелей қарсы келіп қалған альфа-бөлшектер
ғана онымен әсерлесіп, кері ұшады. Мұндай бөлшектер
саны ядро радиусының атом радиусына қатынасымен
анықталады.
14 слайд
Атомның ішіндегі бос кеңістік «өте үлкен». Сондықтан, фольга арқылы өткенде альфа-бөлшектерінің көбі ядродан алыс өтеді де, шашырамайды. Электрондар альфа-бөлшектен 8 мың еседей жеңіл болғандықтан, оның қозғалыс траекториясын өзгерте алмайды. Тек ядроға тікелей қарсы келіп қалған альфа-бөлшектер ғана онымен әсерлесіп, кері ұшады. Мұндай бөлшектер саны ядро радиусының атом радиусына қатынасымен анықталады.
15 слайд
15 слайд
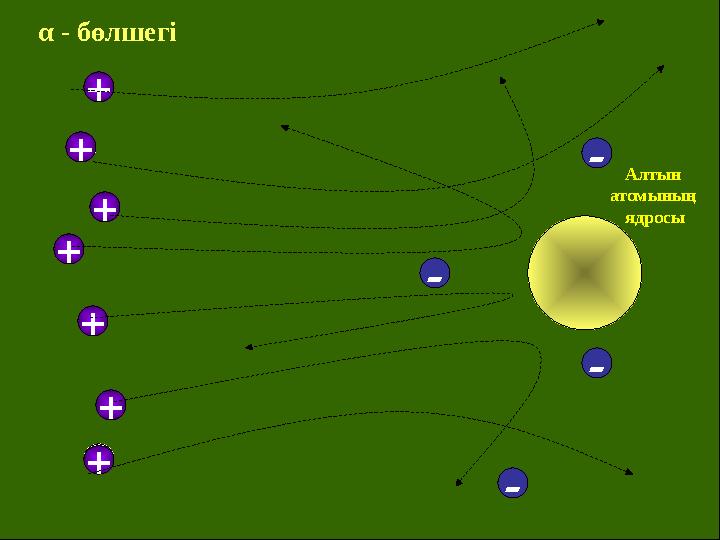
16 слайд
+
++
++
++ Алтын
атомының
ядросы
-
--
-α - бөлшегі
16 слайд
+ ++ ++ ++ Алтын атомының ядросы - -- -α - бөлшегі
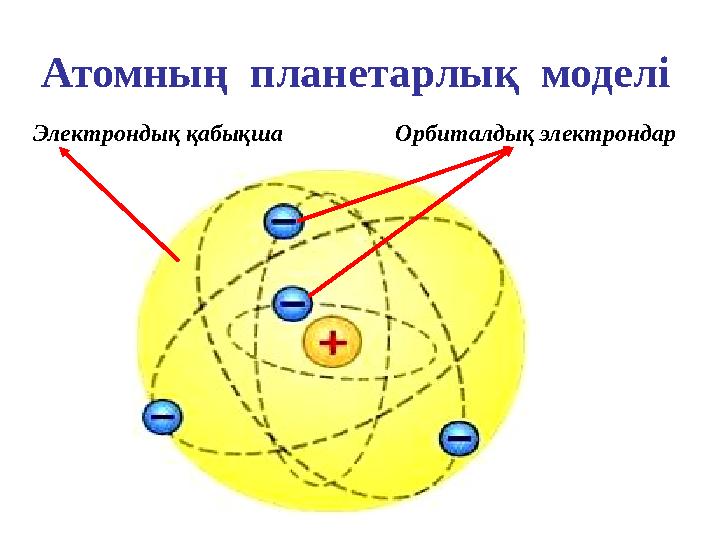
17 слайд
Атомның планетарлық моделі
Орбиталдық электрондарЭлектрондық қабықша
17 слайд
Атомның планетарлық моделі Орбиталдық электрондарЭлектрондық қабықша

18 слайд
q я = + Z • e
Z-элементтің Менделеев кестесіндегі
реттік саны, протон саны; Ядроның өлшемі, заряды
Ядро ның диаметрі 10 -12
- 10 -13
см,
атомның диаметрі 10 - 8
см
q э = - Z • e
- әрбір электронның немесе протонның заряды бір элемен-
тар зарядқа ( е =-1,6 • 10 - 1 9
Кл) тең;
- кез келген элемент атомының ядросындағы протондар са-
ны сол элементтің Менделеев кестесіндегі Z реттік санына
тең.
Z =1 Z=92 U
235
92
H
1
1q я = + Z • e
Z-элементтің Менделеев кестесіндегі
реттік саны, протон саны; q э = - Z • e
18 слайд
q я = + Z • e Z-элементтің Менделеев кестесіндегі реттік саны, протон саны; Ядроның өлшемі, заряды Ядро ның диаметрі 10 -12 - 10 -13 см, атомның диаметрі 10 - 8 см q э = - Z • e - әрбір электронның немесе протонның заряды бір элемен- тар зарядқа ( е =-1,6 • 10 - 1 9 Кл) тең; - кез келген элемент атомының ядросындағы протондар са- ны сол элементтің Менделеев кестесіндегі Z реттік санына тең. Z =1 Z=92 U 235 92 H 1 1q я = + Z • e Z-элементтің Менделеев кестесіндегі реттік саны, протон саны; q э = - Z • e
19 слайд
Протон Нейтрон
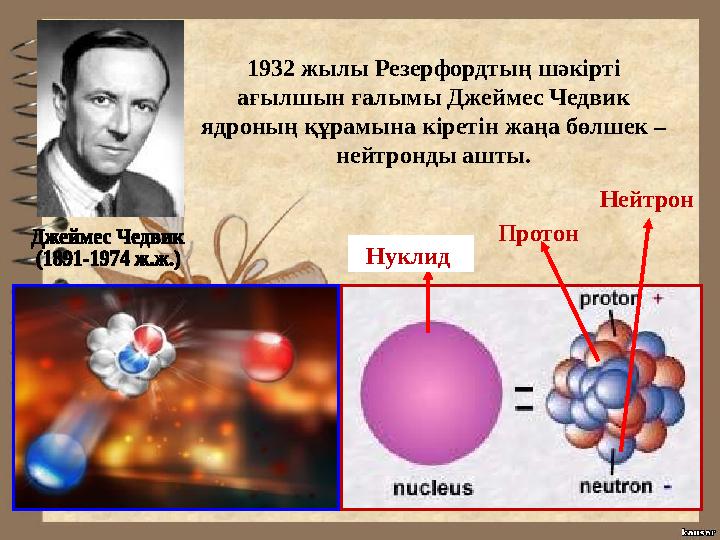
Нуклид 1932 жылы Резерфордтың шәкірті
ағылшын ғалымы Джеймес Чедвик
ядроның құрамына кіретін жаңа бөлшек –
нейтронды ашты.
19 слайд
Протон Нейтрон Нуклид 1932 жылы Резерфордтың шәкірті ағылшын ғалымы Джеймес Чедвик ядроның құрамына кіретін жаңа бөлшек – нейтронды ашты.
20 слайд
Химиялы қ элемент
z Х А
A = N + Z
Сутегі ядросы
z Н А
Уран ядросы
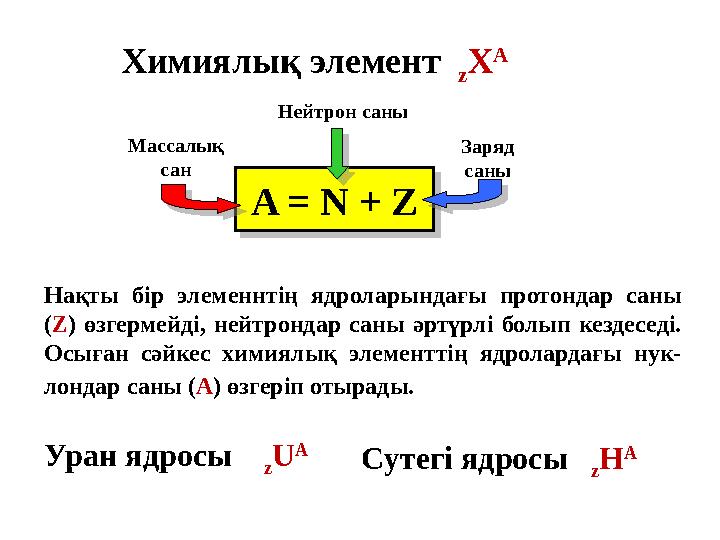
z U A Нақты бір элеменнтің ядроларындағы протондар саны
( Z ) өзгермейді, нейтрондар саны әртүрлі болып кездеседі.
Осыған сәйкес химиялық элементтің ядролардағы нук-
лондар саны ( А ) өзгеріп отырады. Массалық
сан Заряд
саныНейтрон саныA = N + Z
20 слайд
Химиялы қ элемент z Х А A = N + Z Сутегі ядросы z Н А Уран ядросы z U A Нақты бір элеменнтің ядроларындағы протондар саны ( Z ) өзгермейді, нейтрондар саны әртүрлі болып кездеседі. Осыған сәйкес химиялық элементтің ядролардағы нук- лондар саны ( А ) өзгеріп отырады. Массалық сан Заряд саныНейтрон саныA = N + Z
21 слайд
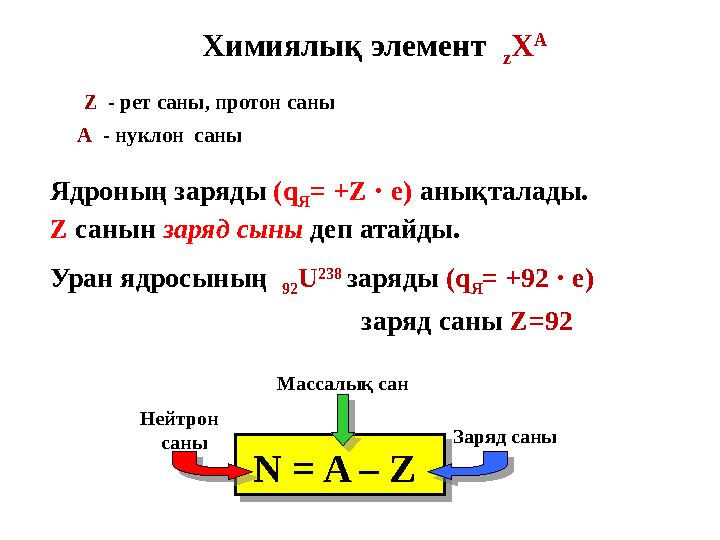
Уран ядросының
92 U 238
заряды (q
Я = + 92 · е) Химиялы қ элемент
z Х А
Z - рет саны, протон саны
А - нуклон саны
заряд саны Z =92 Ядроның заряды (q
Я = +Z · е) анықталады.
Z санын заряд сыны деп атайды.
N = A – Z Заряд саны
Массалық сан
Нейтрон
саны
N = A – Z Заряд саны
Массалық сан
Нейтрон
саныN = A – Z N = A – Z
21 слайд
Уран ядросының 92 U 238 заряды (q Я = + 92 · е) Химиялы қ элемент z Х А Z - рет саны, протон саны А - нуклон саны заряд саны Z =92 Ядроның заряды (q Я = +Z · е) анықталады. Z санын заряд сыны деп атайды. N = A – Z Заряд саны Массалық сан Нейтрон саны N = A – Z Заряд саны Массалық сан Нейтрон саныN = A – Z N = A – Z
22 слайд
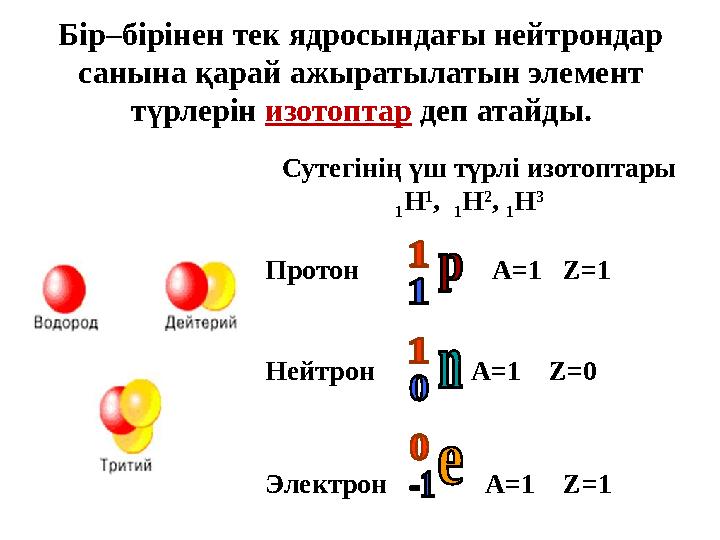
Бір – бірінен тек ядросындағы нейтрондар
санына қарай ажыратылатын элемент
түрлерін изотоптар деп атайды.
Сутегінің үш түрлі изотоптары
1 Н 1
,
1 Н 2
,
1 Н 3
Протон А=1 Z=1
Нейтрон
А =1 Z=0
Электрон А =1 Z=1
22 слайд
Бір – бірінен тек ядросындағы нейтрондар санына қарай ажыратылатын элемент түрлерін изотоптар деп атайды. Сутегінің үш түрлі изотоптары 1 Н 1 , 1 Н 2 , 1 Н 3 Протон А=1 Z=1 Нейтрон А =1 Z=0 Электрон А =1 Z=1

23 слайд
23 слайд

24 слайд
Атом ядросында 51 р және 71 n бар. Бұл қандай элемент?
Атом ядросында 101 р және 155 n бар. Бұл қандай элемент?
Магнийдің үш изотобы: ядроларының
құрамына енетін протондар мен нейтрондарының санын табыңдар.
Менделеев кестесін пайдаланып, аргон, күміс, алтын, уран атомда-
ры ядроларындағы протондар саны мен нейтрондар санын анық-
таңдар. Mg ,24
12 Mg ,25
12 Mg26
12
24 слайд
Атом ядросында 51 р және 71 n бар. Бұл қандай элемент? Атом ядросында 101 р және 155 n бар. Бұл қандай элемент? Магнийдің үш изотобы: ядроларының құрамына енетін протондар мен нейтрондарының санын табыңдар. Менделеев кестесін пайдаланып, аргон, күміс, алтын, уран атомда- ры ядроларындағы протондар саны мен нейтрондар санын анық- таңдар. Mg ,24 12 Mg ,25 12 Mg26 12
25 слайд
а
n ре -
Я
25 слайд
а n ре - Я

26 слайд
Назарларыңызға
рахмет !!!
26 слайд
Назарларыңызға рахмет !!!



