|
Ұйымдастыру. Студенттермен
сәлемдесу
Топта ынтымақтастықтық
атмосферасын және қалыпты оқу ортасын
қалыптастыру.
Лотерея
әдісі арқылы 2 топқа
бөлемін.
1.топ-Аккумулятор
2.топ-Электролит
Үй
тапсырмасы.
Кубик әдісі
бойынша:
Сұрақтар:
1.Электродтық
потенциал деген не?
2.Анодта қандай процес
жүреді. (тотығу/тотықсыздану)
3.Катодта қандай процес жүреді
(тотығу/тотықсыздану)
4.Электр қозғаушы
күшін (ЭҚК) немен есептейді
5.Электродты потенциалының
мәні үлкен металдар кернеу қатарының қай жағында
тұрады.
6.Электродты потенциалының
мәні кіші металдар кернеу қатарының қай жағында
тұрады.
PISA
тапсырмалары:
Назгүл алма және
лимон шырынымен эксперимент жасайтын болды. Ол алманы екіге бөліп,
кесілген жағымен жайпақ ыдысқа салып қойды. Алманың бір бөлігіне
лимон шырынын сығып тамызды. Біраз уақыттан кейін лимон шырынымен
қорғалған бөлігінің ақ қалпында қалғанын, ал алманың таза бөлігі
қарайғанын байқады.
Сұрақ: Алманың «таза» бөлігі
неліктен қарайды?
Аккумуляторларда
жүретін химиялық процестер
Аккумулятор – өзіне
электр энергиясын жинайтын құрылғы, ол қажет кезінде энергияны
сыртқы тізбекке бере алатын химиялық ток көзі болып
табылады.
Аккумуляторлар
бір-бірінен электродтармен, электролиттердің химиялық табиғатымен
және құрылымымен ерекшеленеді.
Аккумуляторлардың
түрлері:
1.Қышқылдық
(қорғасын);
2.Сілтілік
(кадмий-никель және күміс-мырыш);
Қорғасын
аккумуляторы қорғасын (ІІ) оксидімен PbO толтырылған торлы қорғасын
тақташаларынан тұрады. Тақташалар 20 -- 25%- дық күкірт қышқылының
(тығыздығы 1,18-1,22г/см3
) ерітіндісіне
батырылады.
Тақташаның бетінде
қорғасын (ІІ) оксиді мен күкірт қышқылының әрекеттесуі нәтижесінде
ерімейтін қорғасын сульфаты
түзіледі.
PbO +
H2SO4
=
PbSO4
+
H2O
Уақыт өте келе
қорғасын сульфаты кристалданып, тақташаның бір бөлігін қаптайды.
Осы процестің нәтижесінде тақташа химиялық реакцияға түспейді.
Сөйтіп аккумулятор зарядсызданады.
Мұндай құбылыс сульфаттану деп
аталады.
Аккумуляторда
химиялық энергияның қорын жинау үшін оны зарядтау керек.
Аккумуляторды зарядтау барысында электр энергиясы химиялық
энергияға айналады. Жүретін электролиз процесінің
теңдеуі:
Катод:
PbSO4
+ 2e =
Pb0
+
SO4
Анод:PbSO4
+
2H2O-2e =
PbO2
+
SO4+4Н+
Аккумулятордың
зарядталу процесін мынадай жиынтық теңдеумен көрсетуге
болады.
2PbSO4
+
2H2O =
Pb0
+
PbO2+2SO4+4Н+
Бұл процесті
аккумуляторды зарядтау деп атайды. Зарядталған оң пластина
қара-қоңыр түсті, теріс пластина-қара-сұр түсті
болады.
Егер аккумуляторға
тұтынушы қосса, ол разрядтала бастайды. Разрядталу кезінде
пластиналар түсі өзгереді : оң пластина ақшыл қоңыр, теріс
пластина-ақшыл сұр болады. Аккумулятор қажет мөлшерде ток беру үшін
оны қайта тұрақты ток көзінен зарядтау
керек.
Гальваникалық
элемент дегеніміз– химиялық тотығу –
тотықсыздану реакцияларының энергиясын электр энергиясына
айналдыратын қондырғы
Заманауи гальваникалық
элемент
Гальваникалық элемент бұл химиялық электр
тогының көзі, бұл құбылысты бірінші анықтаған Гальвани, соның
құрметіне гальваникалық элементтер деп
аталады.
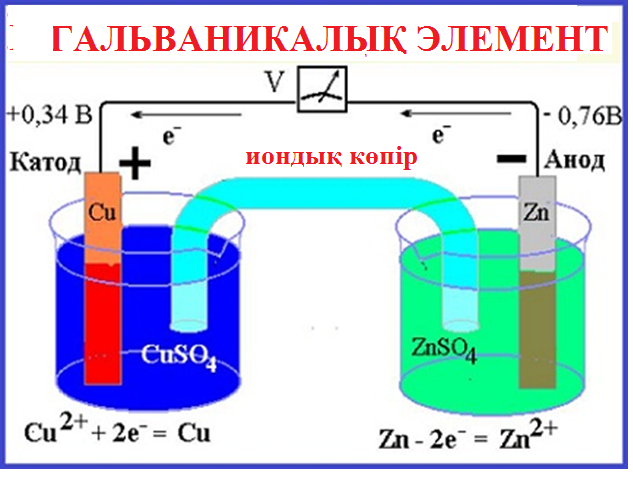
Өзара металл өткізгішпен
жалғанған және бір-бірімен байланысқан ерітінділерге салынған екі
электродтан тұратын жүйені электрохимиялық тізбек деп
атайды.
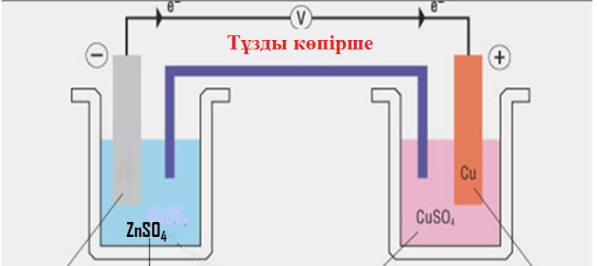
Видео
көрсетілім:  
|










