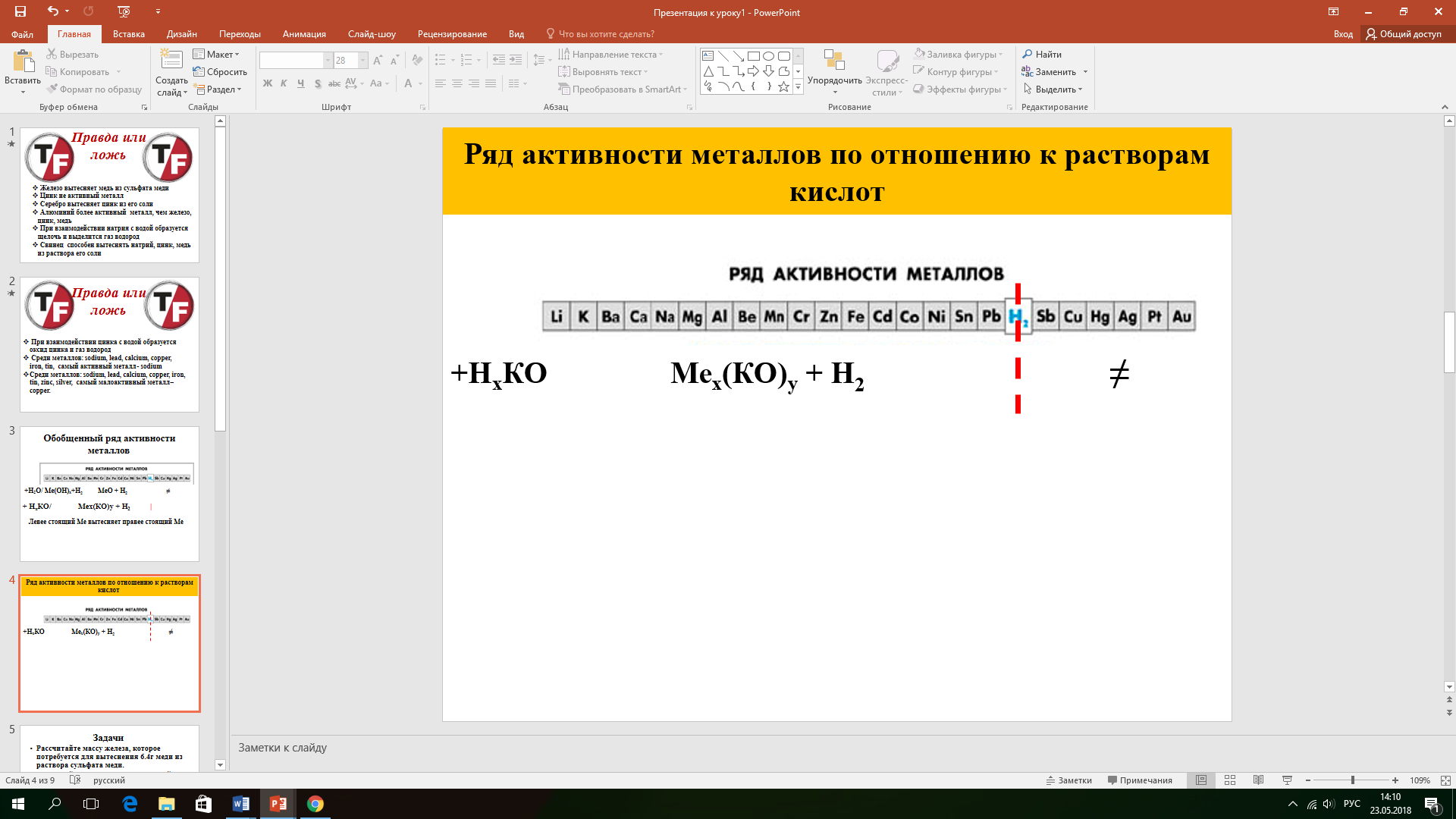
Материалдар / Реакции металлов с растворами кислот. Лабораторный опыт №3 «Взаимодействие металлов с равторами кислот» 8 сынып
2023-2024 оқу жылына арналған
қысқа мерзімді сабақ жоспарларын
жүктеп алғыңыз келеді ма?
ҚР Білім және Ғылым министірлігінің стандартымен 2022-2023 оқу жылына арналған 472-бұйрыққа сай жасалған

Реакции металлов с растворами кислот. Лабораторный опыт №3 «Взаимодействие металлов с равторами кислот» 8 сынып
Материал туралы қысқаша түсінік
Химия пәні мұғалімдері үшін
Авторы:
Автор материалды ақылы түрде жариялады.
Сатылымнан түскен қаражат авторға автоматты түрде аударылады. Толығырақ
Сатылымнан түскен қаражат авторға автоматты түрде аударылады. Толығырақ
Бүгін алсаңыз
25% жеңілдік
беріледі
беріледі
770 тг 578 тг

Тегін турнир Мұғалімдер мен Тәрбиешілерге
Дипломдар мен сертификаттарды алып үлгеріңіз!
Дипломдар мен сертификаттарды алып үлгеріңіз!

Бұл бетте материалдың қысқаша нұсқасы ұсынылған. Материалдың толық нұсқасын жүктеп алып, көруге болады

Материалдың толық нұсқасын
жүктеп алып көруге болады
Материал жариялап тегін сертификат алыңыз!
Бұл сертификат «Ustaz tilegi» Республикалық ғылыми – әдістемелік журналының желілік басылымына өз авторлық жұмысын жарияланғанын растайды. Журнал Қазақстан Республикасы Ақпарат және Қоғамдық даму министрлігінің №KZ09VPY00029937 куәлігін алған. Сондықтан аттестацияға жарамды

Материал іздеу
Сіз үшін 400 000 ұстаздардың еңбегі мен тәжірибесін біріктіріп, ең үлкен материалдар базасын жасадық. Төменде пәніңізді белгілеп, керек материалды алып сабағыңызға қолдана аласыз
Барлығы 663 959 материал жиналған
Ұқсас материалдар
 Дайын ҚМЖ. Барлық пәндерден 2022-2023 оқу жылына, жаңа бұйрыққа сай жасалған
Дайын ҚМЖ. Барлық пәндерден 2022-2023 оқу жылына, жаңа бұйрыққа сай жасалған
ҚР Білім және Ғылым министірлігінің стандарты бойынша жасалған. 2022-2023 оқу жылына арналған
Барлық пәндер
Барлық материалдар
Барлық сыныптар
Іс-шаралар кестесі
Педагогтардың біліктілігін арттыру курстары