Азотқышқылы және оның қолданылуы 9 сынып


#1 слайд
1 слайд

#2 слайд
Сабақ мақсаты:
оксидтердің жіктеліун, құрлысын
қасиеттері мен қолданылыуын және
азот қышқылының негізгі
қасиеттері мен күшті тотықтырғыш
ретінде металдармен әрекеттесіуі
туралы білімді қалыптастыру.
2 слайд
Сабақ мақсаты: оксидтердің жіктеліун, құрлысын қасиеттері мен қолданылыуын және азот қышқылының негізгі қасиеттері мен күшті тотықтырғыш ретінде металдармен әрекеттесіуі туралы білімді қалыптастыру.

#3 слайд
Сабақтың барысы:
үйымдастыру ( 2 минут)
үй тапсырмасын тексеру. ( 10 минут)
Жаңа сабақ. ( 2 0минут)
Жаңа сабақты бекіту. (10минут)
Үй тапсырмасы. ( 1 минут)
Білімді бағалау. ( 1 минут)
Сабақты қортыу. ( 1 минут)
3 слайд
Сабақтың барысы: үйымдастыру ( 2 минут) үй тапсырмасын тексеру. ( 10 минут) Жаңа сабақ. ( 2 0минут) Жаңа сабақты бекіту. (10минут) Үй тапсырмасы. ( 1 минут) Білімді бағалау. ( 1 минут) Сабақты қортыу. ( 1 минут)

#4 слайд
үй тапсырмасын тексеру:
1. Аммиактың химиялық қасиетіне мысал келтіріу.
2. Аммоний тұздарына мысал келтіріп, оның қандай
ерекше қасиеті бар екенін айтып беріңдер.
3. Өршіткі қатысында 1,12 л (Қ.Ж) аммиакты
тотықтырғанда, қанша моль азот (II)оксиді
алынатынын есептеңдер.
4. Өршіткі қатыспса 2,24 л ( ҚЖ ) аммиакты
тотықтырғанда, қанша мол газ алынатынын
есептеңдер.
5. Аммиактың қолданылыуын айтып беріңдер.
4 слайд
үй тапсырмасын тексеру: 1. Аммиактың химиялық қасиетіне мысал келтіріу. 2. Аммоний тұздарына мысал келтіріп, оның қандай ерекше қасиеті бар екенін айтып беріңдер. 3. Өршіткі қатысында 1,12 л (Қ.Ж) аммиакты тотықтырғанда, қанша моль азот (II)оксиді алынатынын есептеңдер. 4. Өршіткі қатыспса 2,24 л ( ҚЖ ) аммиакты тотықтырғанда, қанша мол газ алынатынын есептеңдер. 5. Аммиактың қолданылыуын айтып беріңдер.

#5 слайд
5 слайд

#6 слайд
Азот ты ң тотығу дәрежесі -3 ден +5.ге дейін өзгереді
Азоттың негізгі оксидтері.
+1 +2 +3 +4 +5
Т үз түзетін оксидтері: N2O3 NO2 N2O4 N2O5
димер
оксида азота( IV)
Түз түзбейтін оксидтер: N2O NO N2O
5N2O NO N2O3 NO2
6 слайд
Азот ты ң тотығу дәрежесі -3 ден +5.ге дейін өзгереді Азоттың негізгі оксидтері. +1 +2 +3 +4 +5 Т үз түзетін оксидтері: N2O3 NO2 N2O4 N2O5 димер оксида азота( IV) Түз түзбейтін оксидтер: N2O NO N2O 5N2O NO N2O3 NO2

#7 слайд
Азот( II )оксиді
Табиғатта пайда болуы: атмосфера азотынан найзағай
жарқылдағанда пайда болады.
N2 + O2 2 NO
Зетханада алынуы : 8 С u + 3 HNO3 = 3 Cu(NO3)2 +
2 NO + 4 H2O
с ұйылт .II II
N = О
Ауадағы оттекпен оңай
тотығады :
2 NO + O2 = 2 NO2 (улы!) Күкірт оксидімен әрекеттесіп:
2 NO + 2 SO2 = 2 SO3 + N2
Бос күйдегі азотты алуға боладыNO
Ол түссіз, суда өте аз еритін газ. Ол тұз
түзбейтін оксид
қатарына жатады.
7 слайд
Азот( II )оксиді Табиғатта пайда болуы: атмосфера азотынан найзағай жарқылдағанда пайда болады. N2 + O2 2 NO Зетханада алынуы : 8 С u + 3 HNO3 = 3 Cu(NO3)2 + 2 NO + 4 H2O с ұйылт .II II N = О Ауадағы оттекпен оңай тотығады : 2 NO + O2 = 2 NO2 (улы!) Күкірт оксидімен әрекеттесіп: 2 NO + 2 SO2 = 2 SO3 + N2 Бос күйдегі азотты алуға боладыNO Ол түссіз, суда өте аз еритін газ. Ол тұз түзбейтін оксид қатарына жатады.

#8 слайд
Азот ( IV) оксиді
+3
+5
2 NO2 + H2O = HNO2 +
HNO3 II III III II
O=N-N=O
Ол суда ерігенде, азот қышқылымен қатар
азотты қышкыл да түзіледі:
Азот (IV) оксиді N0
2 оттек қатысында сумен
әрекеттесіп, азот қышқылын түзеді:
8 слайд
Азот ( IV) оксиді +3 +5 2 NO2 + H2O = HNO2 + HNO3 II III III II O=N-N=O Ол суда ерігенде, азот қышқылымен қатар азотты қышкыл да түзіледі: Азот (IV) оксиді N0 2 оттек қатысында сумен әрекеттесіп, азот қышқылын түзеді:

#9 слайд
Азот қышкылы. Азоттьщ маңызды
қосылыстарының бірі — азот
қышқылы НNО
3 . Онда азот +5
тотығу дәрежесін көрсетеді. Онын
судағы ерітіндісі қышқыл қалдығына
және гидроксоний ионға
диссоциацияланады:
9 слайд
Азот қышкылы. Азоттьщ маңызды қосылыстарының бірі — азот қышқылы НNО 3 . Онда азот +5 тотығу дәрежесін көрсетеді. Онын судағы ерітіндісі қышқыл қалдығына және гидроксоний ионға диссоциацияланады:

#10 слайд
Алынуы .
Зертханада қатты натрий нитратына концентрациялы
күкірт қышқылымен әсер етіп, азот кышқылын алуға
болады:
NaNO
3 +H
2 SO
4 NaHSO
4 +HNO
3
т ү з і лген азот қ ыш қ ылынь ң буын конденсациялау азот
қ ыш қ ылын аммиакты тотыктыру аркылы
концентрациялы азот қ ыш қ ылын алады.
ө неркес іп те ды, ол б і р не ш е сатыдан т ү рады.
NH
3 NO
NO
2 HNO
3
10 слайд
Алынуы . Зертханада қатты натрий нитратына концентрациялы күкірт қышқылымен әсер етіп, азот кышқылын алуға болады: NaNO 3 +H 2 SO 4 NaHSO 4 +HNO 3 т ү з і лген азот қ ыш қ ылынь ң буын конденсациялау азот қ ыш қ ылын аммиакты тотыктыру аркылы концентрациялы азот қ ыш қ ылын алады. ө неркес іп те ды, ол б і р не ш е сатыдан т ү рады. NH 3 NO NO 2 HNO 3

#11 слайд
Физикалық қасиеттері.
С Т Н NO
3
Ұ И Mr = 63
Й У T
қату = -42 0
C
Ы T
балқу = 86 0
C
Қ + H
2 O → ерид і
11 слайд
Физикалық қасиеттері. С Т Н NO 3 Ұ И Mr = 63 Й У T қату = -42 0 C Ы T балқу = 86 0 C Қ + H 2 O → ерид і

#12 слайд
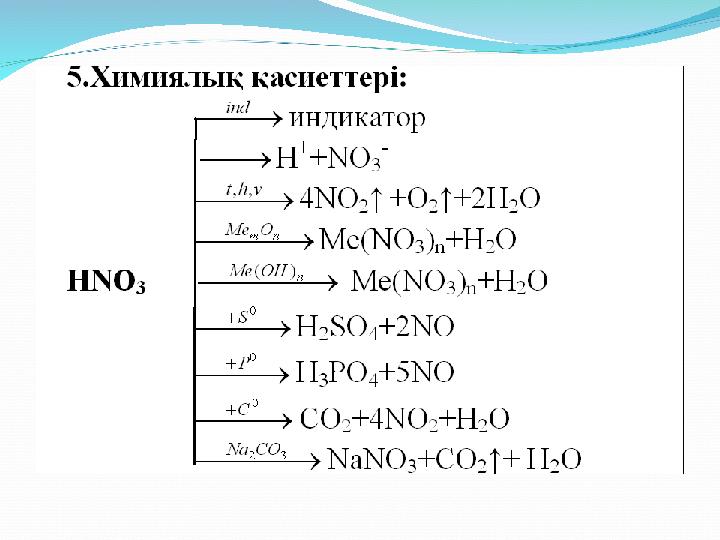
Химиялық қасиеттері:
азот қышқылы концентрлі және сұйытылған ерітінділері
тотықтырғыш қасиет көрсетеді.
Жарықтың әсерінен азот қышқылы азот(IV) оксидіне,
суға және оттекке ыдырайды:
4HNO
3 = 4NO
2 +O
2 + 3H
2 O
азот қышқылы HNO
3 ба сқа қышқылдар тәрізді негіздік
оксидтермен әрекеттесіп тұз түзеді:
С uO + 2HNO
3 = Cu(NO
3 )
2 +H
2 O
CuO + 2H = Cu 2+
+ H
2 O
А зот қышқылы негіздермен әрекеттеседі:
Cu(OH)
2 + 2HNO
3 = Cu(NO
3 )
2 + H
2 O
Cu(OH)
2 + 2H +
= Cu 2+
+ 2H
2 O
12 слайд
Химиялық қасиеттері: азот қышқылы концентрлі және сұйытылған ерітінділері тотықтырғыш қасиет көрсетеді. Жарықтың әсерінен азот қышқылы азот(IV) оксидіне, суға және оттекке ыдырайды: 4HNO 3 = 4NO 2 +O 2 + 3H 2 O азот қышқылы HNO 3 ба сқа қышқылдар тәрізді негіздік оксидтермен әрекеттесіп тұз түзеді: С uO + 2HNO 3 = Cu(NO 3 ) 2 +H 2 O CuO + 2H = Cu 2+ + H 2 O А зот қышқылы негіздермен әрекеттеседі: Cu(OH) 2 + 2HNO 3 = Cu(NO 3 ) 2 + H 2 O Cu(OH) 2 + 2H + = Cu 2+ + 2H 2 O

#13 слайд
Металмен азот қышқылы басқаша әрекеттеседі
Cu + 4HNO
3 = Cu(NO
3 )
2 +2NO
2 +2H
2 O
Тотықсыздандырғыш Сu – 2e = Cu 1 тотығады
Тотықтырғыш N + e = N 2 тотықсызданады
Сұйылтылған азот қышқылы мыспен әрекеттескенде азот(II)
оксиді NO түзіледі:
3Cu + 8HNO
3 ( сұйық ) = Cu(NO
3 )
2 +2NO+4H
2 O
Тотықсыздандырғыш Сu – 2e = Cu 3 тотығады
Тотықтырғыш N + 3e = N 2 тотықсызданады
Азот қышқылы кейбір металдармен әрекеттеспейді.
Мысалы:Алюминиймен және темірмен әрекеттеспейді, себебі
металдардың сыртында тұрақты оксидтік қабат
түзеді.сондықтан азот қышқылын тасымалдауда болат немесе
алюминий ыдыстар қолданады.
13 слайд
Металмен азот қышқылы басқаша әрекеттеседі Cu + 4HNO 3 = Cu(NO 3 ) 2 +2NO 2 +2H 2 O Тотықсыздандырғыш Сu – 2e = Cu 1 тотығады Тотықтырғыш N + e = N 2 тотықсызданады Сұйылтылған азот қышқылы мыспен әрекеттескенде азот(II) оксиді NO түзіледі: 3Cu + 8HNO 3 ( сұйық ) = Cu(NO 3 ) 2 +2NO+4H 2 O Тотықсыздандырғыш Сu – 2e = Cu 3 тотығады Тотықтырғыш N + 3e = N 2 тотықсызданады Азот қышқылы кейбір металдармен әрекеттеспейді. Мысалы:Алюминиймен және темірмен әрекеттеспейді, себебі металдардың сыртында тұрақты оксидтік қабат түзеді.сондықтан азот қышқылын тасымалдауда болат немесе алюминий ыдыстар қолданады.

#14 слайд
Сұйылтылған азот қышқылы мыспен әрекеттескенде
азот(II) оксиді NO түзіледі:
3Cu + 8HNO
3 ( сұйық ) = Cu(NO
3 )
2 +2NO+4H
2 O
Тотықсыздандырғыш Сu – 2e = Cu 3 тотығады
Тотықтырғыш N + 3e = N 2 тотықсызданады
Азот қышқылы кейбір металдармен
әрекеттеспейді. Мысалы:Алюминиймен және
темірмен әрекеттеспейді, себебі металдардың
сыртында тұрақты оксидтік қабат
түзеді.сондықтан азот қышқылын тасымалдауда
болат немесе алюминий ыдыстар қолданады.
14 слайд
Сұйылтылған азот қышқылы мыспен әрекеттескенде азот(II) оксиді NO түзіледі: 3Cu + 8HNO 3 ( сұйық ) = Cu(NO 3 ) 2 +2NO+4H 2 O Тотықсыздандырғыш Сu – 2e = Cu 3 тотығады Тотықтырғыш N + 3e = N 2 тотықсызданады Азот қышқылы кейбір металдармен әрекеттеспейді. Мысалы:Алюминиймен және темірмен әрекеттеспейді, себебі металдардың сыртында тұрақты оксидтік қабат түзеді.сондықтан азот қышқылын тасымалдауда болат немесе алюминий ыдыстар қолданады.
#15 слайд
15 слайд
#16 слайд
HNO 3
концентрлі сұйытылған өте
сұйытылған
Ca,Mg,Zn Fe,Cr,
Ni
Pb,Cu,Hg,Ag Fe,Cr,Ni
Ca,Mg,
Zn
Pb,Cu,Hg,Ag
Ca,Mg,Zn
әрекеттес -
пейді
NO NO 2
концентра -
циясына
байланысты
NO 2, NO ,
N 2O, NH 3
N 2O,
N 2
NO
NH 3
Au,Pt,Os,Ir
әрекеттеспейді
16 слайд
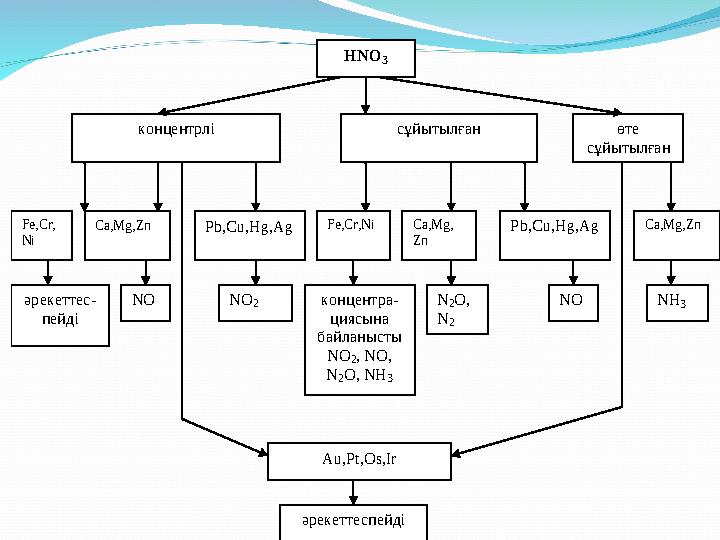
HNO 3 концентрлі сұйытылған өте сұйытылған Ca,Mg,Zn Fe,Cr, Ni Pb,Cu,Hg,Ag Fe,Cr,Ni Ca,Mg, Zn Pb,Cu,Hg,Ag Ca,Mg,Zn әрекеттес - пейді NO NO 2 концентра - циясына байланысты NO 2, NO , N 2O, NH 3 N 2O, N 2 NO NH 3 Au,Pt,Os,Ir әрекеттеспейді
#17 слайд
Азот қышқылының қолданылуы
Азот қышқылы
HNO
3
17 слайд
Азот қышқылының қолданылуы Азот қышқылы HNO 3

#18 слайд
Жа ңа сабақты бекіту
1. Үш колба берілген: азот (IV) оксиді , азот, аммиак бар.
Оттекпен әрекеттескенде қандай газ бөлінеді реакция теңдеуін
жаз
NO2NH3 N 2
18 слайд
Жа ңа сабақты бекіту 1. Үш колба берілген: азот (IV) оксиді , азот, аммиак бар. Оттекпен әрекеттескенде қандай газ бөлінеді реакция теңдеуін жаз NO2NH3 N 2
#19 слайд
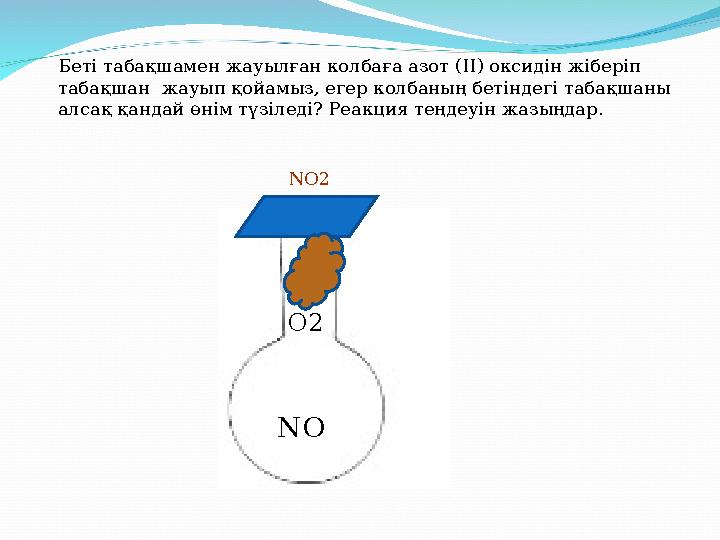
Беті табақшамен жауылған колбаға азот ( II ) оксидін жіберіп
табақшан жауып қойамыз, егер колбаның бетіндегі табақшаны
алсақ қандай өнім түзіледі? Реакция теңдеуін жазыңдар.
NO O2NO2
19 слайд
Беті табақшамен жауылған колбаға азот ( II ) оксидін жіберіп табақшан жауып қойамыз, егер колбаның бетіндегі табақшаны алсақ қандай өнім түзіледі? Реакция теңдеуін жазыңдар. NO O2NO2

#20 слайд
Концентрациялы күкірт
қышқылымен азот қышқылына
салыстырмалы сипаттама
беріңдер.
Cұйытылған азот қышқылы
темірмен әрекеттескенде
шығатын өнімдеріді атап
көрсетіңдер.
20 слайд
Концентрациялы күкірт қышқылымен азот қышқылына салыстырмалы сипаттама беріңдер. Cұйытылған азот қышқылы темірмен әрекеттескенде шығатын өнімдеріді атап көрсетіңдер.

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
