Қышқылдар. 8 сынып ашық сабаққа презентация
Қышқылдар. 8 сынып ашық сабаққа презентация


#1 слайд
§ 44 Қышқылдар Ақкөз Қосанұлы атындағы №18 жалпы білім беретін тірек
мектебі (р/о)
Джайылова Б.А
1 слайд
§ 44 Қышқылдар Ақкөз Қосанұлы атындағы №18 жалпы білім беретін тірек мектебі (р/о) Джайылова Б.А

#2 слайд
«Болжау» әдісі«Болжау» әдісі
2 слайд
«Болжау» әдісі«Болжау» әдісі

#3 слайд
ҚЫШҚЫЛДАР
Сутек атомы
Н
қышқыл қалдығы
СІ
SO 4
PO 4
НСІ
Н 2 SO 4
Н 3 PO 4
3 слайд
ҚЫШҚЫЛДАР Сутек атомы Н қышқыл қалдығы СІ SO 4 PO 4 НСІ Н 2 SO 4 Н 3 PO 4
#4 слайд
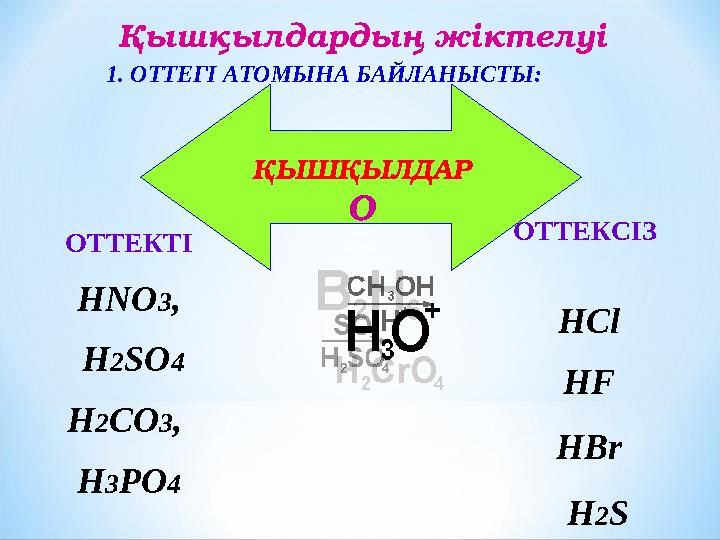
Қышқылдардың жіктелуі
ОТТЕКСІЗ
HCl
HF
HBr
H 2 S 1. ОТТЕГІ АТОМЫНА БАЙЛАНЫСТЫ:
ОТТЕКТІ
HNO 3 ,
H 2 SO 4
H 2 CO 3 ,
H 3 PO 4 ҚЫШҚЫЛДАР
О
4 слайд
Қышқылдардың жіктелуі ОТТЕКСІЗ HCl HF HBr H 2 S 1. ОТТЕГІ АТОМЫНА БАЙЛАНЫСТЫ: ОТТЕКТІ HNO 3 , H 2 SO 4 H 2 CO 3 , H 3 PO 4 ҚЫШҚЫЛДАР О
#5 слайд
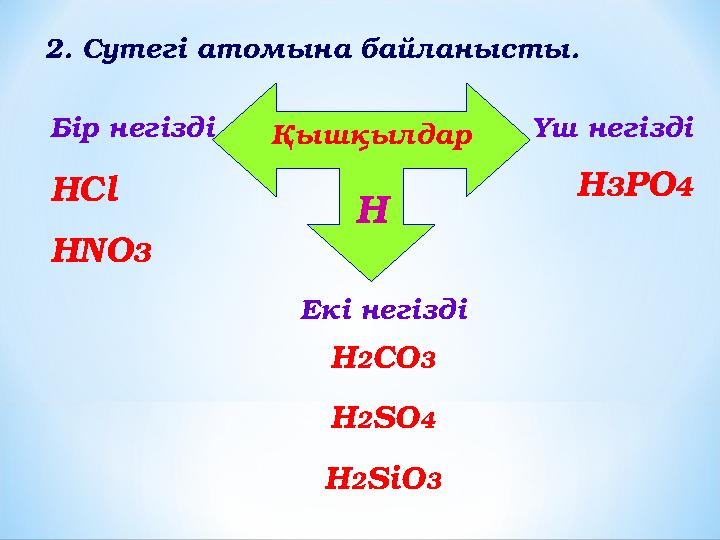
2. Сутегі атомына байланысты.
Қышқылдар
НБір негізді
HCl
HNO 3
Екі негізді Үш негізді
H 3 PO 4
H 2 CO 3
H 2 SO 4
H 2 SiO 3
5 слайд
2. Сутегі атомына байланысты. Қышқылдар НБір негізді HCl HNO 3 Екі негізді Үш негізді H 3 PO 4 H 2 CO 3 H 2 SO 4 H 2 SiO 3
#6 слайд
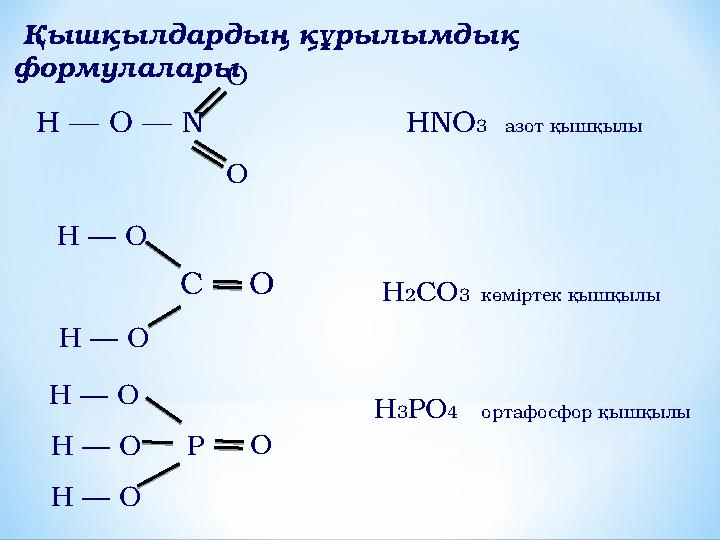
Қышқылдардың құрылымдық
формулалары
O
Н ─ О ─ N HNO 3 азот қышқылы
O
Н ─ О
Н ─ О C O
H 2 CO 3 көміртек қышқылы
Н ─ О
Н ─ О
Н ─ О P O H 3 PO 4 ортафосфор қышқылы
6 слайд
Қышқылдардың құрылымдық формулалары O Н ─ О ─ N HNO 3 азот қышқылы O Н ─ О Н ─ О C O H 2 CO 3 көміртек қышқылы Н ─ О Н ─ О Н ─ О P O H 3 PO 4 ортафосфор қышқылы
#7 слайд
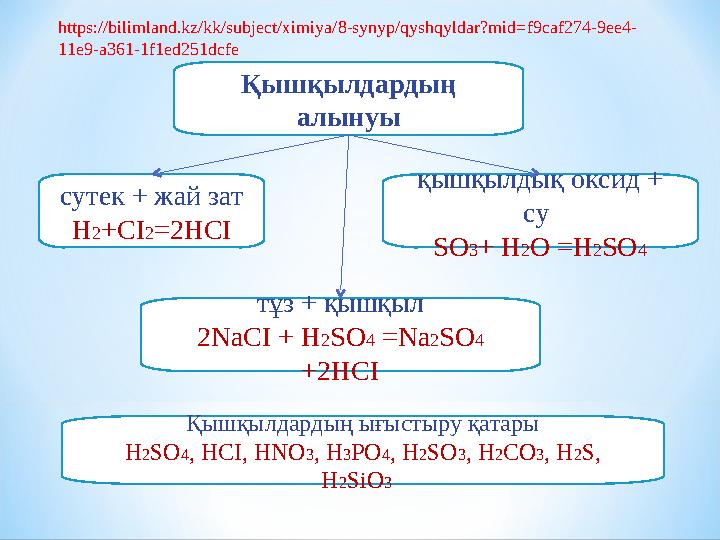
Қышқылдардың
алынуы
c утек + жай зат
Н 2 +СІ 2 =2HCI
тұз + қышқыл
2Na СІ + H 2 SO 4 =Na 2 SO 4
+2HCI қышқылдық оксид +
су
SO 3 + H 2 O = Н 2 SO 4
Қышқылдардың ығыстыру қатары
H 2 SO 4 , HCI , HNO 3 , H 3 PO 4 , H 2 SO 3 , H 2 CO 3 , H 2 S,
H 2 SiO 3 https://bilimland.kz/kk/subject/ximiya/8-synyp/qyshqyldar?mid=f9caf274-9ee4-
11e9-a361-1f1ed251dcfe
7 слайд
Қышқылдардың алынуы c утек + жай зат Н 2 +СІ 2 =2HCI тұз + қышқыл 2Na СІ + H 2 SO 4 =Na 2 SO 4 +2HCI қышқылдық оксид + су SO 3 + H 2 O = Н 2 SO 4 Қышқылдардың ығыстыру қатары H 2 SO 4 , HCI , HNO 3 , H 3 PO 4 , H 2 SO 3 , H 2 CO 3 , H 2 S, H 2 SiO 3 https://bilimland.kz/kk/subject/ximiya/8-synyp/qyshqyldar?mid=f9caf274-9ee4- 11e9-a361-1f1ed251dcfe
#8 слайд
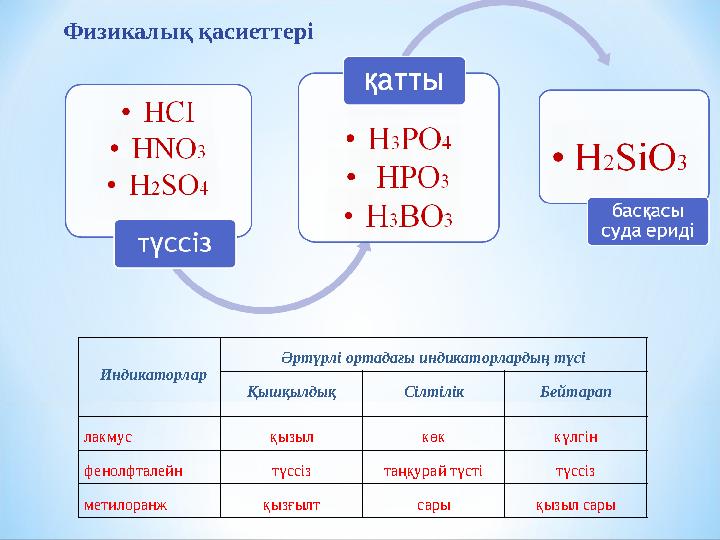
Физикалық қасиеттері
Индикаторлар Әртүрлі ортадағы индикаторлардың түсі
Қышқылдық Сілтілік Бейтарап
лакмус қызыл көк күлгін
фенолфталейн түссіз таңқурай түсті түссіз
метилоранж қызғылт сары қызыл сары
8 слайд
Физикалық қасиеттері Индикаторлар Әртүрлі ортадағы индикаторлардың түсі Қышқылдық Сілтілік Бейтарап лакмус қызыл көк күлгін фенолфталейн түссіз таңқурай түсті түссіз метилоранж қызғылт сары қызыл сары
#9 слайд
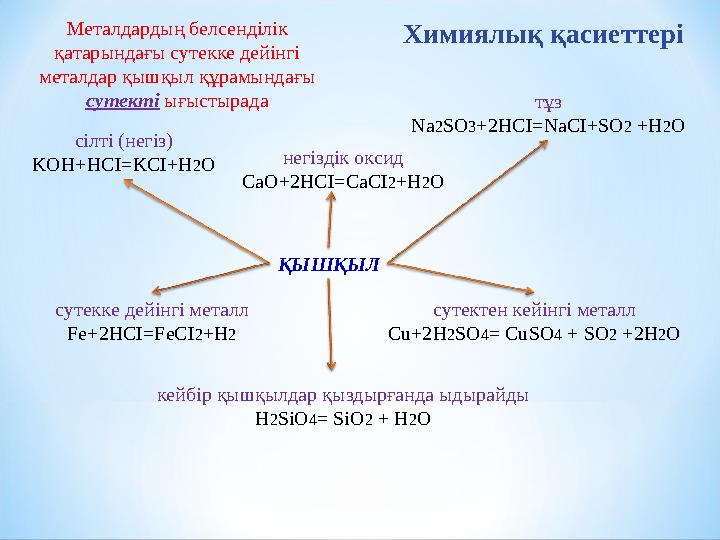
Химиялық қасиеттері
ҚЫШҚЫЛ
сутекке дейінгі металл
Fe+2HCI=FeCI 2 +H 2 сутек т ен кейінгі металл
С u+2H 2 SO 4 = CuSO 4 + SO 2 +2H 2 Oсі лт і (негіз)
KOH+HCI=KCI+H 2 O негіздік оксид
CaO+2HCI=CaCI 2 +H 2 O тұз
Na 2 SO 3 +2HCI=NaCI+SO 2 +H 2 O
кейбір қышқылдар қыздырғанда ыдырайды
H 2 SiO 4 = SiO 2 + H 2 OМеталдардың белсенділік
қатарындағы сутекке дейінгі
металдар қышқыл құрамындағы
сутекті ығыстырада
9 слайд
Химиялық қасиеттері ҚЫШҚЫЛ сутекке дейінгі металл Fe+2HCI=FeCI 2 +H 2 сутек т ен кейінгі металл С u+2H 2 SO 4 = CuSO 4 + SO 2 +2H 2 Oсі лт і (негіз) KOH+HCI=KCI+H 2 O негіздік оксид CaO+2HCI=CaCI 2 +H 2 O тұз Na 2 SO 3 +2HCI=NaCI+SO 2 +H 2 O кейбір қышқылдар қыздырғанда ыдырайды H 2 SiO 4 = SiO 2 + H 2 OМеталдардың белсенділік қатарындағы сутекке дейінгі металдар қышқыл құрамындағы сутекті ығыстырада

#10 слайд
БЕКІТУ
1. Қышқылдар дегеніміз не?
2. Қышқылдарды қалай жіктейміз?
3. Қышқылдарды алудың қандай әдістері бар?
4. Қышқылдарға қандай химиялық қасиеттер тән?
10 слайд
БЕКІТУ 1. Қышқылдар дегеніміз не? 2. Қышқылдарды қалай жіктейміз? 3. Қышқылдарды алудың қандай әдістері бар? 4. Қышқылдарға қандай химиялық қасиеттер тән?
#11 слайд
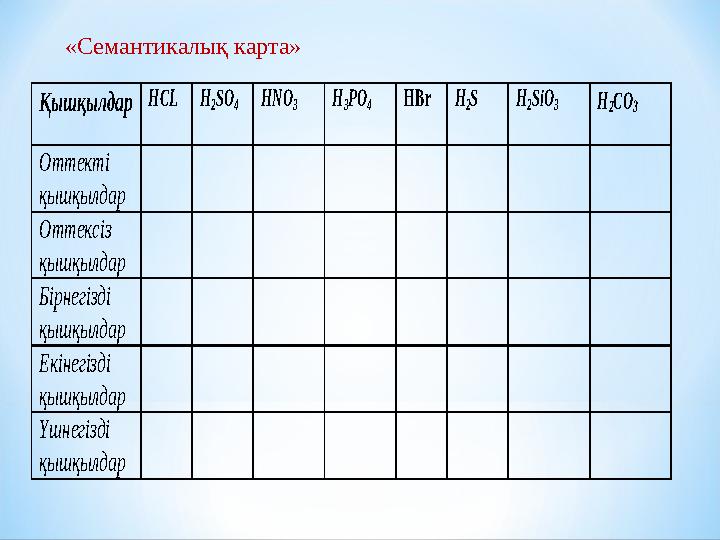
« Семантикалық карта» Қышқылдар HCL H 2SO 4 HNO 3 H 3PO 4 H Br Н 2S H 2SіO 3 Н 2СО 3
Оттекті
қышқылдар
Оттексіз
қышқылдар
Бірнегізді
қышқылдар
Екі негізді
қышқылдар
Үш негізді
қышқылдар
11 слайд
« Семантикалық карта» Қышқылдар HCL H 2SO 4 HNO 3 H 3PO 4 H Br Н 2S H 2SіO 3 Н 2СО 3 Оттекті қышқылдар Оттексіз қышқылдар Бірнегізді қышқылдар Екі негізді қышқылдар Үш негізді қышқылдар

#12 слайд
Шешуі:
m(Ғе)=2,8г
Т/к: V ( H 2 )=? Берілгені:
Fe + 2НСІ = Fe СІ 2 + Н 2 12,6 г
2 2,4 л 56 г х л
2,8 г
56 г х л
22,4 л
22,4 л:
Х = 2,8 г *
56 г = 1,12 л
Жауабы: V ( H 2 )=1,12 л КітаппенКітаппен
жұмыс жұмыс
163 бет №3
12 слайд
Шешуі: m(Ғе)=2,8г Т/к: V ( H 2 )=? Берілгені: Fe + 2НСІ = Fe СІ 2 + Н 2 12,6 г 2 2,4 л 56 г х л 2,8 г 56 г х л 22,4 л 22,4 л: Х = 2,8 г * 56 г = 1,12 л Жауабы: V ( H 2 )=1,12 л КітаппенКітаппен жұмыс жұмыс 163 бет №3

#13 слайд
Үйге тапсырма
§ 44-45 оқу
№ 1 және №2 есеп 163 бет
13 слайд
Үйге тапсырма § 44-45 оқу № 1 және №2 есеп 163 бет

#14 слайд
Кері байланыс
14 слайд
Кері байланыс

шағым қалдыра аласыз
















