Семинар. Сабақ


#1 слайд
№17 М.Ю.Лермонтов атындағы жалпы орта
мектептің химия пәнінің мұғалімі
Пердебаев Ө.С.
Тақырыбы: Жаңа форматтағы
тест тапсырмаларын талдауға
оқушыларды дайындау
1 слайд
№17 М.Ю.Лермонтов атындағы жалпы орта мектептің химия пәнінің мұғалімі Пердебаев Ө.С. Тақырыбы: Жаңа форматтағы тест тапсырмаларын талдауға оқушыларды дайындау

#2 слайд
Жалпы білімді бағалаудың тесттік
жүйесі Англия, АҚШ-та жақсы дамыған.
Елімізде соңғы жылдары білімді
бағалаудың тесттік жүйесі енгізілді.
Бүгінде тест қолдану оқытушылармен
қатар оқушылар үшін де көп тиімді екенін
өмірдің өзі дәлелдеп отыр. Тестілеуде
нәтиже тікелей белгілі болады.
2 слайд
Жалпы білімді бағалаудың тесттік жүйесі Англия, АҚШ-та жақсы дамыған. Елімізде соңғы жылдары білімді бағалаудың тесттік жүйесі енгізілді. Бүгінде тест қолдану оқытушылармен қатар оқушылар үшін де көп тиімді екенін өмірдің өзі дәлелдеп отыр. Тестілеуде нәтиже тікелей белгілі болады.
#3 слайд
білім беру жағдайын талдауына қажет
оқытудың объективті нәтижесін алу
мүмкіндігі (адамның қатысуынсыз алу)
кері байланыстың жылдамдығы, оқытудың
нәтижесін тексеру әдісінің көптүрлілігі
оқытудың нәтижесінің статистикасын
алу ыңғайлылығы
Тест технологиясының білім
сапасына әсері:
3 слайд
білім беру жағдайын талдауына қажет оқытудың объективті нәтижесін алу мүмкіндігі (адамның қатысуынсыз алу) кері байланыстың жылдамдығы, оқытудың нәтижесін тексеру әдісінің көптүрлілігі оқытудың нәтижесінің статистикасын алу ыңғайлылығы Тест технологиясының білім сапасына әсері:
#4 слайд
Берілетін сұрақтары
және тапсырмалары
нақты
жеткілікті анық
және түсінікті
ой тұжырымын
жасауға ыңғайлы
Тестке қойылатын талаптар
4 слайд
Берілетін сұрақтары және тапсырмалары нақты жеткілікті анық және түсінікті ой тұжырымын жасауға ыңғайлы Тестке қойылатын талаптар

#5 слайд
Тестілеудің артықшылықтары
1
•тест тапсырмаларын орындауға аз уақыт кетеді, мұғалімнің де,
оқушылардың да уақыты үнемделеді.
2
•әр оқушыға жеке тапсырма берілетіндіктен көшіріп алу мүмкіндіктері
болмайды.
3
•тест тек білімді тексеріп қана қоймай, оқыту функциясын
атқаратындықтан әр бір тестілеуден кейін оқушы білімі терендей түседі.
4
•тестілеу сапалы және объективті бағалау әдісі болып табылады
5
•Тестілеу арқылы білім алушының курстың барлық тақырыптарын қалай
меңгергенін байқап жалпы пәнді немесе бөлек тақырыптарды қалай
меңгергенін анықтауға болады.
5 слайд
Тестілеудің артықшылықтары 1 •тест тапсырмаларын орындауға аз уақыт кетеді, мұғалімнің де, оқушылардың да уақыты үнемделеді. 2 •әр оқушыға жеке тапсырма берілетіндіктен көшіріп алу мүмкіндіктері болмайды. 3 •тест тек білімді тексеріп қана қоймай, оқыту функциясын атқаратындықтан әр бір тестілеуден кейін оқушы білімі терендей түседі. 4 •тестілеу сапалы және объективті бағалау әдісі болып табылады 5 •Тестілеу арқылы білім алушының курстың барлық тақырыптарын қалай меңгергенін байқап жалпы пәнді немесе бөлек тақырыптарды қалай меңгергенін анықтауға болады.

#6 слайд
Тестілеу формалары
бір дұрыс жауапты таңдауды қажет ететін
тапсырмалар
бірнеше дұрыс жауапты таңдауды қажет
ететін тапсырмалар
сәйкестікті құру бойынша
тапсырмалар, жауапты тіркеуді талап ететін
тапсырмалар (жауапты толықтырып жазу)
логикалық және алгоритмдік реттілікті құру
бойынша тапсырмалар.
6 слайд
Тестілеу формалары бір дұрыс жауапты таңдауды қажет ететін тапсырмалар бірнеше дұрыс жауапты таңдауды қажет ететін тапсырмалар сәйкестікті құру бойынша тапсырмалар, жауапты тіркеуді талап ететін тапсырмалар (жауапты толықтырып жазу) логикалық және алгоритмдік реттілікті құру бойынша тапсырмалар.
#7 слайд
Бірнеше дұрыс жауапты таңдауды қажет
ететін тапсырмалардың қолданылу аясы
ҰБТ
Ұлттық бірыңғай тесттілеу
ОБ ОЖСБ
Орта білімдегі оқу
жетістіктерін сырттай
бағалау
7 слайд
Бірнеше дұрыс жауапты таңдауды қажет ететін тапсырмалардың қолданылу аясы ҰБТ Ұлттық бірыңғай тесттілеу ОБ ОЖСБ Орта білімдегі оқу жетістіктерін сырттай бағалау

#8 слайд
Бір немесе бірнеше дұрыс жауабы бар
тапсырмаларды бағалау
Бір дұрыс жауабы бар тест тапсырмасы – әрбір
дұрыс жауап үшін 1 бвлл
Екі немесе үш дұрыс жауабы бар тест тапсырмасы
– дұрыс жауаптың бәрін таңдағанда 2 балл
Бір қате жіберілсе (дұрыс жауаптың біреуі
табылмаса немесе 1 дұрыс емес жауап таңдалса) 1
бвлл, екі немесе одан да көп қате 0 бвлл
8 слайд
Бір немесе бірнеше дұрыс жауабы бар тапсырмаларды бағалау Бір дұрыс жауабы бар тест тапсырмасы – әрбір дұрыс жауап үшін 1 бвлл Екі немесе үш дұрыс жауабы бар тест тапсырмасы – дұрыс жауаптың бәрін таңдағанда 2 балл Бір қате жіберілсе (дұрыс жауаптың біреуі табылмаса немесе 1 дұрыс емес жауап таңдалса) 1 бвлл, екі немесе одан да көп қате 0 бвлл

#9 слайд
Бейорганикалық
қосылыстардың негізгі
кластары
9 слайд
Бейорганикалық қосылыстардың негізгі кластары
#10 слайд
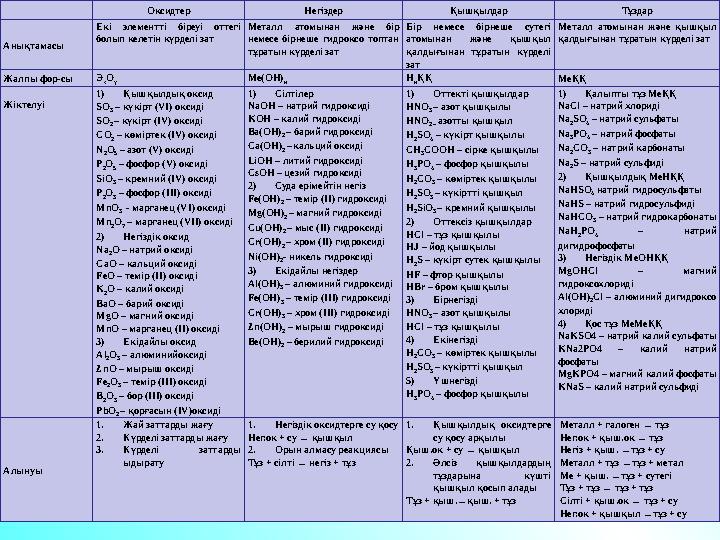
Оксидтер Негіздер Қышқылдар Тұздар
Анықтамасы
Екі элементті біреуі оттегі
болып келетін күрделі зат
Металл атомынан және бір
немесе бірнеше гидроксо топтан
тұратын күрделі зат
Бір немесе бірнеше сутегі
атомынан және қышқыл
қалдығынан тұратын күрделі
зат
Металл атомынан және қышқыл
қалдығынан тұратын күрделі зат
Жалпы фор-сы Э
х
О
у
Ме(ОН)
н
Н
н
ҚҚ МеҚҚ
Жіктелуі
1)Қышқылдық оксид
SO
3 – күкірт (VІ) оксиді
SO
2 – күкірт (ІV) оксиді
CO
2 – көміртек (ІV) оксиді
N
2O
5 – азот (V) оксиді
P
2O
5 – фосфор (V) оксиді
SiO
3 – кремний (ІV) оксиді
P
2O
3 – фосфор (ІІІ) оксиді
MnO
3 - марганец (VI) оксиді
Mn
2O
7 – марганец (VII) оксиді
2)Негіздік оксид
Na
2O – натрий оксиді
CaO – кальций оксиді
FeO – темір (ІІ) оксиді
K
2O – калий оксиді
BaO – барий оксиді
MgO – магний оксиді
MnO – марганец (ІІ) оксиді
3)Екідайлы оксид
Al
2O
3 – алюминийоксиді
ZnO – мырыш оксиді
Fe
2O
3 – темір (ІІІ) оксиді
B
2O
3 – бор (ІІІ) оксиді
PbO
2 – қорғасын (ІV)оксиді
1)Сілтілер
NaOH – натрий гидроксиді
KOH – калий гидроксиді
Ba(OH)
2 – барий гидроксиді
Ca(OH)
2 –
кальций оксиді
LiOH – литий гидроксиді
CsOH – цезий гидроксиді
2)Суда ерімейтін негіз
Fe(OH)
2 – темір (ІІ) гидроксиді
Mg(OH)
2 – магний гидроксиді
Cu(OH)
2 – мыс (ІІ) гидроксиді
Cr(OH)
2 – хром (ІІ) гидроксиді
Ni(OH)
2- никель гидроксиді
3)Екідайлы негіздер
Al(OH)
3 – алюминий гидроксиді
Fe(OH)
3 – темір (ІІІ) гидроксиді
Cr(OH)
3 – хром (ІІІ) гидроксиді
Zn(OH)
2 – мырыш гидроксиді
Be(OH)
2 – берилий гидроксиді
1)Оттекті қышқылдар
HNO
3 – азот қышқылы
HNO
2 – азотты қышқыл
H
2SO
4 – күкірт қышқылы
CH
3COOH – сірке қышқылы
H
3PO
4 – фосфор қышқылы
H
2CO
3 – көміртек қышқылы
H
2SO
3 – күкіртті қышқыл
H
2SiO
3 – кремний қышқылы
2)Оттексіз қышқылдар
HCl – тұз қышқылы
HJ – йод қышқылы
H
2S – күкірт сутек қышқылы
HF – фтор қышқылы
HBr – бром қышқылы
3)Бірнегізді
HNO
3 – азот қышқылы
HCl – тұз қышқылы
4)Екінегізді
H
2CO
3 – көміртек қышқылы
H
2SO
3 – күкіртті қышқыл
5)Үшнегізді
H
3PO
4 – фосфор қышқылы
1)Қалыпты тұз МеҚҚ
NaCl – натрий хлориді
Na
2SO
4 – натрий сульфаты
Na
3PO
4 – натрий фосфаты
Na
2CO
3 – натрий карбонаты
Na
2S – натрий сульфиді
2)Қышқылдық МеНҚҚ
NaHSO
4 натрий гидросульфаты
NaHS – натрий гидросульфиді
NaHСO
3 – натрий гидрокарбонаты
NaH
2PO
4 – натрий
дигидрофосфаты
3)Негіздік МеОНҚҚ
MgOHCl – магний
гидроксохлориді
Al(OH)
2Cl – алюминий дигидроксо
хлориді
4)Қос тұз МеМеҚҚ
NaKSO4 – натрий калий сульфаты
KNa2PO4 – калий натрий
фосфаты
MgKPO4 – магний калий фосфаты
KNaS – калий натрий сульфиді
Алынуы
1.Жай заттарды жағу
2.Күрделі заттарды жағу
3.Күрделі заттарды
ыдырату
1.Негіздік оксидтерге су қосу
Нег.ок + су → қышқыл
2.Орын алмасу реакциясы
Тұз + сілті → негіз + тұз
1.Қышқылдық оксидтерге
су қосу арқылы
Қыш.ок + су → қышқыл
2.Әлсіз қышқылдардың
тұздарына күшті
қышқыл қосып алады
Тұз + қыш.→қыш. + тұз
Металл + галоген → тұз
Нег.ок + қыш.ок → тұз
Негіз + қыш. →тұз + су
Металл + тұз →тұз + метал
Ме + қыш. →тұз + сутегі
Тұз + тұз → тұз + тұз
Сілті + қыш.ок → тұз + су
Нег.ок + қышқыл →тұз + су
10 слайд
Оксидтер Негіздер Қышқылдар Тұздар Анықтамасы Екі элементті біреуі оттегі болып келетін күрделі зат Металл атомынан және бір немесе бірнеше гидроксо топтан тұратын күрделі зат Бір немесе бірнеше сутегі атомынан және қышқыл қалдығынан тұратын күрделі зат Металл атомынан және қышқыл қалдығынан тұратын күрделі зат Жалпы фор-сы Э х О у Ме(ОН) н Н н ҚҚ МеҚҚ Жіктелуі 1)Қышқылдық оксид SO 3 – күкірт (VІ) оксиді SO 2 – күкірт (ІV) оксиді CO 2 – көміртек (ІV) оксиді N 2O 5 – азот (V) оксиді P 2O 5 – фосфор (V) оксиді SiO 3 – кремний (ІV) оксиді P 2O 3 – фосфор (ІІІ) оксиді MnO 3 - марганец (VI) оксиді Mn 2O 7 – марганец (VII) оксиді 2)Негіздік оксид Na 2O – натрий оксиді CaO – кальций оксиді FeO – темір (ІІ) оксиді K 2O – калий оксиді BaO – барий оксиді MgO – магний оксиді MnO – марганец (ІІ) оксиді 3)Екідайлы оксид Al 2O 3 – алюминийоксиді ZnO – мырыш оксиді Fe 2O 3 – темір (ІІІ) оксиді B 2O 3 – бор (ІІІ) оксиді PbO 2 – қорғасын (ІV)оксиді 1)Сілтілер NaOH – натрий гидроксиді KOH – калий гидроксиді Ba(OH) 2 – барий гидроксиді Ca(OH) 2 – кальций оксиді LiOH – литий гидроксиді CsOH – цезий гидроксиді 2)Суда ерімейтін негіз Fe(OH) 2 – темір (ІІ) гидроксиді Mg(OH) 2 – магний гидроксиді Cu(OH) 2 – мыс (ІІ) гидроксиді Cr(OH) 2 – хром (ІІ) гидроксиді Ni(OH) 2- никель гидроксиді 3)Екідайлы негіздер Al(OH) 3 – алюминий гидроксиді Fe(OH) 3 – темір (ІІІ) гидроксиді Cr(OH) 3 – хром (ІІІ) гидроксиді Zn(OH) 2 – мырыш гидроксиді Be(OH) 2 – берилий гидроксиді 1)Оттекті қышқылдар HNO 3 – азот қышқылы HNO 2 – азотты қышқыл H 2SO 4 – күкірт қышқылы CH 3COOH – сірке қышқылы H 3PO 4 – фосфор қышқылы H 2CO 3 – көміртек қышқылы H 2SO 3 – күкіртті қышқыл H 2SiO 3 – кремний қышқылы 2)Оттексіз қышқылдар HCl – тұз қышқылы HJ – йод қышқылы H 2S – күкірт сутек қышқылы HF – фтор қышқылы HBr – бром қышқылы 3)Бірнегізді HNO 3 – азот қышқылы HCl – тұз қышқылы 4)Екінегізді H 2CO 3 – көміртек қышқылы H 2SO 3 – күкіртті қышқыл 5)Үшнегізді H 3PO 4 – фосфор қышқылы 1)Қалыпты тұз МеҚҚ NaCl – натрий хлориді Na 2SO 4 – натрий сульфаты Na 3PO 4 – натрий фосфаты Na 2CO 3 – натрий карбонаты Na 2S – натрий сульфиді 2)Қышқылдық МеНҚҚ NaHSO 4 натрий гидросульфаты NaHS – натрий гидросульфиді NaHСO 3 – натрий гидрокарбонаты NaH 2PO 4 – натрий дигидрофосфаты 3)Негіздік МеОНҚҚ MgOHCl – магний гидроксохлориді Al(OH) 2Cl – алюминий дигидроксо хлориді 4)Қос тұз МеМеҚҚ NaKSO4 – натрий калий сульфаты KNa2PO4 – калий натрий фосфаты MgKPO4 – магний калий фосфаты KNaS – калий натрий сульфиді Алынуы 1.Жай заттарды жағу 2.Күрделі заттарды жағу 3.Күрделі заттарды ыдырату 1.Негіздік оксидтерге су қосу Нег.ок + су → қышқыл 2.Орын алмасу реакциясы Тұз + сілті → негіз + тұз 1.Қышқылдық оксидтерге су қосу арқылы Қыш.ок + су → қышқыл 2.Әлсіз қышқылдардың тұздарына күшті қышқыл қосып алады Тұз + қыш.→қыш. + тұз Металл + галоген → тұз Нег.ок + қыш.ок → тұз Негіз + қыш. →тұз + су Металл + тұз →тұз + метал Ме + қыш. →тұз + сутегі Тұз + тұз → тұз + тұз Сілті + қыш.ок → тұз + су Нег.ок + қышқыл →тұз + су

#11 слайд
№Химиялық
формуласы
Аталуы Жіктелуі Химиялық
байланыстың
типтері
Тотығу
дәрежесі
Құрылым
дық
формулас
ы
Сигма пи
байланыс
саны
1HNO3 Азот
қышқылы
Бірнегізді
оттекті
қышқыл
Иондық
ковалентті
полюсті
H-O-N˭О
=O
4 сигма
2 пи
Төмендегі Mn
2
O
7
, SO
3
, K
2
O, KNO
3
, Mg(OH)
2
, Ca(NO
3
)
2
, Fe
2
O
3
, Al
2
O
3
, AlOHCl
2
,
Ba(OH)
2
, CaO, CO
2
, P
2
O
5
, H
3
PO
4
, H
2
S, H
2
SO
4
, K
2
CO
3
, NaHCO
3
, MgOHNO
3
,
KH
2
PO
4
, KNaSO
4
, CrO, HNO
3
, HBr, NaOH, AgNO
3
, Fe
2
(SO
4
)
3
, SiO
2
, Ca
3
(PO
4
)
2
,
H
2
CO
3
, Cl
2
O
5
, BaSO
4
, ZnO, CuSO
4
, Cu(OH)
2
, Fe(OH)
3
, Al(OH)
2
Cl, Ca(HCO
3
)
2
заттардың
11 слайд
№Химиялық формуласы Аталуы Жіктелуі Химиялық байланыстың типтері Тотығу дәрежесі Құрылым дық формулас ы Сигма пи байланыс саны 1HNO3 Азот қышқылы Бірнегізді оттекті қышқыл Иондық ковалентті полюсті H-O-N˭О =O 4 сигма 2 пи Төмендегі Mn 2 O 7 , SO 3 , K 2 O, KNO 3 , Mg(OH) 2 , Ca(NO 3 ) 2 , Fe 2 O 3 , Al 2 O 3 , AlOHCl 2 , Ba(OH) 2 , CaO, CO 2 , P 2 O 5 , H 3 PO 4 , H 2 S, H 2 SO 4 , K 2 CO 3 , NaHCO 3 , MgOHNO 3 , KH 2 PO 4 , KNaSO 4 , CrO, HNO 3 , HBr, NaOH, AgNO 3 , Fe 2 (SO 4 ) 3 , SiO 2 , Ca 3 (PO 4 ) 2 , H 2 CO 3 , Cl 2 O 5 , BaSO 4 , ZnO, CuSO 4 , Cu(OH) 2 , Fe(OH) 3 , Al(OH) 2 Cl, Ca(HCO 3 ) 2 заттардың

#12 слайд
Келтірілген заттардың ішінде негіздік
гидроксидтерді табыңыз
A.Zn(OH)
2
B.Al(OH)
3
C.Ca(OH)
2
D.Cr(OH)
3 3 дұрыс жауапқа 2 балл
E.H
3
PO
4
F.Cr(OH)
2
G.H
2SO
4
H.Cu(OH)
2
12 слайд
Келтірілген заттардың ішінде негіздік гидроксидтерді табыңыз A.Zn(OH) 2 B.Al(OH) 3 C.Ca(OH) 2 D.Cr(OH) 3 3 дұрыс жауапқа 2 балл E.H 3 PO 4 F.Cr(OH) 2 G.H 2SO 4 H.Cu(OH) 2

#13 слайд
Келтірілген заттардың ішінде негіздік
гидроксидтерді табыңыз
A.Zn(OH)
2
B.Al(OH)
3
C.Ca(OH)
2
D.Cr(OH)
3 2 дұрыс жауапқа 1 балл
E.H
3
PO
4
F.Cr(OH)
2
G.H
2
SO
4
H.Cu(OH)
2
13 слайд
Келтірілген заттардың ішінде негіздік гидроксидтерді табыңыз A.Zn(OH) 2 B.Al(OH) 3 C.Ca(OH) 2 D.Cr(OH) 3 2 дұрыс жауапқа 1 балл E.H 3 PO 4 F.Cr(OH) 2 G.H 2 SO 4 H.Cu(OH) 2

#14 слайд
Бейорганикалық
қосылыстар арасындағы
генетикалық байланыс
14 слайд
Бейорганикалық қосылыстар арасындағы генетикалық байланыс

#15 слайд
15 слайд

#16 слайд
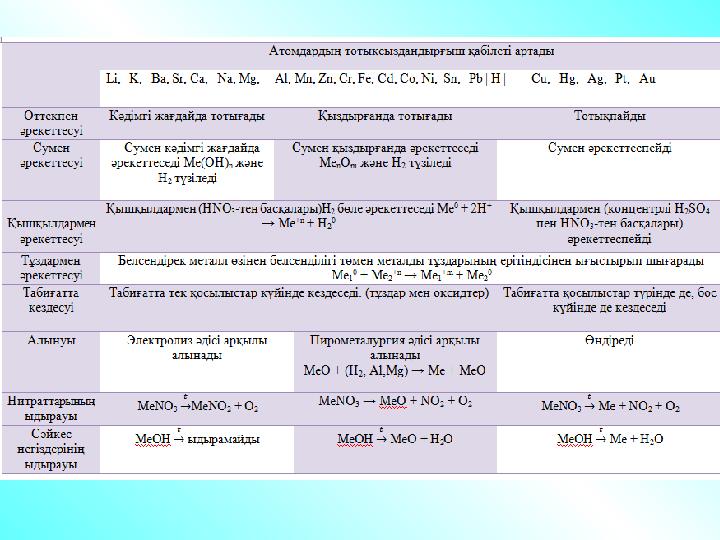
*1 Қышқылдармен (HNO
3
-тен басқалары)Н
2
бөле әрекеттеседі
*2 Белсендірек металл өзінен белсенділігі төмен металды
тұздарының ерітіндісінен ығыстырып шығарады
*3 Сумен кәдімгі жағдайда әрекеттеседі Ме(ОН)
n
және H
2
түзіледі
(Li, K, Ba, Sr, Ca, Na, Mg), Сумен қыздырғанда әрекеттеседі
Ме
n
О
m
және Н
2
түзіледі (Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb),
Сумен әрекеттеспейді (Cu, Hg, Ag, Pt, Au)
*4 Сілтімен тек галогендер әрекеттесе алады
*5 Тұздың құрамындағы қышқыл қалдығына байланысты
*6 Суда еритін тұздар әркеттеседі
*7 Суда жақсы еритін (Cl), Суда нашар еритін (P, H, I), суда
ерімейтін (С, Si, S, N)
16 слайд
*1 Қышқылдармен (HNO 3 -тен басқалары)Н 2 бөле әрекеттеседі *2 Белсендірек металл өзінен белсенділігі төмен металды тұздарының ерітіндісінен ығыстырып шығарады *3 Сумен кәдімгі жағдайда әрекеттеседі Ме(ОН) n және H 2 түзіледі (Li, K, Ba, Sr, Ca, Na, Mg), Сумен қыздырғанда әрекеттеседі Ме n О m және Н 2 түзіледі (Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb), Сумен әрекеттеспейді (Cu, Hg, Ag, Pt, Au) *4 Сілтімен тек галогендер әрекеттесе алады *5 Тұздың құрамындағы қышқыл қалдығына байланысты *6 Суда еритін тұздар әркеттеседі *7 Суда жақсы еритін (Cl), Суда нашар еритін (P, H, I), суда ерімейтін (С, Si, S, N)

#17 слайд
Іс жүзінде жүзеге аспайтын
реакцияларды көрсетіңіз
A.H
2
SO
4(конц)
+ Cu →
B.S + Al →
C.H
2SO
4 + BaCl
2 → 2-де дұрыс 2 балл
D.H
2SO
4 (сұй.) + Cu →
E.H
2S + NaOH→
F.NaCl
(крист) + H
2SO
4
(конц) →
G.NaCl
(еріт) + H
2SO
4 (сұй) →
H.Na + H
2O →
17 слайд
Іс жүзінде жүзеге аспайтын реакцияларды көрсетіңіз A.H 2 SO 4(конц) + Cu → B.S + Al → C.H 2SO 4 + BaCl 2 → 2-де дұрыс 2 балл D.H 2SO 4 (сұй.) + Cu → E.H 2S + NaOH→ F.NaCl (крист) + H 2SO 4 (конц) → G.NaCl (еріт) + H 2SO 4 (сұй) → H.Na + H 2O →

#18 слайд
Іс жүзінде жүзеге аспайтын
реакцияларды көрсетіңіз
A.H
2
SO
4(конц)
+ Cu →
B.S + Al →
C.H
2SO
4 + BaCl
2 →
D.H
2SO
4 (сұй.) + Cu → 1 жауабы дұрыс 1 балл
E.H
2S + NaOH→
F.NaCl
(крист) + H
2SO
4
(конц) →
G.NaCl
(еріт) + H
2SO
4 (сұй) →
H.Na + H
2O →
18 слайд
Іс жүзінде жүзеге аспайтын реакцияларды көрсетіңіз A.H 2 SO 4(конц) + Cu → B.S + Al → C.H 2SO 4 + BaCl 2 → D.H 2SO 4 (сұй.) + Cu → 1 жауабы дұрыс 1 балл E.H 2S + NaOH→ F.NaCl (крист) + H 2SO 4 (конц) → G.NaCl (еріт) + H 2SO 4 (сұй) → H.Na + H 2O →

#19 слайд
Металдардың химиялық
қасиеттері
19 слайд
Металдардың химиялық қасиеттері
#20 слайд
20 слайд

#21 слайд
Реакция теңдеуін аяқта
NaOH
Fe + AgCl
Zn + H
2O
Na + HNO
3
Al + H
2O
Mg + HCl
Fe(OH)
3
Hg(NO
3) + Cu
Ag + O
2
Na + O
2
KNO
3
Cu(NO
3) →
21 слайд
Реакция теңдеуін аяқта NaOH Fe + AgCl Zn + H 2O Na + HNO 3 Al + H 2O Mg + HCl Fe(OH) 3 Hg(NO 3) + Cu Ag + O 2 Na + O 2 KNO 3 Cu(NO 3) →

#22 слайд
1)ІІІ А топ
элементтеріне B, Al,
Ga, Ln, Tl
2)ІІІ А топ элементтерін
р-элемент деп атайды
3)ІІІ А топ
элементтерінің
электрондық
конфигурациясы
«ns
2
np
1
»
4)Тотығу дәрежелері +3
болады
5)Топ бойынша
жоғарыдан төмен
қарай металдық
қасиеті артады.
6) Қосылыстарының
қасиеттері
қышқылдық (В)
eкідайлы (Al, Ga, Ln)
негіздікке
(Tl)ауысады.
7) Топ бойынша
жоғарыдан төмен
қарай атом радиусы
металдық қасиеті
артып, иондану
энергиясы кемиді.
1)Периодтық жүйедегі орны: 3 периодта, ІІІ А топ орналасқан екідайлы элемент.
2)Валенттілігі тұрақты ІІІ-ке тең
3)Қосылыстардағы тотығу дәрежесі: +3
4)Табиғаттағы қосылыстары: боксид Al
2O
3*nH
2O, Каолин Al
2O
3*2SiO
2*2H
2O, нефелин Na
2O, Al
2O
3*2SiO2, және
алунит K
2SO
4*Al
2(SO
4)
3*2Al
2O
3*6H
2O
5)Өндірісте электролиз әдісі арқылы алынады.
2Al
2O
3 4Al + 3O
2
6)Күмістей ақ түсті, жылтыр жеңіл, электрді жақсы өткізетін, майысқақ 160 балқитын коррозияға төзімді металл
7)Жай заттармен
I
2 →
Cl
2 →
Al + N
2
S →
C →
8)Күрделі заттармен
Al + HOH → Al(OH)
3
+ 3H
2
9)Алюминийдің сұйытылған қышқылдармен әркеттесуі.
Al + H
2
SO
4
→ Al
2
(SO
4
)
3
+ H
2
10)Алюминийдің екідайлы қысылыстардың негізздерімен әркеттесуі
2Al + 6NaOH + 6H
2
O → 2Na
3
[Al(OH)
6
] + 3H
2
O
11)Мателл оксидтерімен әрекеттесуі
Al + Fe
2
O
3
→ Fe + Al
2
O
3
12)Алюминий концентрлі HNO3, H2SO4 пен әрекеттеспейдң. Пассивтелу процесі жүреді.
13)Алюминийдің маңызды қосылыстары Al(OH)
3
, AlCl
3
, Al
2
O
3
14)Алюминийді әртүрлі металдар жасауда фольга даярлауда, электр өткізгіш сымдарда, өндірісте кейбір
металлдарды алуға қолданылады.
15)Алюминийдің құймалары силумин деп аталады.
16)Алюминийді сынапқа батырғанда амалгама деп аталатын құйма түзеді.
17)Алюминийдің кең қолданатын тұздары
AlCl
3
– катализатор ретінде
KAl(SO
4)
3 – тері өңдеуде
Al
2(SO
4)
3 – су тазалауда қолданылады
IIІ А топ элементтерінің жалпы сипаттамасы Al – тән қасиеттер
22 слайд
1)ІІІ А топ элементтеріне B, Al, Ga, Ln, Tl 2)ІІІ А топ элементтерін р-элемент деп атайды 3)ІІІ А топ элементтерінің электрондық конфигурациясы «ns 2 np 1 » 4)Тотығу дәрежелері +3 болады 5)Топ бойынша жоғарыдан төмен қарай металдық қасиеті артады. 6) Қосылыстарының қасиеттері қышқылдық (В) eкідайлы (Al, Ga, Ln) негіздікке (Tl)ауысады. 7) Топ бойынша жоғарыдан төмен қарай атом радиусы металдық қасиеті артып, иондану энергиясы кемиді. 1)Периодтық жүйедегі орны: 3 периодта, ІІІ А топ орналасқан екідайлы элемент. 2)Валенттілігі тұрақты ІІІ-ке тең 3)Қосылыстардағы тотығу дәрежесі: +3 4)Табиғаттағы қосылыстары: боксид Al 2O 3*nH 2O, Каолин Al 2O 3*2SiO 2*2H 2O, нефелин Na 2O, Al 2O 3*2SiO2, және алунит K 2SO 4*Al 2(SO 4) 3*2Al 2O 3*6H 2O 5)Өндірісте электролиз әдісі арқылы алынады. 2Al 2O 3 4Al + 3O 2 6)Күмістей ақ түсті, жылтыр жеңіл, электрді жақсы өткізетін, майысқақ 160 балқитын коррозияға төзімді металл 7)Жай заттармен I 2 → Cl 2 → Al + N 2 S → C → 8)Күрделі заттармен Al + HOH → Al(OH) 3 + 3H 2 9)Алюминийдің сұйытылған қышқылдармен әркеттесуі. Al + H 2 SO 4 → Al 2 (SO 4 ) 3 + H 2 10)Алюминийдің екідайлы қысылыстардың негізздерімен әркеттесуі 2Al + 6NaOH + 6H 2 O → 2Na 3 [Al(OH) 6 ] + 3H 2 O 11)Мателл оксидтерімен әрекеттесуі Al + Fe 2 O 3 → Fe + Al 2 O 3 12)Алюминий концентрлі HNO3, H2SO4 пен әрекеттеспейдң. Пассивтелу процесі жүреді. 13)Алюминийдің маңызды қосылыстары Al(OH) 3 , AlCl 3 , Al 2 O 3 14)Алюминийді әртүрлі металдар жасауда фольга даярлауда, электр өткізгіш сымдарда, өндірісте кейбір металлдарды алуға қолданылады. 15)Алюминийдің құймалары силумин деп аталады. 16)Алюминийді сынапқа батырғанда амалгама деп аталатын құйма түзеді. 17)Алюминийдің кең қолданатын тұздары AlCl 3 – катализатор ретінде KAl(SO 4) 3 – тері өңдеуде Al 2(SO 4) 3 – су тазалауда қолданылады IIІ А топ элементтерінің жалпы сипаттамасы Al – тән қасиеттер

#23 слайд
Алюминий жайлы қате тұжырым
A.Электрондық конфигурациясы ns
2
np
1
сәйкес келеді.
B.Өндірісте электролиз әдісі арқылы алынады
C.Табиғатта қосылысы магнетит деп аталады
D.Ядро құрамы 13р 14n тұрады
E.Табиғатта бір ғана изотобы бар
F.Алюминийдің күкіртпен қосылысы сульфат деп аталады
G.AlCl
3
органикалық заттарды синтездеуде катализатор
ретінде қолданылады.
H.Барлық металл оксидтерінен металдарды алуға
қолданады
3 дұрыс жауапқа 2 балл
23 слайд
Алюминий жайлы қате тұжырым A.Электрондық конфигурациясы ns 2 np 1 сәйкес келеді. B.Өндірісте электролиз әдісі арқылы алынады C.Табиғатта қосылысы магнетит деп аталады D.Ядро құрамы 13р 14n тұрады E.Табиғатта бір ғана изотобы бар F.Алюминийдің күкіртпен қосылысы сульфат деп аталады G.AlCl 3 органикалық заттарды синтездеуде катализатор ретінде қолданылады. H.Барлық металл оксидтерінен металдарды алуға қолданады 3 дұрыс жауапқа 2 балл

#24 слайд
Алюминий жайлы қате тұжырым
A.Электрондық конфигурациясы ns
2
np
1
сәйкес келеді.
B.Өндірісте электролиз әдісі арқылы алынады
C.Табиғатта қосылысы магнетит деп аталады
D.Ядро құрамы 13р 14n тұрады
E.Табиғатта бір ғана изотобы бар
F.Алюминийдің күкіртпен қосылысы сульфат деп аталады
G.AlCl
3
органикалық заттарды синтездеуде катализатор
ретінде қолданылады.
H.Барлық металл оксидтерінен металдарды алуға
қолданады
2 дұрыс жауапқа 1 балл
24 слайд
Алюминий жайлы қате тұжырым A.Электрондық конфигурациясы ns 2 np 1 сәйкес келеді. B.Өндірісте электролиз әдісі арқылы алынады C.Табиғатта қосылысы магнетит деп аталады D.Ядро құрамы 13р 14n тұрады E.Табиғатта бір ғана изотобы бар F.Алюминийдің күкіртпен қосылысы сульфат деп аталады G.AlCl 3 органикалық заттарды синтездеуде катализатор ретінде қолданылады. H.Барлық металл оксидтерінен металдарды алуға қолданады 2 дұрыс жауапқа 1 балл

#25 слайд
1)V А топ элементтерге N,P,Bi,As,Sb
жатады
2)Жалпы электрондық
конфигурациясы ... ns
2
np
3
3) Тотығу дәрежесі +3, +5 азоттан
басқасы
4)Физикалық қасиеттері бойынша N-газ
қалғандары қатты заттар
5)Сутектік қосылыстың жалпы
формуласы RH3 жоғарыдан төмен
қарай
тұрақтылығы кемиді
6)Сутектік қосылыстарда -3 тотығу
дәрежесін көрсетеді
7)Судағы қосылыстарын әлсіз негіздік
қасиет көрсетеді
8)Реттік номері өскен сайын қасиеттері
бейметалдықтан металдыққа ауысады
9)Жоғарғы оксидтерінің жалпы
формуласы R
2
O
5
10)Қышқылдық екідайлы негіздік
қасиетке тән
11)Галогендермен қосылысының жалпы
формуласы ЭҒ
3
1)ІІІ период ІІІА топта орналасқан
2)Ядро құрамы 15р, 16n тұрады
3)Электрондық формуласы 1s2 2s2 2p6 3s2 3p3
4)Қосылыстардың валентігі ауыспалы ІІІ және V
5)Қосылыстардың тотығу дәрежесі -3, 0,+3, +5
6)Табиғаттағы қосылыстары апатит, фосфорит Ca
3
(PO
4
)
2
*2CaF
2
, Ca
3
(PO
4
)
2
7)Өмір мен өлі элементі атанған – Фереман
8)Өндірісте Ca
3
(PO
4
)
2
+ 5C + 3SiO
2
→ 2P + 3CaSiO
3
+ 5CO
9) Фосфордан пестицидтер, снарядтар, түтеткіш аспап, гранаталарда,
сіріңке өндірісінде қолданады
10)Фосфордың үштүрлі аллотропиялық түрөзгерісі бар. Ақ фосфор мөлдір
кристалды зат, суда ерімейді, органикалық еріткіштерде ериді, өте улы,
тұрақсыз зат. Қызыл фосфор аморфты, полимерлі зат. Суда, күкіртте,
көміртекте ерімейді. Улы емес.
11)Фосфордың оттекті қосылыстары P2O5, P2O3
12)Фосфор галогендермен, күкіртпен әрекеттестіреді
13)Фосфор су қатысында сілтілермен әрекеттеседі
14)Фосфордың сутектік қосылысы фосфин деп аталады
15)Фосфордың оттекті қосылысы гидроскопиялық кристалды зат. Химия
өндірісінде газдарды құрғату мақсатында қолданылады.
V А топ элементтеріне сипаттама Р-тән қасиет
25 слайд
1)V А топ элементтерге N,P,Bi,As,Sb жатады 2)Жалпы электрондық конфигурациясы ... ns 2 np 3 3) Тотығу дәрежесі +3, +5 азоттан басқасы 4)Физикалық қасиеттері бойынша N-газ қалғандары қатты заттар 5)Сутектік қосылыстың жалпы формуласы RH3 жоғарыдан төмен қарай тұрақтылығы кемиді 6)Сутектік қосылыстарда -3 тотығу дәрежесін көрсетеді 7)Судағы қосылыстарын әлсіз негіздік қасиет көрсетеді 8)Реттік номері өскен сайын қасиеттері бейметалдықтан металдыққа ауысады 9)Жоғарғы оксидтерінің жалпы формуласы R 2 O 5 10)Қышқылдық екідайлы негіздік қасиетке тән 11)Галогендермен қосылысының жалпы формуласы ЭҒ 3 1)ІІІ период ІІІА топта орналасқан 2)Ядро құрамы 15р, 16n тұрады 3)Электрондық формуласы 1s2 2s2 2p6 3s2 3p3 4)Қосылыстардың валентігі ауыспалы ІІІ және V 5)Қосылыстардың тотығу дәрежесі -3, 0,+3, +5 6)Табиғаттағы қосылыстары апатит, фосфорит Ca 3 (PO 4 ) 2 *2CaF 2 , Ca 3 (PO 4 ) 2 7)Өмір мен өлі элементі атанған – Фереман 8)Өндірісте Ca 3 (PO 4 ) 2 + 5C + 3SiO 2 → 2P + 3CaSiO 3 + 5CO 9) Фосфордан пестицидтер, снарядтар, түтеткіш аспап, гранаталарда, сіріңке өндірісінде қолданады 10)Фосфордың үштүрлі аллотропиялық түрөзгерісі бар. Ақ фосфор мөлдір кристалды зат, суда ерімейді, органикалық еріткіштерде ериді, өте улы, тұрақсыз зат. Қызыл фосфор аморфты, полимерлі зат. Суда, күкіртте, көміртекте ерімейді. Улы емес. 11)Фосфордың оттекті қосылыстары P2O5, P2O3 12)Фосфор галогендермен, күкіртпен әрекеттестіреді 13)Фосфор су қатысында сілтілермен әрекеттеседі 14)Фосфордың сутектік қосылысы фосфин деп аталады 15)Фосфордың оттекті қосылысы гидроскопиялық кристалды зат. Химия өндірісінде газдарды құрғату мақсатында қолданылады. V А топ элементтеріне сипаттама Р-тән қасиет

#26 слайд
Мына Р
2О
5, РН
3, Р, Са
3(РО
4)
2 қосылыстардағы
фосфордың тотығу дәрежелерінің
қосындысы тең болады
A.0
B.11
C.7
D.8
E.10
F.15
G.20
H.6
26 слайд
Мына Р 2О 5, РН 3, Р, Са 3(РО 4) 2 қосылыстардағы фосфордың тотығу дәрежелерінің қосындысы тең болады A.0 B.11 C.7 D.8 E.10 F.15 G.20 H.6

#27 слайд
Құрамында фосфоры бар қосылыс
A. Пирит
B. Нәруыз
C. Фюлирен
D. Карбид
E. Апатит
F. Боксид
G.Доломит
H.Гематит
27 слайд
Құрамында фосфоры бар қосылыс A. Пирит B. Нәруыз C. Фюлирен D. Карбид E. Апатит F. Боксид G.Доломит H.Гематит

#28 слайд
28 слайд

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
