Алюминий және оның қосылыстары


#1 слайд
§35 Алюминий.
§36 Алюминий қосылыстары. Алюминий
құймалары№ 39 жалпы орта білім беретін мектеп КММ
Пәні: Химия
Сыныбы: 9 « Б »
Дайындаған: Мүтәш А.Б
Тексерген: Кисыкова Г.Т
Өткізілген уақыты :24.01.18ж§35 Алюминий.
§36 Алюминий қосылыстары. Алюминий
құймалары
1 слайд
§35 Алюминий. §36 Алюминий қосылыстары. Алюминий құймалары№ 39 жалпы орта білім беретін мектеп КММ Пәні: Химия Сыныбы: 9 « Б » Дайындаған: Мүтәш А.Б Тексерген: Кисыкова Г.Т Өткізілген уақыты :24.01.18ж§35 Алюминий. §36 Алюминий қосылыстары. Алюминий құймалары

#2 слайд
Сабақтың тақырыбы : §35 Алюминий.
§36 Алюминий қосылыстары.
Мақсаты: Білімділік: оқушылар алюминийдің
маңызды қосылыстары мен құймаларын
сипаттап үйрену, тұрмыста, техникада
қолданылуы,алюминий өндірісі туралы
білім алу;
Дамытушылық: ой-өрісін, танымдық
белсенділігін арттырып, зейінін, өз
бетімен қорытынды жасауға дағдылану;
Тәрбиелік : дүниетанымдық,
адамгершілік, топтық жұмыс жасауға
тәрбиелеу;
2 слайд
Сабақтың тақырыбы : §35 Алюминий. §36 Алюминий қосылыстары. Мақсаты: Білімділік: оқушылар алюминийдің маңызды қосылыстары мен құймаларын сипаттап үйрену, тұрмыста, техникада қолданылуы,алюминий өндірісі туралы білім алу; Дамытушылық: ой-өрісін, танымдық белсенділігін арттырып, зейінін, өз бетімен қорытынды жасауға дағдылану; Тәрбиелік : дүниетанымдық, адамгершілік, топтық жұмыс жасауға тәрбиелеу;

#3 слайд
Сабақтың барысы: І. Ұйымдастыру бөлімі(3 минут)
Сәлемдесу, оқушыларды түгелдеу.
Оқушылардың назарын сабаққа
аудару.
Сабақтың жүру барысын түсіндіру:
II.Үй тапсырмасын сұрау (7 минут)
III.Жаңа сабақты түсіндіру
(15 минут)
IV.Жаңа сабақты қорытындылау
(5 минут)
V . Тапсырмалар орындау (7 минут)
VI. Үйге тапсырма: (2 минут)
VIІ. Бағалау.
3 слайд
Сабақтың барысы: І. Ұйымдастыру бөлімі(3 минут) Сәлемдесу, оқушыларды түгелдеу. Оқушылардың назарын сабаққа аудару. Сабақтың жүру барысын түсіндіру: II.Үй тапсырмасын сұрау (7 минут) III.Жаңа сабақты түсіндіру (15 минут) IV.Жаңа сабақты қорытындылау (5 минут) V . Тапсырмалар орындау (7 минут) VI. Үйге тапсырма: (2 минут) VIІ. Бағалау.

#4 слайд
1-қатар
Судың кермектілігі дегеніміз не?
Суда кальций және магний тұздарының болуы судың
кермектігі деп аталады .
Судың кермектілігінің неше түрі бар?
2
Кермек суды көп пайдаланудың зияны?
Кермек суды көп пайдаланудан адамның асқазаны
ауырыпорганизмге тұз жиналуы мүмкін.
4 слайд
1-қатар Судың кермектілігі дегеніміз не? Суда кальций және магний тұздарының болуы судың кермектігі деп аталады . Судың кермектілігінің неше түрі бар? 2 Кермек суды көп пайдаланудың зияны? Кермек суды көп пайдаланудан адамның асқазаны ауырыпорганизмге тұз жиналуы мүмкін.

#5 слайд
2-қатар
Уақытша кермектілік дегеніміз не?
Егер суда кальций және магний гидрокарбонаттары
болса,онда уақытша карбонатты кермектік деп аталады .
Тұрақты кермектілік дегеніміз не?
Ал сульфаттар,хлоридтер және басқа да тұздар
болса, тұрақты кермектік деп аталады
Тұрақты кермектікті жою жолы?
Тұрақты кермектікті химиялық әдістермен
кетіреді.Мысалы,соданың көмегімен:
5 слайд
2-қатар Уақытша кермектілік дегеніміз не? Егер суда кальций және магний гидрокарбонаттары болса,онда уақытша карбонатты кермектік деп аталады . Тұрақты кермектілік дегеніміз не? Ал сульфаттар,хлоридтер және басқа да тұздар болса, тұрақты кермектік деп аталады Тұрақты кермектікті жою жолы? Тұрақты кермектікті химиялық әдістермен кетіреді.Мысалы,соданың көмегімен:

#6 слайд
3-қатар
Уақытша кермектікті жою жолдары қандай?
Уақытша кермектік суды қайнатса кетеді:
Судың кермектілігінің неше түрі бар?
2
Табиғи сулар кермектік дәрежесіне қарай нешеге
бөлінеді?
5-ке
6 слайд
3-қатар Уақытша кермектікті жою жолдары қандай? Уақытша кермектік суды қайнатса кетеді: Судың кермектілігінің неше түрі бар? 2 Табиғи сулар кермектік дәрежесіне қарай нешеге бөлінеді? 5-ке

#7 слайд
Болмасада айтарлықтай салмағым
Көп металдан ардақтымын алдамын
Ұшақ болып аспанға ұшып, қалықтап.
Жердің жүзін, көк аспанды шарладым.
( Алюминий )
7 слайд
Болмасада айтарлықтай салмағым Көп металдан ардақтымын алдамын Ұшақ болып аспанға ұшып, қалықтап. Жердің жүзін, көк аспанды шарладым. ( Алюминий )

#8 слайд
Сабақтың тақырыбы :
Алюминий және оның маңызды
қосылыстары. Алюминий
құймасы және оның қолданылуы.
8 слайд
Сабақтың тақырыбы : Алюминий және оның маңызды қосылыстары. Алюминий құймасы және оның қолданылуы.
#9 слайд
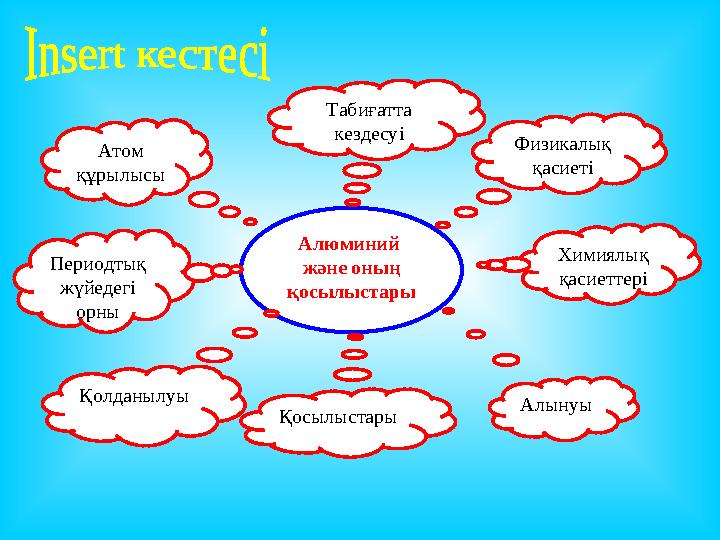
Алюминий
және оның
қосылыстарыПериодтық
жүйедегі
орны Атом
құрылысы Табиғатта
кездесуі
Физикалық
қасиеті
Химиялық
қасиеттері
Алынуы
Қосылыстары Қолданылуы
9 слайд
Алюминий және оның қосылыстарыПериодтық жүйедегі орны Атом құрылысы Табиғатта кездесуі Физикалық қасиеті Химиялық қасиеттері Алынуы Қосылыстары Қолданылуы

#10 слайд
Жоспары:
Алюминийдің периодтық жүйедегі орны
мен атом құрылысы
Табиғатта таралуы
Алынуы
Физикалық қасиеттері
Химиялық қасиеттері
Маңызды қосылыстары
ҚолданылуыЖоспары:
Алюминийдің периодтық жүйедегі орны
мен атом құрылысы
Табиғатта таралуы
Алынуы
Физикалық қасиеттері
Химиялық қасиеттері
Маңызды қосылыстары
Қолданылуы
10 слайд
Жоспары: Алюминийдің периодтық жүйедегі орны мен атом құрылысы Табиғатта таралуы Алынуы Физикалық қасиеттері Химиялық қасиеттері Маңызды қосылыстары ҚолданылуыЖоспары: Алюминийдің периодтық жүйедегі орны мен атом құрылысы Табиғатта таралуы Алынуы Физикалық қасиеттері Химиялық қасиеттері Маңызды қосылыстары Қолданылуы

#11 слайд
Периодтық жүйедегі орны
1.Химиялық таңбасы- Al
2. Реттік нөмірі- 13
3. Ar(Al)- 27
4. Период нөмірі- ІІІ (кіші)
5.Топ нөмірі-ІІІ (негізгі)
Атом құрылысы:
1.Ядро заряды- +13
2.Электрон саны- 13
3.Протон саны- 13
4.Нейтрон саны -14
5.Энергетикалық деңгей саны -3
6.Валенттілік электрондары- 3
7. Электрондық конфигурациясы 1 s2 /2s22 p 6/3s2 3p1
11 слайд
Периодтық жүйедегі орны 1.Химиялық таңбасы- Al 2. Реттік нөмірі- 13 3. Ar(Al)- 27 4. Период нөмірі- ІІІ (кіші) 5.Топ нөмірі-ІІІ (негізгі) Атом құрылысы: 1.Ядро заряды- +13 2.Электрон саны- 13 3.Протон саны- 13 4.Нейтрон саны -14 5.Энергетикалық деңгей саны -3 6.Валенттілік электрондары- 3 7. Электрондық конфигурациясы 1 s2 /2s22 p 6/3s2 3p1

#12 слайд
Табиғатта таралуы.
Алюминий табиғатта таралуы бойынша химиялық элементтер арасында
оттек пен кремнийден кейінгі үшінші орында тұр,масса бойынша
8,8%.Табиғаттағы металдар ішінде ол таралуы бойынша бірінші орында.
Белсенді металл болғандықтан люминий тек қосылыстар түрінде
кездеседі.Жер қыртысының негізгі массасын алюмосиликаттар
құрайды.Олардың құрамына алюминий,оттек,кремний,сілтілік және сілтілік
жер металдары кіреді.
Корунд Al2O3 -ө те қатты түссіз минерал.Егер оның құрамында қоспа
болса,ол әртүрлі түсті бағалы және әшекейлік тастарға
айналады:рубин(қызыл),аметист(күлгін),сапфир(көк).
Боксит Al2O3*nH2O- т ау жынысы,ол негізгі өнеркәсіпте алюминийді
алуға арналған шикізат болып саналады.Қазақс танда бокситтердің белгілі
кен орындары бар.Олар Қостанай және Ақтөбе облыстарында
орналасқан.Жалпы алғанда біздің Республикамызда боксит кендерінің
мөлшері 1млрд т-дан асады.
12 слайд
Табиғатта таралуы. Алюминий табиғатта таралуы бойынша химиялық элементтер арасында оттек пен кремнийден кейінгі үшінші орында тұр,масса бойынша 8,8%.Табиғаттағы металдар ішінде ол таралуы бойынша бірінші орында. Белсенді металл болғандықтан люминий тек қосылыстар түрінде кездеседі.Жер қыртысының негізгі массасын алюмосиликаттар құрайды.Олардың құрамына алюминий,оттек,кремний,сілтілік және сілтілік жер металдары кіреді. Корунд Al2O3 -ө те қатты түссіз минерал.Егер оның құрамында қоспа болса,ол әртүрлі түсті бағалы және әшекейлік тастарға айналады:рубин(қызыл),аметист(күлгін),сапфир(көк). Боксит Al2O3*nH2O- т ау жынысы,ол негізгі өнеркәсіпте алюминийді алуға арналған шикізат болып саналады.Қазақс танда бокситтердің белгілі кен орындары бар.Олар Қостанай және Ақтөбе облыстарында орналасқан.Жалпы алғанда біздің Республикамызда боксит кендерінің мөлшері 1млрд т-дан асады.

#13 слайд
13 слайд

#14 слайд
Алынуы.
Өнеркәсіпте алынуы:
Алюминийді электролиз әдіспен алуға болады. Алюминий
өндірісінде, шикізат ретінде көбінесе боскситтер жиі
қолданады. Қыздырғанда олар суын жоғалтып, алюминий
оксидіне айналады. Алюминий оксидінің балқу
температурасы жоғары (20450С) және ол электр тоғын
өткізбейді. Сондықтан AI2O3– ті фторидтерді қоса отырып
( CaF2, MgF2 немесе AIF3), балқытылған криолитте ерітеді.
Бұл қоспа шамамен 1000 С температурада балқиды.
Электролиз кезінде катодта- алюминий , ал анодта – оттек
бөлінеді. Электролиз реакциясының жалпы теңдеуі:
14 слайд
Алынуы. Өнеркәсіпте алынуы: Алюминийді электролиз әдіспен алуға болады. Алюминий өндірісінде, шикізат ретінде көбінесе боскситтер жиі қолданады. Қыздырғанда олар суын жоғалтып, алюминий оксидіне айналады. Алюминий оксидінің балқу температурасы жоғары (20450С) және ол электр тоғын өткізбейді. Сондықтан AI2O3– ті фторидтерді қоса отырып ( CaF2, MgF2 немесе AIF3), балқытылған криолитте ерітеді. Бұл қоспа шамамен 1000 С температурада балқиды. Электролиз кезінде катодта- алюминий , ал анодта – оттек бөлінеді. Электролиз реакциясының жалпы теңдеуі:

#15 слайд
Физикалық қасиеттері.
Алюминий – жеңіл, күміс түстес ақ металл, оның
тығыздығы – 2,7 г/см3. Қ айнау температурасы-
650 º С. Алюминий иілгіштік қасиеті жоғары, оңай
фольга болып жайылады және сым түрінде
созылады.
Алюминийдің электрөткізгіштігі, жылуөткізгіштігі
жоғары. Металдың беті жұқа және өте тығыз оксид
қабықшасымен қапталған. Бұл қабықша оптикалық
мөлдір және металдық шағылдырғыш қабілетін
сақтайды.Физикалық қасиеттері.
15 слайд
Физикалық қасиеттері. Алюминий – жеңіл, күміс түстес ақ металл, оның тығыздығы – 2,7 г/см3. Қ айнау температурасы- 650 º С. Алюминий иілгіштік қасиеті жоғары, оңай фольга болып жайылады және сым түрінде созылады. Алюминийдің электрөткізгіштігі, жылуөткізгіштігі жоғары. Металдың беті жұқа және өте тығыз оксид қабықшасымен қапталған. Бұл қабықша оптикалық мөлдір және металдық шағылдырғыш қабілетін сақтайды.Физикалық қасиеттері.

#16 слайд
Химиялық қасиеттері.
Алюминий өте белсенді металл, оттекпен оңай
әрекеттеседі. Сондықтан ауада алюминий бетін оксид
қабығы жауып, оны әрі қарай бұзылудан сақтап тұрады. Ол
жұқа болғанымен, өте берік, металдық жылтырын
бәсендетеді. Осы оксит қабыршағынан тазаласа, алюминий
атомы өзінің сыртындағы 3 электронын жылдам беріп,
тотықсыздандырғыш қасиет көрсетеді. Оксид қабыршағын
алып тастау үшін оны сынапқа батырады, ол алюминиймен
амалъгама деп аталатын құйма түзеді. Бұл құймада
алюминий өзінің белсенділік қасиетін сақтап, барлық
заттармен шабытты әрекеттеседі.Химиялық қасиеттері.
16 слайд
Химиялық қасиеттері. Алюминий өте белсенді металл, оттекпен оңай әрекеттеседі. Сондықтан ауада алюминий бетін оксид қабығы жауып, оны әрі қарай бұзылудан сақтап тұрады. Ол жұқа болғанымен, өте берік, металдық жылтырын бәсендетеді. Осы оксит қабыршағынан тазаласа, алюминий атомы өзінің сыртындағы 3 электронын жылдам беріп, тотықсыздандырғыш қасиет көрсетеді. Оксид қабыршағын алып тастау үшін оны сынапқа батырады, ол алюминиймен амалъгама деп аталатын құйма түзеді. Бұл құймада алюминий өзінің белсенділік қасиетін сақтап, барлық заттармен шабытты әрекеттеседі.Химиялық қасиеттері.

#17 слайд
17 слайд
#18 слайд
18 слайд

#19 слайд
Маңызды қосылыстары .
Al
2 O
3 - қиын балқитын, ақ түсті зат. Табиғатта корунд деген
атпен кездеседі. Алюминий оксиді суда ерімейді, екідайлы
қасиет көрсетеді:
Al
2 O
3 +6HCl = 2AlCl
3 +3H
2 O
Al
2 O
3 +2NaOH+3H
2 O = 2Na[Al(OH)
4 ]
Al(OH)
3 –ақ түсті суда ерімейтін зат.
Алюминий гидроксидін
алюминий тұздары ерітінділеріне сілтімен әсер ету арқылы
алады:
AlCl
3 + 3NaOH = Al(OH)
3 + 3NaCl
Жаңа тұнған Al(OH)
3 ақ қоймалжың тұнба, суда мүлдем
ерімейді және типтік екідайлы гидроксид болып табылады:
Al(OH)
3 +3HCl = AlCl
3 +3H
2 O
Al(OH)
3 +NaOH = Na[Al(OH)
4 ]
19 слайд
Маңызды қосылыстары . Al 2 O 3 - қиын балқитын, ақ түсті зат. Табиғатта корунд деген атпен кездеседі. Алюминий оксиді суда ерімейді, екідайлы қасиет көрсетеді: Al 2 O 3 +6HCl = 2AlCl 3 +3H 2 O Al 2 O 3 +2NaOH+3H 2 O = 2Na[Al(OH) 4 ] Al(OH) 3 –ақ түсті суда ерімейтін зат. Алюминий гидроксидін алюминий тұздары ерітінділеріне сілтімен әсер ету арқылы алады: AlCl 3 + 3NaOH = Al(OH) 3 + 3NaCl Жаңа тұнған Al(OH) 3 ақ қоймалжың тұнба, суда мүлдем ерімейді және типтік екідайлы гидроксид болып табылады: Al(OH) 3 +3HCl = AlCl 3 +3H 2 O Al(OH) 3 +NaOH = Na[Al(OH) 4 ]

#20 слайд
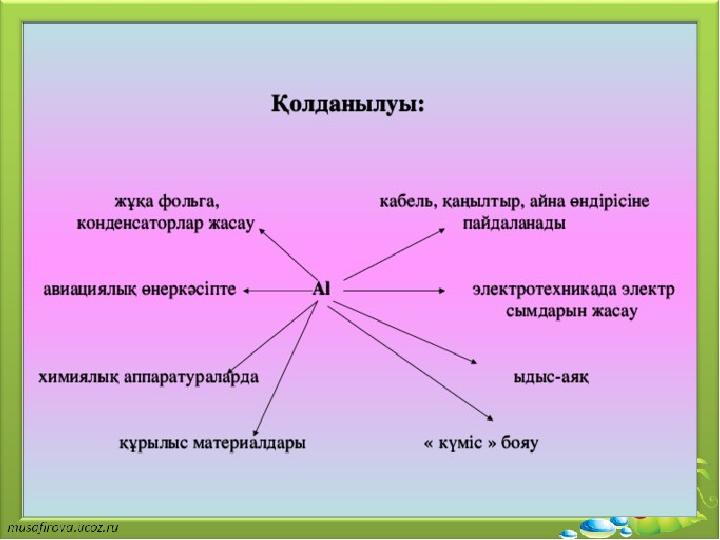
Алюминийдің құймалары. Алюминийдің қолданылатын
маңызды аймағы- оның негізіндегі жеңіл құймалар өндірісі.
Металдық алюминийді – мыс, магний, титан, никель, мырыш,
темір құймаларын лигерлейтін (шыңдайтын) қоспа ретінде
кеңінен қолданады. Кең таралған құймалар:
Силумин – алюминийдің кремниймен құймасы, оны
негізінен құю үшін пайдаланады. Дюралюмин – құрамында
алюминиймен бірге магний темір, мыс және марганец кіреді.
Магналий – алюминийдің магниймен құймасы. Бұл
құймалардың бәрі жеңіл берік, сондықтан ұшақ, машина
және ыдыстар жасау үшін қолданылады. Алюминиймен темір
бұйымдардың бетіни қаптайды, бұл оларды жемірілуден
сақтайды. Металдарды тотығудан қорғаудың бұл әдісі
алитерлеу деп аталады.
20 слайд
Алюминийдің құймалары. Алюминийдің қолданылатын маңызды аймағы- оның негізіндегі жеңіл құймалар өндірісі. Металдық алюминийді – мыс, магний, титан, никель, мырыш, темір құймаларын лигерлейтін (шыңдайтын) қоспа ретінде кеңінен қолданады. Кең таралған құймалар: Силумин – алюминийдің кремниймен құймасы, оны негізінен құю үшін пайдаланады. Дюралюмин – құрамында алюминиймен бірге магний темір, мыс және марганец кіреді. Магналий – алюминийдің магниймен құймасы. Бұл құймалардың бәрі жеңіл берік, сондықтан ұшақ, машина және ыдыстар жасау үшін қолданылады. Алюминиймен темір бұйымдардың бетіни қаптайды, бұл оларды жемірілуден сақтайды. Металдарды тотығудан қорғаудың бұл әдісі алитерлеу деп аталады.

#21 слайд
21 слайд
#22 слайд
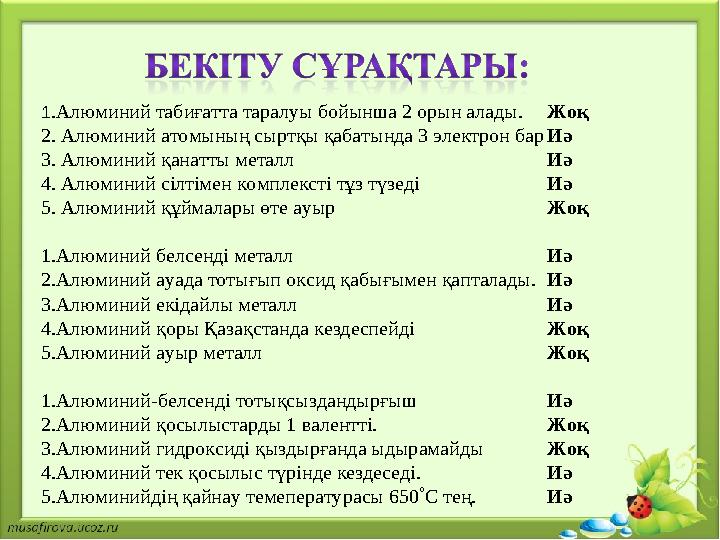
1 . Алюминий табиғатта таралуы бойынша 2 орын алады.
2. Алюминий атомының сыртқы қабатында 3 электрон бар
3. Алюминий қанатты металл
4. Алюминий сілтімен комплексті тұз түзеді
5. Алюминий құймалары өте ауыр
1.Алюминий белсенді металл
2.Алюминий ауада тотығып оксид қабығымен қапталады.
3.Алюминий екідайлы металл
4.Алюминий қоры Қазақстанда кездеспейді
5.Алюминий ауыр металл
1. Алюминий-белсенді тотықсыздандырғыш
2. Алюминий қосылыстарды 1 валентті.
3. Алюминий гидроксиді қыздырғанда ыдырамайды
4. Алюминий тек қосылыс түрінде кездеседі.
5. Алюминийдің қайнау темепературасы 650 С тең. Жоқ
Иә
Иә
Иә
Жоқ
Иә
Иә
Иә
Жоқ
Жоқ
Иә
Жоқ
Жоқ
Иә
Иә
22 слайд
1 . Алюминий табиғатта таралуы бойынша 2 орын алады. 2. Алюминий атомының сыртқы қабатында 3 электрон бар 3. Алюминий қанатты металл 4. Алюминий сілтімен комплексті тұз түзеді 5. Алюминий құймалары өте ауыр 1.Алюминий белсенді металл 2.Алюминий ауада тотығып оксид қабығымен қапталады. 3.Алюминий екідайлы металл 4.Алюминий қоры Қазақстанда кездеспейді 5.Алюминий ауыр металл 1. Алюминий-белсенді тотықсыздандырғыш 2. Алюминий қосылыстарды 1 валентті. 3. Алюминий гидроксиді қыздырғанда ыдырамайды 4. Алюминий тек қосылыс түрінде кездеседі. 5. Алюминийдің қайнау темепературасы 650 С тең. Жоқ Иә Иә Иә Жоқ Иә Иә Иә Жоқ Жоқ Иә Жоқ Жоқ Иә Иә

#23 слайд
Алюминий – алюминий- Aluminum
Боксит- боксит- Bauxites
Корунд- корунд- Corundum
Амальгама- амальгама- Amalgam
Дюралюмин- дюралюмин- Duralumin
Силумин- силумин- Silumin
Алюминий оксиді- оксид алюминия- O xide Alumina
Алюминий гидроксиді- гидроксид алюминия-
Aluminum hydroxide
Алюминотермия- алюминотермия- Aluminothermy
23 слайд
Алюминий – алюминий- Aluminum Боксит- боксит- Bauxites Корунд- корунд- Corundum Амальгама- амальгама- Amalgam Дюралюмин- дюралюмин- Duralumin Силумин- силумин- Silumin Алюминий оксиді- оксид алюминия- O xide Alumina Алюминий гидроксиді- гидроксид алюминия- Aluminum hydroxide Алюминотермия- алюминотермия- Aluminothermy
#24 слайд
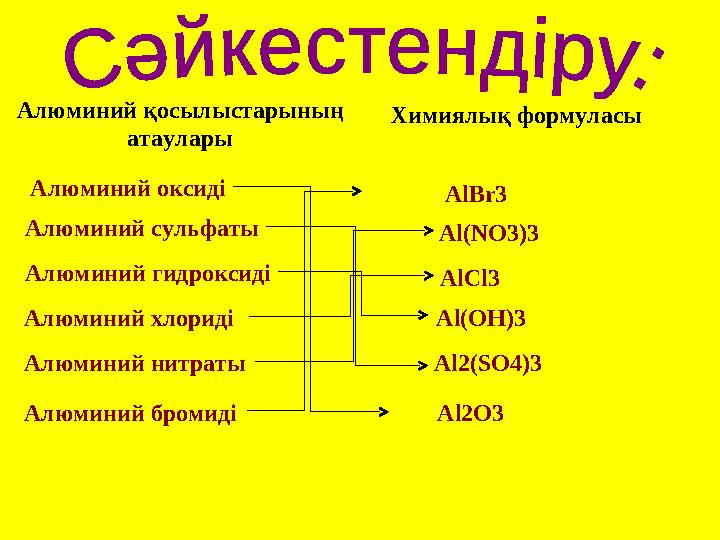
Алюминий қосылыстарының
атаулары Химиялық формуласы
Алюминий оксиді
Алюминий сульфаты
Алюминий гидроксиді
Алюминий хлориді
Алюминий нитраты
Алюминий бромиді Al2O3 Al2(SO4)3 Al(OH)3 AlCl3 Al(NO3)3 AlBr3
24 слайд
Алюминий қосылыстарының атаулары Химиялық формуласы Алюминий оксиді Алюминий сульфаты Алюминий гидроксиді Алюминий хлориді Алюминий нитраты Алюминий бромиді Al2O3 Al2(SO4)3 Al(OH)3 AlCl3 Al(NO3)3 AlBr3

#25 слайд
1 . Мына айналуларды жүзеге асыруға болатын реакция
теңдеулерін
жаз.
Al→ Al
2 O
3 → Al(OH)
3 → AlCl
3 → Al(NO
3 )
3
2 . Массасы 48 грамм алюминийді оттекпен
әрекеттестіріп, алюминий оксидінің массасын табыңдар.
3.Келесі реакция теңдеулерін аяқтап,теңестіріңдер:
Al+O2
Al2O3+ HCl
Al2O3 + NaOH
Al + Fe2O3
25 слайд
1 . Мына айналуларды жүзеге асыруға болатын реакция теңдеулерін жаз. Al→ Al 2 O 3 → Al(OH) 3 → AlCl 3 → Al(NO 3 ) 3 2 . Массасы 48 грамм алюминийді оттекпен әрекеттестіріп, алюминий оксидінің массасын табыңдар. 3.Келесі реакция теңдеулерін аяқтап,теңестіріңдер: Al+O2 Al2O3+ HCl Al2O3 + NaOH Al + Fe2O3

#26 слайд
§35 Алюминий.
§36 Алюминий қосылыстары.
160-бет:6,7 жаттығу
162-бет: № 6 есеп
26 слайд
§35 Алюминий. §36 Алюминий қосылыстары. 160-бет:6,7 жаттығу 162-бет: № 6 есеп

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
