Ашық сабақ Авогадро заңы


#1 слайд
Сабақтың тақырыбы:
«Авогадро з аңы .
Газдардың мольдік көлемі »
1 слайд
Сабақтың тақырыбы: «Авогадро з аңы . Газдардың мольдік көлемі »

#2 слайд
Оқыту мақсаты:
8.2.3.6 Авогадрозаңын біліп, қалыпты
жағдайда және стандартты
жағдайда газдардың мольдік
көлемін пайдаларып есептер
құрастыру және шығару.
2 слайд
Оқыту мақсаты: 8.2.3.6 Авогадрозаңын біліп, қалыпты жағдайда және стандартты жағдайда газдардың мольдік көлемін пайдаларып есептер құрастыру және шығару.

#3 слайд
Answer the question
•
W hat state of matter you know?
•
Give examples of substances and their
aggregative states.
•
W hat gases are in the atmosphere?
•
What is the topic of our lesson ?
3 слайд
Answer the question • W hat state of matter you know? • Give examples of substances and their aggregative states. • W hat gases are in the atmosphere? • What is the topic of our lesson ?

#4 слайд
lesson topic
Avogadro law. Molar volume.
Авогадро заңы . Мольдік көлем .
Амедео Авогадро
(1776 – 1856) Италия ғалымы .
1811 г. Заңды ашқан,
Кейін заң оның атымен аталған.
4 слайд
lesson topic Avogadro law. Molar volume. Авогадро заңы . Мольдік көлем . Амедео Авогадро (1776 – 1856) Италия ғалымы . 1811 г. Заңды ашқан, Кейін заң оның атымен аталған.
#5 слайд
group work
H 2
1 топ
O 2
3 топ CO 2
4 топ N 2
2 топ
5 слайд
group work H 2 1 топ O 2 3 топ CO 2 4 топ N 2 2 топ
#6 слайд
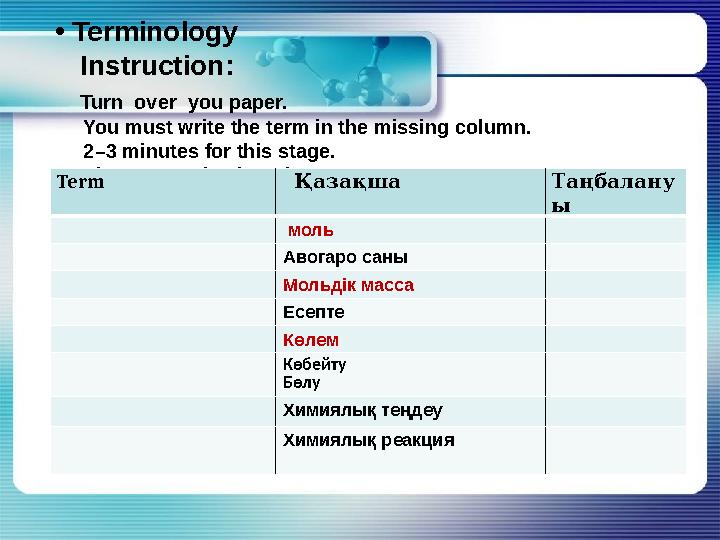
•
Terminology
Instruction:
Turn over you paper.
You must write the term in the missing column.
2–3 minutes for this stage.
The group’s leader takes papers .
Term Қазақша Таңбалану
ы
моль
Авогаро саны
Мольдік масса
Есепте
Көлем
Көбейту
Бөлу
Химиялық теңдеу
Химиялық реакция
6 слайд
• Terminology Instruction: Turn over you paper. You must write the term in the missing column. 2–3 minutes for this stage. The group’s leader takes papers . Term Қазақша Таңбалану ы моль Авогаро саны Мольдік масса Есепте Көлем Көбейту Бөлу Химиялық теңдеу Химиялық реакция
#7 слайд
•
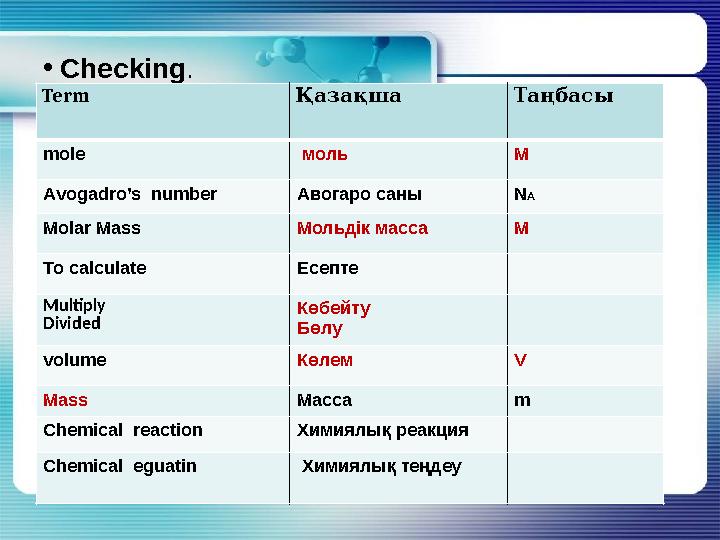
С hecking .
Term Қазақша Таңбасы
mole моль M
Avogadro’s n u mber Авогаро саны N A
Molar Mass Мольдік масса M
To calculate Есепте
Multiply
Divided Көбейту
Бөлу
volume Көлем V
Mass Масса m
Chemical reaction Химиялық реакция
Chemical eguatin Химиялық теңдеу
7 слайд
• С hecking . Term Қазақша Таңбасы mole моль M Avogadro’s n u mber Авогаро саны N A Molar Mass Мольдік масса M To calculate Есепте Multiply Divided Көбейту Бөлу volume Көлем V Mass Масса m Chemical reaction Химиялық реакция Chemical eguatin Химиялық теңдеу

#8 слайд
Questions;
•
What is the relative atomic mass?
•
What is the relative molecular mass ?
•
What is the Avogadro number?
•
Number of molecules
•
How to calculate the mole?
•
How to calculate the mass?
•
How to с alculating the Molar Mass
8 слайд
Questions; • What is the relative atomic mass? • What is the relative molecular mass ? • What is the Avogadro number? • Number of molecules • How to calculate the mole? • How to calculate the mass? • How to с alculating the Molar Mass

#9 слайд
Molar mass M = m/n
Quantity of mole n = m/M
Number of molecules N = N
A ∙ n
9 слайд
Molar mass M = m/n Quantity of mole n = m/M Number of molecules N = N A ∙ n

#10 слайд
Termin
•
Газ - gas
•
Көлем - volume
•
Молярлық көлем - Molar Volume
•
Қатынас - ratio
•
Стандартты жағдай – normal conditions
•
Қысым - Pressure
•
Температура -Temperature
10 слайд
Termin • Газ - gas • Көлем - volume • Молярлық көлем - Molar Volume • Қатынас - ratio • Стандартты жағдай – normal conditions • Қысым - Pressure • Температура -Temperature

#11 слайд
Watch the video
11 слайд
Watch the video
#12 слайд
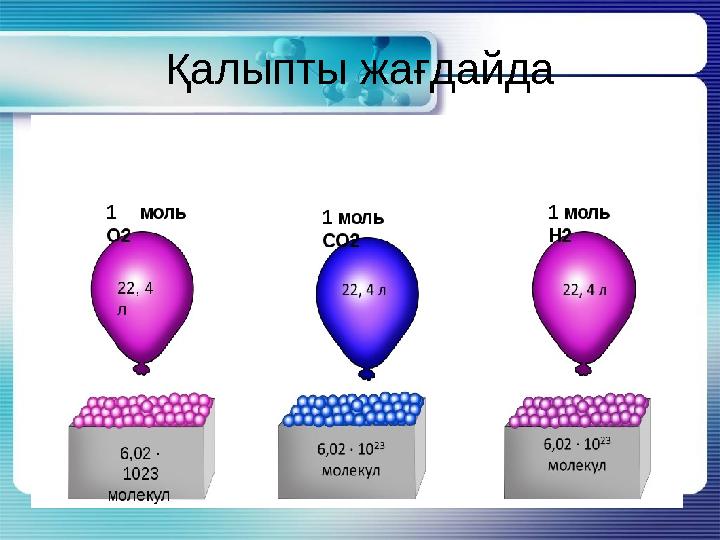
Қалыпты жағдайда
12 слайд
Қалыпты жағдайда

#13 слайд
A вогадро заңы
•
Газдардың көлемі
газдардың моль
санына ( n ) тура
пропоционал
шама .
•
T және P тұрақты .
V
1 = V
2
n
1 n
2
13 слайд
A вогадро заңы • Газдардың көлемі газдардың моль санына ( n ) тура пропоционал шама . • T және P тұрақты . V 1 = V 2 n 1 n 2

#14 слайд
Молдік көлем– V
m Бірдей жағдайда (температура мен қысымда) əртүрлі
газдардың бірдей көлеміндегі молекулалар саны бірдей болады.
1. Кез келген газдың молекулаларының белгілі саны ( бірдей қысым мен
температурада ) тұрақты көлем алады .
2. Қалыпты жағдайда ( қ . ж Т =273 К ) p=101.3 кПа немесе 0 С температура ,
1 атомосфералық қысым ) кез келген газдың 1 молі 22,4 л көлем алады . Ол мольдік
көлем деп аталып ,Vm деп белгіленеді .
V=n*Vm n=V/Vm
In equal volumes of different gases under the same conditions, the same number
of
molecules are contained.
1. A certain amount of any gas molecules (at the same pressure and temperature)
receives
a constant volume.
2. Under normal conditions (for example, T = 273 K), p = 101.3 kPa or 0 C, 1
atmospheric pressure) 1 mole of any gas occupies 22.4 liters. It is called the molecular
volume and is denoted as Vm.Avogadro law
14 слайд
Молдік көлем– V m Бірдей жағдайда (температура мен қысымда) əртүрлі газдардың бірдей көлеміндегі молекулалар саны бірдей болады. 1. Кез келген газдың молекулаларының белгілі саны ( бірдей қысым мен температурада ) тұрақты көлем алады . 2. Қалыпты жағдайда ( қ . ж Т =273 К ) p=101.3 кПа немесе 0 С температура , 1 атомосфералық қысым ) кез келген газдың 1 молі 22,4 л көлем алады . Ол мольдік көлем деп аталып ,Vm деп белгіленеді . V=n*Vm n=V/Vm In equal volumes of different gases under the same conditions, the same number of molecules are contained. 1. A certain amount of any gas molecules (at the same pressure and temperature) receives a constant volume. 2. Under normal conditions (for example, T = 273 K), p = 101.3 kPa or 0 C, 1 atmospheric pressure) 1 mole of any gas occupies 22.4 liters. It is called the molecular volume and is denoted as Vm.Avogadro law

#15 слайд
Есепту формулалары: m
V
V
v
m
V
v
V
m
V V v
15 слайд
Есепту формулалары: m V V v m V v V m V V v

#16 слайд
Мольік көлемді өлшем
бірлігі:
V
m = 22,4 л/моль
V
m = 22,4 м 3
/кмоль
V
m = 22,4 мл/ммоль
16 слайд
Мольік көлемді өлшем бірлігі: V m = 22,4 л/моль V m = 22,4 м 3 /кмоль V m = 22,4 мл/ммоль

#17 слайд
Решение задач
Problem solving
•
Қ.Ж. азот молекуласы қанша көлем
алады?
•
84 г.азот ( қ.ж. ) қанша көлем алады?
17 слайд
Решение задач Problem solving • Қ.Ж. азот молекуласы қанша көлем алады? • 84 г.азот ( қ.ж. ) қанша көлем алады?
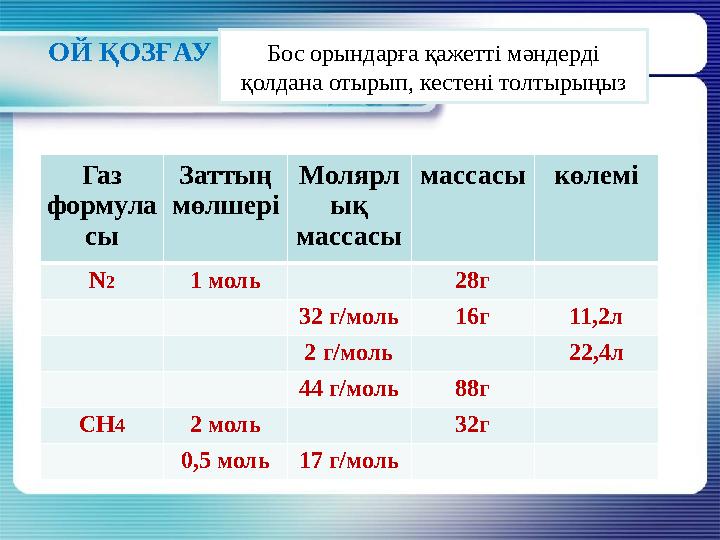
#18 слайд
ОЙ ҚОЗҒАУ
Бос орындарға қажетті мәндерді
қолдана отырып, кестені толтырыңыз
Газ
формула
сы Заттың
мөлшері Молярл
ық
массасы массасы көлемі
N 2 1 моль 28г
32 г/моль 16г 11,2л
2 г/моль 22,4л
44 г/моль 88г
СН 4 2 моль 32г
0,5 моль 17 г/моль
18 слайд
ОЙ ҚОЗҒАУ Бос орындарға қажетті мәндерді қолдана отырып, кестені толтырыңыз Газ формула сы Заттың мөлшері Молярл ық массасы массасы көлемі N 2 1 моль 28г 32 г/моль 16г 11,2л 2 г/моль 22,4л 44 г/моль 88г СН 4 2 моль 32г 0,5 моль 17 г/моль
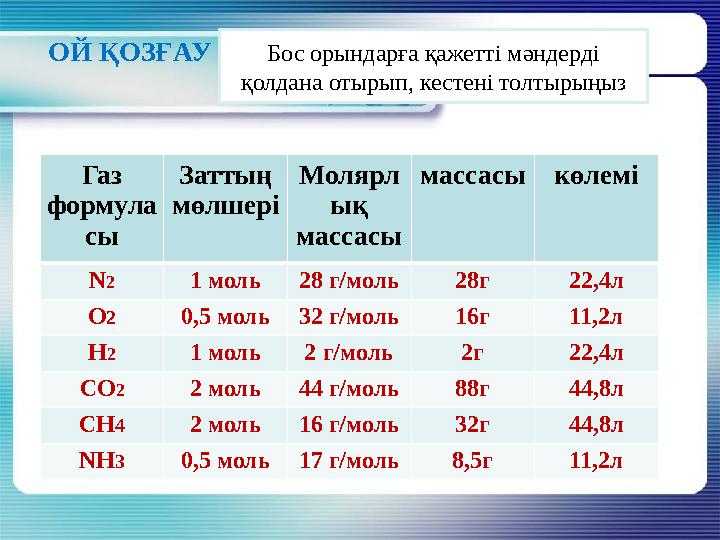
#19 слайд
ОЙ ҚОЗҒАУ
Бос орындарға қажетті мәндерді
қолдана отырып, кестені толтырыңыз
Газ
формула
сы Заттың
мөлшері Молярл
ық
массасы массасы көлемі
N 2 1 моль 28 г/моль 28г 22,4л
О 2 0,5 моль 32 г/моль 16г 11,2л
Н 2 1 моль 2 г/моль 2г 22,4л
CO 2 2 моль 44 г/моль 88г 44,8л
СН 4 2 моль 16 г/моль 32г 44,8л
N Н 3 0,5 моль 17 г/моль 8,5г 11,2л
19 слайд
ОЙ ҚОЗҒАУ Бос орындарға қажетті мәндерді қолдана отырып, кестені толтырыңыз Газ формула сы Заттың мөлшері Молярл ық массасы массасы көлемі N 2 1 моль 28 г/моль 28г 22,4л О 2 0,5 моль 32 г/моль 16г 11,2л Н 2 1 моль 2 г/моль 2г 22,4л CO 2 2 моль 44 г/моль 88г 44,8л СН 4 2 моль 16 г/моль 32г 44,8л N Н 3 0,5 моль 17 г/моль 8,5г 11,2л

#20 слайд
True/False Questions
•
1. Molar volume is equal to 22,4 L
True False
•
2. Standard conditions affect gas volume
•
(Қ.Ж газдың көлеміне әсер етеді)
True False
•
3. Oxygen consists of 2 atoms
True False
4. The amount of substance is measured in grams
(Зат мөлшері граммен өлшенеді)
True False
5. The pollutant is gas (ластаушы газ) CO2
True False
20 слайд
True/False Questions • 1. Molar volume is equal to 22,4 L True False • 2. Standard conditions affect gas volume • (Қ.Ж газдың көлеміне әсер етеді) True False • 3. Oxygen consists of 2 atoms True False 4. The amount of substance is measured in grams (Зат мөлшері граммен өлшенеді) True False 5. The pollutant is gas (ластаушы газ) CO2 True False

#21 слайд
•
С hecking
•
1 True
•
2 False
•
3 True
•
4 False
•
5 True
21 слайд
• С hecking • 1 True • 2 False • 3 True • 4 False • 5 True

#22 слайд
Write your opinion about
the lesson :
•
It was interesting _____
•
It was important ________
•
It was needs _____
22 слайд
Write your opinion about the lesson : • It was interesting _____ • It was important ________ • It was needs _____

#23 слайд
Рефлексия «Таңдау» әдісі.
Не білдім, нені үйрендім?
•
What did you Le а rn ?
•
Не нәрсе түсініксіз болып қалды?
•
What was not clear ?
•
Қай сұрақ бойынша қайта жұмыс жасау
керек? What more work needs to be
done ?
23 слайд
Рефлексия «Таңдау» әдісі. Не білдім, нені үйрендім? • What did you Le а rn ? • Не нәрсе түсініксіз болып қалды? • What was not clear ? • Қай сұрақ бойынша қайта жұмыс жасау керек? What more work needs to be done ?

#24 слайд
Үй тапсырмасы:
§ 18 .бет 67-
69 №2,3
Chemistry grade 8 p.39
24 слайд
Үй тапсырмасы: § 18 .бет 67- 69 №2,3 Chemistry grade 8 p.39

#25 слайд
Thanks
for your
work !
25 слайд
Thanks for your work !

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
