Ашық сабақ "Кальций" 9 сынып


#1 слайд
Кальций
Ca
Ca
1 слайд
Кальций Ca Ca

#2 слайд
IІ топтың негізгі
топшасындағы металдың
жалпы сипаттамасы. Ca
2 слайд
IІ топтың негізгі топшасындағы металдың жалпы сипаттамасы. Ca

#3 слайд
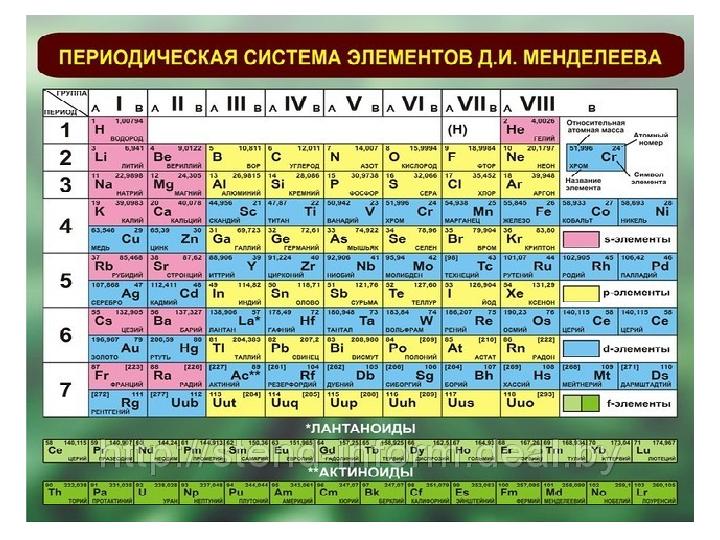
Периодтық жүйедегі орны.
•Кальций IV период, II топтың негізгі
топшасының элементі, реттік нөмірі 20,
ядросында 20 протон мен 20 нейтроны
бар.Ar =40. Электрондарының жалпы саны
да 20.Кальцийдің электрондық формуласы
1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
, валенттілік
электрондары 4s
2
болғандықтан кальций
қосылыстарында тұрақты II валентті.
3 слайд
Периодтық жүйедегі орны. •Кальций IV период, II топтың негізгі топшасының элементі, реттік нөмірі 20, ядросында 20 протон мен 20 нейтроны бар.Ar =40. Электрондарының жалпы саны да 20.Кальцийдің электрондық формуласы 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 , валенттілік электрондары 4s 2 болғандықтан кальций қосылыстарында тұрақты II валентті.

#4 слайд
4 слайд
#5 слайд
5 слайд

#6 слайд
6 слайд
#7 слайд
Дәрі-дәрмектердің
құрамында кальций
кездеседі.
7 слайд
Дәрі-дәрмектердің құрамында кальций кездеседі.

#8 слайд
Физикалық қасиеттері.
Кальций ақ түсті, жеңіл (р=1,55 г/см3),
сілтілік металдардан қаттырақ зат, t°балқу =
851°С, керосиннің астында сақталады.
Ат. н. 20; ат. м. 40,08; балқу t 842°С; қайнау
t 1495°С тығыздығы 1,55 г/см2.
Кальцийді 1808 жылы ағылшын ғалымы
Г.Дэви ашқан. Түсі күмістей ақ, жеңіл металл,
белгілі изотоптары 14, табиғи изотоптары 6.
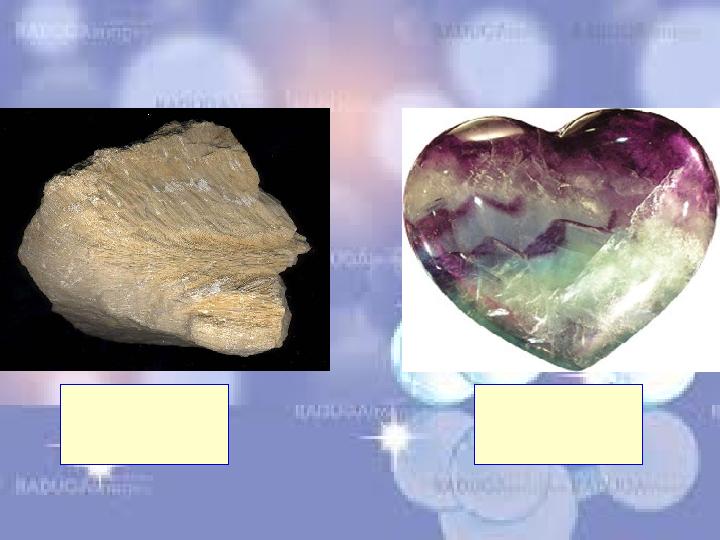
Негізгі минералдары: кальцит , ангидрит, гипс,
флюорит, апатит.
8 слайд
Физикалық қасиеттері. Кальций ақ түсті, жеңіл (р=1,55 г/см3), сілтілік металдардан қаттырақ зат, t°балқу = 851°С, керосиннің астында сақталады. Ат. н. 20; ат. м. 40,08; балқу t 842°С; қайнау t 1495°С тығыздығы 1,55 г/см2. Кальцийді 1808 жылы ағылшын ғалымы Г.Дэви ашқан. Түсі күмістей ақ, жеңіл металл, белгілі изотоптары 14, табиғи изотоптары 6. Негізгі минералдары: кальцит , ангидрит, гипс, флюорит, апатит.

#9 слайд
Химиялық қасиеттері.
Кальций оттекпен әрекеттесіп, оксид түзеді:
2Сa+O2=2CaO
Бейметалдармен әрекеттеседі:
Сa+Br2 =CaBr2
Ca+S=CaS
Ca+H2=CaH2
Қышқылдармен әрекеттеседі:
Ca+2HCl=CaCl2+H2
Кальций сумен қуатты әрекеттеседі:
Ca+2H2O=Ca(OH)2 +H2
9 слайд
Химиялық қасиеттері. Кальций оттекпен әрекеттесіп, оксид түзеді: 2Сa+O2=2CaO Бейметалдармен әрекеттеседі: Сa+Br2 =CaBr2 Ca+S=CaS Ca+H2=CaH2 Қышқылдармен әрекеттеседі: Ca+2HCl=CaCl2+H2 Кальций сумен қуатты әрекеттеседі: Ca+2H2O=Ca(OH)2 +H2

#10 слайд
Са + Н2 = СаН2 кальций гидриді
Са + Сl2 = СаСl2 кальций хлориді
2Са + О2 = 2СаО кальций оксиді
6Са + 2N2=2Са3N2 кальций нитриді
Ca + 2С =СаС2 кальций карбиді
Жай заттар
10 слайд
Са + Н2 = СаН2 кальций гидриді Са + Сl2 = СаСl2 кальций хлориді 2Са + О2 = 2СаО кальций оксиді 6Са + 2N2=2Са3N2 кальций нитриді Ca + 2С =СаС2 кальций карбиді Жай заттар

#11 слайд
Кальций оксиді — ақ түсті қиын балқитын зат. Техникада оны
"сөндірілмеген әк" деп атайды. Оны әктасты жоғары температурада
(1000 C0 шамасында) қыздырып, ыдырату арқылы алады:
СаС03 =t= СаО + СО2↑- 180кДж
Кальций оксиді — нағыз негіздік оксид. Кальций сілтілікжер
металл болғандықтан, оның оксиді сумен оңай әрекеттесіп кальций
гидроксидін, яғни сілтісін түзеді:
СаО + Н20 = Са(ОН)2 + 70 кДж
11 слайд
Кальций оксиді — ақ түсті қиын балқитын зат. Техникада оны "сөндірілмеген әк" деп атайды. Оны әктасты жоғары температурада (1000 C0 шамасында) қыздырып, ыдырату арқылы алады: СаС03 =t= СаО + СО2↑- 180кДж Кальций оксиді — нағыз негіздік оксид. Кальций сілтілікжер металл болғандықтан, оның оксиді сумен оңай әрекеттесіп кальций гидроксидін, яғни сілтісін түзеді: СаО + Н20 = Са(ОН)2 + 70 кДж

#12 слайд
Лабороторияда көмірқышқыл газын анықтау үшін
қолданады. Әк суына көмір қышқыл газын жібергенде, ол
алдымен ерімейтін карбонат түзіп, лайлана бастайды:
Са(ОН)2 + CO2 = СаСО3↓ + Н2О
Газды одан әрі жібере берсе, лай көрінбей кетеді, өйткені
суда ерімейтін орта тұз ерімтал қышқыл тұзға айналады:
СаСО3 + Н2О + СО2 = Са(НСО3)2
12 слайд
Лабороторияда көмірқышқыл газын анықтау үшін қолданады. Әк суына көмір қышқыл газын жібергенде, ол алдымен ерімейтін карбонат түзіп, лайлана бастайды: Са(ОН)2 + CO2 = СаСО3↓ + Н2О Газды одан әрі жібере берсе, лай көрінбей кетеді, өйткені суда ерімейтін орта тұз ерімтал қышқыл тұзға айналады: СаСО3 + Н2О + СО2 = Са(НСО3)2

#13 слайд
Жаңбыр және басқа да табиғи сулар ауадағы көмірқышкыл газын
ерітіп, көмір қышқылын түзеді:
H2O + CO2 ↔ H2CO3
Кальций гидрокарбонатының ерітіндісі баяу ыдырайды, ал
кыздырғанда, бұл процесс күшейе түседі:
Са(НС03)2 =t= CaCO3↓ + Н20 + C02↑
Табиғатта гипсті CaS04 • 2Н20 өртегенде, өзінің кристалдық
суының біразын жоғалтып, алебастрға айналады:
CaS04 • 2Н2О = CaS04 • 0,5Н20 + 1,5Н20
13 слайд
Жаңбыр және басқа да табиғи сулар ауадағы көмірқышкыл газын ерітіп, көмір қышқылын түзеді: H2O + CO2 ↔ H2CO3 Кальций гидрокарбонатының ерітіндісі баяу ыдырайды, ал кыздырғанда, бұл процесс күшейе түседі: Са(НС03)2 =t= CaCO3↓ + Н20 + C02↑ Табиғатта гипсті CaS04 • 2Н20 өртегенде, өзінің кристалдық суының біразын жоғалтып, алебастрға айналады: CaS04 • 2Н2О = CaS04 • 0,5Н20 + 1,5Н20
#14 слайд
14 слайд

#15 слайд
15 слайд

#16 слайд
16 слайд

#17 слайд
17 слайд

#18 слайд
Ca
Көкөністердің
құрамына Ca
кіреді.
Құрамында кальцийі
бар тағамдар.
18 слайд
Ca Көкөністердің құрамына Ca кіреді. Құрамында кальцийі бар тағамдар.

#19 слайд
Қорытынды
Кальций-белсенді сілтілікжер металы.
Ол оттекпен, бейметалдармен, сумен,
қышқылдармен әрекеттеседі. Маңызды
қосылыстары: сөндірілген әк CaO,
сөндірілген немесе әк суы, әк сүті
Са(OH)2, әктас немесе бор, мәрмәр,
СаСО3, ғаныш СаSO4·2H2O, фосфорит
Ca3(PO4)2 және т.б
19 слайд
Қорытынды Кальций-белсенді сілтілікжер металы. Ол оттекпен, бейметалдармен, сумен, қышқылдармен әрекеттеседі. Маңызды қосылыстары: сөндірілген әк CaO, сөндірілген немесе әк суы, әк сүті Са(OH)2, әктас немесе бор, мәрмәр, СаСО3, ғаныш СаSO4·2H2O, фосфорит Ca3(PO4)2 және т.б

#20 слайд
Тыңдағандарыңызға Тыңдағандарыңызға
көп-көп рақмет !!!!! көп-көп рақмет !!!!!
Келесі сабақта Келесі сабақта
кездескенше!!!кездескенше!!!
20 слайд
Тыңдағандарыңызға Тыңдағандарыңызға көп-көп рақмет !!!!! көп-көп рақмет !!!!! Келесі сабақта Келесі сабақта кездескенше!!!кездескенше!!!

#21 слайд
21 слайд

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
