Ашық сабақ презентация 11 сынып

#1 слайд
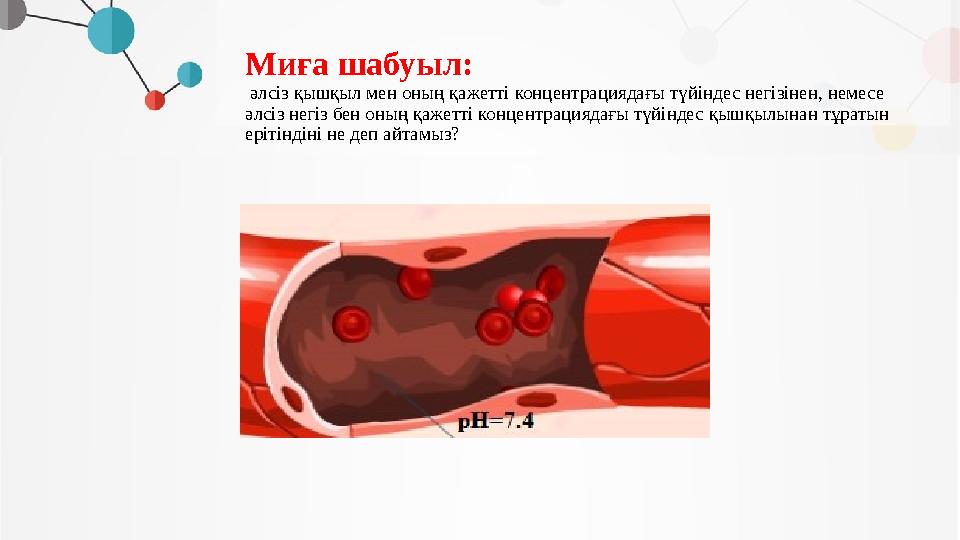
Миға шабуыл:
әлсіз қышқыл мен оның қажетті концентрациядағы түйіндес негізінен, немесе
әлсіз негіз бен оның қажетті концентрациядағы түйіндес қышқылынан тұратын
ерітіндіні не деп айтамыз?
1 слайд
Миға шабуыл: әлсіз қышқыл мен оның қажетті концентрациядағы түйіндес негізінен, немесе әлсіз негіз бен оның қажетті концентрациядағы түйіндес қышқылынан тұратын ерітіндіні не деп айтамыз?

#2 слайд
Буферлі ерітінділер 1
11 ЖМБ сынып химия
18-ші сабақ
2 слайд
Буферлі ерітінділер 1 11 ЖМБ сынып химия 18-ші сабақ

#3 слайд
Оқу мақсаты:
Шаблоны презентаций с сайта presentation-creation.ru
11.3.4.4 - буферлі ерітінділердің қолдану аймағын атау
3 слайд
Оқу мақсаты: Шаблоны презентаций с сайта presentation-creation.ru 11.3.4.4 - буферлі ерітінділердің қолдану аймағын атау

#4 слайд
Сұйылтқанда немесе қышқыл не сілті қосқанда рН–ы өзгермейтiн ертiндiлер буферлiк жүйелер деп
аталады. Буферлiк жүйенiң құрамында протонның доноры және протонның акцепторы болады. Құрамына
байланысты буферлiк жүйелер қышқылдық, негiздiк және амфолиттiк болып бөлiнедi.
Қышқылдық буферлiк жүйе донор болып есептелетiн әлсiз қышқылдан және акцептордың ролiн атқаратын
анионы бар осы қышқылдың тұзынан тұрады. Мысалы, ацетатты, бикарбонатты буферлік жүйелер.
Буферлік жүйелер мен ерітінділер туралы түсініктер,
олардың құрамы және жіктелуі
4 слайд
Сұйылтқанда немесе қышқыл не сілті қосқанда рН–ы өзгермейтiн ертiндiлер буферлiк жүйелер деп аталады. Буферлiк жүйенiң құрамында протонның доноры және протонның акцепторы болады. Құрамына байланысты буферлiк жүйелер қышқылдық, негiздiк және амфолиттiк болып бөлiнедi. Қышқылдық буферлiк жүйе донор болып есептелетiн әлсiз қышқылдан және акцептордың ролiн атқаратын анионы бар осы қышқылдың тұзынан тұрады. Мысалы, ацетатты, бикарбонатты буферлік жүйелер. Буферлік жүйелер мен ерітінділер туралы түсініктер, олардың құрамы және жіктелуі
#5 слайд
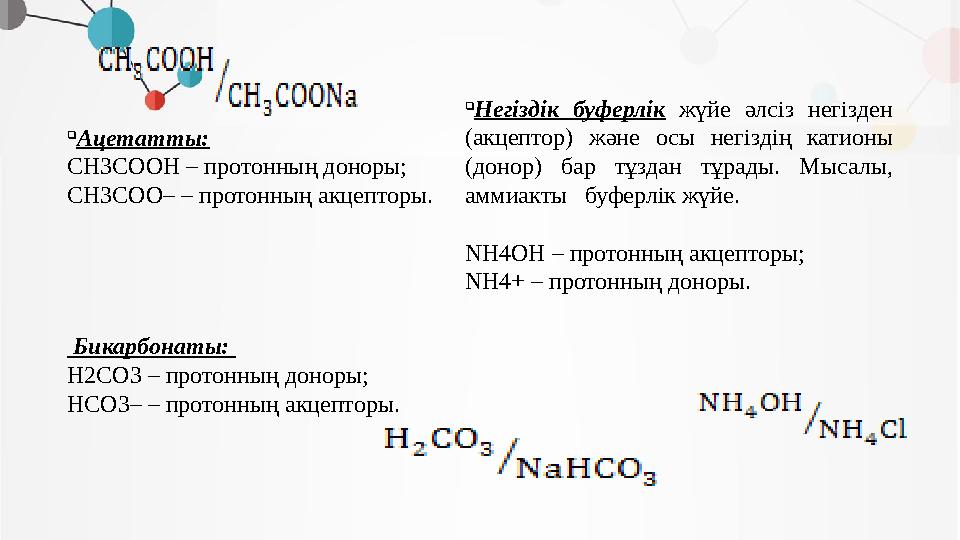
Ацетатты:
CH3COOH – протонның доноры;
CH3COO– – протонның акцепторы.
Негіздік буферлік жүйе әлсіз негізден
(акцептор) және осы негiздiң катионы
(донор) бар тұздан тұрады. Мысалы,
аммиакты буферлік жүйе.
NH4OH – протонның акцепторы;
NH4+ – протонның доноры.
Бикарбонаты:
H2CO3 – протонның доноры;
HCO3– – протонның акцепторы.
5 слайд
Ацетатты: CH3COOH – протонның доноры; CH3COO– – протонның акцепторы. Негіздік буферлік жүйе әлсіз негізден (акцептор) және осы негiздiң катионы (донор) бар тұздан тұрады. Мысалы, аммиакты буферлік жүйе. NH4OH – протонның акцепторы; NH4+ – протонның доноры. Бикарбонаты: H2CO3 – протонның доноры; HCO3– – протонның акцепторы.

#6 слайд
Буферлiк жүйелердiң рН–ына әсер ететiн факторлар
Қышқылдық буферлiк ертiндiлердiң рН–ы мына теңдеумен есептеледi:
Буферлiк ертiндiлердiң рН–ы Гендерсон–Гассельбах теңдеуi бойынша анықталады.
Негiздiк буферлiк ерiтiндiлер үшiн мына теңдеу қолданылады:
немесе
6 слайд
Буферлiк жүйелердiң рН–ына әсер ететiн факторлар Қышқылдық буферлiк ертiндiлердiң рН–ы мына теңдеумен есептеледi: Буферлiк ертiндiлердiң рН–ы Гендерсон–Гассельбах теңдеуi бойынша анықталады. Негiздiк буферлiк ерiтiндiлер үшiн мына теңдеу қолданылады: немесе

#7 слайд
Буферлiк ерiтiндiлердiң әсер ету механизмiнiң жалпы қағидалары
Күштi қышқыл немесе сiлтi қосқанда буферлiк
жүйелердегi сутегi иондары
концентрациясының өзгермеуi олардың негiзгi
қасиетi болып табылады. Күштi қышқыл
қосқанда сутегi иондары буферлiк жүйедегi
протонның акцепторымен әрекеттеседi, соның
нәтижесiнде сутегi иондарының
концентрациясы өзгермейдi. Сiлтi қосқанда
гидроксид–иондар буферлiк жүйедегi
протонның донорымен әрекеттеседi, сол себептi
рН өзгермейдi. Мысалы: Негiздiк буферлiк
жүйеде бұл процесс былай жүредi:
NH4OH + HCl = NH4Cl + H2O
NH4OH + H+ + Cl– = NH4+ + Cl– + H2O
NH4OH + H+ = NH4+ + H2O
NH4Cl + NaOH = NH4OH + NaCl
NH4+ + Cl– + Na+ + OH– = NH4OH + Na+ + Cl–
NH4+ + OH– = NH4OH
7 слайд
Буферлiк ерiтiндiлердiң әсер ету механизмiнiң жалпы қағидалары Күштi қышқыл немесе сiлтi қосқанда буферлiк жүйелердегi сутегi иондары концентрациясының өзгермеуi олардың негiзгi қасиетi болып табылады. Күштi қышқыл қосқанда сутегi иондары буферлiк жүйедегi протонның акцепторымен әрекеттеседi, соның нәтижесiнде сутегi иондарының концентрациясы өзгермейдi. Сiлтi қосқанда гидроксид–иондар буферлiк жүйедегi протонның донорымен әрекеттеседi, сол себептi рН өзгермейдi. Мысалы: Негiздiк буферлiк жүйеде бұл процесс былай жүредi: NH4OH + HCl = NH4Cl + H2O NH4OH + H+ + Cl– = NH4+ + Cl– + H2O NH4OH + H+ = NH4+ + H2O NH4Cl + NaOH = NH4OH + NaCl NH4+ + Cl– + Na+ + OH– = NH4OH + Na+ + Cl– NH4+ + OH– = NH4OH

#8 слайд
Қышқылдық буферлiк жүйелердегi қорғаныс процесiн былай көрсетуге
болады, мысалы :
СН3COONa + HCl = CH3COOH + NaCl
CH3COO– + Na+ + H+ + Cl– = CH3COOH + Na+ + Cl–
CH3COO– + H+ = CH3COOH
Буферлiк жүйе күштi қышқылды әлсiз қышқылға айналдырады, сол себептi рН онша
өзгермейдi.
CH3COOH + NaOH = CH3COONa + Н2О
CH3COOH + Na+ + OH– = CH3COO– + Na+ + H2O
CH3COOH + OH– = CH3COO– + H2O
Буферлiк жүйе OH– ионды суға айналдырады, сол себептi pH өзгермейдi. Осылайша, кез келген
буферлiк жуйеге күштi қышқыл қосқанда буферлiк ерiтiндiдегi протонның акцепторы, ал сiлтi
қосқанда протонның доноры буферлiк жүйенi қорғайды.
8 слайд
Қышқылдық буферлiк жүйелердегi қорғаныс процесiн былай көрсетуге болады, мысалы : СН3COONa + HCl = CH3COOH + NaCl CH3COO– + Na+ + H+ + Cl– = CH3COOH + Na+ + Cl– CH3COO– + H+ = CH3COOH Буферлiк жүйе күштi қышқылды әлсiз қышқылға айналдырады, сол себептi рН онша өзгермейдi. CH3COOH + NaOH = CH3COONa + Н2О CH3COOH + Na+ + OH– = CH3COO– + Na+ + H2O CH3COOH + OH– = CH3COO– + H2O Буферлiк жүйе OH– ионды суға айналдырады, сол себептi pH өзгермейдi. Осылайша, кез келген буферлiк жуйеге күштi қышқыл қосқанда буферлiк ерiтiндiдегi протонның акцепторы, ал сiлтi қосқанда протонның доноры буферлiк жүйенi қорғайды.

#9 слайд
Оксигемоглобин – гемоглобин жүйесi қанның буферлiк сиымдылығының 75%-iн құрайды, ол
гемоглобин ионы (Hb–) мен гемоглобиннiң (HHb) арасындағы тепе-теңдiкпен сипатталады:
HHb – донор
Hb– – акцептор
Hb– + H+ = HHb
HHb + OH– = Hb– + H2O
Сол сияқты бұл жүйе оксигемоглобин ионы (HbO2–) мен окси–гемоглобиннiң (HHbO2)
арасындағы тепе-теңдiкпен де сипатталады:
HHbO2 – протонның доноры
HbO2– – протонның акцепторы
HbO2– + H+ = HHbO2
HHbO2 + OH– = HbO2– + H2O
Екi тепе-теңдiктiң арасындағы байланыс мына теңдеумен көрсетiледi:
HHb + O2 = HHbO2
9 слайд
Оксигемоглобин – гемоглобин жүйесi қанның буферлiк сиымдылығының 75%-iн құрайды, ол гемоглобин ионы (Hb–) мен гемоглобиннiң (HHb) арасындағы тепе-теңдiкпен сипатталады: HHb – донор Hb– – акцептор Hb– + H+ = HHb HHb + OH– = Hb– + H2O Сол сияқты бұл жүйе оксигемоглобин ионы (HbO2–) мен окси–гемоглобиннiң (HHbO2) арасындағы тепе-теңдiкпен де сипатталады: HHbO2 – протонның доноры HbO2– – протонның акцепторы HbO2– + H+ = HHbO2 HHbO2 + OH– = HbO2– + H2O Екi тепе-теңдiктiң арасындағы байланыс мына теңдеумен көрсетiледi: HHb + O2 = HHbO2

#10 слайд
Жұптық жұмыс тапсырмасы:
ҚБ:
Сәйкестендіру
https://wordwall.net/ru/resource/103227203
.
Дескриптор:
буферлі ерітінділердің қолдану аймағын атайды
10 слайд
Жұптық жұмыс тапсырмасы: ҚБ: Сәйкестендіру https://wordwall.net/ru/resource/103227203 . Дескриптор: буферлі ерітінділердің қолдану аймағын атайды
#11 слайд
2топ
1топБуферлі ерітінділер деген не? Олар қалай бөлінеді?
Мысыл келтіріңдер
2 топ Буферлі ерітіндінің әр типіне мысал келтіріп,
сипаттандар
3топ
Буферлі ерітіндінің практикада қолдануына
мысал келтіріңдер
Топтық жұмыс тапсырмасы:
ҚБ:
Дескриптор:
буферлі ерітінділердің қолдану аймағын атайды
11 слайд
2топ 1топБуферлі ерітінділер деген не? Олар қалай бөлінеді? Мысыл келтіріңдер 2 топ Буферлі ерітіндінің әр типіне мысал келтіріп, сипаттандар 3топ Буферлі ерітіндінің практикада қолдануына мысал келтіріңдер Топтық жұмыс тапсырмасы: ҚБ: Дескриптор: буферлі ерітінділердің қолдану аймағын атайды

#12 слайд
Жеке жұмыс тапсырмасы:
Дескриптор:
буферлі ерітінділердің қолдану аймағын атайды
1 тапсырма -6 балл
2 тапсырма -3 балл
3-ші тапсырма-1 балл
2.Функционалдық сауаттылық тапсырмасы
Жағдай:
Сүттің рН ≈ 6,6–6,9. Сүт бұзылғанда бактериялар сүт
қышқылын түзеді → рН төмендейді.
Зауыт сүттің бұзылмауы үшін буфер жүйелері қосады
(фосфат буферлері).
Сұрақ:
Неліктен сүтке буфер қосылады?
Қандай буфер қолайлы?
Егер сүттің рН-ы 6,8-ден 5,8-ге түссе, қандай процесс
жүреді?
3.Берілген жұптардың қайсысы буфер түзеді?
а) HCl + NaCl
ә) CH₃COOH + CH₃COONa
б) NH₃ + NH₄Cl
в) NaOH + NaCl
1.Буферлі ерітінділер
https://wordwall.net/ru/resource/103227604
12 слайд
Жеке жұмыс тапсырмасы: Дескриптор: буферлі ерітінділердің қолдану аймағын атайды 1 тапсырма -6 балл 2 тапсырма -3 балл 3-ші тапсырма-1 балл 2.Функционалдық сауаттылық тапсырмасы Жағдай: Сүттің рН ≈ 6,6–6,9. Сүт бұзылғанда бактериялар сүт қышқылын түзеді → рН төмендейді. Зауыт сүттің бұзылмауы үшін буфер жүйелері қосады (фосфат буферлері). Сұрақ: Неліктен сүтке буфер қосылады? Қандай буфер қолайлы? Егер сүттің рН-ы 6,8-ден 5,8-ге түссе, қандай процесс жүреді? 3.Берілген жұптардың қайсысы буфер түзеді? а) HCl + NaCl ә) CH₃COOH + CH₃COONa б) NH₃ + NH₄Cl в) NaOH + NaCl 1.Буферлі ерітінділер https://wordwall.net/ru/resource/103227604

#13 слайд
Жеке жұмыс жауабы:
2.Функционалдық сауаттылық тапсырмасы
Жауап:
pH-тың түсуі сүттің ұюына, бактерияның көбеюіне әкеледі
→ сақтау мерзімін азайтады.
Фосфат буфері (H₂PO₄ /HPO₄² ).
⁻ ⁻
Сүт қышқылы жиналған → ашу процесі басталған.
3.Жауабы
Буфер түзетіндер:
ә) әлсіз қышқыл + оның тұзы
б) әлсіз негіз + оның тұзы
13 слайд
Жеке жұмыс жауабы: 2.Функционалдық сауаттылық тапсырмасы Жауап: pH-тың түсуі сүттің ұюына, бактерияның көбеюіне әкеледі → сақтау мерзімін азайтады. Фосфат буфері (H₂PO₄ /HPO₄² ). ⁻ ⁻ Сүт қышқылы жиналған → ашу процесі басталған. 3.Жауабы Буфер түзетіндер: ә) әлсіз қышқыл + оның тұзы б) әлсіз негіз + оның тұзы

#14 слайд
ЕББҚ тапсырмасы:
Құрамына қарай буферлік жүйелер қанша түрге бөлінеді?
Берілген жұптардың қайсысы буфер түзеді?
а) HCl + NaCl
ә) CH₃COOH + CH₃COONa
14 слайд
ЕББҚ тапсырмасы: Құрамына қарай буферлік жүйелер қанша түрге бөлінеді? Берілген жұптардың қайсысы буфер түзеді? а) HCl + NaCl ә) CH₃COOH + CH₃COONa

#15 слайд
РЕФЛЕКСИЯ:
Үйге тапсырма: Буферлі ерітінділер
15 слайд
РЕФЛЕКСИЯ: Үйге тапсырма: Буферлі ерітінділер

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
