Атом и молекула


#1 слайд
Атомы и молекулы
1 слайд
Атомы и молекулы

#2 слайд
Атомы
•
Атомы — это маленькие частицы, из
которых состоит вещество. Невозможно
даже представить себе, насколько они
малы. Если сложить в цепочку сто
миллионов атомов, у нас получится
ниточка длиной всего лишь в 1 см. В
тонком листе бумаги, наверное, не меньше
миллиона слоев атомов. Науке известно
более ста видов атомов; соединяясь друг с
другом, они образуют все окружающие
нас вещества.
2 слайд
Атомы • Атомы — это маленькие частицы, из которых состоит вещество. Невозможно даже представить себе, насколько они малы. Если сложить в цепочку сто миллионов атомов, у нас получится ниточка длиной всего лишь в 1 см. В тонком листе бумаги, наверное, не меньше миллиона слоев атомов. Науке известно более ста видов атомов; соединяясь друг с другом, они образуют все окружающие нас вещества.

#3 слайд
СТРУКТУРА АТОМА
•
Атомы состоят из еще меньших,
чем они сами,час-тиц,
называемых элементарными .
Центром атома является его ядро.
Оно состоит из элементарных
частиц двух видов-протонов и
нейтронов. Есть в атоме также
другие элементарные частицы-
электро - ны ; они вращаются
вокруг ядра.
3 слайд
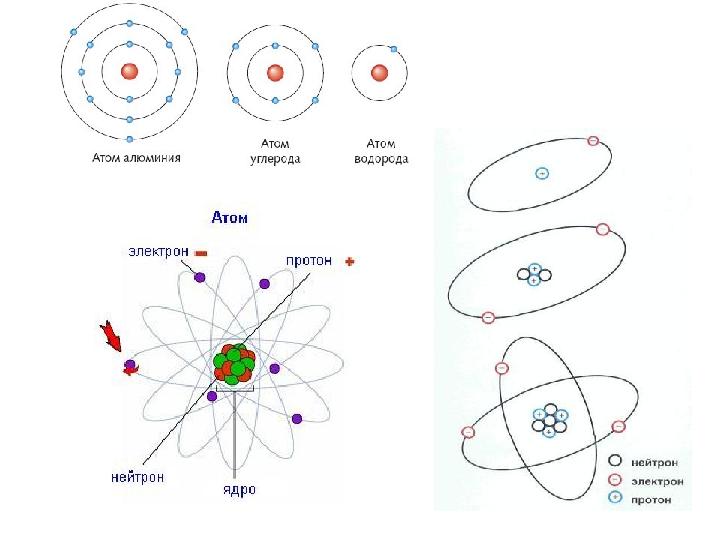
СТРУКТУРА АТОМА • Атомы состоят из еще меньших, чем они сами,час-тиц, называемых элементарными . Центром атома является его ядро. Оно состоит из элементарных частиц двух видов-протонов и нейтронов. Есть в атоме также другие элементарные частицы- электро - ны ; они вращаются вокруг ядра.

#4 слайд
•
Существует множество разных элементарных частиц. Ученые считают, что
протоны и нейтроны состоят из кварков . Элементарные частицы, входящие в
состав атома, удерживаются вместе благодаря своим электрическим зарядам.
Протоны заряжены положительно, а электроны отрицательно. Нейтроны заряда
не имеют, т.е. являются электрически нейтральными. Частицы, несущие
противоположные электрические заряды, притягиваются друг к другу.
Притяжение отрицательно заряженных электронов к положительно заряженным
протонам, находящимся в атомном ядре, удерживает электроны на орбитах около
этого ядра. В состав атома входит одинаковое число положительно заряженных
протонов и отрицательно заряженных электронов, и атом электрически
нейтрален.
4 слайд
• Существует множество разных элементарных частиц. Ученые считают, что протоны и нейтроны состоят из кварков . Элементарные частицы, входящие в состав атома, удерживаются вместе благодаря своим электрическим зарядам. Протоны заряжены положительно, а электроны отрицательно. Нейтроны заряда не имеют, т.е. являются электрически нейтральными. Частицы, несущие противоположные электрические заряды, притягиваются друг к другу. Притяжение отрицательно заряженных электронов к положительно заряженным протонам, находящимся в атомном ядре, удерживает электроны на орбитах около этого ядра. В состав атома входит одинаковое число положительно заряженных протонов и отрицательно заряженных электронов, и атом электрически нейтрален.
#5 слайд
5 слайд

#6 слайд
Электроны
•
Электроны в атоме находятся на разных энергети-ческих
уровнях, или оболочках. Каждая оболочка состоит из
определенного числа электронов. Когда очередная
оболочка заполняется, новые электроны попадают на
следующую оболочку. Большую часть объема атома
занимает пустое пространство между элементарными
частицами. Отрицательно заряжен-ные электроны
удерживаются на своих энергетичес-ких уровнях силой
притяжения к положительно за-ряженным протонам ядра.
6 слайд
Электроны • Электроны в атоме находятся на разных энергети-ческих уровнях, или оболочках. Каждая оболочка состоит из определенного числа электронов. Когда очередная оболочка заполняется, новые электроны попадают на следующую оболочку. Большую часть объема атома занимает пустое пространство между элементарными частицами. Отрицательно заряжен-ные электроны удерживаются на своих энергетичес-ких уровнях силой притяжения к положительно за-ряженным протонам ядра.

#7 слайд
Строения атома
•
Строение атома часто описывают строгой диаграм-
мой,однако сегодня ученые полагают, что электро-ны
существуют на своих орбитах в размытом сос-тоянии. Это
представление отражено на рисунке, где электронные
орбиты представлены в виде «об-лаков». Так вы бы
увидели молекулу под электрон-ным микроскопом.
Равными цветами показаны раз-ные уровни плотности
электронов. Бирюзовым цве-том отмечена область
наибольшей плотности.
7 слайд
Строения атома • Строение атома часто описывают строгой диаграм- мой,однако сегодня ученые полагают, что электро-ны существуют на своих орбитах в размытом сос-тоянии. Это представление отражено на рисунке, где электронные орбиты представлены в виде «об-лаков». Так вы бы увидели молекулу под электрон-ным микроскопом. Равными цветами показаны раз-ные уровни плотности электронов. Бирюзовым цве-том отмечена область наибольшей плотности.

#8 слайд
Атомный номер и атомная масса
•
Атомный номер - это число протонов в
атомном ядре. Как правило, в состав ато-ма
входит одинаковое число протонов и
электронов, поэтому по атомному номе-ру
можно судить и о том, сколько в атоме
электронов. В разных атомах содержится
разное количество протонов. В ядре ато-ма
фосфора 15 протонов и 16 нейтронов, значит,
его атомный номер 15. В ядре атома полония 79
протонов и 118 нейтро-нов: следовательно,
атомный номер золо-та 79.
8 слайд
Атомный номер и атомная масса • Атомный номер - это число протонов в атомном ядре. Как правило, в состав ато-ма входит одинаковое число протонов и электронов, поэтому по атомному номе-ру можно судить и о том, сколько в атоме электронов. В разных атомах содержится разное количество протонов. В ядре ато-ма фосфора 15 протонов и 16 нейтронов, значит, его атомный номер 15. В ядре атома полония 79 протонов и 118 нейтро-нов: следовательно, атомный номер золо-та 79.

#9 слайд
•
Чем больше протонов и нейтронов имеет
атом, тем больше его масса (величина,
показывающая количество вещества в
составе атома). Сумму числа протонов и
числа ней тронов мы называем атомной
массой. Атомная масса фосфора - 31. При
исчислении атомной массы электроны в
расчет не принимаются, так как их масса
ничтожно мала по сравнению с массой атома.
Существует особый прибор- масс-
спектрометр . Он позволяет определить для
каждого данного атома его массу.
9 слайд
• Чем больше протонов и нейтронов имеет атом, тем больше его масса (величина, показывающая количество вещества в составе атома). Сумму числа протонов и числа ней тронов мы называем атомной массой. Атомная масса фосфора - 31. При исчислении атомной массы электроны в расчет не принимаются, так как их масса ничтожно мала по сравнению с массой атома. Существует особый прибор- масс- спектрометр . Он позволяет определить для каждого данного атома его массу.
#10 слайд
•
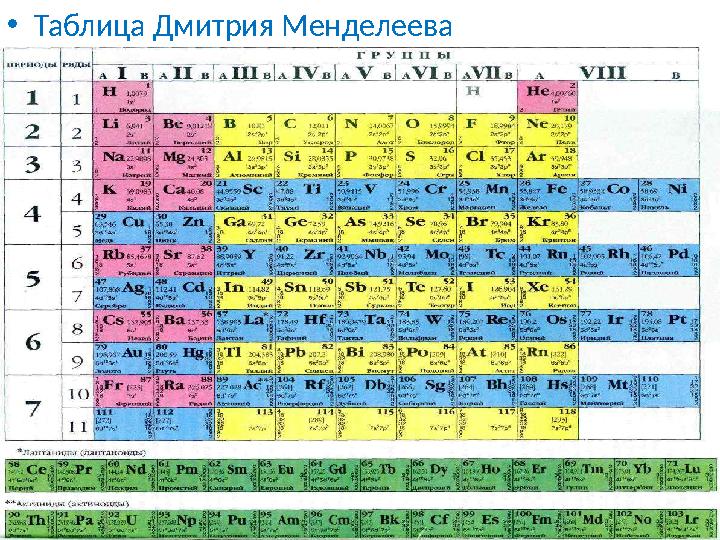
Таблица Дмитрия Менделеева
10 слайд
• Таблица Дмитрия Менделеева

#11 слайд
Изотопы
•
ИзотСЭ пы (от др.-греч . ισος — «равный» , «одинаковый» ,
и τόπος — «место» ) — разновидности атомов (и ядер ) какого-либо
химического элемента , которые имеют одинаковый атомный
(порядковый) номер, но при этом разные массовые числа. Название
связано с тем, что все изотопы одного атома помещаются в одно и то же
место (в одну клетку) таблицы Менделеева. Химические свойства атома
зависят от строения электронной оболочки, которая, в свою очередь,
определяется в основном зарядом ядра Z (то есть количеством протонов
в нём), и почти не зависят от его массового числа A (то есть суммарного
числа протонов Z и нейтронов N ). Все изотопы одного элемента имеют
одинаковый заряд ядра, отличаясь лишь числом нейтронов. Обычно
изотоп обозначается символом химического элемента, к которому он
относится, с добавлением верхнего левого индекса, означающего
массовое число (например, 12
C , 222
Rn ). Можно также написать название
элемента с добавлением через дефис массового числа (например,
углерод-12, радон-222). Некоторые изотопы имеют традиционные
собственные названия (например, дейтерий , актинон ).
Пример изотопов: 16
8 O, 17
8 O, 18
8 O — три стабильных изотопа кислорода.
11 слайд
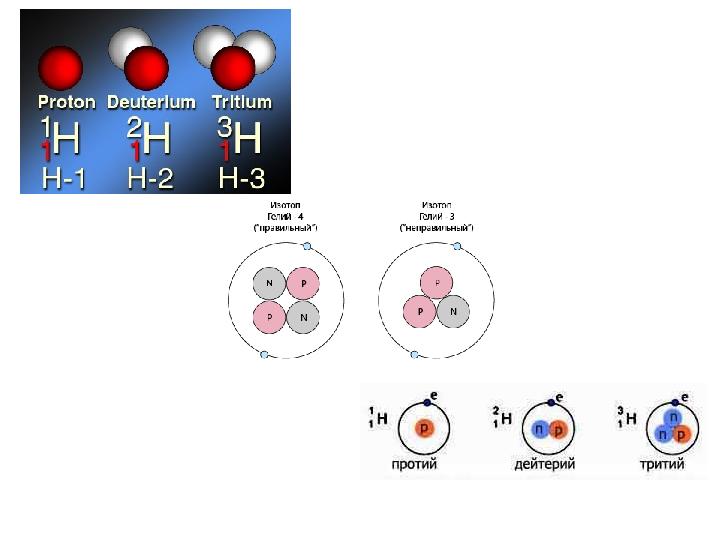
Изотопы • ИзотСЭ пы (от др.-греч . ισος — «равный» , «одинаковый» , и τόπος — «место» ) — разновидности атомов (и ядер ) какого-либо химического элемента , которые имеют одинаковый атомный (порядковый) номер, но при этом разные массовые числа. Название связано с тем, что все изотопы одного атома помещаются в одно и то же место (в одну клетку) таблицы Менделеева. Химические свойства атома зависят от строения электронной оболочки, которая, в свою очередь, определяется в основном зарядом ядра Z (то есть количеством протонов в нём), и почти не зависят от его массового числа A (то есть суммарного числа протонов Z и нейтронов N ). Все изотопы одного элемента имеют одинаковый заряд ядра, отличаясь лишь числом нейтронов. Обычно изотоп обозначается символом химического элемента, к которому он относится, с добавлением верхнего левого индекса, означающего массовое число (например, 12 C , 222 Rn ). Можно также написать название элемента с добавлением через дефис массового числа (например, углерод-12, радон-222). Некоторые изотопы имеют традиционные собственные названия (например, дейтерий , актинон ). Пример изотопов: 16 8 O, 17 8 O, 18 8 O — три стабильных изотопа кислорода.
#12 слайд
12 слайд

#13 слайд
Изотопы
•
У большинства элементов сущест-
вуют изотопы,атомы которых имеют
несколько отличное строение.Коли-
чество протонов и электронов в
атомах изотопов одного элемента
всегда неизменно. Атомы изотопов
различаются числом нейтронов в ядре.
Следовательно, у всех изотопов
одного элемента один и тот же
атомный номер, но разная атомная
масса. На этом рисунке вы видите три
изотопа углерода. У изотопа С 12
есть 6
нейтронов и 6 протонов. С 13
имеет 7
нейтронов. В ядре изотопа С 12
восемь
нейтронов и 6 протонов.
13 слайд
Изотопы • У большинства элементов сущест- вуют изотопы,атомы которых имеют несколько отличное строение.Коли- чество протонов и электронов в атомах изотопов одного элемента всегда неизменно. Атомы изотопов различаются числом нейтронов в ядре. Следовательно, у всех изотопов одного элемента один и тот же атомный номер, но разная атомная масса. На этом рисунке вы видите три изотопа углерода. У изотопа С 12 есть 6 нейтронов и 6 протонов. С 13 имеет 7 нейтронов. В ядре изотопа С 12 восемь нейтронов и 6 протонов.

#14 слайд
•
Физические свойства изотопов различны, но они обла-
дают одинаковыми химическими свойствами. Обычно
большая часть атомов элемента (вещества, состоящего
из атомов одного вида) принадлежит к одному изотопу,
а другие изотопы встречаются в меньших количествах.
14 слайд
• Физические свойства изотопов различны, но они обла- дают одинаковыми химическими свойствами. Обычно большая часть атомов элемента (вещества, состоящего из атомов одного вида) принадлежит к одному изотопу, а другие изотопы встречаются в меньших количествах.

#15 слайд
Представление об атомах
•
Мысль о том, что всё в природе состоит из атомов,
возникла давно. Еще 2500 лет назад древнегреческие
философы полага ли, что вещество состоит из таких
частиц, которые нельзя разделить. Само слово
«атом» восходит к греческому слову «атомос», что
значит «неделимый». В Древней Греции философы
обсуждали гипотезу о том, что всё вещество в мире
состоит из неделимых частиц. Правда, Аристотель в
этом сомневался.
15 слайд
Представление об атомах • Мысль о том, что всё в природе состоит из атомов, возникла давно. Еще 2500 лет назад древнегреческие философы полага ли, что вещество состоит из таких частиц, которые нельзя разделить. Само слово «атом» восходит к греческому слову «атомос», что значит «неделимый». В Древней Греции философы обсуждали гипотезу о том, что всё вещество в мире состоит из неделимых частиц. Правда, Аристотель в этом сомневался.

#16 слайд
•
Термин «атом» был впервые использован английским
химиком Джоном Дальтоном (1766- 1844). В 1807 г.
Дальтон выдвинул свою атомную теорию. Атомами
он назвал составляющие всякое вещество малые час-
тицы, которые не изменяются входе химических
реакций. Согласно Дальтону, химическая реакция -это
процесс, при котором атомы соединяются вместе или
отделяются друг от друга. Атомная теория Дальтона
лежит в основе представлений современных ученых.
16 слайд
• Термин «атом» был впервые использован английским химиком Джоном Дальтоном (1766- 1844). В 1807 г. Дальтон выдвинул свою атомную теорию. Атомами он назвал составляющие всякое вещество малые час- тицы, которые не изменяются входе химических реакций. Согласно Дальтону, химическая реакция -это процесс, при котором атомы соединяются вместе или отделяются друг от друга. Атомная теория Дальтона лежит в основе представлений современных ученых.

#17 слайд
•
В начале нашего столетия ученые начали строить
модели атомов. Эрнест Резерфорд (1871-1937)
показал, что отрицательно заряженные электроны
обращаются вокруг положительно заряженного ядра.
Нильс Бор (1885-1962) утверждал, что электроны об-
ращаются по определенным орбитам. В 1932 г.
Джеймс Чедвик (1891-1974) установил, что ядро ато-
ма состоит из частиц, которые он назвал протонами
и нейтронами .
Э .Резерфорд Н.Бор Д.Чедвик
17 слайд
• В начале нашего столетия ученые начали строить модели атомов. Эрнест Резерфорд (1871-1937) показал, что отрицательно заряженные электроны обращаются вокруг положительно заряженного ядра. Нильс Бор (1885-1962) утверждал, что электроны об- ращаются по определенным орбитам. В 1932 г. Джеймс Чедвик (1891-1974) установил, что ядро ато- ма состоит из частиц, которые он назвал протонами и нейтронами . Э .Резерфорд Н.Бор Д.Чедвик

#18 слайд
18 слайд

#19 слайд
Молекулы
•
МолоЭкула — электрически нейтральная частица, образованная из двух или
более связанных ковалентными связями атомов
В физике к молекулам
причисляют также одноатомные молекулы, то есть свободные (химически не
связанные) атомы.Причисление к молекулам одноатомных молекул, то есть
свободных атомов, например одноатомных газов, приво-дит к совмещению
понятий «молекула» и «атом». Обычно подразуме-вается, что молекулы
нейтральны (не несут электрических зарядов) и не несут
неспаренных электронов (все валентности насыщены); заряжен-ные
молекулы называют ионами, молекулы с мультиплетностью, отлич-ной
от единицы (то есть с неспаренными электронами и ненасыщенными
валентностями)-радикалами.
•
Молекулы относительно высокой молекулярной массы , состоящие из
повторяющихся низкомолекулярных фрагментов , называются макромо-
лекулами .
•
С точки зрения квантовой механики молекула представляет собой сис-тему
не из атомов, а из электронов и атомных ядер, взаимодействующих между
собой.
•
Особенности строения молекул определяют физические свойства вещества,
состоящего из этих молекул.
•
Состав молекул сложных веществ выражается при помощи химических
формул .
19 слайд
Молекулы • МолоЭкула — электрически нейтральная частица, образованная из двух или более связанных ковалентными связями атомов В физике к молекулам причисляют также одноатомные молекулы, то есть свободные (химически не связанные) атомы.Причисление к молекулам одноатомных молекул, то есть свободных атомов, например одноатомных газов, приво-дит к совмещению понятий «молекула» и «атом». Обычно подразуме-вается, что молекулы нейтральны (не несут электрических зарядов) и не несут неспаренных электронов (все валентности насыщены); заряжен-ные молекулы называют ионами, молекулы с мультиплетностью, отлич-ной от единицы (то есть с неспаренными электронами и ненасыщенными валентностями)-радикалами. • Молекулы относительно высокой молекулярной массы , состоящие из повторяющихся низкомолекулярных фрагментов , называются макромо- лекулами . • С точки зрения квантовой механики молекула представляет собой сис-тему не из атомов, а из электронов и атомных ядер, взаимодействующих между собой. • Особенности строения молекул определяют физические свойства вещества, состоящего из этих молекул. • Состав молекул сложных веществ выражается при помощи химических формул .
#20 слайд
•
Атомы редко встречаются и свободном состоянии. Как правило, они
связываются друг с другом и образуют молекулы либо другие, более
массивные структуры. Молекула-это мельчайшая частица вещества, которая
может существовать самостоятельно. Она состоит из атомов, удерживающихся
вместе при помощи связей. Например, у молекулы воды два
атома
водорода связанны с атомом кислорода. Атомы удер-живаются вместе
благодаря
электрическим зарядам частиц, из которых они состоят. Описывая
строение молекул, ученые прибегают к помощи моделей . Как правило, они
пользуются структурными и пространствен-ными моделями. Структурные
модели представляют связи, удерживаю-щие атомы вместе, в виде палочек. В
пространственных моделях атомы плотно соединены друг с другом. Конечно,
модель не похожа на настоящую молекулу. Модели строятся для того, что
бы
показать, из каких атомов та или иная молекула состоит.
20 слайд
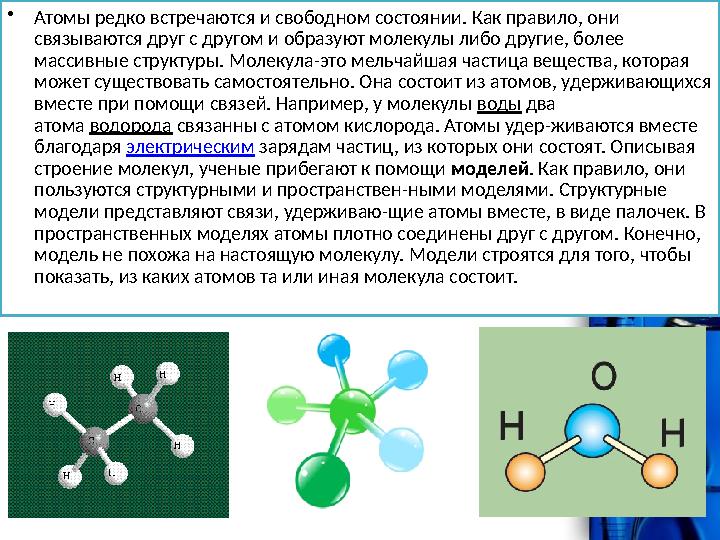
• Атомы редко встречаются и свободном состоянии. Как правило, они связываются друг с другом и образуют молекулы либо другие, более массивные структуры. Молекула-это мельчайшая частица вещества, которая может существовать самостоятельно. Она состоит из атомов, удерживающихся вместе при помощи связей. Например, у молекулы воды два атома водорода связанны с атомом кислорода. Атомы удер-живаются вместе благодаря электрическим зарядам частиц, из которых они состоят. Описывая строение молекул, ученые прибегают к помощи моделей . Как правило, они пользуются структурными и пространствен-ными моделями. Структурные модели представляют связи, удерживаю-щие атомы вместе, в виде палочек. В пространственных моделях атомы плотно соединены друг с другом. Конечно, модель не похожа на настоящую молекулу. Модели строятся для того, что бы показать, из каких атомов та или иная молекула состоит.
#21 слайд
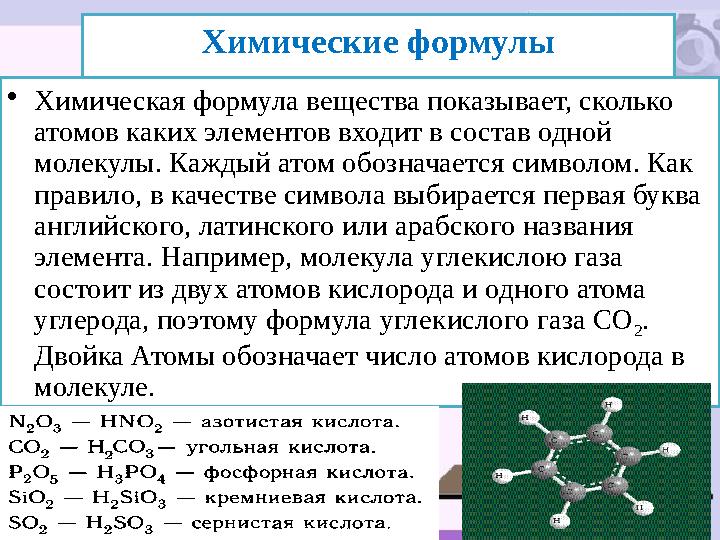
Химические формулы
•
Химическая формула вещества показывает, сколько
атомов каких элементов входит в состав одной
молекулы. Каждый атом обозначается символом. Как
правило, в качестве символа выбирается первая буква
английского, латинского или арабского названия
элемента. Например, молекула углекислою газа
состоит из двух атомов кислорода и одного атома
углерода, поэтому формула угле кислого газа СО
2 .
Двойка Атомы обозначает число атомов кислорода в
молекуле.
21 слайд
Химические формулы • Химическая формула вещества показывает, сколько атомов каких элементов входит в состав одной молекулы. Каждый атом обозначается символом. Как правило, в качестве символа выбирается первая буква английского, латинского или арабского названия элемента. Например, молекула углекислою газа состоит из двух атомов кислорода и одного атома углерода, поэтому формула угле кислого газа СО 2 . Двойка Атомы обозначает число атомов кислорода в молекуле.

#22 слайд
•
Этот опыт продемонстрирует вам, что
молекулы вещества удерживают ся вместе
силами притя-жения. На
полните стакан водой
до краев. Осто-рожно опустите в стакан
несколько монет. Вы увидите, что над краями
стакана приподнялся водяной купол. Сила ,
притягивающая молекулы воды друг к другу,
может удержать некоторое количество воды
над краями стакана. Эта сила называется
силой поверхностного натяжения .
22 слайд
• Этот опыт продемонстрирует вам, что молекулы вещества удерживают ся вместе силами притя-жения. На полните стакан водой до краев. Осто-рожно опустите в стакан несколько монет. Вы увидите, что над краями стакана приподнялся водяной купол. Сила , притягивающая молекулы воды друг к другу, может удержать некоторое количество воды над краями стакана. Эта сила называется силой поверхностного натяжения .

#23 слайд
Спасибо за
внимания!
Слайд подготовила : Еламан Аружан
23 слайд
Спасибо за внимания! Слайд подготовила : Еламан Аружан

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
