Авогадро заңы. Молярлық көлем


#1 слайд
Тақырыбы: Авогадро заңы. Молярлық көлем
8-сынып
1 слайд
Тақырыбы: Авогадро заңы. Молярлық көлем 8-сынып

#2 слайд
2
8.2.3.6 - Авогадро заңын білу, қалыпты және стандартты жағдайлардағы
газдар көлемін есептеуде молярлық көлемді қолдану
заттың жану реакциясының өнімі көбінесе оксид екенін және
Оқу мақсаты
Бағалау критерийлері
Авогадро заңын білу, қалыпты және стандартты жағдайлардағы
газдар көлемін есептеуде молярлық көлемді қолданады
2 слайд
2 8.2.3.6 - Авогадро заңын білу, қалыпты және стандартты жағдайлардағы газдар көлемін есептеуде молярлық көлемді қолдану заттың жану реакциясының өнімі көбінесе оксид екенін және Оқу мақсаты Бағалау критерийлері Авогадро заңын білу, қалыпты және стандартты жағдайлардағы газдар көлемін есептеуде молярлық көлемді қолданады

#3 слайд
Авогадро заңы
Газдарға арналған заңдардың бірі – Авогадро заңы
Газ (фр. «gaz», грек «chaos» - бей - берекет) – заттың атомдары
мен молекулалары бір- бірімен әлсіз байланысқандықтан, кез
келген бағытта еркін қозғалатын және өзіне берілген көлемге
толық жайылып орналасатын агрегаттық күйі.
3
3 слайд
Авогадро заңы Газдарға арналған заңдардың бірі – Авогадро заңы Газ (фр. «gaz», грек «chaos» - бей - берекет) – заттың атомдары мен молекулалары бір- бірімен әлсіз байланысқандықтан, кез келген бағытта еркін қозғалатын және өзіне берілген көлемге толық жайылып орналасатын агрегаттық күйі. 3

#4 слайд
Авогадро заңы
Өзінің зерттеулері мен Бойль-Мариотт және Гей-Люссак заңдарына
сүйеніп (барлық газдар бірдей сығылады және термиялық ұлғаю
коэффициенттері бірдей), итальяндық ғалым Амадео Авогадро 1811
жылы болжам жасап, газдар жайлы заң ұсынды
4
4 слайд
Авогадро заңы Өзінің зерттеулері мен Бойль-Мариотт және Гей-Люссак заңдарына сүйеніп (барлық газдар бірдей сығылады және термиялық ұлғаю коэффициенттері бірдей), итальяндық ғалым Амадео Авогадро 1811 жылы болжам жасап, газдар жайлы заң ұсынды 4
#5 слайд
Отын
5
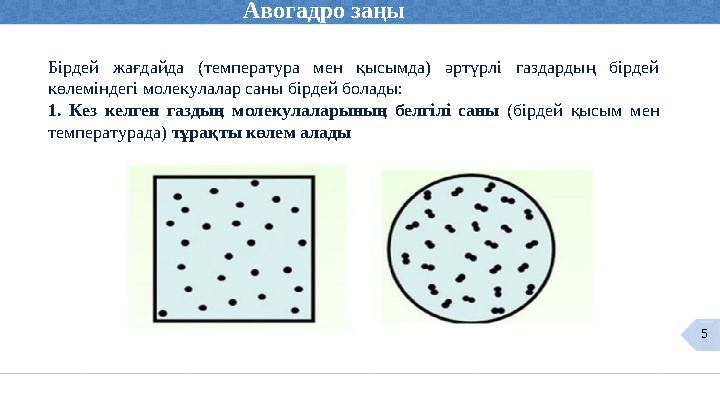
Бірдей жағдайда (температура мен қысымда) әртүрлі газдардың бірдей
көлеміндегі молекулалар саны бірдей болады:
1. Кез келген газдың молекулаларының белгілі саны (бірдей қысым мен
температурада) тұрақты көлем алады
Авогадро заңы
5
5 слайд
Отын 5 Бірдей жағдайда (температура мен қысымда) әртүрлі газдардың бірдей көлеміндегі молекулалар саны бірдей болады: 1. Кез келген газдың молекулаларының белгілі саны (бірдей қысым мен температурада) тұрақты көлем алады Авогадро заңы 5

#6 слайд
Авогадро заңы
6
2. Қалыпты жағдайда (қ.ж. Т=273
0
K, p=101,3 кПа немесе 0
0
температура, 1 атмосфералық қысым)
кез келген газдың 1 молі 22,4 л көлем алады,
ол мольдік көлем деп аталып, V
m
деп белгіленеді, өлшемі л/моль
6 слайд
Авогадро заңы 6 2. Қалыпты жағдайда (қ.ж. Т=273 0 K, p=101,3 кПа немесе 0 0 температура, 1 атмосфералық қысым) кез келген газдың 1 молі 22,4 л көлем алады, ол мольдік көлем деп аталып, V m деп белгіленеді, өлшемі л/моль
#7 слайд
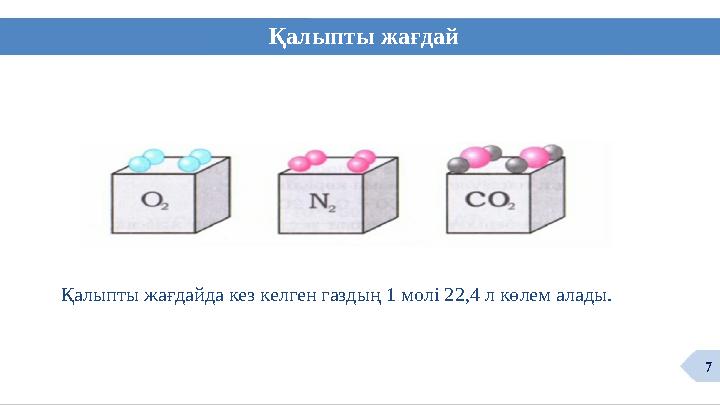
Қалыпты жағдай
Қалыпты жағдайда кез келген газдың 1 молі 22,4 л көлем алады.
7
7 слайд
Қалыпты жағдай Қалыпты жағдайда кез келген газдың 1 молі 22,4 л көлем алады. 7
#8 слайд
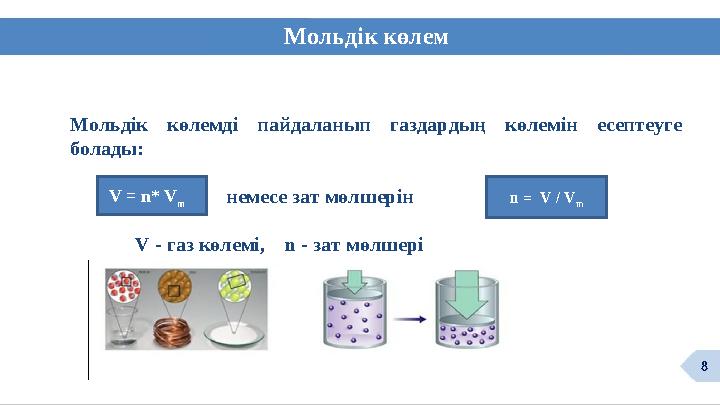
Мольдік көлем
Мольдік көлемді пайдаланып газдардың көлемін есептеуге
болады:
немесе зат мөлшерін
V - газ көлемі, n - зат мөлшері
8
V = n* V
m
n = V / V
m
8 слайд
Мольдік көлем Мольдік көлемді пайдаланып газдардың көлемін есептеуге болады: немесе зат мөлшерін V - газ көлемі, n - зат мөлшері 8 V = n* V m n = V / V m

#9 слайд
9
Есептер шығару
1 - есеп. Зат мөлшері 2 моль азот (қ.ж) қандай көлем алады?
Берілгені: Шешуі:
n (N
2
) = 2 моль V (N
2
) = n* V
m
= 2 моль * 22,4 л/моль =44,8 л
V
m
= 22,4 л/моль
Жауабы: V (N
2
) = 44,8 л
V (N
2
) - ?
9
9 слайд
9 Есептер шығару 1 - есеп. Зат мөлшері 2 моль азот (қ.ж) қандай көлем алады? Берілгені: Шешуі: n (N 2 ) = 2 моль V (N 2 ) = n* V m = 2 моль * 22,4 л/моль =44,8 л V m = 22,4 л/моль Жауабы: V (N 2 ) = 44,8 л V (N 2 ) - ? 9
#10 слайд
10
Есептер шығару
2 - есеп. Көлемі 112 л (қ.ж) азоттың зат мөлшерін есептеңіз?
Берілгені: Шешуі:
Зат мөлшерін мына формуламен табамыз: n= V / V
m
V (N
2
) = 112 литр n (N
2
) = 112 л / 22,4 л/моль = 5 моль
V
m = 22,4 л/моль
Жауабы: n (N
2
) = 5 моль
n (N
2
) - ?
10 слайд
10 Есептер шығару 2 - есеп. Көлемі 112 л (қ.ж) азоттың зат мөлшерін есептеңіз? Берілгені: Шешуі: Зат мөлшерін мына формуламен табамыз: n= V / V m V (N 2 ) = 112 литр n (N 2 ) = 112 л / 22,4 л/моль = 5 моль V m = 22,4 л/моль Жауабы: n (N 2 ) = 5 моль n (N 2 ) - ?

#11 слайд
Есептер шығару
11
11 слайд
Есептер шығару 11

#12 слайд
12
Бекіту тапсырмасы
1 тапсырма:
Массасы 4 г метан (CH
4
) газының көлемін қ.ж табыңыз.
12 слайд
12 Бекіту тапсырмасы 1 тапсырма: Массасы 4 г метан (CH 4 ) газының көлемін қ.ж табыңыз.

#13 слайд
13
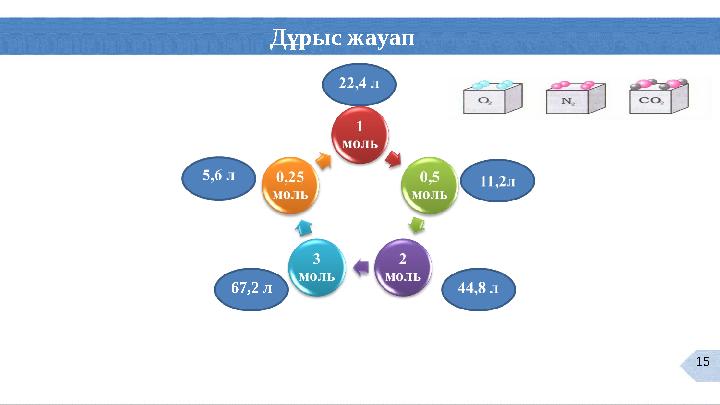
Дұрыс жауап
13 слайд
13 Дұрыс жауап

#14 слайд
Бекіту тапсырмасы
14
2 тапсырма
Берілген зат мөлшерін газдың (қ.ж) көлемдерімен сәйкестендіріңіз.
11,2л
22,4 л
5,6 л
67,2 л
44,8 л
14
14 слайд
Бекіту тапсырмасы 14 2 тапсырма Берілген зат мөлшерін газдың (қ.ж) көлемдерімен сәйкестендіріңіз. 11,2л 22,4 л 5,6 л 67,2 л 44,8 л 14
#15 слайд
15
Дұрыс жауап
44,8 л
67,2 л
15
15 слайд
15 Дұрыс жауап 44,8 л 67,2 л 15

#16 слайд
16
Оқу тапсырмасы
Қандай жағдайлар қалыпты және стандартты деп
аталады?
Молярлық көлемнің мәні қандай?
16 слайд
16 Оқу тапсырмасы Қандай жағдайлар қалыпты және стандартты деп аталады? Молярлық көлемнің мәні қандай?

#17 слайд
17
Қорытынды
Бүгінгі сабақта:
Авогадро заңын білдіңіз, қалыпты және
стандартты жағдайлардағы газдар көлемін
есептеуде молярлық көлемді қолдануды үйрендіңіз.
17 слайд
17 Қорытынды Бүгінгі сабақта: Авогадро заңын білдіңіз, қалыпты және стандартты жағдайлардағы газдар көлемін есептеуде молярлық көлемді қолдануды үйрендіңіз.

#18 слайд
18
Қосымша ресурстар
М.Б.Усманова, Қ.Н. Сақариянова, Б.Н.Сахариева
Химия оқулығы 8- сынып.
https://bilimland.kz/kk/subject/ximiya/8-synyp/
18 слайд
18 Қосымша ресурстар М.Б.Усманова, Қ.Н. Сақариянова, Б.Н.Сахариева Химия оқулығы 8- сынып. https://bilimland.kz/kk/subject/ximiya/8-synyp/

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
