Химиялық реакциялардың жылдамдығы


#1 слайд
Сабақтың тақырыбы:
Масса, молярлық масса және зат мөлшері арасындағы
байланыс
1 слайд
Сабақтың тақырыбы: Масса, молярлық масса және зат мөлшері арасындағы байланыс

#2 слайд
8.1.1.3 -масса, зат мөлшері және
құрылымдық бөлшектер санын есептеу
Сабақтың мақсаты:
2 слайд
8.1.1.3 -масса, зат мөлшері және құрылымдық бөлшектер санын есептеу Сабақтың мақсаты:

#3 слайд
Топтарға бөлу
«Тілек алаңы»
1-топ «Лавуазье»
2-топ «Ломоносов»
3-топ «Авогадро»
3 слайд
Топтарға бөлу «Тілек алаңы» 1-топ «Лавуазье» 2-топ «Ломоносов» 3-топ «Авогадро»

#4 слайд
Сабақтағы көңіл күйің қандай?
4 слайд
Сабақтағы көңіл күйің қандай?

#5 слайд
Ой қозғау
«Атаулар кестесі» әдісі
Физикалық
өлшемдер
Белгіленуі Өлшем
бірліктері
Зат мөлшері моль
N
Көлем л
М
N
A
моль
-1
Дескриптор:
Физикалық
өлшем
бірліктерді және
белгіленуін
табады.
5 слайд
Ой қозғау «Атаулар кестесі» әдісі Физикалық өлшемдер Белгіленуі Өлшем бірліктері Зат мөлшері моль N Көлем л М N A моль -1 Дескриптор: Физикалық өлшем бірліктерді және белгіленуін табады.
#6 слайд
Физикалық
өлшемдер
Белгіленуі Өлшем бірліктері
Зат мөлшері
n
моль
Бөлшектер саны
N
Құрылымдық
бөлшектердің атауы
Көлем
V
л
Молярлық масса
М
г/моль
Авогадро саны
N
A
моль
-1
6 слайд
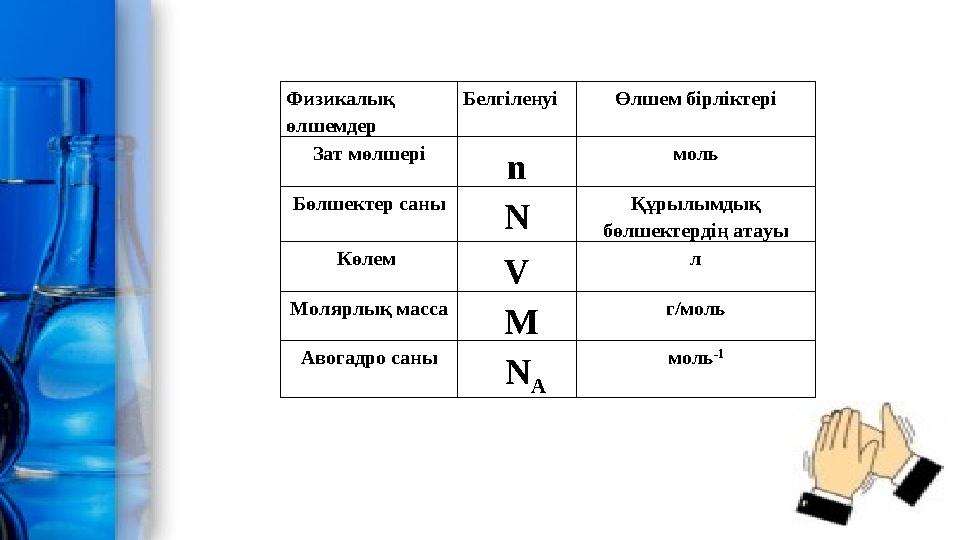
Физикалық өлшемдер Белгіленуі Өлшем бірліктері Зат мөлшері n моль Бөлшектер саны N Құрылымдық бөлшектердің атауы Көлем V л Молярлық масса М г/моль Авогадро саны N A моль -1
#7 слайд
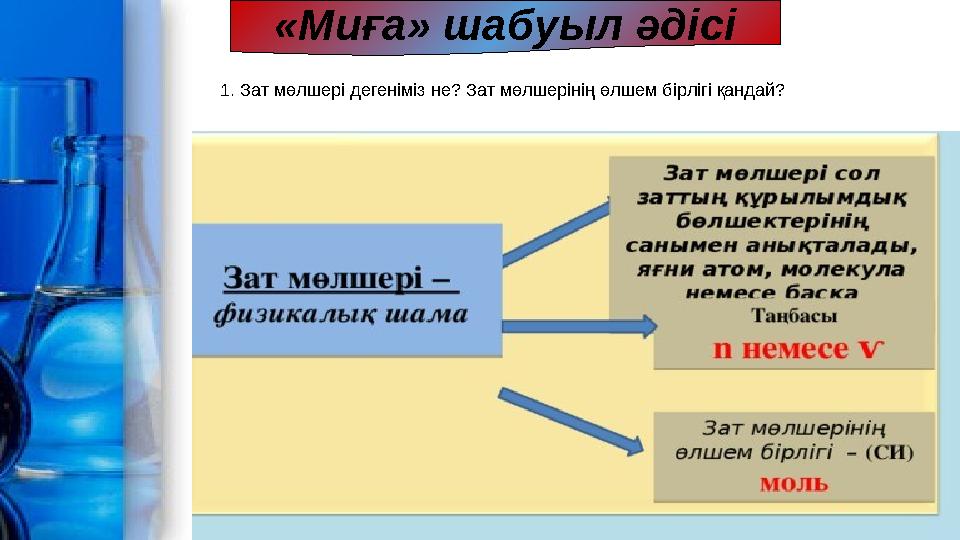
1. Зат мөлшері дегеніміз не? Зат мөлшерінің өлшем бірлігі қандай?
«Миға» шабуыл әдісі
7 слайд
1. Зат мөлшері дегеніміз не? Зат мөлшерінің өлшем бірлігі қандай? «Миға» шабуыл әдісі

#8 слайд
8 слайд

#9 слайд
«Зат мөлшері» аялдамасы
1-топ 126 г азот қышқылының
(HNO
3
) (қ.ж) зат мөлшері қанша?
2-топ 128г оттегінің (O
2
)(қ.ж) зат
мөлшері қанша?
3-топ 51г аммиактың (NH
3
)(қ.ж) зат
мөлшері қанша?
«Ойлан, жұптас, бөліс» әдісі
Дескриптор:
•Азот қышқылының зат мөлшерін табады
•Оттегінің зат мөлшерін табады
•Аммиактың зат мөлшерін дұрыс есептейді
9 слайд
«Зат мөлшері» аялдамасы 1-топ 126 г азот қышқылының (HNO 3 ) (қ.ж) зат мөлшері қанша? 2-топ 128г оттегінің (O 2 )(қ.ж) зат мөлшері қанша? 3-топ 51г аммиактың (NH 3 )(қ.ж) зат мөлшері қанша? «Ойлан, жұптас, бөліс» әдісі Дескриптор: •Азот қышқылының зат мөлшерін табады •Оттегінің зат мөлшерін табады •Аммиактың зат мөлшерін дұрыс есептейді

#10 слайд
Амедео Авогадро (1776-1856)
1776 жылы 9 тамызда Туринде
дүниеге келген итальяндық физик. Ол
зат құрылысының атомдық теориясын
дамытуға
үлесін қосқан елеулі ғалымдардың бірі.
Турин Университетінің математикалық
физика профессоры Авогадро саны
ұғымын алғаш боп енгізді, Авогадро
заңын шығарып,
атомдық және молекулалық массаны
анықтау әдісін ойлап тапты.
10 слайд
Амедео Авогадро (1776-1856) 1776 жылы 9 тамызда Туринде дүниеге келген итальяндық физик. Ол зат құрылысының атомдық теориясын дамытуға үлесін қосқан елеулі ғалымдардың бірі. Турин Университетінің математикалық физика профессоры Авогадро саны ұғымын алғаш боп енгізді, Авогадро заңын шығарып, атомдық және молекулалық массаны анықтау әдісін ойлап тапты.

#11 слайд
Авогадро заңы бойынша сұйық және газ тәрізді заттардың
қалыпты жағдайдағы көлемі қандай? Авогадро тұрақтысы
қаншаға тең?
11 слайд
Авогадро заңы бойынша сұйық және газ тәрізді заттардың қалыпты жағдайдағы көлемі қандай? Авогадро тұрақтысы қаншаға тең?

#12 слайд
«Авогадро заңы» аялдамасы
3-тапсырма тестпен жұмыс
1.Идеал газдардың бірдей көлемдерінде молекула саны бірдей болатынын ашқан ғалым
А) М.В.Ломоносов
В) Д.И.Менделеев
С) А.Авогадро
D) А.Л.Лавуазье
2.Авогадро тұрақтысы қаншаға тең?
А) 60,2*10
23
В) 12,4*10
23
С) 602*10
23
D) 6,02*10
23
3.Қалыпты жағдайда газдың 1молінің көлемі қаншаға тең?
А) 224л
В) 2,24л
С) 22,4л
D) 6,02*10
23
л
4.Авогадро тұрақтысы қандай белгіленеді?
А) N
В) N
A
С) M
D) M
A
5. 2моль оттектің молекула саны қанша?
А) 1,204*10
23
В) 3,01*10
23
С) 12,04*10
23
D) 6,02*10
23
«Кім жылдам» әдісі
Дескриптор:
Тест тапсырмаларын орындайды
12 слайд
«Авогадро заңы» аялдамасы 3-тапсырма тестпен жұмыс 1.Идеал газдардың бірдей көлемдерінде молекула саны бірдей болатынын ашқан ғалым А) М.В.Ломоносов В) Д.И.Менделеев С) А.Авогадро D) А.Л.Лавуазье 2.Авогадро тұрақтысы қаншаға тең? А) 60,2*10 23 В) 12,4*10 23 С) 602*10 23 D) 6,02*10 23 3.Қалыпты жағдайда газдың 1молінің көлемі қаншаға тең? А) 224л В) 2,24л С) 22,4л D) 6,02*10 23 л 4.Авогадро тұрақтысы қандай белгіленеді? А) N В) N A С) M D) M A 5. 2моль оттектің молекула саны қанша? А) 1,204*10 23 В) 3,01*10 23 С) 12,04*10 23 D) 6,02*10 23 «Кім жылдам» әдісі Дескриптор: Тест тапсырмаларын орындайды

#13 слайд
«Авогадро заңы» аялдамасы
3-тапсырма тестпен жұмыс
1.Идеал газдардың бірдей көлемдерінде молекула саны бірдей болатынын ашқан ғалым
А) М.В.Ломоносов
В) Д.И.Менделеев
С) А.Авогадро
D) А.Л.Лавуазье
2.Авогадро тұрақтысы қаншаға тең?
А) 60,2*10
23
В) 12,4*10
23
С) 602*10
23
D) 6,02*10
23
3.Қалыпты жағдайда газдың 1молінің көлемі қаншаға тең?
А) 224л
В) 2,24л
С) 22,4л
D) 6,02*10
23
л
4.Авогадро тұрақтысы қандай белгіленеді?
А) N
В) N
A
С) M
D) M
A
5. 2моль оттектің молекула саны қанша?
А) 1,204*10
23
В) 3,01*10
23
С) 12,04*10
23
D) 6,02*10
23
«Кім жылдам» әдісі
Дескриптор:
Тест тапсырмаларын орындайды
13 слайд
«Авогадро заңы» аялдамасы 3-тапсырма тестпен жұмыс 1.Идеал газдардың бірдей көлемдерінде молекула саны бірдей болатынын ашқан ғалым А) М.В.Ломоносов В) Д.И.Менделеев С) А.Авогадро D) А.Л.Лавуазье 2.Авогадро тұрақтысы қаншаға тең? А) 60,2*10 23 В) 12,4*10 23 С) 602*10 23 D) 6,02*10 23 3.Қалыпты жағдайда газдың 1молінің көлемі қаншаға тең? А) 224л В) 2,24л С) 22,4л D) 6,02*10 23 л 4.Авогадро тұрақтысы қандай белгіленеді? А) N В) N A С) M D) M A 5. 2моль оттектің молекула саны қанша? А) 1,204*10 23 В) 3,01*10 23 С) 12,04*10 23 D) 6,02*10 23 «Кім жылдам» әдісі Дескриптор: Тест тапсырмаларын орындайды

#14 слайд
Жауаптары
1.С
2.D
3.C
4.B
5.C
14 слайд
Жауаптары 1.С 2.D 3.C 4.B 5.C
#15 слайд
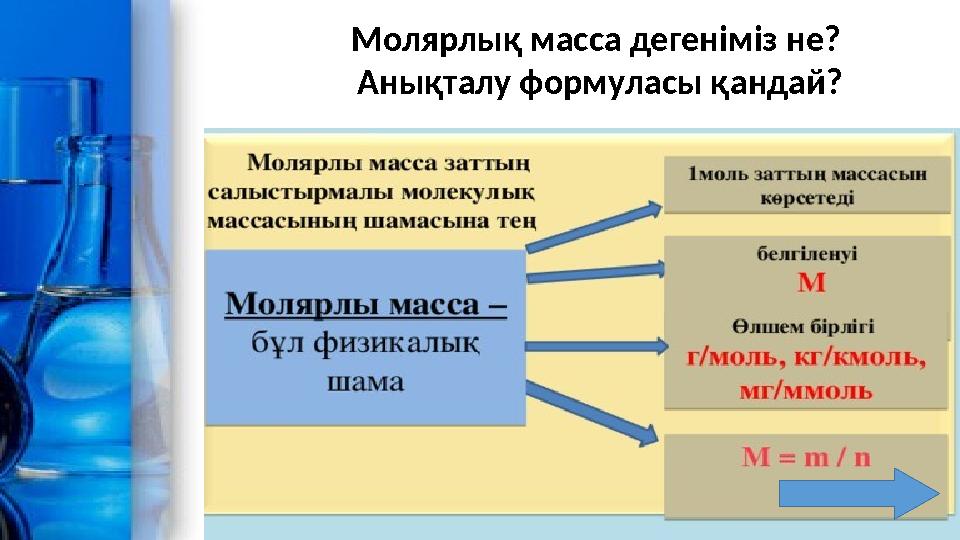
Молярлық масса дегеніміз не?
Анықталу формуласы қандай?
15 слайд
Молярлық масса дегеніміз не? Анықталу формуласы қандай?

#16 слайд
Заттың керекті мөлшерін қалай өлшеп
алуға болады?
16 слайд
Заттың керекті мөлшерін қалай өлшеп алуға болады?
#17 слайд
Зат Молекула саны
N = N
A ∙ n
Молярлық масса
M = m/n
Моль саны
n = m/M
Заттың массасы
m = M ∙ n
1-топ:H
2
5 Моль
2-топ :S 32г
3-топ:Fe 12,04*10
23
«Молярлық масса» аялдамасы
«Біліміңді шыңда» әдісі
Дескриптор:
-Элементтердің массасын, молекула санын, молярлық массасын, моль санын табады
17 слайд
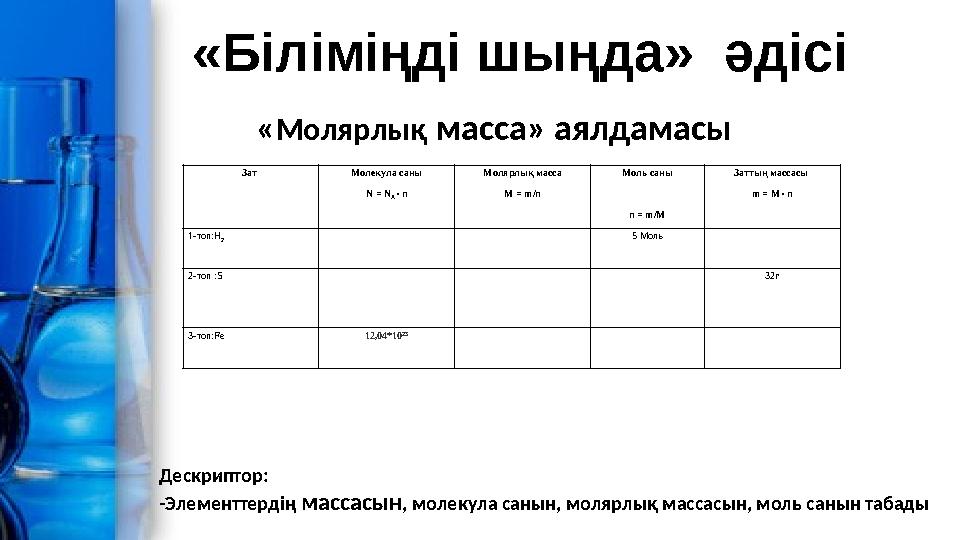
Зат Молекула саны N = N A ∙ n Молярлық масса M = m/n Моль саны n = m/M Заттың массасы m = M ∙ n 1-топ:H 2 5 Моль 2-топ :S 32г 3-топ:Fe 12,04*10 23 «Молярлық масса» аялдамасы «Біліміңді шыңда» әдісі Дескриптор: -Элементтердің массасын, молекула санын, молярлық массасын, моль санын табады

#18 слайд
Зат Молекула
саны
N = N
A
∙ n
Молярлық
масса
M = m/n
Моль саны
n = m/M
Заттың
массасы
m = M ∙ n
1-топ:H
2
30,1*10
23
2г/моль 5 Моль 10г
2-топ :S 6,02*10
23
32г/моль 1 моль 32г
3-топ:Fe 12,04*10
23
56 г/моль 2 моль 112г
18 слайд
Зат Молекула саны N = N A ∙ n Молярлық масса M = m/n Моль саны n = m/M Заттың массасы m = M ∙ n 1-топ:H 2 30,1*10 23 2г/моль 5 Моль 10г 2-топ :S 6,02*10 23 32г/моль 1 моль 32г 3-топ:Fe 12,04*10 23 56 г/моль 2 моль 112г

#19 слайд
19 слайд

#20 слайд
«Озық ойлау» әдісі
«Мәреге жету» аялдамасы
0,5 моль әктастың (СаCO
3
) массасын
есептеңіз.
Дескриптор:
•әктастың салыстырмалық молекулық массасын
есептейді
•формула бойынша әктастың массасын табады
20 слайд
«Озық ойлау» әдісі «Мәреге жету» аялдамасы 0,5 моль әктастың (СаCO 3 ) массасын есептеңіз. Дескриптор: •әктастың салыстырмалық молекулық массасын есептейді •формула бойынша әктастың массасын табады

#21 слайд
Берілгені: Шешу жолы:
n(СаСО
3 ) = 0,5моль
Табу кк: m(HCl) -? Mr(CaCO
3) = 40+12+16*3= 100 м.а.б.
Мr=M
m=n*M
m=0,5моль *100г/моль =50г
21 слайд
Берілгені: Шешу жолы: n(СаСО 3 ) = 0,5моль Табу кк: m(HCl) -? Mr(CaCO 3) = 40+12+16*3= 100 м.а.б. Мr=M m=n*M m=0,5моль *100г/моль =50г
#22 слайд
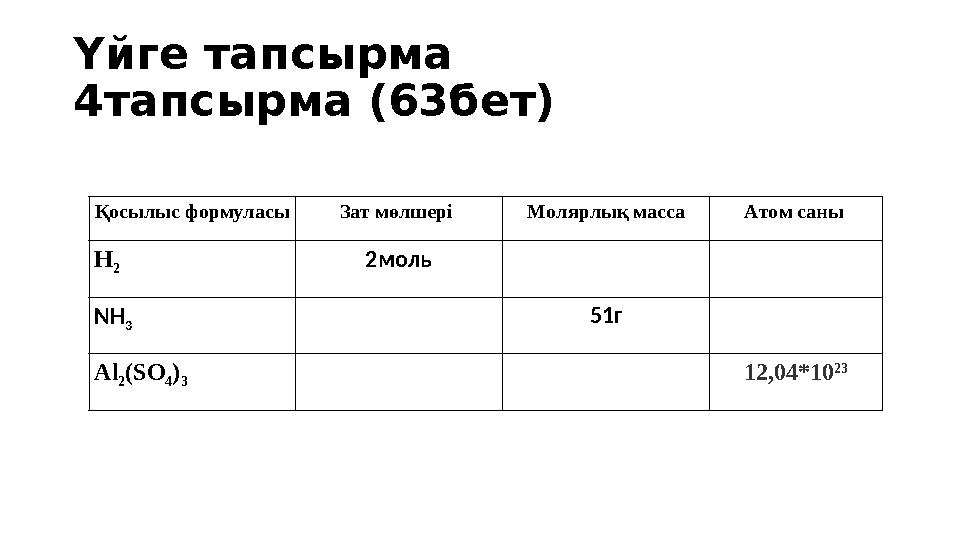
Үйге тапсырма
4тапсырма (63бет)
Қосылыс формуласы Зат мөлшері Молярлық масса Атом саны
H
2
2моль
NH
3
51г
Al
2
(SO
4
)
3
12,04*10
23
22 слайд
Үйге тапсырма 4тапсырма (63бет) Қосылыс формуласы Зат мөлшері Молярлық масса Атом саны H 2 2моль NH 3 51г Al 2 (SO 4 ) 3 12,04*10 23

#23 слайд
23 слайд

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
