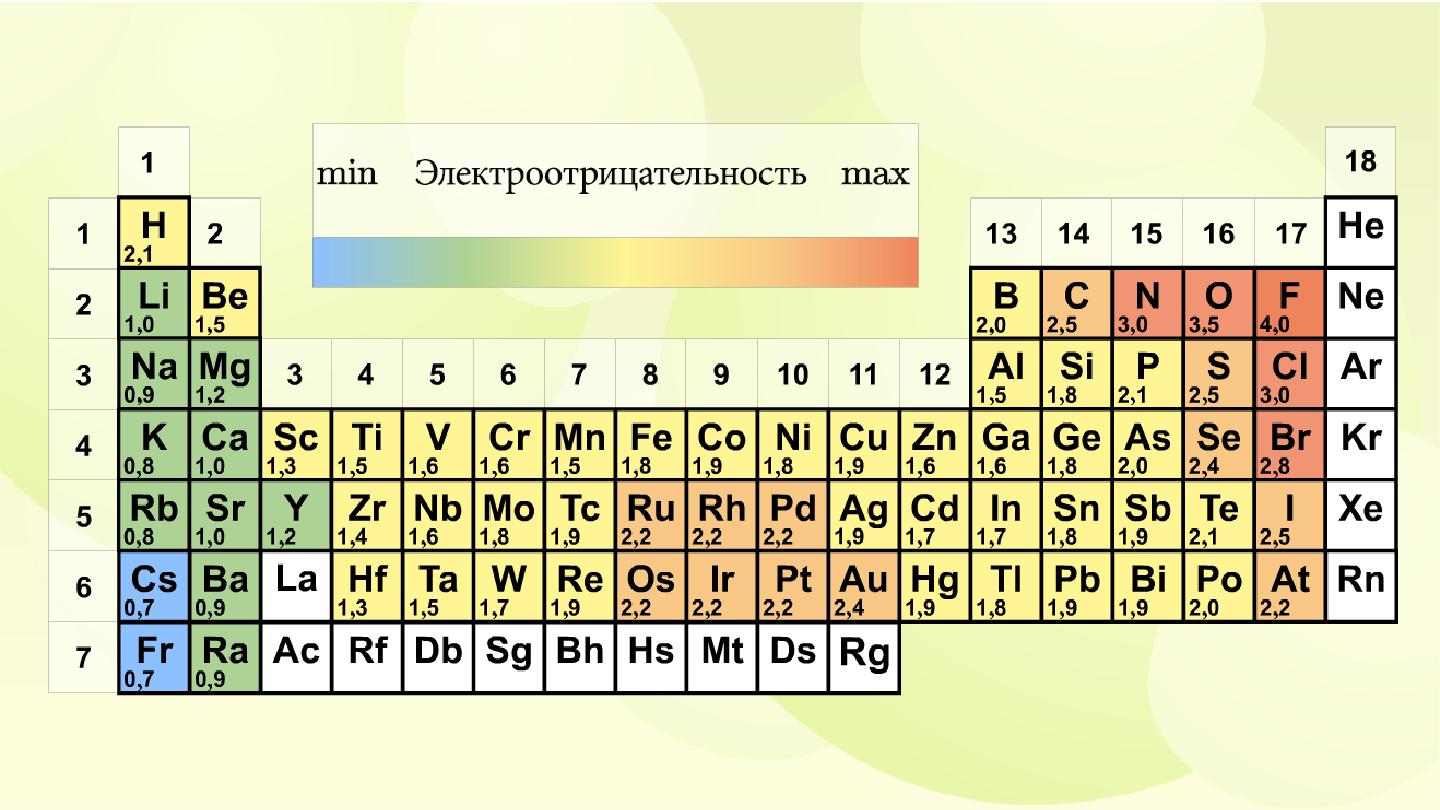
Ковалентная связь

#1 слайд
1 слайд
#2 слайд
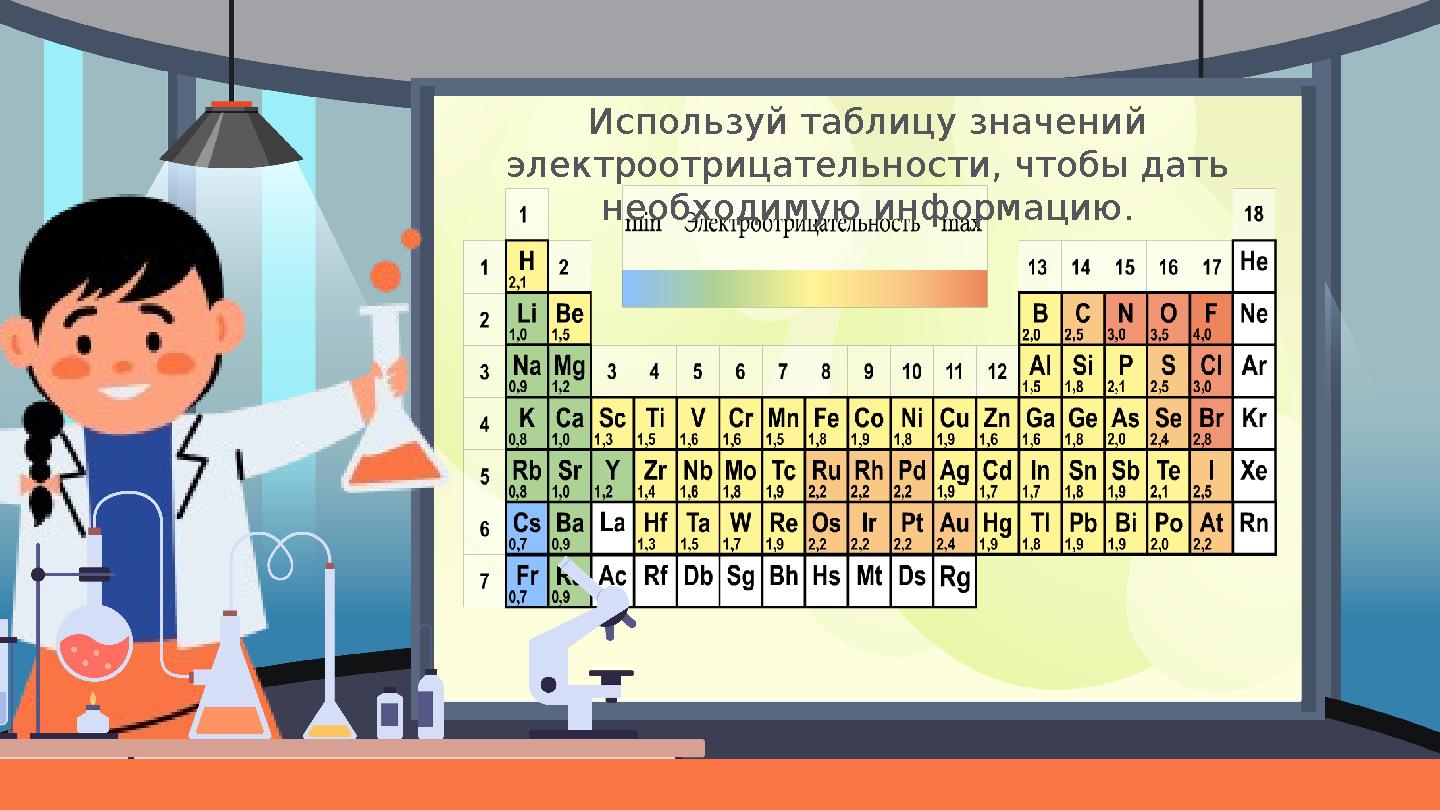
Используй таблицу значений
электроотрицательности, чтобы дать
необходимую информацию.
2 слайд
Используй таблицу значений электроотрицательности, чтобы дать необходимую информацию.

#3 слайд
Наиболее
электроотрицательный
элемент
Символ
элемент
а
Названи
я
элемент
а
FФто
р
3 слайд
Наиболее электроотрицательный элемент Символ элемент а Названи я элемент а FФто р

#4 слайд
Элементынаименьшей
электроотрицательност
и
Символ
элемент
а
Названи
я
элемент
а
Cs,
Fr
Цезий,
Франц
ий
4 слайд
Элементынаименьшей электроотрицательност и Символ элемент а Названи я элемент а Cs, Fr Цезий, Франц ий

#5 слайд
Электроотрицательност
ь
,
ТипичногометаллаСа
1
5 слайд
Электроотрицательност ь , ТипичногометаллаСа 1

#6 слайд
Электроотрицательност
ь
,
типичногонеметалла
(
азота
N)
3
6 слайд
Электроотрицательност ь , типичногонеметалла ( азота N) 3

#7 слайд
Электроотрицательност
ь
,
типичногометаллиода
(
кремний
Si)
1,8
7 слайд
Электроотрицательност ь , типичногометаллиода ( кремний Si) 1,8

#8 слайд
Дополни предложения.
8 слайд
Дополни предложения.

#9 слайд
Расположи элементы
третьего периода в порядке
возрастания их значения
электроотрицательности.
9 слайд
Расположи элементы третьего периода в порядке возрастания их значения электроотрицательности.

#10 слайд
Расположи элементы
третьего периода в порядке
возрастания их значения
электроотрицательности.
10 слайд
Расположи элементы третьего периода в порядке возрастания их значения электроотрицательности.

#11 слайд
Расположи элементы
третьего периода в порядке
возрастания их значения
электроотрицательности.
11 слайд
Расположи элементы третьего периода в порядке возрастания их значения электроотрицательности.

#12 слайд
Ковалентно
полярная связь
12 слайд
Ковалентно полярная связь

#13 слайд
Образование ковалентной полярной и не
полярной связи.
13 слайд
Образование ковалентной полярной и не полярной связи.

#14 слайд
Химическаясвязьмежду
атомаминеметаллови
металлоидовзасчет
обобществленияэлектронов
( ),
электроннаяпара
находящихсянавнешней
,
электроннойорбитали
называется
ковалентной
.
связью
A + B → A : B
14 слайд
Химическаясвязьмежду атомаминеметаллови металлоидовзасчет обобществленияэлектронов ( ), электроннаяпара находящихсянавнешней , электроннойорбитали называется ковалентной . связью A + B → A : B

#15 слайд
Междуатомамиразных
неметалловобразуетсяполярностьза
счетразностизначений
.
электроотрицательностейТакаясвязь
называется
ковалентнойполярной
.
связью
Ковалентнаянеполярнаясвязь
формируетсязасчётобразования
электронныхпаратомамис
одинаковымизначениями
.
электроотрицательности
15 слайд
Междуатомамиразных неметалловобразуетсяполярностьза счетразностизначений . электроотрицательностейТакаясвязь называется ковалентнойполярной . связью Ковалентнаянеполярнаясвязь формируетсязасчётобразования электронныхпаратомамис одинаковымизначениями . электроотрицательности

#16 слайд
Междуатомамиразных
неметалловобразуетсяполярностьза
счетразностизначений
.
электроотрицательностейТакаясвязь
называется
ковалентнойполярной
связью.
,
Кпримеруводородвстречаетсяв
газообразномсостоянииввиде
двухатомноймолекулы
(H
2
),
вкоторой
дваатомасвязаныоднойковалентной
.
связьюОбщаяпараэлектронов
эквивалентнаоднойковалентной
связи
(
Н
–)
Н
.
Такаясистемасвязи
называется
одинарной
. ковалентной
16 слайд
Междуатомамиразных неметалловобразуетсяполярностьза счетразностизначений . электроотрицательностейТакаясвязь называется ковалентнойполярной связью. , Кпримеруводородвстречаетсяв газообразномсостоянииввиде двухатомноймолекулы (H 2 ), вкоторой дваатомасвязаныоднойковалентной . связьюОбщаяпараэлектронов эквивалентнаоднойковалентной связи ( Н –) Н . Такаясистемасвязи называется одинарной . ковалентной

#17 слайд
Вдвухатомноймолекуле
кислорода
(O
2
)
существуютдвепарыэлектронов
,
междуатомамикислородаобразующиедве
связи
( = )
О О
.
Такаясистемаиздвухсвязей
называется
двойнойсвязью
.
Междуатомами
.
кислородаимеютсядвеподеленныепары
17 слайд
Вдвухатомноймолекуле кислорода (O 2 ) существуютдвепарыэлектронов , междуатомамикислородаобразующиедве связи ( = ) О О . Такаясистемаиздвухсвязей называется двойнойсвязью . Междуатомами . кислородаимеютсядвеподеленныепары

#18 слайд
Вдвухатомноймолекуле
азота
(N
2
)
существуюттрипарыэлектронов
,
междуатомамиобразующиетрисвязи
(N ≡ N).
Такаясистемасвязейназывается
тройной
.
связью
18 слайд
Вдвухатомноймолекуле азота (N 2 ) существуюттрипарыэлектронов , междуатомамиобразующиетрисвязи (N ≡ N). Такаясистемасвязейназывается тройной . связью

#19 слайд
Ms. Maria
SCIENCE
TEACHER
Дополни предложения используя следующие слова:
(ионной, ковалентной)
19 слайд
Ms. Maria SCIENCE TEACHER Дополни предложения используя следующие слова: (ионной, ковалентной)

#20 слайд
Ms. Maria
SCIENCE
TEACHER
20 слайд
Ms. Maria SCIENCE TEACHER

#21 слайд
Ms. Maria
SCIENCE
TEACHER
Структурой Льюиса называют
электронную формулу вещества,
отображенную с электронами в
виде точек и крестиков вокруг
символов элементов. Эти точки и
крестики обозначают электроны
внешнего уровня каждого атома.
Общая пара электронов
обозначается в виде точки и
крестика.
21 слайд
Ms. Maria SCIENCE TEACHER Структурой Льюиса называют электронную формулу вещества, отображенную с электронами в виде точек и крестиков вокруг символов элементов. Эти точки и крестики обозначают электроны внешнего уровня каждого атома. Общая пара электронов обозначается в виде точки и крестика.

#22 слайд
Ms. Maria
SCIENCE
TEACHER
Напиши структуру Льиса
состоящий из двух атомов
водорода.
Н:H
22 слайд
Ms. Maria SCIENCE TEACHER Напиши структуру Льиса состоящий из двух атомов водорода. Н:H

#23 слайд
Ms. Maria
SCIENCE
TEACHER
Напиши структуру Льиса
состоящий из атома кислорода и
двух атомов водорода.
Н:О:H
..
..
23 слайд
Ms. Maria SCIENCE TEACHER Напиши структуру Льиса состоящий из атома кислорода и двух атомов водорода. Н:О:H .. ..

#24 слайд
Ms. Maria
SCIENCE
TEACHER
Напиши структуру Льиса
состоящий из атома йода и
атомов водорода.
Н:I:
..
..
24 слайд
Ms. Maria SCIENCE TEACHER Напиши структуру Льиса состоящий из атома йода и атомов водорода. Н:I: .. ..

#25 слайд
Ms. Maria
SCIENCE
TEACHER
Используя структуру Льюиса, можно составить
также структурную формулу соединения. В
этом случае пары электронов, связывающие
атомы между собой, указывают в виде линий.
В случае молекулярной формулы указывают
только тип и число атомов, образующих
молекулу.
F2 H 2
O
25 слайд
Ms. Maria SCIENCE TEACHER Используя структуру Льюиса, можно составить также структурную формулу соединения. В этом случае пары электронов, связывающие атомы между собой, указывают в виде линий. В случае молекулярной формулы указывают только тип и число атомов, образующих молекулу. F2 H 2 O

#26 слайд
26 слайд

#27 слайд
Закрепите
свои
знания,
отвечая
на
тестовые
вопросы.
https://ковалентная с
вязь.
my.canva.site/c041cxatzh2rp
het
27 слайд
Закрепите свои знания, отвечая на тестовые вопросы. https://ковалентная с вязь. my.canva.site/c041cxatzh2rp het

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
