презентация


#1 слайд
ТЕРМОХИМИЯЛЫҚ
РЕАКЦИЯЛАР Саба қ тақырыбы:
1 слайд
ТЕРМОХИМИЯЛЫҚ РЕАКЦИЯЛАР Саба қ тақырыбы:
#2 слайд
2 слайд
#3 слайд
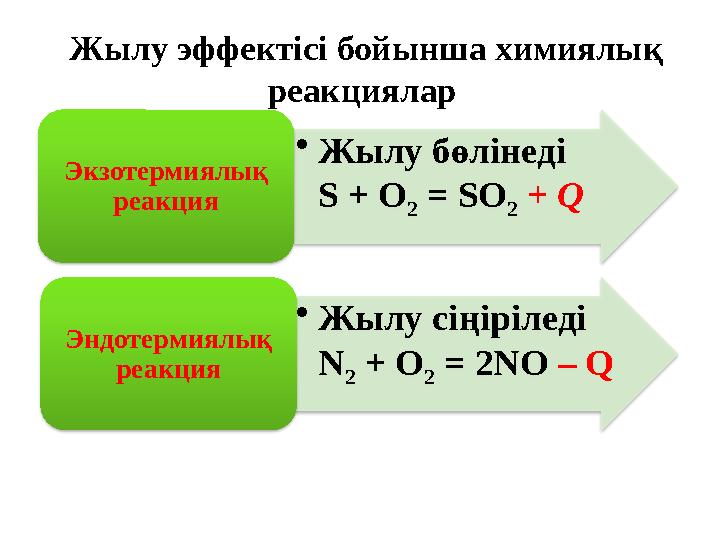
Жылу эффектісі бойынша химиялық
реакциялар
•
Жылу бөлінеді
S + O
2 = SO
2 + Q Экзотермиялық
реакция
•
Жылу сіңіріледі
N
2 + O
2 = 2NO – Q Эндотермиялық
реакция
3 слайд
Жылу эффектісі бойынша химиялық реакциялар • Жылу бөлінеді S + O 2 = SO 2 + Q Экзотермиялық реакция • Жылу сіңіріледі N 2 + O 2 = 2NO – Q Эндотермиялық реакция
#4 слайд
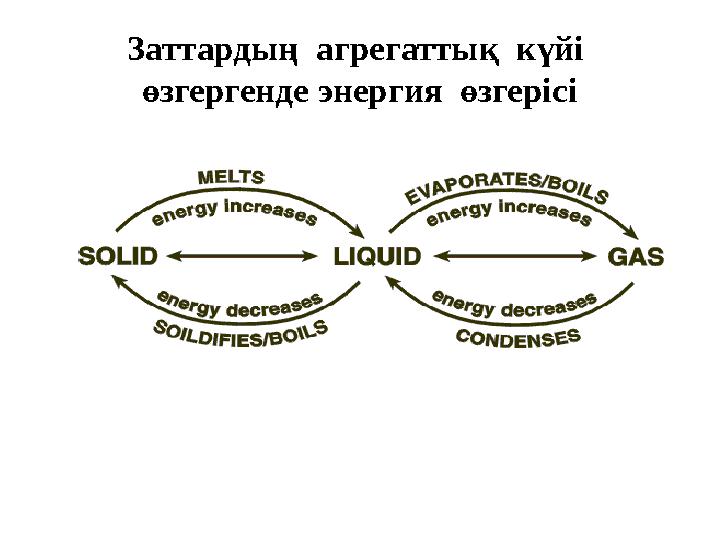
Заттардың агрегаттық күйі
өзгергенде энергия өзгерісі
4 слайд
Заттардың агрегаттық күйі өзгергенде энергия өзгерісі
#5 слайд
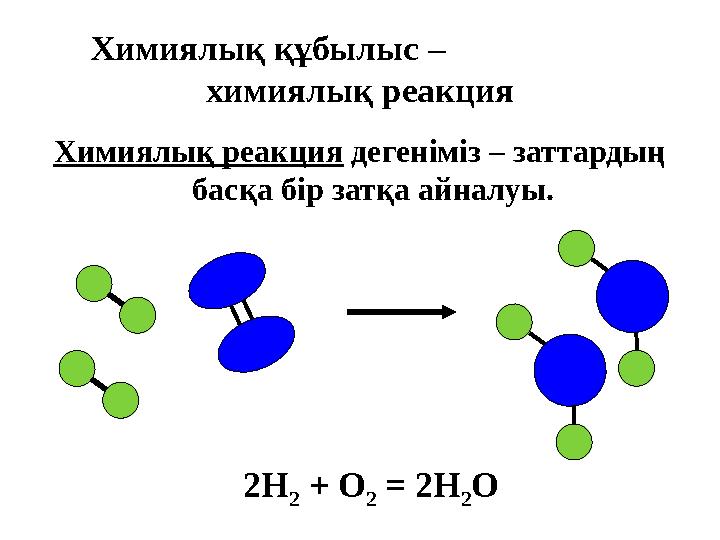
Хими ялық құбылыс –
химиялық реакция
Химиялық реакция дегеніміз – заттардың
басқа бір затқа айналуы.
2Н
2 + О
2 = 2Н
2 О
5 слайд
Хими ялық құбылыс – химиялық реакция Химиялық реакция дегеніміз – заттардың басқа бір затқа айналуы. 2Н 2 + О 2 = 2Н 2 О
#6 слайд
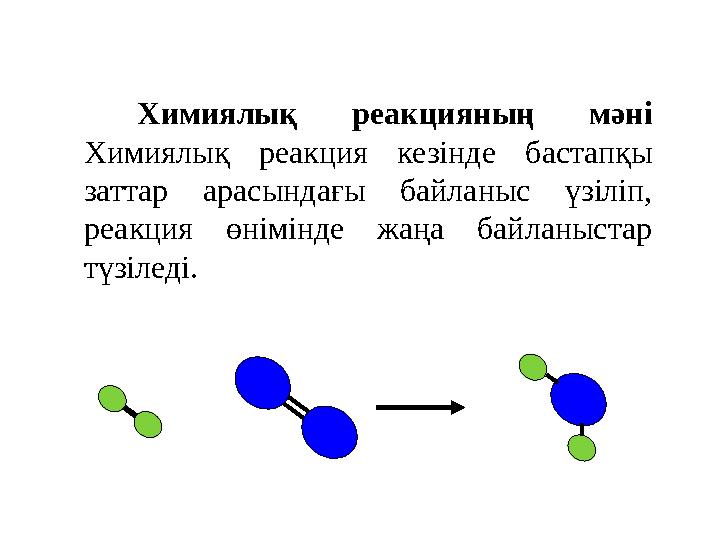
Химиялық реакцияның мәні
Химиялық реакция кезінде бастапқы
заттар арасындағы байланыс үзіліп,
реакция өнімінде жаңа байланыстар
түзіледі.
6 слайд
Химиялық реакцияның мәні Химиялық реакция кезінде бастапқы заттар арасындағы байланыс үзіліп, реакция өнімінде жаңа байланыстар түзіледі.

#7 слайд
Жылу эффектісінің себебі
– бастапқы заттар ішкі энергиясы мен
реакция өнімінің ішкі энергиясының
айырмашылығында
E баст. > E өнім.
Q = E
баст. - E
өнім.
Q > 0 E баст. < E өнім.
Q = E
баст. - E
өнім.
Q < 0
7 слайд
Жылу эффектісінің себебі – бастапқы заттар ішкі энергиясы мен реакция өнімінің ішкі энергиясының айырмашылығында E баст. > E өнім. Q = E баст. - E өнім. Q > 0 E баст. < E өнім. Q = E баст. - E өнім. Q < 0

#8 слайд
Термодинамика – өзара энергия айналымын
зерттейтін ғылым
Термодинамиканың бірінші заңы —
энергия сақталу заңы: энергия жоқтан
пайда болмайды, жоғалмайды, бір
түрден екінші түрге ауысады.
8 слайд
Термодинамика – өзара энергия айналымын зерттейтін ғылым Термодинамиканың бірінші заңы — энергия сақталу заңы: энергия жоқтан пайда болмайды, жоғалмайды, бір түрден екінші түрге ауысады.
#9 слайд
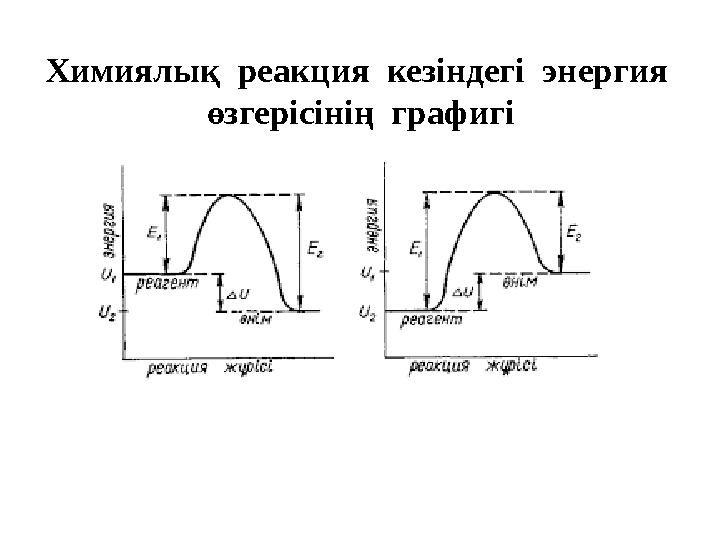
Химиялық реакция кезіндегі энергия
өзгерісінің графигі
9 слайд
Химиялық реакция кезіндегі энергия өзгерісінің графигі

#10 слайд
10 слайд

#11 слайд
Екі жағдайды қарастырайық:
1. E реагент > E өнім . Энергия сақталу заңы бойынша
бұл реакциялар нәтижесінде энергия сыртқа
бөлінеді: атмосфера жылынады,
2. Қоршаған ортаға жылу бөле жүретін
реакцияларды экзотермиялық реакция деп
атайды.
11 слайд
Екі жағдайды қарастырайық: 1. E реагент > E өнім . Энергия сақталу заңы бойынша бұл реакциялар нәтижесінде энергия сыртқа бөлінеді: атмосфера жылынады, 2. Қоршаған ортаға жылу бөле жүретін реакцияларды экзотермиялық реакция деп атайды.

#12 слайд
1. Е реагент < Е өнім. Энергия сақталу заңына сәйкес
бастапқы заттар энергияны қоршаған ортадан сіңіреді.
2. Қоршаған ортаға жылу бөле жүретін реакцияларды
эндотермиялық реакция деп атайды.
12 слайд
1. Е реагент < Е өнім. Энергия сақталу заңына сәйкес бастапқы заттар энергияны қоршаған ортадан сіңіреді. 2. Қоршаған ортаға жылу бөле жүретін реакцияларды эндотермиялық реакция деп атайды.

#13 слайд
1. Бұл графикалық сурет судың сутек пен
оттекке ыдырау реакциясын көрсетеді
2 . Эндотермиялық реакция Е – бұл
реакцияның жылу эффектісі = 286 кДж.
(Q= E). E – бұл сіңірілген энергия
3 . Х осінде заттардың түзілуі көрсетілген.
Мұнда 100% заттардың толық түзілгенін
көрсетеді.
13 слайд
1. Бұл графикалық сурет судың сутек пен оттекке ыдырау реакциясын көрсетеді 2 . Эндотермиялық реакция Е – бұл реакцияның жылу эффектісі = 286 кДж. (Q= E). E – бұл сіңірілген энергия 3 . Х осінде заттардың түзілуі көрсетілген. Мұнда 100% заттардың толық түзілгенін көрсетеді.

#14 слайд
•
Реакциялар теңдеуінің қатары берілген:
A) CaCO
3 = CaO + CO
2
B) CaCO
3 = CaO + CO
2 -157 кДж
A) S(кр) + O
2 (г) = SO
2 (г)
B) S(кр) + O
2 (г) = SO
2 (г) + 297 кДж
A) 4Al( кр) + 3 O2( г) = 2 Al
2 O
3 ( кр)
B) 4Al( кр) + 3 O2( г) = 2 Al
2 O
3 ( кр) + 3350 кДж
А реакцияларының теңдеулері В теңдеулерінен қандай
айырмашылықтары бар?
14 слайд
• Реакциялар теңдеуінің қатары берілген: A) CaCO 3 = CaO + CO 2 B) CaCO 3 = CaO + CO 2 -157 кДж A) S(кр) + O 2 (г) = SO 2 (г) B) S(кр) + O 2 (г) = SO 2 (г) + 297 кДж A) 4Al( кр) + 3 O2( г) = 2 Al 2 O 3 ( кр) B) 4Al( кр) + 3 O2( г) = 2 Al 2 O 3 ( кр) + 3350 кДж А реакцияларының теңдеулері В теңдеулерінен қандай айырмашылықтары бар?

#15 слайд
Үй тапсырмасы
Есептерді шығару.
1. Массасы 8 г кальций жанғанда 127 кДж жылу
бөлінді. Термохимиялық реакция теңдеуін жаз.
2. Массасы 8,68 г сынап (ІІ) оксидін ыдырату
үшін 3,64 кДж жылу жұмсалды. Термохимиялық
реакция теңдеуін жаз.
3. Егер 1 моль теллур оксиді түзілгенде 322 кДж
жылу бөлінсе, массасы 1,92 г теллур жанғанда
қанша жылу бөлінеді?
4. Термохимиялық теңдеу 2 KNO
3 =2KNO
2 + O
2 –
255 кДж бойынша 12 г оттегі алғанда қанша жылу
сіңіріледі?
15 слайд
Үй тапсырмасы Есептерді шығару. 1. Массасы 8 г кальций жанғанда 127 кДж жылу бөлінді. Термохимиялық реакция теңдеуін жаз. 2. Массасы 8,68 г сынап (ІІ) оксидін ыдырату үшін 3,64 кДж жылу жұмсалды. Термохимиялық реакция теңдеуін жаз. 3. Егер 1 моль теллур оксиді түзілгенде 322 кДж жылу бөлінсе, массасы 1,92 г теллур жанғанда қанша жылу бөлінеді? 4. Термохимиялық теңдеу 2 KNO 3 =2KNO 2 + O 2 – 255 кДж бойынша 12 г оттегі алғанда қанша жылу сіңіріледі?

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
