Стехиометриялық есептеулер


#1 слайд
Тақырыбы: « Химиялық реакция теңдеулері бойынша есептеулер »
8 сынып
1 слайд
Тақырыбы: « Химиялық реакция теңдеулері бойынша есептеулер » 8 сынып

#2 слайд
2
Оқу мақсаты
Бағалау критерийлері
• химиялық реакция теңдеулері бойынша заттың массасын , зат мөлшерін
есептеу
• химиялық реакция теңдеулері бойынша заттың массасын және зат мөлшерін
есептей біледі
2 слайд
2 Оқу мақсаты Бағалау критерийлері • химиялық реакция теңдеулері бойынша заттың массасын , зат мөлшерін есептеу • химиялық реакция теңдеулері бойынша заттың массасын және зат мөлшерін есептей біледі
#3 слайд
3
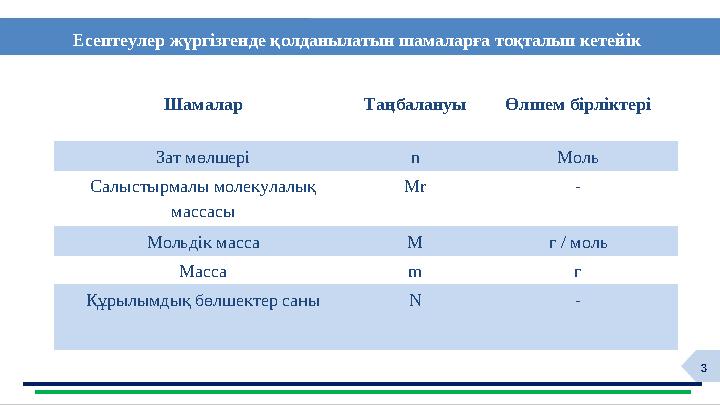
Шамалар Таңбалануы Өлшем бірліктері
Зат мөлшері n Моль
Салыстырмалы молекулалық
массасы
Mr -
Мольдік масса M г / моль
Масса m г
Құрылымдық бөлшектер саны N -
Есептеулер жүргізгенде қолданылатын шамаларға тоқталып кетейік
3 слайд
3 Шамалар Таңбалануы Өлшем бірліктері Зат мөлшері n Моль Салыстырмалы молекулалық массасы Mr - Мольдік масса M г / моль Масса m г Құрылымдық бөлшектер саны N - Есептеулер жүргізгенде қолданылатын шамаларға тоқталып кетейік

#4 слайд
4
ф
Сандық есептер зат массасының сақталу заңына негізделіп шығарылады
4 слайд
4 ф Сандық есептер зат массасының сақталу заңына негізделіп шығарылады

#5 слайд
5
Сандық есептерді шығарудың алгоритмі
1 – мысал. Массасы 224 г темір артық мөлшердегі хлормен
әрекеттескенде түзілетін темір (ІІІ) хлоридінің массасын
есептеңдер.
Берілгені: m (Fe) = 224 г
---------------------------------------
Т/к: m (FeCl
3
) = ? Шешуі:
n (Fe) = m (Fe) / М (Fe)
М (Fe) = Ar (Fe) = 56 г/моль
n (Fe) = 224 г / 56 г/моль = 4 моль
5 слайд
5 Сандық есептерді шығарудың алгоритмі 1 – мысал. Массасы 224 г темір артық мөлшердегі хлормен әрекеттескенде түзілетін темір (ІІІ) хлоридінің массасын есептеңдер. Берілгені: m (Fe) = 224 г --------------------------------------- Т/к: m (FeCl 3 ) = ? Шешуі: n (Fe) = m (Fe) / М (Fe) М (Fe) = Ar (Fe) = 56 г/моль n (Fe) = 224 г / 56 г/моль = 4 моль

#6 слайд
6
1.Химиялық реакция теңдеулерін жазып, тиісті коэффициенттерін қойып теңестіреміз.
2Fe + 3Cl
2
= 2FeCl
3
2. Реакцияға кіріскен және түзілген заттардың формулаларының астына зат мөлшерін жазамыз:
2Fe + 3Cl
2
= 2FeCl
3
2 моль 2 моль
3. Осы заттардың формулаларының үстіне есептің шартында берілген белгілі немесе белгісіз
шамаларды жазамыз:
4 моль x моль
2Fe + 3Cl
2
= 2FeCl
3
2 моль 2 моль
Сандық есептерді шығарудың алгоритмі
6 слайд
6 1.Химиялық реакция теңдеулерін жазып, тиісті коэффициенттерін қойып теңестіреміз. 2Fe + 3Cl 2 = 2FeCl 3 2. Реакцияға кіріскен және түзілген заттардың формулаларының астына зат мөлшерін жазамыз: 2Fe + 3Cl 2 = 2FeCl 3 2 моль 2 моль 3. Осы заттардың формулаларының үстіне есептің шартында берілген белгілі немесе белгісіз шамаларды жазамыз: 4 моль x моль 2Fe + 3Cl 2 = 2FeCl 3 2 моль 2 моль Сандық есептерді шығарудың алгоритмі

#7 слайд
7
Сандық есептерді шығарудың алгоритмі
4. Пропорция құрып, оны шешеміз:
4 моль Fe ---------- x моль FeCl
3
түзіледі
2 моль Fe
----------- 2 моль FeCl
3
түзіледі
2 / 4 = 2 / x ; x = 2 ∙ 4 / 2 = 4 моль
5. FeCl
3
массасын табамыз
m (FeCl
3
) = n (FeCl
3
) ∙ M (FeCl
3
)
Mr(FeCl
3
) = 56 +35,5 ∙ 3 = 162,5
M (FeCl
3
) = 162,5 г/моль
m (FeCl
3
) = 4 моль ∙ 162,5 г/моль = 650 г
Жауабы: m (FeCl
3
) = 650 г
7 слайд
7 Сандық есептерді шығарудың алгоритмі 4. Пропорция құрып, оны шешеміз: 4 моль Fe ---------- x моль FeCl 3 түзіледі 2 моль Fe ----------- 2 моль FeCl 3 түзіледі 2 / 4 = 2 / x ; x = 2 ∙ 4 / 2 = 4 моль 5. FeCl 3 массасын табамыз m (FeCl 3 ) = n (FeCl 3 ) ∙ M (FeCl 3 ) Mr(FeCl 3 ) = 56 +35,5 ∙ 3 = 162,5 M (FeCl 3 ) = 162,5 г/моль m (FeCl 3 ) = 4 моль ∙ 162,5 г/моль = 650 г Жауабы: m (FeCl 3 ) = 650 г

#8 слайд
8
Тапсырма:
Реакция нәтижесінде 3,5 моль алюминий (ІІІ) оксиді түзіледі. Оттекпен
әрекеттескен алюминийдің массасы мен зат мөлшерін есептеңдер ?
Бекіту тапсырмасы
Дескриптор:
Білім алушы
- заттың массасын есептейді
- зат мөлшерін есептейді
8 слайд
8 Тапсырма: Реакция нәтижесінде 3,5 моль алюминий (ІІІ) оксиді түзіледі. Оттекпен әрекеттескен алюминийдің массасы мен зат мөлшерін есептеңдер ? Бекіту тапсырмасы Дескриптор: Білім алушы - заттың массасын есептейді - зат мөлшерін есептейді

#9 слайд
9
Берілгені: n (Al
2
O
3
) = 3,5 моль
----------------------------------------
Т/к: m (Al) = ?
n (Al) = ?
Шешуі: 1. Реакция теңдеуін жазамыз:
x моль 3,5 моль
4Al + 3O
2
= 2Al
2
O
3
4 моль 2 моль
x моль ---------- 3,5 моль
4 моль
----------- 2 моль
x = 4 ∙ 3,5 / 2 = 7 моль
m (Al) = n (Al) ∙ M (Al) = 7 моль ∙ 27 г/моль = 189 г
Жауабы: m (Al) = 189 г n (Al) = 7 моль
Дұрыс жауабы
9 слайд
9 Берілгені: n (Al 2 O 3 ) = 3,5 моль ---------------------------------------- Т/к: m (Al) = ? n (Al) = ? Шешуі: 1. Реакция теңдеуін жазамыз: x моль 3,5 моль 4Al + 3O 2 = 2Al 2 O 3 4 моль 2 моль x моль ---------- 3,5 моль 4 моль ----------- 2 моль x = 4 ∙ 3,5 / 2 = 7 моль m (Al) = n (Al) ∙ M (Al) = 7 моль ∙ 27 г/моль = 189 г Жауабы: m (Al) = 189 г n (Al) = 7 моль Дұрыс жауабы

#10 слайд
10
Қорытынды
Бүгінгі сабақта:
• химиялық реакция теңдеулері бойынша заттың массасын және
зат мөлшері есептеуді үйрендім
10 слайд
10 Қорытынды Бүгінгі сабақта: • химиялық реакция теңдеулері бойынша заттың массасын және зат мөлшері есептеуді үйрендім

#11 слайд
11
Қосымша ресурстар
Химия оқулығы 8 сынып
Оспанова М.Қ , Белоусова Т.Г, Аухадиева Қ.С
https://bilimland.kz/kk/subject/ximiya/8-synyp/
11 слайд
11 Қосымша ресурстар Химия оқулығы 8 сынып Оспанова М.Қ , Белоусова Т.Г, Аухадиева Қ.С https://bilimland.kz/kk/subject/ximiya/8-synyp/

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
