
11-класс Биология зертханалық жұмыстар.
№1 зертханалық жұмыс
«Иммобилизациялаудың ферменттердің белсенділігіне әсерін зерттеу» зертханалық жұмысы
Иммобилизденген фермент дегеніміз – арнайы әдіспен оқшауланып, сақталған фермент.
Ферментті оқшаулап жинап алу үшін альгинат, желатин, поликарбамид сияқты жасанды полимерлер қолданылады. Мысалы, альгинат пен ферментті қосқанда, ол ферменттер альгинатқа жабысып қалады. Ал субстрат пайда болған кезде ол альгинаттан ажырап, белсендендіріледі. Бұл полимермен қоршалған ферментті ұзақ сақтауға болады.
Иммобилизденген ферменттер өнеркәсіпте кеңінен қолданылуда.
-
Медицина: ферменттер бірқатар аурулар мен жүктілікті анықтауда қолданылады.
-
Биотехнология: ферменттер гендердің сплайсингісі сияқты көптеген процестерде қолданылады.
-
Биоотын: ферменттер этанолға негізделген отын өндіру үшін көмірсуларды ыдыратуда қолданылады.
-
Тағам өнімдерін өндіру: ферменттер сүт өнімдері мен сыра өндіруде кеңінен қолданылады.
-
Тоқыма өнеркәсібі: ферменттер мата өндіруге қажетті талшықтарды өңдеуде маңызды.
-
Қағаз: ферменттер ағаш сүректерінен қағаз өндіруде пайдаланылады.
Зертханалық жұмыс: «Иммобилизациялаудың ферменттердің белсенділігіне әсерін зерттеу»
Лактаза ферментін оқшаулау әдісін қарастырып көрейік. Бұл – сүтқоректілердің балаларында ағзаға ана сүтімен келген лактозаны ыдырататын фермент. Аш ішекте лактозаны галактоза мен глюкозаға айналдырады.
Кейбір ересек адамдарда лактазаның түзілуі баяулайды. Сондықтан сүт өнімдерін қабылдай алмаушылық туындайды. Қорытылмаған лактоза тоқ ішекке түсіп, ондағы микрофлора арқылы ыдырай бастайды. Бактериялық ыдыраудың нәтижесінде газ бөлініп, адам іштің кебуі, түйілуі, бұлшықеттің құрысуы, диарея, метеоризмге душар болады. Осыған байланысты лактаза ферментін оқшаулап, оны сүтке қосып қолдану үшін өндіреді. Коммерциялық мақсатта оқшауланған лактазаны картон қорапшалардағы сүтке қосып өндіреді. Ондай сүттер лактазамен байытылған болып келеді.
Бұл зертханалық жұмыстың мақсаты лактозаны натрий альгинатынан жасалған түйіршіктерінде оқшаулап алып, оның сүттегі лактозаға әсерін зерттеу.
Қажетті құрал-жабдықтар:
-
Лактаза ферменті (лактозим) – 2 мл
-
Натрий альгинатының 2% ерітіндісі (2 грамды 100 мл суға қосып, ұзақ араластыру) – 8 мл
-
Пастерленбеген сүт – 50 мл
-
Қандағы глюкозаны анықтауға арналған тест жолақ қағаздары
-
Инесіз пластик 10 мл шприц – 1 дана
-
100 мл мензурка – 3 дана
-
Шай сүзгіш – 1 дана
-
Секундомер
-
Шыны таяқша – 1 дана
Қауіпсіздік ережесі:
Лактоза – қауіпсіз фермент. Бірақ жұмыс барысында онымен тікелей жанасуды болдырмаған жөн. Сонымен қатар иіскеуге, татып көруге болмайды. Көзге түсіп кетсе, таза сумен жақсылап шаю керек.
Жұмыс барысы:
-
Алдымен ферментті натрий альгинатымен араластыр.
-
Осы шприцке қоспаны сорғызып ал.
-
Кальций хлоридінің ерітіндісін бір мензуркаға құй.
-
Шприцтегі қоспаны бір тамшыдан кальций хлориді ерітіндісіне тамшылат.

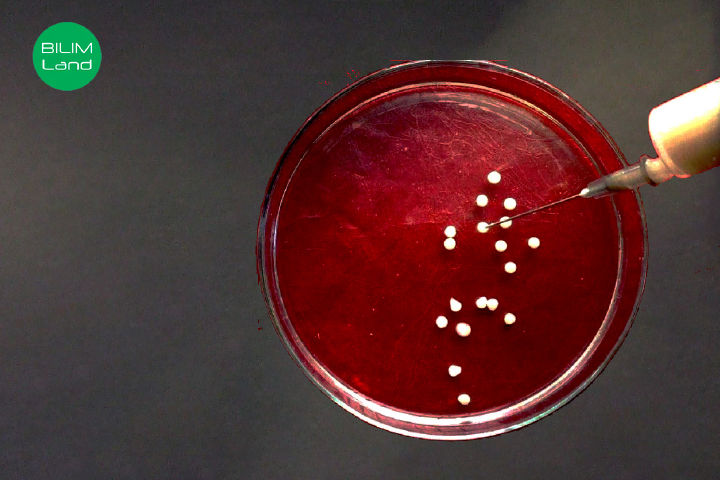
5. Ерітіндіде пайда болған ұсақ түйіршіктерді қатаюы үшін 2-5 минутқа қалдыр.

6. Осы түйіршіктерді шай сүзгішпен сүзіп ал.

7. Түйіршіктерді бос мензуркаға сал.
8. Түйіршіктерді дистильденген су арқылы бірнеше рет шай.

9. Сүтті таза мензуркаға құй.
10. Тест жолақшасы арқылы сүт құрамында глюкоза бар-жоғын тексер.
11. Сүтке түйіршіктен бірнешеуін салып, шыны таяқшамен араластыр.
12. 10 минуттаң соң ондағы сүтте глюкозаның болуын тест арқылы тексер.
13. Тест жолақшасы түсінің өзгеруін бақыла. Түстің өзгеруі сүтте лактаза арқылы лактозаның глюкоза мен галактозаға ыдырағанын көрсетеді.
Артқа
№2 зертханалық жұмыс
«Активаторлар мен ингибиторлардың ферменттік реакцияның жылдамдығына әсерін зерттеу» зертханалық жұмысы
Өте төмен концентрацияда ферменттердің белсенділігін арттыратын (активаторлар) немесе, керісінше, оны төмендететін заттар бар (ингибиторлар). Мысалы, асқазан сөліндегі пепсиногеннің активаторы (пепсиннің ізашары) – тұз қышқылы, сол тұз қышқылы сілекей амилазасының ингибиторы болып саналады.
Активаторлар мен ингибиторлар белсенді орталықта немесе одан алыс орналасқан фермент молекуласының аллостериялық орталығында әрекет ете алады.
Ферменттердің белсенділігін арттыратын заттар қатарына металл катиондары немесе аниондар және басқа да заттар жатады. Көбінесе ферменттердің активаторы ретінде Ca2+, Mg2+ , K+ және Na+ катиондары, Cl- аниондары қызмет атқара алады. Активаторлар фермент-субстрат кешенін түзуге немесе оны тұрақтандыруға көмектеседі.
Ферментативті реакцияның барысын тежейтін ингибиторлар арнайы емес (денатурациялайтын реактивтер – ауыр металдардың тұздары, қышқыл, сілтілер, барлық ферментті белсенді етпейтін) және арнайы болып бөлінеді. Соңғылары тек белгілі бір ферменттерге әсер ететін қайтымсыз және қайтымды болып бөлінеді. Қайтымсыз реакция кезінде ферменттің белсенді орталығын немесе бүкіл молекуласын өзгертеді және олар жойылғаннан кейін белсенділігі қалпына келмейді. Қайтымды рекция кезінде фермент жұмысын уақытша тежейді, сондықтан ферменттердің белсенділігі қалпына келеді. Қайтымды ингибиторлар бәсекелес және бәсекелес емес болып бөлінеді.
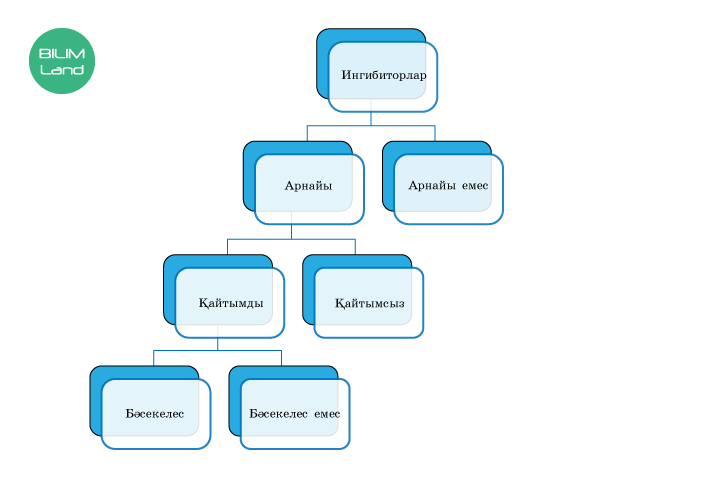
Зертханалық жұмыста фермент ингибиторларының әсерін зерделеу үшін келесі тәжірибелерді жүргізу ұсынылады:
1. CuSO4 мыс тұзының ингибиторын қолданып, тәжірибе жасау.
2. Бақылау эксперименті (CuSO4 мыс тұз ингибиторынсыз).
Зерттеудің теориялық бөлігі
Каталаза ферменті сутек асқын тотығының ыдырауын катализдейді:
2H2O2 2H2O + O2
Каталаза жасушаларда өте жиі кездеседі. Бұл фермент жасушалардың қорғаныс механизмі ретінде қызмет етеді. Сутек асқын тотығы – белгілі бір метаболикалық реакциялардың жиі кездесетін өнімі және өте улы зат. Каталаза сутек асқын тотығын жасуша зақымдалуы мүмкін болғанға дейін түзеді.
Тәжірибелік бөлім
Іс жүзінде реакция ферменттерінің катализденуі жылдамдық реакция қоспасынан кететін субстрат мөлшері немесе белгілі бір уақыт аралығында жинақталған өнім мөлшері ретінде қабылданады. Каталазамен жұмыс кезінде өнімнің (оттектің) жиналу жылдамдығын өлшеу ыңғайлы. 30 секундта босатылған оттегі көпіршіктерінің саны бойынша реакцияның бастапқы жылдамдығын есептеуге болады.
Материалдар мен жабдықтар:
Жапқыштары бар сынауықтар – 4 дана
Тамшуыр – 2 дана
Өлшейтін стақан – 2 дана
Газды бұрғыш түтікшелер – 4 дана
Секундомер
Су моншасы
Ашытқы суспензиясы
0,1 М CuSO4 ерітіндісі
Дистильденген H2O
Пайдаланылған құрылғы төмендегі суретте көрсетілген.
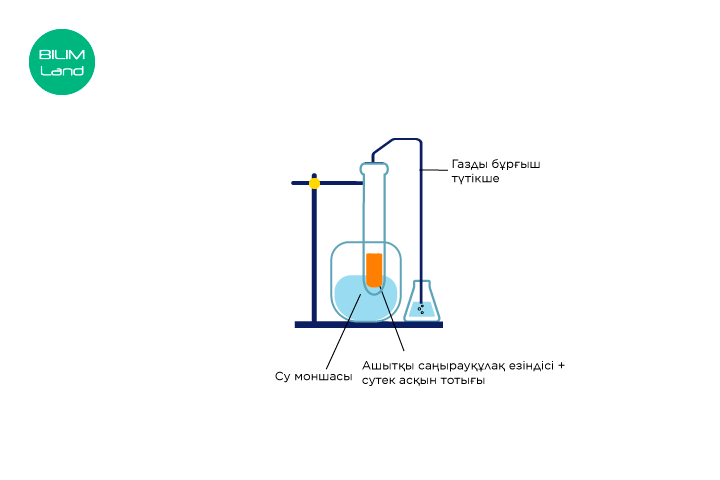
Ашытқы суспензиясы фермент көзі ретінде пайдаланылды. Жарты минуттық аралықта шығарылған көпіршіктердің саны есептеліп, әр реакция қоспасы үшін екі минут ішінде тіркелді.
Пайдаланылған реакция қоспалары және алынған нәтижелер төмендегі кестеде көрсетілген.
1-кесте. Ферменттің жұмысы кезінде ауыр металдардың тұздарын қолданудың әсері
|
1-тәжірибе |
Сынауық нөмірі
|
||||
|
Дистильденген су (см3) |
|
||||
|
0,1 CuSO4 |
|
||||
|
H2O мөлшері (мл) |
|
||||
|
Ашытқы саңырауқұлақ езіндісі(см3) |
|
||||
|
Реакцияның бастапқы жылдамдығы (30 cекундта бөлінген көпіршік саны) |
|
2-кесте. Ферментті ингибиторсыз қолданудың әсері.
|
2-тәжірибе |
Сынауық нөмірі
|
||||
|
Дистильденген су (см3) |
|
||||
|
H2O мөлшері (мл) |
|
||||
|
Ашытқы саңырауқұлақ езіндісі (см3) |
|
||||
|
Реакцияның бастапқы жылдамдығы (30 cекундта бөлінген көпіршік саны) |
|
Тәжірибе нәтижелері мыс тұздарын қолданғандағы реакцияның бастапқы жылдамдығы фермент ингибиторсыз жұмыс істеген жағдайға қарағанда әлдеқайда төмен екенін көрсетті.
№3 зертханалық жұмыс
«Әртүрлі өсімдік жасушаларында фотосинтездеуші пигменттердің болуын зерттеу» зертханалық жұмысы
Өсімдік жапырағының түсі маңызды морфологиялық белгілердің бірі болып табылады. Өсімдік жапырағында негізгі төрт пигмент: хлорофилл a, хлорофилл b, ксантофилл, каратиноид кездеседі. Жасыл өсімдік пигменттері жарық энергиясын сіңіріп, химиялық энергияға айналдырады. Жарықты сіңіруге әртүрлі пигменттер қатысады. Жапырақтағы пигменттердің қоспасын хроматография қағазы бойынша түсті жолақтарға бөлуге болады.

Хроматография әдісі таңдалған еріткіштегі молекулалардың әртүрлі ерігіштігіне байланысты молекулаларды ажыратады. Хроматографиялық әдістің негізін салушы орыс ботанигі М.С.Цвет «Хроматография грекше «түсті жазу» дегенді білдіреді. Бұл әдіс арқылы жапырақ пигменттерінің сұйық қоспасын әртүрлі компоненттерге бөлуге болады» деген.
Бұл тәжірибе өсімдік жапырағынан фотосинтетикалық пигменттерді шығарып алуды және хроматографиялық немесе сүзгі қағаздарын қолдану арқылы пигмент түрлерін өзара бөліп ажыратуды көрсетеді.
Жапырақтағы пигменттер қоспасын хроматография қағазы арқылы ұқсас компоненттерге бөлуге болады. Қоспа құрамындағы полярлы заттар целлюлозамен әрекеттесіп, тез тежеліп қалады. Ал полярлығы төмен заттар алдыға қарай жылжи береді. Пигменттер қағазға сіңеді де, еріткіштің капиллярлық әрекеті оларды қағазға қарай тартады. Әр пигменттің бастапқы сызықтан жылжу қашықтығы әртүрлі болады. Еріткіште пигменттердің еруі бірдей болмайды. Ерігіштігі жоғары пигменттер (каратиноид) ерітінді шекарасына жақын орналасса, аз еритін пигмент қысқа қашықтыққа жылжып, бастапқы сызыққа жақын орналасады. Бөлінген компоненттердің үлгісі хроматограммада түрлі түсті жолақ түрінде көрінеді. Еріткіште хлорофилл а пигментінің ерігіштігі хлорофилл b пигментіне қарағанда жоғары болып келеді. Ал ксантофилл пигментінің ерігіштігі хлорофилл b пигментінен жоғары.
Rf (ұстап қалу коэффициенті) мәнін есептеу арқылы бір түрге жататын өсімдік жапырақтарының пигмент түрі мен санын немесе екі түрлі өсімдік жапырақ пигменттерін салыстырып анықтауға болады. Rf (ұстап қалу коэффициенті) мәнін пигмент жылжыған қашықтық/ерітінді жылжыған қашық арқылы анықтайды.
Rf (ұстап қалу коэффициенті) мәнін есептеу формуласы:
Rf =
пигмент жылжыған қашықтығы (mm)
–––––––––––––––––––––––––––––––––
ерітінді жылжыған қашықтығы (mm)
№4 зертханалық жұмыс
«С3 және С4 өсімдіктер жапырақтарының мезофилін микропрепараттар арқылы зерттеу» зертханалық жұмысы
1-конспект
Мезофилл жасушаларының
хлоропластарында жарық реакцияларының
жүруі басым және АТФ-тың көп мөлшері, НАДФН
және O2 түзіледі. Іс жүзінде
РиБФ-карбоксилаза
болмағандықтан, CO2Жүктеу
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
11 сынып зертханалық жұмыс жауаптарымен
11-класс Биология зертханалық жұмыстар.
№1 зертханалық жұмыс
«Иммобилизациялаудың ферменттердің белсенділігіне әсерін зерттеу» зертханалық жұмысы
Иммобилизденген фермент дегеніміз – арнайы әдіспен оқшауланып, сақталған фермент.
Ферментті оқшаулап жинап алу үшін альгинат, желатин, поликарбамид сияқты жасанды полимерлер қолданылады. Мысалы, альгинат пен ферментті қосқанда, ол ферменттер альгинатқа жабысып қалады. Ал субстрат пайда болған кезде ол альгинаттан ажырап, белсендендіріледі. Бұл полимермен қоршалған ферментті ұзақ сақтауға болады.
Иммобилизденген ферменттер өнеркәсіпте кеңінен қолданылуда.
-
Медицина: ферменттер бірқатар аурулар мен жүктілікті анықтауда қолданылады.
-
Биотехнология: ферменттер гендердің сплайсингісі сияқты көптеген процестерде қолданылады.
-
Биоотын: ферменттер этанолға негізделген отын өндіру үшін көмірсуларды ыдыратуда қолданылады.
-
Тағам өнімдерін өндіру: ферменттер сүт өнімдері мен сыра өндіруде кеңінен қолданылады.
-
Тоқыма өнеркәсібі: ферменттер мата өндіруге қажетті талшықтарды өңдеуде маңызды.
-
Қағаз: ферменттер ағаш сүректерінен қағаз өндіруде пайдаланылады.
Зертханалық жұмыс: «Иммобилизациялаудың ферменттердің белсенділігіне әсерін зерттеу»
Лактаза ферментін оқшаулау әдісін қарастырып көрейік. Бұл – сүтқоректілердің балаларында ағзаға ана сүтімен келген лактозаны ыдырататын фермент. Аш ішекте лактозаны галактоза мен глюкозаға айналдырады.
Кейбір ересек адамдарда лактазаның түзілуі баяулайды. Сондықтан сүт өнімдерін қабылдай алмаушылық туындайды. Қорытылмаған лактоза тоқ ішекке түсіп, ондағы микрофлора арқылы ыдырай бастайды. Бактериялық ыдыраудың нәтижесінде газ бөлініп, адам іштің кебуі, түйілуі, бұлшықеттің құрысуы, диарея, метеоризмге душар болады. Осыған байланысты лактаза ферментін оқшаулап, оны сүтке қосып қолдану үшін өндіреді. Коммерциялық мақсатта оқшауланған лактазаны картон қорапшалардағы сүтке қосып өндіреді. Ондай сүттер лактазамен байытылған болып келеді.
Бұл зертханалық жұмыстың мақсаты лактозаны натрий альгинатынан жасалған түйіршіктерінде оқшаулап алып, оның сүттегі лактозаға әсерін зерттеу.
Қажетті құрал-жабдықтар:
-
Лактаза ферменті (лактозим) – 2 мл
-
Натрий альгинатының 2% ерітіндісі (2 грамды 100 мл суға қосып, ұзақ араластыру) – 8 мл
-
Пастерленбеген сүт – 50 мл
-
Қандағы глюкозаны анықтауға арналған тест жолақ қағаздары
-
Инесіз пластик 10 мл шприц – 1 дана
-
100 мл мензурка – 3 дана
-
Шай сүзгіш – 1 дана
-
Секундомер
-
Шыны таяқша – 1 дана
Қауіпсіздік ережесі:
Лактоза – қауіпсіз фермент. Бірақ жұмыс барысында онымен тікелей жанасуды болдырмаған жөн. Сонымен қатар иіскеуге, татып көруге болмайды. Көзге түсіп кетсе, таза сумен жақсылап шаю керек.
Жұмыс барысы:
-
Алдымен ферментті натрий альгинатымен араластыр.
-
Осы шприцке қоспаны сорғызып ал.
-
Кальций хлоридінің ерітіндісін бір мензуркаға құй.
-
Шприцтегі қоспаны бір тамшыдан кальций хлориді ерітіндісіне тамшылат.


5. Ерітіндіде пайда болған ұсақ түйіршіктерді қатаюы үшін 2-5 минутқа қалдыр.

6. Осы түйіршіктерді шай сүзгішпен сүзіп ал.

7. Түйіршіктерді бос мензуркаға сал.
8. Түйіршіктерді дистильденген су арқылы бірнеше рет шай.

9. Сүтті таза мензуркаға құй.
10. Тест жолақшасы арқылы сүт құрамында глюкоза бар-жоғын тексер.
11. Сүтке түйіршіктен бірнешеуін салып, шыны таяқшамен араластыр.
12. 10 минуттаң соң ондағы сүтте глюкозаның болуын тест арқылы тексер.
13. Тест жолақшасы түсінің өзгеруін бақыла. Түстің өзгеруі сүтте лактаза арқылы лактозаның глюкоза мен галактозаға ыдырағанын көрсетеді.
Артқа
№2 зертханалық жұмыс
«Активаторлар мен ингибиторлардың ферменттік реакцияның жылдамдығына әсерін зерттеу» зертханалық жұмысы
Өте төмен концентрацияда ферменттердің белсенділігін арттыратын (активаторлар) немесе, керісінше, оны төмендететін заттар бар (ингибиторлар). Мысалы, асқазан сөліндегі пепсиногеннің активаторы (пепсиннің ізашары) – тұз қышқылы, сол тұз қышқылы сілекей амилазасының ингибиторы болып саналады.
Активаторлар мен ингибиторлар белсенді орталықта немесе одан алыс орналасқан фермент молекуласының аллостериялық орталығында әрекет ете алады.
Ферменттердің белсенділігін арттыратын заттар қатарына металл катиондары немесе аниондар және басқа да заттар жатады. Көбінесе ферменттердің активаторы ретінде Ca2+, Mg2+ , K+ және Na+ катиондары, Cl- аниондары қызмет атқара алады. Активаторлар фермент-субстрат кешенін түзуге немесе оны тұрақтандыруға көмектеседі.
Ферментативті реакцияның барысын тежейтін ингибиторлар арнайы емес (денатурациялайтын реактивтер – ауыр металдардың тұздары, қышқыл, сілтілер, барлық ферментті белсенді етпейтін) және арнайы болып бөлінеді. Соңғылары тек белгілі бір ферменттерге әсер ететін қайтымсыз және қайтымды болып бөлінеді. Қайтымсыз реакция кезінде ферменттің белсенді орталығын немесе бүкіл молекуласын өзгертеді және олар жойылғаннан кейін белсенділігі қалпына келмейді. Қайтымды рекция кезінде фермент жұмысын уақытша тежейді, сондықтан ферменттердің белсенділігі қалпына келеді. Қайтымды ингибиторлар бәсекелес және бәсекелес емес болып бөлінеді.

Зертханалық жұмыста фермент ингибиторларының әсерін зерделеу үшін келесі тәжірибелерді жүргізу ұсынылады:
1. CuSO4 мыс тұзының ингибиторын қолданып, тәжірибе жасау.
2. Бақылау эксперименті (CuSO4 мыс тұз ингибиторынсыз).
Зерттеудің теориялық бөлігі
Каталаза ферменті сутек асқын тотығының ыдырауын катализдейді:
2H2O2 2H2O + O2
Каталаза жасушаларда өте жиі кездеседі. Бұл фермент жасушалардың қорғаныс механизмі ретінде қызмет етеді. Сутек асқын тотығы – белгілі бір метаболикалық реакциялардың жиі кездесетін өнімі және өте улы зат. Каталаза сутек асқын тотығын жасуша зақымдалуы мүмкін болғанға дейін түзеді.
Тәжірибелік бөлім
Іс жүзінде реакция ферменттерінің катализденуі жылдамдық реакция қоспасынан кететін субстрат мөлшері немесе белгілі бір уақыт аралығында жинақталған өнім мөлшері ретінде қабылданады. Каталазамен жұмыс кезінде өнімнің (оттектің) жиналу жылдамдығын өлшеу ыңғайлы. 30 секундта босатылған оттегі көпіршіктерінің саны бойынша реакцияның бастапқы жылдамдығын есептеуге болады.
Материалдар мен жабдықтар:
Жапқыштары бар сынауықтар – 4 дана
Тамшуыр – 2 дана
Өлшейтін стақан – 2 дана
Газды бұрғыш түтікшелер – 4 дана
Секундомер
Су моншасы
Ашытқы суспензиясы
0,1 М CuSO4 ерітіндісі
Дистильденген H2O
Пайдаланылған құрылғы төмендегі суретте көрсетілген.

Ашытқы суспензиясы фермент көзі ретінде пайдаланылды. Жарты минуттық аралықта шығарылған көпіршіктердің саны есептеліп, әр реакция қоспасы үшін екі минут ішінде тіркелді.
Пайдаланылған реакция қоспалары және алынған нәтижелер төмендегі кестеде көрсетілген.
1-кесте. Ферменттің жұмысы кезінде ауыр металдардың тұздарын қолданудың әсері
|
1-тәжірибе |
Сынауық нөмірі
|
||||
|
Дистильденген су (см3) |
|
||||
|
0,1 CuSO4 |
|
||||
|
H2O мөлшері (мл) |
|
||||
|
Ашытқы саңырауқұлақ езіндісі(см3) |
|
||||
|
Реакцияның бастапқы жылдамдығы (30 cекундта бөлінген көпіршік саны) |
|
2-кесте. Ферментті ингибиторсыз қолданудың әсері.
|
2-тәжірибе |
Сынауық нөмірі
|
||||
|
Дистильденген су (см3) |
|
||||
|
H2O мөлшері (мл) |
|
||||
|
Ашытқы саңырауқұлақ езіндісі (см3) |
|
||||
|
Реакцияның бастапқы жылдамдығы (30 cекундта бөлінген көпіршік саны) |
|
Тәжірибе нәтижелері мыс тұздарын қолданғандағы реакцияның бастапқы жылдамдығы фермент ингибиторсыз жұмыс істеген жағдайға қарағанда әлдеқайда төмен екенін көрсетті.
№3 зертханалық жұмыс
«Әртүрлі өсімдік жасушаларында фотосинтездеуші пигменттердің болуын зерттеу» зертханалық жұмысы
Өсімдік жапырағының түсі маңызды морфологиялық белгілердің бірі болып табылады. Өсімдік жапырағында негізгі төрт пигмент: хлорофилл a, хлорофилл b, ксантофилл, каратиноид кездеседі. Жасыл өсімдік пигменттері жарық энергиясын сіңіріп, химиялық энергияға айналдырады. Жарықты сіңіруге әртүрлі пигменттер қатысады. Жапырақтағы пигменттердің қоспасын хроматография қағазы бойынша түсті жолақтарға бөлуге болады.

Хроматография әдісі таңдалған еріткіштегі молекулалардың әртүрлі ерігіштігіне байланысты молекулаларды ажыратады. Хроматографиялық әдістің негізін салушы орыс ботанигі М.С.Цвет «Хроматография грекше «түсті жазу» дегенді білдіреді. Бұл әдіс арқылы жапырақ пигменттерінің сұйық қоспасын әртүрлі компоненттерге бөлуге болады» деген.
Бұл тәжірибе өсімдік жапырағынан фотосинтетикалық пигменттерді шығарып алуды және хроматографиялық немесе сүзгі қағаздарын қолдану арқылы пигмент түрлерін өзара бөліп ажыратуды көрсетеді.
Жапырақтағы пигменттер қоспасын хроматография қағазы арқылы ұқсас компоненттерге бөлуге болады. Қоспа құрамындағы полярлы заттар целлюлозамен әрекеттесіп, тез тежеліп қалады. Ал полярлығы төмен заттар алдыға қарай жылжи береді. Пигменттер қағазға сіңеді де, еріткіштің капиллярлық әрекеті оларды қағазға қарай тартады. Әр пигменттің бастапқы сызықтан жылжу қашықтығы әртүрлі болады. Еріткіште пигменттердің еруі бірдей болмайды. Ерігіштігі жоғары пигменттер (каратиноид) ерітінді шекарасына жақын орналасса, аз еритін пигмент қысқа қашықтыққа жылжып, бастапқы сызыққа жақын орналасады. Бөлінген компоненттердің үлгісі хроматограммада түрлі түсті жолақ түрінде көрінеді. Еріткіште хлорофилл а пигментінің ерігіштігі хлорофилл b пигментіне қарағанда жоғары болып келеді. Ал ксантофилл пигментінің ерігіштігі хлорофилл b пигментінен жоғары.
Rf (ұстап қалу коэффициенті) мәнін есептеу арқылы бір түрге жататын өсімдік жапырақтарының пигмент түрі мен санын немесе екі түрлі өсімдік жапырақ пигменттерін салыстырып анықтауға болады. Rf (ұстап қалу коэффициенті) мәнін пигмент жылжыған қашықтық/ерітінді жылжыған қашық арқылы анықтайды.
Rf (ұстап қалу коэффициенті) мәнін есептеу формуласы:
Rf =
пигмент жылжыған қашықтығы (mm)
–––––––––––––––––––––––––––––––––
ерітінді жылжыған қашықтығы (mm)
№4 зертханалық жұмыс
«С3 және С4 өсімдіктер жапырақтарының мезофилін микропрепараттар арқылы зерттеу» зертханалық жұмысы
1-конспект
Мезофилл жасушаларының
хлоропластарында жарық реакцияларының
жүруі басым және АТФ-тың көп мөлшері, НАДФН
және O2 түзіледі. Іс жүзінде
РиБФ-карбоксилаза
болмағандықтан, CO2

шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
