
Суммативной работы за 2 четверть по Химий для 8-го класса
Критерии оценивания:
-
Правильное определение молярной массы.
-
Корректно рассчитанные молярные массы.
-
Рассчитано количество вещества.
-
Определения экзотермической и эндотермической реакций.
-
Указывает, что для экзотермических реакций энергия продуктов меньше энергии исходных веществ, а для эндотермических — наоборот.
-
Водород.Кислород.Озон
Инструкция для выполнения работы:
• Время выполнения: 40–60 минут.
• Заполните ответы чётко и по существу.
• Приводите расчёты в решении задач.
1. Количество вещества и стехиометрические расчёты
Задание 1 (Понимание)
-
Что такое молярная масса вещества? Укажите её единицы измерения.
2. Рассчитайте молярную массу следующих веществ:
• KNO3
• AqNO3
Задание 2 (Применение)
Сколько молекул содержится в 36 г воды?
(Молярная масса , число Авогадро ).
Задание 3 (Анализ)
1.Определите массовую долю углерода в веществе C2H6O .
Задание 4 (Понимание)
1. Чем экзотермическая реакция отличается от эндотермической?
-
Приведите пример реакции каждого типа.
Задание 5 (Применение)
Тепловой эффект реакции горения метана CH4 равен -890 кДж на 1 моль. Сколько энергии выделится при сжигании 5 моль CH4?
Задание 6 (Анализ)
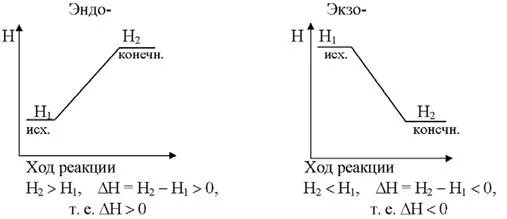
Проанализируйте график энергетических профилей экзотермической и эндотермической реакций. Объясните разницу в положениях исходных веществ и продуктов по энергии.
Задание 7 (Понимание)
-
Какие свойства делает водород перспективным топливом?
-
Почему озон называют “защитником планеты”?
Задание 8 (Работа с таблицей)
Заполните таблицу, используя данные о химических элементах водорода, кислорода и озона.
|
Вещество |
Химическая формула |
Молекулярная масса (г/моль) |
Область применения |
|
Водород |
|
|
|
|
Кислород |
|
|
|
|
Озон |
|
|
|
Задание 9 (Практическое задание)
Представьте, что вы проводите эксперимент по разложению пероксида водорода (H2O2) с использованием катализатора.
1. Опишите, какие меры безопасности нужно соблюдать при проведении эксперимента.
Задание 10 (Решение задачи)
Рассчитайте массу воды, которая образуется при сгорании 10 г водорода.
Задание 11 (Творческое задание)
Представьте, что водород стал основным топливом на планете. Перечислите плюсы и минусы этого сценария.
Задание 12 (Обобщение)
Какие свойства водорода, кислорода и озона делают их жизненно важными для природы и человека? Ответ аргументируйте.
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
8 класс соч 2 четверть
Суммативной работы за 2 четверть по Химий для 8-го класса
Критерии оценивания:
-
Правильное определение молярной массы.
-
Корректно рассчитанные молярные массы.
-
Рассчитано количество вещества.
-
Определения экзотермической и эндотермической реакций.
-
Указывает, что для экзотермических реакций энергия продуктов меньше энергии исходных веществ, а для эндотермических — наоборот.
-
Водород.Кислород.Озон
Инструкция для выполнения работы:
• Время выполнения: 40–60 минут.
• Заполните ответы чётко и по существу.
• Приводите расчёты в решении задач.
1. Количество вещества и стехиометрические расчёты
Задание 1 (Понимание)
-
Что такое молярная масса вещества? Укажите её единицы измерения.
2. Рассчитайте молярную массу следующих веществ:
• KNO3
• AqNO3
Задание 2 (Применение)
Сколько молекул содержится в 36 г воды?
(Молярная масса , число Авогадро ).
Задание 3 (Анализ)
1.Определите массовую долю углерода в веществе C2H6O .
Задание 4 (Понимание)
1. Чем экзотермическая реакция отличается от эндотермической?
-
Приведите пример реакции каждого типа.
Задание 5 (Применение)
Тепловой эффект реакции горения метана CH4 равен -890 кДж на 1 моль. Сколько энергии выделится при сжигании 5 моль CH4?
Задание 6 (Анализ)

Проанализируйте график энергетических профилей экзотермической и эндотермической реакций. Объясните разницу в положениях исходных веществ и продуктов по энергии.
Задание 7 (Понимание)
-
Какие свойства делает водород перспективным топливом?
-
Почему озон называют “защитником планеты”?
Задание 8 (Работа с таблицей)
Заполните таблицу, используя данные о химических элементах водорода, кислорода и озона.
|
Вещество |
Химическая формула |
Молекулярная масса (г/моль) |
Область применения |
|
Водород |
|
|
|
|
Кислород |
|
|
|
|
Озон |
|
|
|
Задание 9 (Практическое задание)
Представьте, что вы проводите эксперимент по разложению пероксида водорода (H2O2) с использованием катализатора.
1. Опишите, какие меры безопасности нужно соблюдать при проведении эксперимента.
Задание 10 (Решение задачи)
Рассчитайте массу воды, которая образуется при сгорании 10 г водорода.
Задание 11 (Творческое задание)
Представьте, что водород стал основным топливом на планете. Перечислите плюсы и минусы этого сценария.
Задание 12 (Обобщение)
Какие свойства водорода, кислорода и озона делают их жизненно важными для природы и человека? Ответ аргументируйте.

шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
