
Сабақтың тақырыбы: Алюминий.
Сабақтың білімділік мақсаты: Алюминийдің периодтық жүйедегі орны
мен атом құрылысын, физикалық-химиялық қасиет-
терін, қолданылуын, табиғатта таралуы мен маңызды
қосылыстарын үйрету.
Сабақтыңy2nb;tc3 : Деңгейлік тапсырмаларды орындау арқылы
оқушылардың өз бетінше ойлай білу, қорытынды
жасай білу қабілеттерін дамытады.
Пәнаралық байланыс: физика, биология, география, медицина ғылымы.
Сабақтың түрі: аралас сабақ.
Сабақтың әдісі: сұрак-жауап, түсіндіру, СТО, ақпараттық технология бойынша дамыта оқыту.
Көрнекілігі: сызба-кесте, графопроектор, фотосуреттер.
Сабақтың барысы:
І кезең. Ұйымдастыру кезеңі: сәлемдесу, кезекшіні анықтап, оқушыларды түгендеу.
ІІ кезең. «Ой қозғау» кезеңінде оқушыларға тапсырмалар беру арқылы үй тапсырмасы пысықталады.
-
Кальцийдің периодтық жүйедегі орны, электрондық формуласы.
-
Тотығу дәрежесі.
-
1-қатар: кальцийдің оттекпен;
2-қатар: кальцийдің күкіртпен;
3-қатар: кальцийдің сумен;
4-қатар: қышқылмен әрекеттесу реакциясының теңдеуін жазыңдар.
4. Судың уақытша, тұрақты кермектіліг туралы не білесіздер?
ІІІ кезең. «Ұғыну» кезеңі: жаңа сабақ түсіндіріледі.
Мұғалімнің кіріспе сөзі:
Болмаса да айтарлықтай салмағым
Көп металдан ардақтымын алдамын
Ұшақ болып аспанға ұшып, қалықтап,
Жердің жүзін,көк аспанды шарладым.
Дюралюмин дейтін менің қоспамды,
Әспеттейді химияның достары
Тұрмыста үстел,ыдыс-аяқ кереует,
Бағандардың бұйдаларын қостым мен
Қағаз да мен кәмпит,шайды сәндеген
Токқа балқып келіп тұрған ән де мен.
(Балалар, бұл өлең жолдарында айтылған қай металл?)
Алюминий – «Қанатты металл».
Периодтық жүйедегі орны:
1.Химиялық таңбасы- Al
2.Реттік нөмірі- 13
3.Ar(Al)- 27
4.Период нөмірі- ІІІ (кіші)
5.Топ нөмірі-ІІІ (негізгі)
Атом құрылысы:
1.Ядро заряды- +13
2.Электрон саны- 13
3.Протон саны- 13
4.Нейтрон саны -14
5.Энергетикалық деңгей саны -3
Электрондық формуласы: 13Al 1S2 2S2 2p6 3S2 3p1
Графиктік формуласы.
1s 2s 2p 3s 3p
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑
Алюминийдің табиғатта таралуы.
Алюминий табиғатта таралуы жөнінен оттек пен кремнийден кейінгі үшінші орында, металлдар арасында бірінші орында. Жер қыртысындағы массалық үлесі 88%. Белсенді металл болғандықтан алюминий табиғатта тек қосылыстар түрінде кездеседі. Жер қыртысының негізгі бөлігін алюмосиликаттар құрайды. Алюмосиликаттар мүжілгенде (каолинит) балшық түзіледі.



![]()
![]()
![]()
Табиғатта таралуы


![]()
![]()
![]()
![]()
![]()



Корунд Al2O3 - өте қатты, түссіз минерал. Егер оның құрамында қоспа көп болса, ол әр түрлі бағалы тастарға айналады: рубин, сапфир, аметист, бирюза.
Боксит Al2O3* n H2O – тау жынысы. Ол негізгі өнеркәсіпте алюминий алуға арналған шикізат болып табылады.
Алюминий кендерінің бай қорлары Қазақстанда, Оралда, Хибин тауларында, Башкирияда, Сібірде кездеседі. Қазақстанда бокситтердің белгілі кен орындары бар. Олар Қостанай және Ақтөбе облыстарында орналасқан. Павлодар алюминий зауытында металл күйіндегі алюминий өндіріледі.
Алюминийдің биологиялық рөлі.
Ересек адам күніне алюминийдің 30-50 мг қажет етеді. Күнделікті өмірде оны нан өнімдерінен аламыз. Шайдың құрамында суға қарағанда 20-200 есе көп болады. Алюминий судың, ауаның, дәрілік препараттың, иіссулардың, алюминийден жасалған ыдыстардың құрамында болады. Ол эпителий мен байланыстырғыш ұлпалардың дамуына, сүйек ұлпаларының түзілуіне, фосфор алмасуына әсер етеді. Алюминий зат алмасуға, жүйке жүйесінің қызметіне, жасушаның көбеюі мен өсуіне кері әсерін тигізеді. Сонымен қатар ағзадағы көп мөлшері қозғалыс белсенділігінің төмендеуіне, есінен тануына да әсер етеді. Кейбір зерттеулерде алюминий мидың зақымдануына да әсер етеді. Алюминий тұздарының көп болуы ағзадағы кальцийді төмендетеді, фосфордың адсорбциялануын азайтады, сүйектегі, бауырдағы, мидағы алюминийдің құрамын 10-20 есеге артырады.
Алюминийдің алынуы.
2![]() Al2O3
электролиз 4Al +
3O2
– 3352
кДж
Al2O3
электролиз 4Al +
3O2
– 3352
кДж
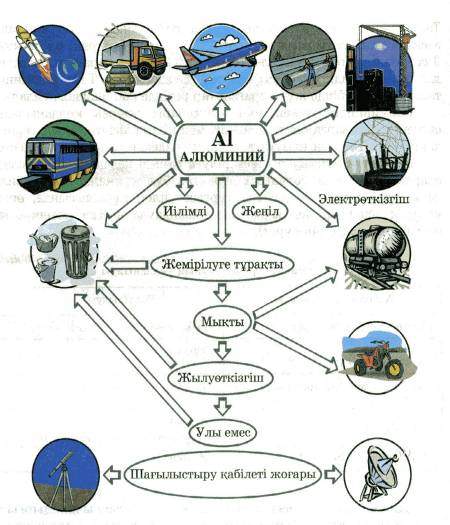
Алюминийдің физикалық қасиеті.
Алюминий – күміс түсті, ақ, жеңіл металл. Тығыздығы – 2,7 г/см3, балқу температурасы – 660,40С, қайнау температурасы – 24670С.
Өте иілімді, одан жіңішке сым жасауға болады. Сондай-ақ фольгаға айналдырып таптауға болады. Электр өткізгіштігі күміс пен мыстан кейінгі деңгейде.
Химиялық қасиеттері.
-
4Al + 3O2 = Al2 O3
Al2 O3 қабықшасының қалыңдығы 0,00001 мм. Балқу температурасы – 20500С. Оксид қабықшасы металлдың бетіне күңгірт түс береді.
-
Сұйық алюминий сумен қарқынды әрекеттеседі:
2Al + 6H2O = 2Al(OH)3 + 3H2 ↑
-
Алюминий қышқылдардағы сутекті тотықсыздандырады:
2 Al + HCl = 2AlCl3 + 3H2↑
-
Екідайлы болғандықтан сілтілермен де оңай әрекеттеседі:
2Al + 6NaOH = 2Na3AlO3 + 3H2↑
Алюминий құймаларының қолданылуы.
|
Алюминий құймалары |
Қолданылуы |
|
1. Магиалий Al – Mn - Mg |
Кеме және ракета жасау |
|
2. Дуралюминдер (Al – Mg – Si – Cu) |
Ұшақ жасау |
|
3. Al – Cu – Mn |
Ғарыш кемелері |
|
4. Al – Mg – Si |
Құрылыс Тікұшақтардың бұрамалары (винттері) |
|
5. Силумин (Al – Si – Na) |
Машина жасау |
ІҮ кезең. «Деңгейлік тапсырмалар» кезеңі: оқулықтан, тақтадан тапсырма-лар орындау.
1-деңгей:
а) Алюминийдің периодтық жүйедегі орны.
ә) Табиғатта кездесуі.
б) Алюминийдің физикалық қасиетін айтыңдар.
2-деңгей:
а) Алюминийдің оттекпен әрекеттесуінің реакциясын жазыңдар.
ә) Алюминийдің күкіртпен әрекеттесуінің реакциясын жазыңдар.
б) Алюминийдің тұз қышқылымен әрекеттесуінің реакциясын жазыңдар.
3-деңгей:
(Оқулықпен жұмыс, №9 есеп, 135-бет)
Массасы 15,2 хром оксидін Cr2 O3 алюминиймен тотықсыздандырғанда 9 грамм хром түзіледі. Хромның теориялықпен салыстырғандағы шығымын процентпен көрсетіңдер.
Сабақты қорытындылау.
Білімдерін бағалау.
Үйге тапсырма: Алюминий. №8 жаттығу.
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Алюминий және оның қосылыстары
Сабақтың тақырыбы: Алюминий.
Сабақтың білімділік мақсаты: Алюминийдің периодтық жүйедегі орны
мен атом құрылысын, физикалық-химиялық қасиет-
терін, қолданылуын, табиғатта таралуы мен маңызды
қосылыстарын үйрету.
Сабақтыңy2nb;tc3 : Деңгейлік тапсырмаларды орындау арқылы
оқушылардың өз бетінше ойлай білу, қорытынды
жасай білу қабілеттерін дамытады.
Пәнаралық байланыс: физика, биология, география, медицина ғылымы.
Сабақтың түрі: аралас сабақ.
Сабақтың әдісі: сұрак-жауап, түсіндіру, СТО, ақпараттық технология бойынша дамыта оқыту.
Көрнекілігі: сызба-кесте, графопроектор, фотосуреттер.
Сабақтың барысы:
І кезең. Ұйымдастыру кезеңі: сәлемдесу, кезекшіні анықтап, оқушыларды түгендеу.
ІІ кезең. «Ой қозғау» кезеңінде оқушыларға тапсырмалар беру арқылы үй тапсырмасы пысықталады.
-
Кальцийдің периодтық жүйедегі орны, электрондық формуласы.
-
Тотығу дәрежесі.
-
1-қатар: кальцийдің оттекпен;
2-қатар: кальцийдің күкіртпен;
3-қатар: кальцийдің сумен;
4-қатар: қышқылмен әрекеттесу реакциясының теңдеуін жазыңдар.
4. Судың уақытша, тұрақты кермектіліг туралы не білесіздер?
ІІІ кезең. «Ұғыну» кезеңі: жаңа сабақ түсіндіріледі.
Мұғалімнің кіріспе сөзі:
Болмаса да айтарлықтай салмағым
Көп металдан ардақтымын алдамын
Ұшақ болып аспанға ұшып, қалықтап,
Жердің жүзін,көк аспанды шарладым.
Дюралюмин дейтін менің қоспамды,
Әспеттейді химияның достары
Тұрмыста үстел,ыдыс-аяқ кереует,
Бағандардың бұйдаларын қостым мен
Қағаз да мен кәмпит,шайды сәндеген
Токқа балқып келіп тұрған ән де мен.
(Балалар, бұл өлең жолдарында айтылған қай металл?)
Алюминий – «Қанатты металл».
Периодтық жүйедегі орны:
1.Химиялық таңбасы- Al
2.Реттік нөмірі- 13
3.Ar(Al)- 27
4.Период нөмірі- ІІІ (кіші)
5.Топ нөмірі-ІІІ (негізгі)
Атом құрылысы:
1.Ядро заряды- +13
2.Электрон саны- 13
3.Протон саны- 13
4.Нейтрон саны -14
5.Энергетикалық деңгей саны -3
Электрондық формуласы: 13Al 1S2 2S2 2p6 3S2 3p1
Графиктік формуласы.
1s 2s 2p 3s 3p
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑
Алюминийдің табиғатта таралуы.
Алюминий табиғатта таралуы жөнінен оттек пен кремнийден кейінгі үшінші орында, металлдар арасында бірінші орында. Жер қыртысындағы массалық үлесі 88%. Белсенді металл болғандықтан алюминий табиғатта тек қосылыстар түрінде кездеседі. Жер қыртысының негізгі бөлігін алюмосиликаттар құрайды. Алюмосиликаттар мүжілгенде (каолинит) балшық түзіледі.



![]()
![]()
![]()
Табиғатта таралуы


![]()
![]()
![]()
![]()
![]()



Корунд Al2O3 - өте қатты, түссіз минерал. Егер оның құрамында қоспа көп болса, ол әр түрлі бағалы тастарға айналады: рубин, сапфир, аметист, бирюза.
Боксит Al2O3* n H2O – тау жынысы. Ол негізгі өнеркәсіпте алюминий алуға арналған шикізат болып табылады.
Алюминий кендерінің бай қорлары Қазақстанда, Оралда, Хибин тауларында, Башкирияда, Сібірде кездеседі. Қазақстанда бокситтердің белгілі кен орындары бар. Олар Қостанай және Ақтөбе облыстарында орналасқан. Павлодар алюминий зауытында металл күйіндегі алюминий өндіріледі.
Алюминийдің биологиялық рөлі.
Ересек адам күніне алюминийдің 30-50 мг қажет етеді. Күнделікті өмірде оны нан өнімдерінен аламыз. Шайдың құрамында суға қарағанда 20-200 есе көп болады. Алюминий судың, ауаның, дәрілік препараттың, иіссулардың, алюминийден жасалған ыдыстардың құрамында болады. Ол эпителий мен байланыстырғыш ұлпалардың дамуына, сүйек ұлпаларының түзілуіне, фосфор алмасуына әсер етеді. Алюминий зат алмасуға, жүйке жүйесінің қызметіне, жасушаның көбеюі мен өсуіне кері әсерін тигізеді. Сонымен қатар ағзадағы көп мөлшері қозғалыс белсенділігінің төмендеуіне, есінен тануына да әсер етеді. Кейбір зерттеулерде алюминий мидың зақымдануына да әсер етеді. Алюминий тұздарының көп болуы ағзадағы кальцийді төмендетеді, фосфордың адсорбциялануын азайтады, сүйектегі, бауырдағы, мидағы алюминийдің құрамын 10-20 есеге артырады.
Алюминийдің алынуы.
2![]() Al2O3
электролиз 4Al +
3O2
– 3352
кДж
Al2O3
электролиз 4Al +
3O2
– 3352
кДж
Алюминийдің физикалық қасиеті.
Алюминий – күміс түсті, ақ, жеңіл металл. Тығыздығы – 2,7 г/см3, балқу температурасы – 660,40С, қайнау температурасы – 24670С.
Өте иілімді, одан жіңішке сым жасауға болады. Сондай-ақ фольгаға айналдырып таптауға болады. Электр өткізгіштігі күміс пен мыстан кейінгі деңгейде.
Химиялық қасиеттері.
-
4Al + 3O2 = Al2 O3
Al2 O3 қабықшасының қалыңдығы 0,00001 мм. Балқу температурасы – 20500С. Оксид қабықшасы металлдың бетіне күңгірт түс береді.
-
Сұйық алюминий сумен қарқынды әрекеттеседі:
2Al + 6H2O = 2Al(OH)3 + 3H2 ↑
-
Алюминий қышқылдардағы сутекті тотықсыздандырады:
2 Al + HCl = 2AlCl3 + 3H2↑
-
Екідайлы болғандықтан сілтілермен де оңай әрекеттеседі:
2Al + 6NaOH = 2Na3AlO3 + 3H2↑
Алюминий құймаларының қолданылуы.
|
Алюминий құймалары |
Қолданылуы |
|
1. Магиалий Al – Mn - Mg |
Кеме және ракета жасау |
|
2. Дуралюминдер (Al – Mg – Si – Cu) |
Ұшақ жасау |
|
3. Al – Cu – Mn |
Ғарыш кемелері |
|
4. Al – Mg – Si |
Құрылыс Тікұшақтардың бұрамалары (винттері) |
|
5. Силумин (Al – Si – Na) |
Машина жасау |

ІҮ кезең. «Деңгейлік тапсырмалар» кезеңі: оқулықтан, тақтадан тапсырма-лар орындау.
1-деңгей:
а) Алюминийдің периодтық жүйедегі орны.
ә) Табиғатта кездесуі.
б) Алюминийдің физикалық қасиетін айтыңдар.
2-деңгей:
а) Алюминийдің оттекпен әрекеттесуінің реакциясын жазыңдар.
ә) Алюминийдің күкіртпен әрекеттесуінің реакциясын жазыңдар.
б) Алюминийдің тұз қышқылымен әрекеттесуінің реакциясын жазыңдар.
3-деңгей:
(Оқулықпен жұмыс, №9 есеп, 135-бет)
Массасы 15,2 хром оксидін Cr2 O3 алюминиймен тотықсыздандырғанда 9 грамм хром түзіледі. Хромның теориялықпен салыстырғандағы шығымын процентпен көрсетіңдер.
Сабақты қорытындылау.
Білімдерін бағалау.
Үйге тапсырма: Алюминий. №8 жаттығу.

шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
