
М.ТЫНЫШБАЕВ АТЫНДАҒЫ ҚАЗАҚ КӨЛІК
ЖӘНЕ КОММУНИКАЦИЯЛАР АКАДЕМИЯСЫНЫҢ
ШЫМКЕНТ КӨЛІК КОЛЛЕДЖІ
2022-2023 оқу жылы
Сабақ жоспары №53
|
Модуль/пән атауы |
Химия |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Сабақ тақырыбы: |
Фенолдар |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Педагог |
Билалова Нафасат Хикматовна |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Курс |
1 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Топ |
ЭНС22-9-1 |
ЭНС 22-9-2 |
ПМ-22-9 |
Л-22-9-1 |
Л -22-9-2 |
В-22-9 |
РЭТ 22-9 |
СЖД 22-9 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Сабақтың өткізілу уақыты |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Жалпы мақсаттар: |
фенолдар жайлы түсініктер береді. Оның құрылысы, қасиеттері мен қолданылуын қарастыру. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Күтілетін нәтижесі |
фенолдар жайлы түсініктер беру. Оның құрылысы, қасиеттері мен қолданылуын қарастырады. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Сабақта қолданылатын модульдер |
Оқыту мен оқудағы жаңа тәсілдер: топтық жұмыс, диалогтық оқыту, сергіту сәті; СТО: Блум таксономиясы бойынша жұмыстандыру Оқыту мен оқуда АКТ қолдану компьютер, ғаламтор Оқушылардың жас ерекшеліктеріне сәйкес оқыту және оқу: деңгейлі тапсырмалар Оқыту үшін бағалау және оқуды бағалау: ынталандыру, кері байланыс; Талантты және дарынды балаларды оқыту: кеңейтілген тапсырмалар Оқытуды басқару және көшбасшылық: мұғалім мен оқушы бірге көшбасшы |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Сабақтың көрнекілігі |
Интерактивті тақта, маркер, қарындаш, плакаттар, слайдтар. 11-сынып электрондық оқулық. АКТ-ны пайдаланып, жас ерекшеліктеріне сай сұрақтар мен тапсырмалар, ББү кестесі |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Ұйымдастыру кезеңі |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Қызығушылықты ояту (20 минут) |
І-тапсырма.т Сұрақ –жауап. 1.Көпатомды спирттерге кандай заттар жатады? 2. Глицериннін суда шексіз еру себебін калай түсіндіруге болады? 3. Глицериннің өзінен кейінгі гомологының формуласын жазып, халықаралық атау жүйесі бойынша атаңдар. 4. 1,2,3-трибромпропаннан глицерин алу теңдеуін жазыңдар. 5. а) Атаулары бойынша мына заттардын формулаларын жазыңдар: пропанол-1, пропандиол-1,2, пропантриол-1,2,3; ә) осы заттарды өзара гомолог немесе изомер деуге бола ма? Дәлелді жауап беріңдер. 6. Мына этилен қатарының көмірсутектерін гидратациялап, спирт алу қажет: а) 2-метил-2-пентенді; б) 4-метил-2-пентенді. Алынған спирттердің аттарын атау керек. 7. Галогеналкилдерге а) 3-метил-1-хлорбутанға; б) 2,2-диметил-1-бромгексанға; в) 3,3-диметил-3-иодгептанға; д) иод-изопропанға сілтінің судағы ерітіндісін қосып, алынған спирттерді атау керек. 8. Мына гликолдерді а) 1,3-пропандиолді б) 2-метил-1,4-бутандиолды сәйкесінше галогентуындыларды гидролиздеп алу керек, реакция теңдеулерін жазу қажет. 9. Мына көмірсутектерден а) СН2 = СН - СН2 - СН3; б) СН3 – СН = СН - СН3; в) СН3 - СН(СН3) – СН = СН2 гликолдерді алу реакция теңдеулерін жазу керек. ІІ-тапсырма. Өзіндік жұмысы. І-деңгей 1. Көпатомды спирттердің біратомды спирттерден қандай өзгешеліктері бар? 2.Екіатомды және үшатомды спирттердің алгашқы өкілдерінің (этиленгликоль мен глицериннің) қүрылым формулаларын жазып, оларды халықаралық атау жүйесі бойынша атаңдар. ІІІ-тапсырма. Есеп шығару. 1. 0,7 моль глицерин мен натрий әрекеттескенде түзілетін сутектің (қ.ж.) көлемі Шешуі: 2С3Н8О3 + 6Na → 2C3H5(ОNa)3 +3Н2 ν (С3Н8О3)= 2 моль 3V(Н2) = 67,2 л/моль х л Н2---- 0,7 моль С3Н8О3 67,2 л Н2 ---- 2 моль С3Н8О3
2. 0,5 моль натриймен әрекеттесетін этиленгликольдің массасы Шешуі: С2Н4(ОН)2 + 2Nа → (СН2ОNа)2 + Н2 М(С2Н4(ОН)2) = 62 г/моль ν(Na) = 2 моль х г С2Н4(ОН)2 ------ 0,5 моль Na 62 г С2Н4(ОН)2 ------2 моль Na
3. Массасы 217 грамм этиленгликольдің зат мөлшері (моль) Шешуі: v (С2Н4(ОН)2) = 1 моль М(С2Н4(ОН)2) = 64 г/моль х моль С4Н8 ----217 г С2Н4(ОН)2 1 моль С4Н8 ---- 62 г С2Н4(ОН)2
ІV-тапсырма. Тест жұмысы. (4-сұрақтан) І-нұсқа. 1. Көп атомды спирт: А) фенол;В) толуол;С) стирол;Д) этиленгликоль. 2. Мына заттардың әрекеттесуі нәтижесінде көп атомды спирт алуға болады: А) хлорэтан және спиртті сілті ерітіндісі; В) хлорэтан және сулы сілті ерітіндісі; С) дихлорэтан және сулы сілті ерітіндісі;Д) дихлорэтан және спиртті сілті ерітіндісі. 3. Спирттердің ішінде тек көп атомды спирт әрекеттесетін зат: А) О2;В) Nа;С) НВr;Д) Си(ОН)2; 4. Динамит ойлап тапкан және оны әр турлі елге патент ретінде ұсынған ғалым: А) А.Бутлеров;В) А.Нобель;С) Ш.Вюрц;Д) С.Лебедев. ІІ-нұсқа. 1. Этиленгликоль алуда қолданылатын реакция: А) этиленнің сілтімен әрекеттесуі;В) ацетиленнің сумен әрекеттесуі; С) хлорэтанның сілтімен әрекеттесуі; Д) этиленнің перманганат ерітіндісімен әрекеттесуі. 2. Көп атомды спирттерге сапалық реакция: А) NаОН;В)ҒеСІ3; С) СиО; Д)Си(ОН)2. 3. Этиленгликольдің қолданылуы: А) оның сулы ерітінділерінің кату температурасының төмендігімен байланысты; В) оның ерітіндісінің адам организміне әсеріне байланысты; С) оның жағымды иісіне байланысты; Д) оның ерітінділерінің тұткырлығына байланысты. 4. Лавсан талшығын алуда қолданылатын спирт: А) этанол;В) глицерин;С) этиленгликоль;Д) метанол. V-тапсырма. Кесте толтыру. Көпатомды спирттердің химиялық қасиеттерін біратомды спирттермен салыстырып, берілген кестені толтырыңдар:
2. Көпатомды спиртердің негізгі қолдану салаларын көрсетіңдер:
VІ-тапсырма. Жауабы 1-кесте бойынша. Көп атомды спирттер деп: 1. көмірсутек радикалдармен байланысқан бір гидроксил тобы бар күрделі молекулалар; 2. молекуласында оттек болатын органикалық заттар; 3. молекуласында әртүрлі функционал топтар болатын қосылыстар; 4. молекуласында көмірсутек радикалымен байланысқан бірнеше гидроксил тобы бар органикалық заттар. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Жаңа сабақ (40 минут) |
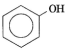
Фенолдар — бензол сақинасындагы бір немесе бірнеше сутек атомдарының орнын гидроксотоп басқан ароматты көмірсутектердің туындылары. Ең қарапайым өкілі—фенолС₆Н₅ОНнемесегидроксибензол.
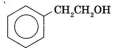
Ароматты көмірсутектердің бүйір тізбектеріндегі сутек атомдарының орнын гидроксотоп баскан өнімдер ароматты спирттер деп аталады:
Алынуы. Фенолды көбіне тас көмір шайырын өңдеу арқылы алады. Сондай-ак ароматты көмірсутектерінің галогентуындыларын сілтімен әрекеттестіріп те алады:
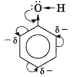
Өндірісте бастапқы шикізаттар ретінде бензол мен пропиленді пайдаланып, кумольді әдіспен фенол алу іске асырылған. Физикалық қасиеттері. Фенол — түссіз кристалдық зат. 43°С-та балқиды. Ауада ашық қалғанда тотығатындықтан, қызғылт түсті болады. Бөлме температурасында аздап қана ериді, ал 60°С-тан жоғары қыздырғанда, суда шексіз ериді. Фенол — улы зат, теріні күйдіреді. Ерітіндісі антисептик ретінде қолданылады. Химиялық қасиеттері. Фенол молекуласындағы атомдар бір-біріне өзара әсер ететіндіктен, полярлы қосылыс болады:
Молекуладағы гидроксотоптың
оттек атомының бөліспеген электрон жүптары ығысуы әсерінен
сақинадағы π-электрондар жүйесінің біркелкілігі бұзылып, сақинаның
үш жерінде (2,4,6) электрон тығыздығы артады. Сондықтан өз
кезегіңде гидроксотоптағы сутек атомы қозғалғыш болады. Бұл жағдай
фенолдың судағы ерітіңдісінде қышқыл сияқты диссоциациялануына
себеп болады. Сол себепті, фенолдың 1 %-тік
ерітіндісін карбол
қышқылы Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз М.ТЫНЫШБАЕВ АТЫНДАҒЫ ҚАЗАҚ
КӨЛІК ЖӘНЕ КОММУНИКАЦИЯЛАР
АКАДЕМИЯСЫНЫҢ
ШЫМКЕНТ КӨЛІК
КОЛЛЕДЖІ
2022-2023 оқу
жылы
Сабақ жоспары
№53 Модуль/пән
атауы Химия Сабақ
тақырыбы: Фенолдар Педагог Билалова Нафасат
Хикматовна Курс 1 Топ ЭНС22-9-1 ЭНС
22-9-2 ПМ-22-9 Л-22-9-1 Л
-22-9-2 В-22-9 РЭТ
22-9 СЖД
22-9 Сабақтың өткізілу
уақыты Жалпы
мақсаттар: фенолдар жайлы түсініктер
береді. Оның құрылысы, қасиеттері мен қолданылуын
қарастыру. Күтілетін нәтижесі фенолдар жайлы түсініктер
беру. Оның құрылысы, қасиеттері мен қолданылуын
қарастырады. Сабақта
қолданылатын модульдер Оқыту мен
оқудағы жаңа тәсілдер: топтық
жұмыс, диалогтық оқыту, сергіту
сәті; СТО: Блум таксономиясы бойынша
жұмыстандыру Оқыту
мен оқуда АКТ қолдану компьютер,
ғаламтор Оқушылардың жас ерекшеліктеріне сәйкес оқыту және оқу:
деңгейлі тапсырмалар Оқыту
үшін бағалау және оқуды бағалау: ынталандыру, кері
байланыс; Талантты
және дарынды балаларды оқыту: кеңейтілген
тапсырмалар Оқытуды басқару және
көшбасшылық: мұғалім мен оқушы бірге
көшбасшы Сабақтың
көрнекілігі Интерактивті тақта,
маркер, қарындаш, плакаттар, слайдтар. 11-сынып электрондық
оқулық. АКТ-ны пайдаланып, жас ерекшеліктеріне сай
сұрақтар мен тапсырмалар, ББү
кестесі Ұйымдастыру
кезеңі Оқушылармен сәлемдесу,
түгелдеу. Оқушыларды топқа бөлу
элементер таңбасы арқылы. Оқушыларға бағалау
парақшалары таратылады. Қызығушылықты
ояту (20
минут)
І-тапсырма.т Сұрақ
–жауап.
1.Көпатомды спирттерге кандай заттар
жатады?
2. Глицериннін суда шексіз еру себебін калай
түсіндіруге болады?
3. Глицериннің өзінен кейінгі гомологының
формуласын жазып, халықаралық атау жүйесі бойынша
атаңдар.
4. 1,2,3-трибромпропаннан глицерин алу теңдеуін
жазыңдар.
5. а) Атаулары бойынша мына заттардын
формулаларын жазыңдар: пропанол-1, пропандиол-1,2,
пропантриол-1,2,3;
ә) осы заттарды өзара гомолог
немесе изомер деуге бола ма? Дәлелді жауап
беріңдер. 6. Мына этилен қатарының
көмірсутектерін гидратациялап, спирт алу қажет: а)
2-метил-2-пентенді; б) 4-метил-2-пентенді. Алынған спирттердің
аттарын атау керек. 7. Галогеналкилдерге а)
3-метил-1-хлорбутанға; б) 2,2-диметил-1-бромгексанға; в)
3,3-диметил-3-иодгептанға; д) иод-изопропанға сілтінің судағы
ерітіндісін қосып, алынған спирттерді атау
керек. 8. Мына гликолдерді а)
1,3-пропандиолді б) 2-метил-1,4-бутандиолды сәйкесінше
галогентуындыларды гидролиздеп алу керек, реакция теңдеулерін жазу
қажет. 9. Мына көмірсутектерден а)
СН2
= СН -
СН2
-
СН3; б)
СН3
– СН = СН -
СН3; в)
СН3
-
СН(СН3) – СН =
СН2
гликолдерді алу реакция
теңдеулерін жазу керек. ІІ-тапсырма. Өзіндік
жұмысы. І-деңгей
1. Көпатомды спирттердің
біратомды спирттерден қандай өзгешеліктері
бар? 2.Екіатомды және үшатомды
спирттердің алгашқы өкілдерінің (этиленгликоль мен глицериннің)
қүрылым формулаларын жазып, оларды халықаралық атау жүйесі бойынша
атаңдар. ІІІ-тапсырма. Есеп
шығару.
1. 0,7 моль глицерин мен
натрий әрекеттескенде түзілетін сутектің (қ.ж.)
көлемі Шешуі: 2С3Н8О3 +
6Na
→ 2C3H5(ОNa)3 +3Н2 ν
(С3Н8О3)=
2 моль 3V(Н2) =
67,2 л/моль х л
Н2---- 0,7 моль С3Н8О3 67,2 л Н2 ---- 2 моль С3Н8О3
2.
0,5 моль натриймен әрекеттесетін
этиленгликольдің массасы Шешуі: С2Н4(ОН)2 +
2Nа → (СН2ОNа)2 +
Н2 М(С2Н4(ОН)2) =
62 г/моль ν(Na) = 2 моль х г
С2Н4(ОН)2 ------ 0,5 моль Na 62
г С2Н4(ОН)2 ------2 моль Na
3.
Массасы 217 грамм этиленгликольдің зат мөлшері
(моль) Шешуі: v
(С2Н4(ОН)2) =
1 моль
М(С2Н4(ОН)2) =
64 г/моль х
моль С4Н8 ----217 г С2Н4(ОН)2 1
моль С4Н8 ---- 62 г С2Н4(ОН)2
ІV-тапсырма. Тест жұмысы.
(4-сұрақтан)
І-нұсқа.
1. Көп атомды
спирт:
А) фенол;В) толуол;С)
стирол;Д) этиленгликоль.
2.
Мына заттардың әрекеттесуі нәтижесінде көп атомды спирт алуға
болады:
А) хлорэтан
және
спиртті сілті ерітіндісі; В) хлорэтан және
сулы сілті ерітіндісі;
С) дихлорэтан және сулы
сілті ерітіндісі;Д) дихлорэтан және спиртті
сілті ерітіндісі.
3. Спирттердің ішінде тек көп
атомды спирт әрекеттесетін зат:
А) О2;В)
Nа;С) НВr;Д) Си(ОН)2;
4.
Динамит ойлап тапкан және оны әр
турлі елге патент ретінде ұсынған ғалым:
А) А.Бутлеров;В) А.Нобель;С)
Ш.Вюрц;Д) С.Лебедев.
ІІ-нұсқа.
1.
Этиленгликоль алуда қолданылатын реакция:
А)
этиленнің сілтімен
әрекеттесуі;В) ацетиленнің сумен
әрекеттесуі;
С) хлорэтанның сілтімен
әрекеттесуі;
Д) этиленнің перманганат
ерітіндісімен әрекеттесуі.
2.
Көп атомды спирттерге сапалық реакция:
А) NаОН;В)ҒеСІ3;
С) СиО; Д)Си(ОН)2.
3. Этиленгликольдің қолданылуы:
А) оның сулы ерітінділерінің кату
температурасының төмендігімен байланысты;
В) оның ерітіндісінің адам
организміне әсеріне байланысты;
С) оның
жағымды иісіне байланысты;
Д) оның ерітінділерінің
тұткырлығына
байланысты.
4. Лавсан талшығын алуда
қолданылатын спирт:
А) этанол;В) глицерин;С) этиленгликоль;Д)
метанол. V-тапсырма. Кесте
толтыру. Көпатомды спирттердің химиялық
қасиеттерін біратомды спирттермен салыстырып, берілген кестені
толтырыңдар:
Заттар
Реакция
теңдеулері
Этиленгликольмен
Этанолмен
Nа
NаОН
Сu(ОН)2
НВr
НNО3 2. Көпатомды спиртердің
негізгі қолдану салаларын көрсетіңдер:
Этиленгликоль
Глицерин VІ-тапсырма. Жауабы 1-кесте
бойынша. Көп атомды спирттер
деп: 1. көмірсутек радикалдармен
байланысқан бір гидроксил тобы бар күрделі
молекулалар; 2. молекуласында оттек болатын
органикалық заттар; 3. молекуласында әртүрлі
функционал топтар болатын қосылыстар; 4. молекуласында көмірсутек
радикалымен байланысқан бірнеше гидроксил тобы бар органикалық
заттар. Жаңа
сабақ (40
минут) Фенолдар
—
бензол сақинасындагы бір
немесе бірнеше сутек атомдарының орнын гидроксотоп басқан ароматты
көмірсутектердің туындылары. Ең қарапайым
өкілі—фенолС₆Н₅ОНнемесегидроксибензол. Ароматты көмірсутектердің
бүйір тізбектеріндегі сутек атомдарының
орнын гидроксотоп баскан
өнімдер ароматты
спирттер деп
аталады:
Алынуы. Фенолды көбіне тас көмір
шайырын өңдеу арқылы алады. Сондай-ак ароматты көмірсутектерінің
галогентуындыларын сілтімен әрекеттестіріп те
алады:
Өндірісте бастапқы шикізаттар
ретінде бензол мен пропиленді пайдаланып,
кумольді
әдіспен фенол алу іске
асырылған.
Физикалық
қасиеттері. Фенол — түссіз кристалдық зат.
43°С-та балқиды. Ауада ашық қалғанда тотығатындықтан, қызғылт түсті
болады. Бөлме температурасында аздап қана ериді, ал 60°С-тан жоғары
қыздырғанда, суда шексіз ериді. Фенол — улы зат, теріні күйдіреді.
Ерітіндісі антисептик ретінде қолданылады.
Химиялық
қасиеттері. Фенол молекуласындағы атомдар
бір-біріне өзара әсер ететіндіктен, полярлы қосылыс
болады:
Молекуладағы гидроксотоптың
оттек атомының бөліспеген электрон жүптары ығысуы әсерінен
сақинадағы π-электрондар жүйесінің біркелкілігі бұзылып, сақинаның
үш жерінде (2,4,6) электрон тығыздығы артады. Сондықтан өз
кезегіңде гидроксотоптағы сутек атомы қозғалғыш болады. Бұл жағдай
фенолдың судағы ерітіңдісінде қышқыл сияқты диссоциациялануына
себеп болады. Сол себепті, фенолдың 1 %-тік
ерітіндісін карбол
қышқылы | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||





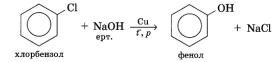




 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
