
Идеал газ күйінің теңдеуі.Изопроцестер.
Газдың қандай күйде тұратынын
білу үшіноның термодинамикалық параметрлерін, яғни қысымды,
температураны, көлемді білу қажет. Термопараметрлердің біреуінің
өзгерісі, оның басқа параметрлерінің өзгеруіне әкеп соғады.
Термодинамикалық параметрлерді байланыстыратын теңдеу идеал газ
күйінің теңдеуі деп аталады. ![]()

Бұл теңдеу Менделеев–Клапейрон теңдеуі деп те аталынады.
Газдың бір параметрінің мәні тағайындалып, қалған екеуінің арасындағы сандық тәуелділікті айқындайтын заңдарды газ заңдары деп атайды.
Параметрлердің біреуінің мәні өзгермей қалған кезде өтетін процестер изопроцестер деп аталады. Изопроцестер табиғатта кең таралған және техникада жиі пайдаланылады.




1. Изотермиялық процесс. Ағылшын физигі Р.Бойль 1667 ж. және оған тәуелсіз француз физигі Э.Мариотт тәжірибе жүзінде тұрақты температура кезінде газдың берілген массасы үшін оның қысымының газ алып тұрған көлемге көбейтіндісі тұрақты шамаға тең болатынын тағайындады, яғни pV=const немесе p1V1= p2V2. Бұл заң Бойль–Мариотт заңы деп аталады.

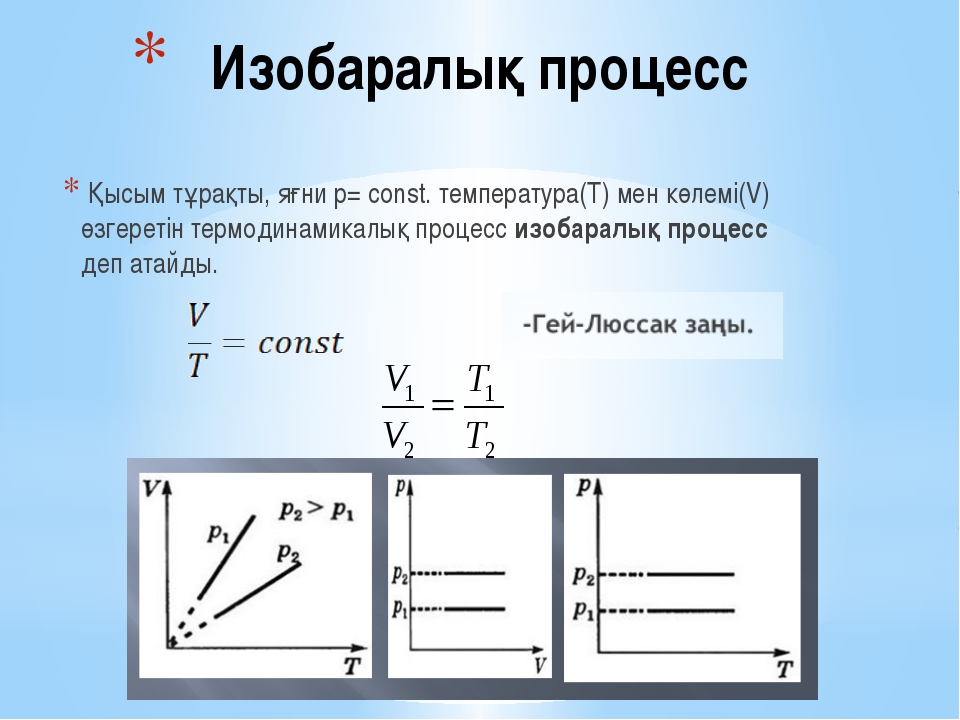
2. Изобаралық процесс. Француз физигі Гей–Люссак 1802 ж. тәжірибе жүзінде тұрақты қысымда газдың берілген массасы көлемінің температураға сызықты тәуелді болатынын тағайындады. Бұл заң Гей–Люссак заңы деп аталады.
3. Изохоралық процесс. Бұл процесті француз физигі Ж.Шарль зерттеген. 1787 ж. ол тәжірибе жүзінде тұрақты көлемде берілген газ массасының оның температурасына тура пропорционал болатынын тағайындады, яғни Бұл Шарль заңы.

Дальтон заңы
Қоспа газдардың қысымы Дальтон заңының көмегімен анықталады:

![]()
![]()
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Физика пәні идеал газ
Идеал газ күйінің теңдеуі.Изопроцестер.
Газдың қандай күйде тұратынын
білу үшіноның термодинамикалық параметрлерін, яғни қысымды,
температураны, көлемді білу қажет. Термопараметрлердің біреуінің
өзгерісі, оның басқа параметрлерінің өзгеруіне әкеп соғады.
Термодинамикалық параметрлерді байланыстыратын теңдеу идеал газ
күйінің теңдеуі деп аталады. ![]()

Бұл теңдеу Менделеев–Клапейрон теңдеуі деп те аталынады.
Газдың бір параметрінің мәні тағайындалып, қалған екеуінің арасындағы сандық тәуелділікті айқындайтын заңдарды газ заңдары деп атайды.
Параметрлердің біреуінің мәні өзгермей қалған кезде өтетін процестер изопроцестер деп аталады. Изопроцестер табиғатта кең таралған және техникада жиі пайдаланылады.




1. Изотермиялық процесс. Ағылшын физигі Р.Бойль 1667 ж. және оған тәуелсіз француз физигі Э.Мариотт тәжірибе жүзінде тұрақты температура кезінде газдың берілген массасы үшін оның қысымының газ алып тұрған көлемге көбейтіндісі тұрақты шамаға тең болатынын тағайындады, яғни pV=const немесе p1V1= p2V2. Бұл заң Бойль–Мариотт заңы деп аталады.

2. Изобаралық процесс. Француз физигі Гей–Люссак 1802 ж. тәжірибе жүзінде тұрақты қысымда газдың берілген массасы көлемінің температураға сызықты тәуелді болатынын тағайындады. Бұл заң Гей–Люссак заңы деп аталады.

3. Изохоралық процесс. Бұл процесті француз физигі Ж.Шарль зерттеген. 1787 ж. ол тәжірибе жүзінде тұрақты көлемде берілген газ массасының оның температурасына тура пропорционал болатынын тағайындады, яғни Бұл Шарль заңы.

Дальтон заңы
Қоспа газдардың қысымы Дальтон заңының көмегімен анықталады:

![]()
![]()

шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
