
Бекітемін
Мектеп директоры
__________Ш.Абиткожаева
|
Бөлім: |
9.3А 17 (VII), 16 (VI), 15 (VI), 14 (IV) -топ элементтері және олардың қосылыстары |
|
Педагогтің аты-жөні: |
Хасенова.А |
|
Күні:19.02.26 |
|
|
Сыныбы:9а |
Қатысушылар саны: Қатыспағандар саны: |
|
Сабақтың тақырыбы: |
Фосфор және оның қосылыстары |
|
Оқу бағдарламасына сәйкес оқу мақсаты |
9.2.1.22-фосфордың аллотропиялық түрөзгерістерін салыстыру 9.4.2.2 -фосфор қосылыстарының Қазақстандағы кен орындарын атау 9.2.1.23-фосфор және оның қосылыстарының жалпы химиялық қасиеттерін түсіндіру |
|
Сабақтың мақсаты: |
Фосфордың аллотропиялық түрөзгерістерін салыстырады Фосфор қосылыстарының Қазақстандағы кен орындарын анықтайды Фосфор және оның қосылыстарының жалпы химиялық қасиеттерін сипаттайды. |
|
Құндылықтар |
ЖАСАМПАЗДЫҚ ЖӘНЕ ЖАҢАШЫЛДЫҚ АЙЫ |
|
Аптаның дәйек сөзі: |
«Шығармашыл бала – ойлы бала» |
Сабақтың барысы:
|
Сабақ кезеңі/Уақыты |
Педагогтің іс-әрекеті |
Оқушының іс-әрекеті |
Бағалау |
Ресурстар |
|
Сабақтың басы Ұйымдастыру кезеңі Басы 5 мин
|
(Ұ). Ұйымдастыру кезеңі: 1. Оқушылармен амандасу, түгендеу. 2. Ынтымақтастық атмосферасын қалыптастырады 3. Оқушыларды топтарға біріктіру. |
Оқушылар шеңберге тұрып «Досқа тілек» тәсілі арқылы сыныпта жағымды ахуал орнатады .
«Миға шабуыл» Өткенді қайталау арқылы бастапқы білімді жаңғырту. ? 1. Азот қышқылының қандай ерекше қасиеттері бар? 2.Азот қышқылы металдармен әрекеттескенде қандай газ түзелмейді? 3.Азоттың формуласы Азот қышқылының қандай ерекше қасиеттері бар? 4.Азот қай топша да орналасқан,салыстырмалық массасы қанша 5.Азот қышқылының қандай ерекше қасиеттері бар? |
Кері байланыс: Мадақтау арқылы бағаланады. аланады |
Оқулық, жұмыс дәптері Кітап, дәптер, қалам
Қолданылған ЖИ: Chat gpt,Kling ai Презентация ЖИ арқылы құндылыққа дәріптейтін бейне жазба көрсетіледі
|
|
Жаңа сабаққа кіріспе 8 мин
8 мин |
Жаңа сабақ. Тақырып бойынша қысқаша ақпарат береді. Фосфор — химиялық элемент, таңбасы P, атомдық нөмірі 15. Ол периодтық жүйенің V тобына (15-топ) жататын бейметалл элемент..Физикалық және химиялық қасиеттері,формулалары туралы мәлімет айту |
Жаңа тақырыппен танысу үшін оқулық пен видео ақпараттар қолданылады.
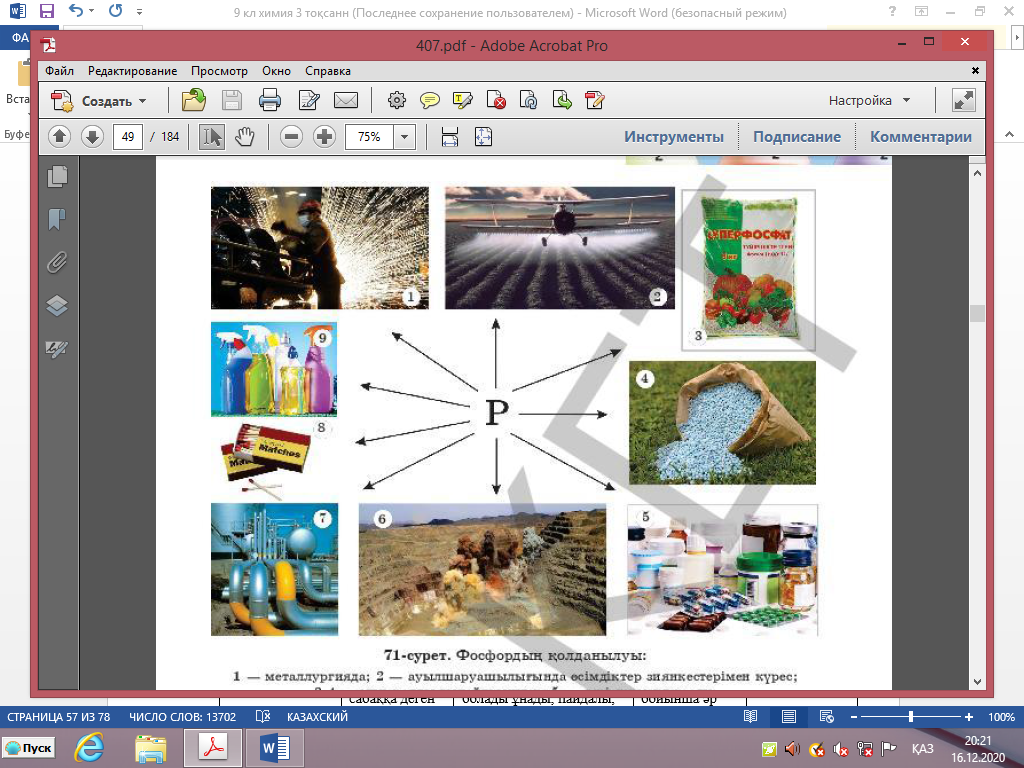
1-тапсырма Кім жылдам топтық тапсырма Фосфордың қолданылуын
анықтайды. |
.
Дескриптор: Жалпы – 2 балл 1.қолданылуын дұрыс анықтайды-1б Жарылғыш заттар барын табады-1б |
Өз ойын дұрыс мағынада білдіріп, талқылауға белсенділікпен қатысқан оқушыға «Жарайсың!» деген мадақтау сөзімен ынталандыру. |
|
Сабақтың ортасы Мағынаны ашу. 5 мин.
|
Оқулықтағы жаңа сабақтың мәтінін оқуға тапсырма береді |
Жеке тапсырма: Фосфор және оның қосылыстарын сәйкестендіру |
1 Фосфор қосылыстарын анықтайды-1балл Қазақстандағы кен орындарын анықтайды-1 балл Формулалларын дұрыс табады-1б Дескриптор: Жалпы - 3 балл |
|
|
6 мин |
Оқулықта берілген тапсырманы орындатады, бақылайды, мысал, үлгі көрсетеді. |
3.Тапсырма Фосфордың аллотропиялық түр өзгерістерін ажырату |
Мадақтау арқылы бағаланады. аланады 1.Суретті талдау |
9-сынып оқулығы. Жұмыс дәптерлері. |
|
5 мин |
Оқулықта берілген тапсырманы орындатады, бақылайды, мысал, үлгі көрсетеді. |
Жеке жұмыс: 4-тапсырма кім жылдам жеке тапсырма тест сұрақтары |
Дескриптор: Жалпы – 3 балл 1. Суретті талдау Дескриптор: Жалпы – 5 балл |
9-сынып оқулығы. Жұмыс дәптерлері. |
|
Сабақтың соңы Ой толғаныс. Рефлексия 5 мин.
|
«Бір ауыз сөз» әдісі. Мұғалім сабақты қорытындылау мақсатында оқушылардың сабаққа деген көзқарасын, рефлексиясын тыңдайды. |
Жеке жұмыс: Оқушылар бір ауыз сөзбен сабақ туралы өз ойларын түсіндіріп береді. Бір ауыз сөздеріне сабақты бағалайтын келесі сөздерді айтуға болады ұнады, пайдалы, қажет, білдім, үйрендім, қызықтым, ұмтылдым, есте сақтадым, жасай аламын. т.б. |
Мұғалім оқушылардың сабаққа қатысқан белсенілігіне қарай 1-10 баллдық жүйе бойынша әр оқушының өзіне тиісті баллын қойып бағалайды. сонымен қатар, оқушыларды ынталандыру үшін «Қошеметтеу» әдісі арқылы бағалайды. |
9-сынып оқулығы. Жұмыс дәптерлері. |
|
Рефлексия 3 мин «3/2/1 әдісі»: 1. Мен білетін үш нәрсе ... 2. Мені таңқалдырған екі нәрсе ... 3. Болашақта тереңірек қарастыратын бір нәрсе....
|
«3/2/1 әдісі»: 1. Мен білетін үш нәрсе ... 2. Мені таңқалдырған екі нәрсе ... 3. Болашақта тереңірек қарастыратын бір нәрсе |
|
Рефлексия |
|
|
Үй тапсырмасы §36. оқып келу 3 мин |
|
|
|
|
Фосфор – периодтық жүйенің V тобының
негізгі топшасына жататын бейметалл элемент.
Атом нөмірі – 15.
Табиғатта бос күйінде кездеспейді, көбінесе қосылыс түрінде болады (фосфаттар).
![]()
? Фосфордың аллотропиялық түрлері
-
Ақ фосфор
-
Өте улы
-
Қараңғыда жарық шығарады
-
Ауада өздігінен тұтанады
-
Суда сақталады
-
-
Қызыл фосфор
-
Усыздау
-
Тұрақты
-
Сіріңке өндірісінде қолданылады
-
-
Қара фосфор
-
Ең тұрақты түрі
-
Металдық қасиетке жақын
-
![]()
⚗️ Фосфордың химиялық қасиеттері
Фосфор белсенді элемент.
1️⃣ Оттекпен әрекеттесуі:
4P+5O2→2P2O54P + 5O_2 → 2P_2O_54P+5O2→2P2O5
2️⃣ Металдармен әрекеттесуі:
Фосфидтер түзеді.
Мысалы:
3Ca+2P→Ca3P23Ca + 2P → Ca_3P_23Ca+2P→Ca3P2
3️⃣ Галогендермен әрекеттесуі:
2P+3Cl2→2PCl32P + 3Cl_2 → 2PCl_32P+3Cl2→2PCl3
![]()
? Фосфордың маңызды қосылыстары
1️⃣ Фосфор оксидтері
-
P₂O₅ (фосфор (V) оксиді) – қышқылдық оксид
-
Сумен әрекеттесіп фосфор қышқылын түзеді:
P2O5+3H2O→2H3PO4P_2O_5 + 3H_2O → 2H_3PO_4P2O5+3H2O→2H3PO4
![]()
2️⃣ Фосфор қышқылы (Phosphoric acid)
-
Формуласы: H₃PO₄
-
Орташа күшті қышқыл
-
Тыңайтқыш өндірісінде қолданылады
-
Тамақ өнеркәсібінде (E338)
![]()
3️⃣ Фосфаттар
-
Кальций фосфаты – сүйек пен тістің негізгі құрамы
-
Минералдары:
-
Апатит
-
Фосфорит
-
![]()
4️⃣ Фосфин (Phosphine)
-
Формуласы: PH₃
-
Өте улы газ
-
Шіріген балық иісі бар
-
Ауада өздігінен жануы мүмкін
![]()
? Фосфордың маңызы
-
? Ауыл шаруашылығында – минералды тыңайтқыштар
-
? Тірі ағзаларда – ДНҚ, РНҚ құрамында
-
? Сүйек және тіс құрамында
-
? Сіріңке өндірісінде
![]()
Егер қаласаңыз, мен осы тақырып бойынша:
-
Қысқаша конспект
-
Реферат
-
Презентация жоспары
-
Тест сұрақтары
дайындап бере аламын ?
фосфордың аллотропиялық түрөзгерістерін салыстыру
? Фосфордың аллотропиялық түрөзгерістерін салыстыру
Фосфордың негізгі үш аллотропиялық түрі бар: ақ, қызыл, қара фосфор. Олар құрылысы мен қасиеттері бойынша бір-бірінен ерекшеленеді.
![]()
? Салыстырмалы кесте
|
Қасиеттері |
Ақ фосфор |
Қызыл фосфор |
Қара фосфор |
|
Түсі |
Ақ немесе сарғыш |
Қою қызыл |
Қара |
|
Құрылысы |
Молекулалық (P₄) |
Полимерлі |
Қабатты кристалдық |
|
Тұрақтылығы |
Тұрақсыз |
Орташа тұрақты |
Ең тұрақты |
|
Улылығы |
Өте улы |
Усыздау |
Усыз |
|
Ауада жануы |
Өздігінен тұтанады |
Жоғары температурада жанады |
Қиын жанады |
|
Суда ерігіштігі |
Ерімейді (суда сақталады) |
Ерімейді |
Ерімейді |
|
Қолданылуы |
Әскери мақсатта, химияда |
Сіріңке өндірісі |
Жартылай өткізгіш материал |
? Жеке сипаттамасы
1️⃣ Ақ фосфор
-
P₄ молекулаларынан тұрады (тетраэдрлік құрылым)
-
Қараңғыда әлсіз жарық шығарады (хемилюминесценция)
-
Ауада оңай тотығады
-
Суда сақталады
![]()
2️⃣ Қызыл фосфор
-
Ақ фосфорды қыздыру арқылы алынады
-
Қауіпсіздеу және тұрақтырақ
-
Сіріңкенің қорабының жанатын бетінде қолданылады
![]()
3️⃣ Қара фосфор
-
Жоғары қысымда алынады
-
Құрылысы графитке ұқсас
-
Электр тогын өткізеді
-
Ең тұрақты түрі
![]()
? Қорытынды
-
Химиялық белсенділігі бойынша: Ақ > Қызыл > Қара
-
Тұрақтылығы бойынша: Қара > Қызыл > Ақ
-
Қауіптілігі бойынша: Ақ фосфор ең қауіпті
Қаласаңыз, мен осыны сызба түрінде немесе қысқаша шпаргалка форматында дайындап бере аламын.
-фосфор қосылыстарының Қазақстандағы кен орындарын атау
?? Фосфор қосылыстарының Қазақстандағы кен орындары
Қазақстан фосфорит қоры бойынша әлемдегі алдыңғы елдердің бірі. Негізгі кен орындары:
![]()
1️⃣ Қаратау фосфорит алабы
-
? Жамбыл облысында орналасқан
-
Қазақстандағы ең ірі фосфорит бассейні
-
Әлемдік маңызы бар
-
Негізгі кен орындары: Жаңатас, Қаратау
-
Тыңайтқыш өндірісінің негізгі шикізат көзі
![]()
2️⃣ Шилісай фосфорит кен орны
-
? Ақтөбе облысында
-
Батыс Қазақстандағы ірі кен орындарының бірі
-
Фосфор тыңайтқыштарын өндіруге пайдаланылады
![]()
3️⃣ Ақтөбе фосфорит алабы
-
? Ақтөбе өңірінде
-
Фосфориттің шөгінді түрлері кездеседі
![]()
4️⃣ Лисаков фосфорит кен орны
-
? Қостанай облысында
-
Солтүстік Қазақстандағы фосфат шикізат көзі
![]()
? Өндіріс орталығы
Фосфор шикізатын өңдеу орталығы:
-
Тараз
(Минералды тыңайтқыштар өндірісі дамыған)
![]()
? Қорытынды
Қазақстандағы негізгі фосфорит кен орындары:
-
Қаратау
-
Шилісай
-
Ақтөбе
-
Лисаков
Ең ірі және стратегиялық маңыздысы — Қаратау фосфорит алабы.
Қаласаңыз, карта бойынша орналасуын да түсіндіріп бере аламын.
фосфор және оның қосылыстарының жалпы химиялық қасиеттерін түсіндіру
? Фосфор және оның қосылыстарының жалпы химиялық қасиеттері
Фосфор (P) – белсенді бейметалл, тотығу дәрежелері: –3, +3, +5. Осыған байланысты оның қосылыстары да әртүрлі химиялық қасиет көрсетеді.
![]()
? I. Фосфордың химиялық қасиеттері
1️⃣ Оттекпен әрекеттесуі (тотығу)
Фосфор оңай тотығады:
-
Оттек жеткілікті болса:
4P+5O2→2P2O54P + 5O_2 → 2P_2O_54P+5O2→2P2O5
-
Оттек жеткіліксіз болса:
4P+3O2→2P2O34P + 3O_2 → 2P_2O_34P+3O2→2P2O3
? Қышқылдық оксидтер түзеді.
![]()
2️⃣ Металдармен әрекеттесуі
Фосфор металдармен әрекеттесіп фосфидтер түзеді:
3Ca+2P→Ca3P23Ca + 2P → Ca_3P_23Ca+2P→Ca3P2
Фосфидтер суда ыдырап, фосфин түзеді.
![]()
3️⃣ Сутекпен әрекеттесуі
Жанама жолмен Phosphine (PH₃) түзіледі.
-
Өте улы
-
Тотықсыздандырғыш қасиет көрсетеді
![]()
4️⃣ Галогендермен әрекеттесуі
Фосфор галогендермен оңай қосылады:
2P+3Cl2→2PCl32P + 3Cl_2 → 2PCl_32P+3Cl2→2PCl3 2P+5Cl2→2PCl52P + 5Cl_2 → 2PCl_52P+5Cl2→2PCl5
![]()
⚗️ II. Фосфор қосылыстарының химиялық қасиеттері
1️⃣ Оксидтері
Фосфор (V) оксиді – P₂O₅
-
Қышқылдық оксид
-
Сумен әрекеттесіп қышқыл түзеді:
P2O5+3H2O→2H3PO4P_2O_5 + 3H_2O → 2H_3PO_4P2O5+3H2O→2H3PO4
![]()
2️⃣ Қышқылдары
? Phosphoric acid (H₃PO₄)
-
Орташа күшті, үш негізді қышқыл
-
Негіздермен әрекеттесіп тұздар (фосфаттар) түзеді:
H3PO4+3NaOH→Na3PO4+3H2OH_3PO_4 + 3NaOH → Na_3PO_4 + 3H_2OH3PO4+3NaOH→Na3PO4+3H2O
-
Металдармен әрекеттесіп сутек бөледі
![]()
3️⃣ Фосфаттар
-
Қышқылдық, орта және негізгі тұздар түзеді
-
Көпшілігі суда нашар ериді
-
Қыздырғанда ыдырауы мүмкін
![]()
4️⃣ Фосфин (PH₃)
-
Әлсіз негіздік қасиет
-
Күшті тотықсыздандырғыш
-
Ауада тотығып, фосфор қышқылына айналуы мүмкін
![]()
? Тотығу-тотықсыздану қасиеті
Фосфор:
-
? Тотықсыздандырғыш бола алады (O₂, галогендермен)
-
? Тотықтырғыш бола алады (металдарға қатысты)
![]()
? Жалпы қорытынды
Фосфор және оның қосылыстары:
-
Қышқылдық қасиет көрсетеді
-
Тотығу-тотықсыздану реакцияларына оңай түседі
-
Тұздар, оксидтер, гидридтер түзеді
-
Химиялық белсенділігі жоғары
Қаласаңыз, осы тақырыпты қысқаша конспект немесе схема түрінде дайындап бере аламын.
осы тақырыпқа тапсырма жауаппен
? «Фосфор және оның қосылыстары» тақырыбына тапсырмалар (жауаптарымен)
![]()
1-тапсырма. Фосфордың мүмкін болатын тотығу дәрежелерін атаңыз.
Жауабы: –3, +3, +5
![]()
2-тапсырма. Реакция теңдеуін аяқтаңыз:
а) P+O2→?P + O_2 → ?P+O2→?
б) P2O5+H2O→?P_2O_5 + H_2O → ?P2O5+H2O→?
в) Ca+P→?Ca + P → ?Ca+P→?
Жауабы:
а)
4P+5O2→2P2O54P + 5O_2 → 2P_2O_54P+5O2→2P2O5
б)
P2O5+3H2O→2H3PO4P_2O_5 + 3H_2O → 2H_3PO_4P2O5+3H2O→2H3PO4
в)
3Ca+2P→Ca3P23Ca + 2P → Ca_3P_23Ca+2P→Ca3P2
![]()
3-тапсырма. Қай қосылыс қышқылдық оксид болып табылады?
A) PH₃
B) P₂O₅
C) Ca₃P₂
D) Na₃P
Жауабы: B) P₂O₅
![]()
4-тапсырма. Сәйкестендіру
|
Зат |
Қасиеті |
|
1. PH₃ |
а) Үш негізді қышқыл |
|
2. H₃PO₄ |
б) Улы газ |
|
3. P₂O₅ |
в) Қышқылдық оксид |
Жауабы:
1 – б
2 – а
3 – в
![]()
5-тапсырма. Фосфор қышқылы қандай тұздар түзеді?
Жауабы:
-
Орта тұздар (Na₃PO₄)
-
Қышқыл тұздар (NaH₂PO₄, Na₂HPO₄)
![]()
6-тапсырма. Есеп
32 г фосфор толық жанғанда қанша грамм P₂O₅ түзіледі?
3/2/1 әдісі»:
1. Мен білетін үш нәрсе ...
2. Мені таңқалдырған екі нәрсе ...
3. Болашақта тереңірек қарастыратын бір нәрсе....
3/2/1 әдісі»:
1. Мен білетін үш нәрсе ...
2. Мені таңқалдырған екі нәрсе ...
3. Болашақта тереңірек қарастыратын бір нәрсе....
3/2/1 әдісі»:
1. Мен білетін үш нәрсе ...
2. Мені таңқалдырған екі нәрсе ...
3. Болашақта тереңірек қарастыратын бір нәрсе....
3/2/1 әдісі»:
1. Мен білетін үш нәрсе ...
2. Мені таңқалдырған екі нәрсе ...
3. Болашақта тереңірек қарастыратын бір нәрсе....
3/2/1 әдісі»:
1. Мен білетін үш нәрсе ...
2. Мені таңқалдырған екі нәрсе ...
3. Болашақта тереңірек қарастыратын бір нәрсе....
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Фосфор және оның қосылыстары
Бекітемін
Мектеп директоры
__________Ш.Абиткожаева
|
Бөлім: |
9.3А 17 (VII), 16 (VI), 15 (VI), 14 (IV) -топ элементтері және олардың қосылыстары |
|
Педагогтің аты-жөні: |
Хасенова.А |
|
Күні:19.02.26 |
|
|
Сыныбы:9а |
Қатысушылар саны: Қатыспағандар саны: |
|
Сабақтың тақырыбы: |
Фосфор және оның қосылыстары |
|
Оқу бағдарламасына сәйкес оқу мақсаты |
9.2.1.22-фосфордың аллотропиялық түрөзгерістерін салыстыру 9.4.2.2 -фосфор қосылыстарының Қазақстандағы кен орындарын атау 9.2.1.23-фосфор және оның қосылыстарының жалпы химиялық қасиеттерін түсіндіру |
|
Сабақтың мақсаты: |
Фосфордың аллотропиялық түрөзгерістерін салыстырады Фосфор қосылыстарының Қазақстандағы кен орындарын анықтайды Фосфор және оның қосылыстарының жалпы химиялық қасиеттерін сипаттайды. |
|
Құндылықтар |
ЖАСАМПАЗДЫҚ ЖӘНЕ ЖАҢАШЫЛДЫҚ АЙЫ |
|
Аптаның дәйек сөзі: |
«Шығармашыл бала – ойлы бала» |
Сабақтың барысы:
|
Сабақ кезеңі/Уақыты |
Педагогтің іс-әрекеті |
Оқушының іс-әрекеті |
Бағалау |
Ресурстар |
|
Сабақтың басы Ұйымдастыру кезеңі Басы 5 мин
|
(Ұ). Ұйымдастыру кезеңі: 1. Оқушылармен амандасу, түгендеу. 2. Ынтымақтастық атмосферасын қалыптастырады 3. Оқушыларды топтарға біріктіру. |
Оқушылар шеңберге тұрып «Досқа тілек» тәсілі арқылы сыныпта жағымды ахуал орнатады .
«Миға шабуыл» Өткенді қайталау арқылы бастапқы білімді жаңғырту. ? 1. Азот қышқылының қандай ерекше қасиеттері бар? 2.Азот қышқылы металдармен әрекеттескенде қандай газ түзелмейді? 3.Азоттың формуласы Азот қышқылының қандай ерекше қасиеттері бар? 4.Азот қай топша да орналасқан,салыстырмалық массасы қанша 5.Азот қышқылының қандай ерекше қасиеттері бар? |
Кері байланыс: Мадақтау арқылы бағаланады. аланады |
Оқулық, жұмыс дәптері Кітап, дәптер, қалам
Қолданылған ЖИ: Chat gpt,Kling ai Презентация ЖИ арқылы құндылыққа дәріптейтін бейне жазба көрсетіледі
|
|
Жаңа сабаққа кіріспе 8 мин
8 мин |
Жаңа сабақ. Тақырып бойынша қысқаша ақпарат береді. Фосфор — химиялық элемент, таңбасы P, атомдық нөмірі 15. Ол периодтық жүйенің V тобына (15-топ) жататын бейметалл элемент..Физикалық және химиялық қасиеттері,формулалары туралы мәлімет айту |
Жаңа тақырыппен танысу үшін оқулық пен видео ақпараттар қолданылады.
1-тапсырма Кім жылдам топтық тапсырма Фосфордың қолданылуын
анықтайды. |
.
Дескриптор: Жалпы – 2 балл 1.қолданылуын дұрыс анықтайды-1б Жарылғыш заттар барын табады-1б |
Өз ойын дұрыс мағынада білдіріп, талқылауға белсенділікпен қатысқан оқушыға «Жарайсың!» деген мадақтау сөзімен ынталандыру. |
|
Сабақтың ортасы Мағынаны ашу. 5 мин.
|
Оқулықтағы жаңа сабақтың мәтінін оқуға тапсырма береді |
Жеке тапсырма: Фосфор және оның қосылыстарын сәйкестендіру |
1 Фосфор қосылыстарын анықтайды-1балл Қазақстандағы кен орындарын анықтайды-1 балл Формулалларын дұрыс табады-1б Дескриптор: Жалпы - 3 балл |
|
|
6 мин |
Оқулықта берілген тапсырманы орындатады, бақылайды, мысал, үлгі көрсетеді. |
3.Тапсырма Фосфордың аллотропиялық түр өзгерістерін ажырату |
Мадақтау арқылы бағаланады. аланады 1.Суретті талдау |
9-сынып оқулығы. Жұмыс дәптерлері. |
|
5 мин |
Оқулықта берілген тапсырманы орындатады, бақылайды, мысал, үлгі көрсетеді. |
Жеке жұмыс: 4-тапсырма кім жылдам жеке тапсырма тест сұрақтары |
Дескриптор: Жалпы – 3 балл 1. Суретті талдау Дескриптор: Жалпы – 5 балл |
9-сынып оқулығы. Жұмыс дәптерлері. |
|
Сабақтың соңы Ой толғаныс. Рефлексия 5 мин.
|
«Бір ауыз сөз» әдісі. Мұғалім сабақты қорытындылау мақсатында оқушылардың сабаққа деген көзқарасын, рефлексиясын тыңдайды. |
Жеке жұмыс: Оқушылар бір ауыз сөзбен сабақ туралы өз ойларын түсіндіріп береді. Бір ауыз сөздеріне сабақты бағалайтын келесі сөздерді айтуға болады ұнады, пайдалы, қажет, білдім, үйрендім, қызықтым, ұмтылдым, есте сақтадым, жасай аламын. т.б. |
Мұғалім оқушылардың сабаққа қатысқан белсенілігіне қарай 1-10 баллдық жүйе бойынша әр оқушының өзіне тиісті баллын қойып бағалайды. сонымен қатар, оқушыларды ынталандыру үшін «Қошеметтеу» әдісі арқылы бағалайды. |
9-сынып оқулығы. Жұмыс дәптерлері. |
|
Рефлексия 3 мин «3/2/1 әдісі»: 1. Мен білетін үш нәрсе ... 2. Мені таңқалдырған екі нәрсе ... 3. Болашақта тереңірек қарастыратын бір нәрсе....
|
«3/2/1 әдісі»: 1. Мен білетін үш нәрсе ... 2. Мені таңқалдырған екі нәрсе ... 3. Болашақта тереңірек қарастыратын бір нәрсе |
|
Рефлексия |
|
|
Үй тапсырмасы §36. оқып келу 3 мин |
|
|
|
|
Фосфор – периодтық жүйенің V тобының
негізгі топшасына жататын бейметалл элемент.
Атом нөмірі – 15.
Табиғатта бос күйінде кездеспейді, көбінесе қосылыс түрінде болады (фосфаттар).
![]()
? Фосфордың аллотропиялық түрлері
-
Ақ фосфор
-
Өте улы
-
Қараңғыда жарық шығарады
-
Ауада өздігінен тұтанады
-
Суда сақталады
-
-
Қызыл фосфор
-
Усыздау
-
Тұрақты
-
Сіріңке өндірісінде қолданылады
-
-
Қара фосфор
-
Ең тұрақты түрі
-
Металдық қасиетке жақын
-
![]()
⚗️ Фосфордың химиялық қасиеттері
Фосфор белсенді элемент.
1️⃣ Оттекпен әрекеттесуі:
4P+5O2→2P2O54P + 5O_2 → 2P_2O_54P+5O2→2P2O5
2️⃣ Металдармен әрекеттесуі:
Фосфидтер түзеді.
Мысалы:
3Ca+2P→Ca3P23Ca + 2P → Ca_3P_23Ca+2P→Ca3P2
3️⃣ Галогендермен әрекеттесуі:
2P+3Cl2→2PCl32P + 3Cl_2 → 2PCl_32P+3Cl2→2PCl3
![]()
? Фосфордың маңызды қосылыстары
1️⃣ Фосфор оксидтері
-
P₂O₅ (фосфор (V) оксиді) – қышқылдық оксид
-
Сумен әрекеттесіп фосфор қышқылын түзеді:
P2O5+3H2O→2H3PO4P_2O_5 + 3H_2O → 2H_3PO_4P2O5+3H2O→2H3PO4
![]()
2️⃣ Фосфор қышқылы (Phosphoric acid)
-
Формуласы: H₃PO₄
-
Орташа күшті қышқыл
-
Тыңайтқыш өндірісінде қолданылады
-
Тамақ өнеркәсібінде (E338)
![]()
3️⃣ Фосфаттар
-
Кальций фосфаты – сүйек пен тістің негізгі құрамы
-
Минералдары:
-
Апатит
-
Фосфорит
-
![]()
4️⃣ Фосфин (Phosphine)
-
Формуласы: PH₃
-
Өте улы газ
-
Шіріген балық иісі бар
-
Ауада өздігінен жануы мүмкін
![]()
? Фосфордың маңызы
-
? Ауыл шаруашылығында – минералды тыңайтқыштар
-
? Тірі ағзаларда – ДНҚ, РНҚ құрамында
-
? Сүйек және тіс құрамында
-
? Сіріңке өндірісінде
![]()
Егер қаласаңыз, мен осы тақырып бойынша:
-
Қысқаша конспект
-
Реферат
-
Презентация жоспары
-
Тест сұрақтары
дайындап бере аламын ?
фосфордың аллотропиялық түрөзгерістерін салыстыру
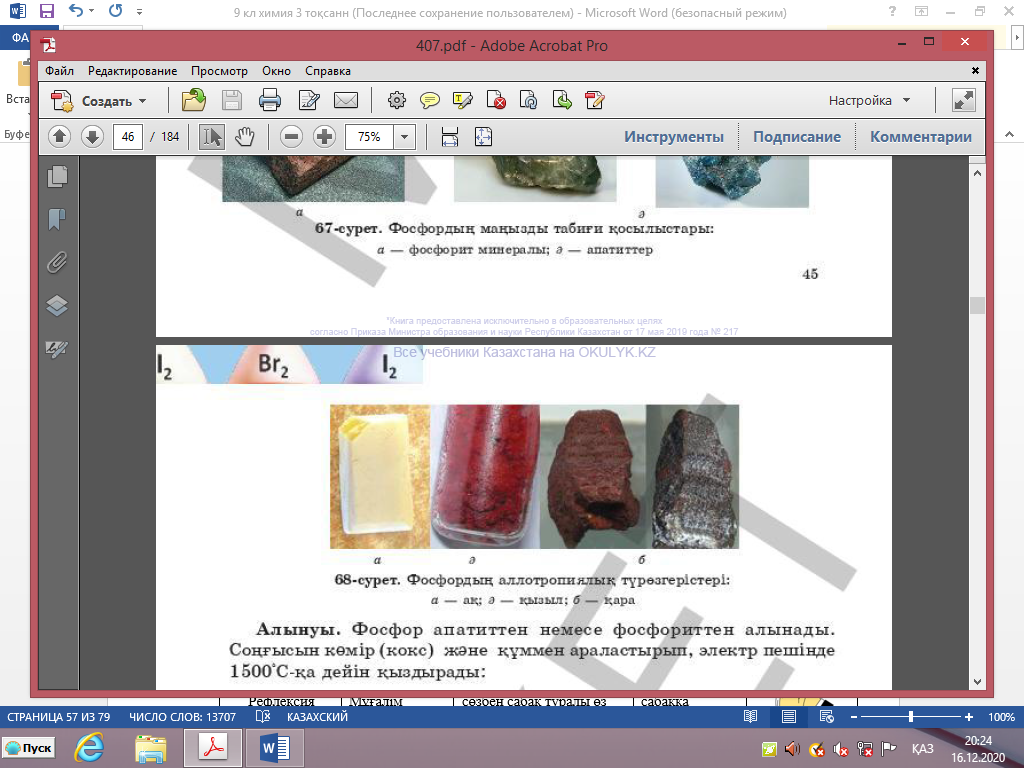
? Фосфордың аллотропиялық түрөзгерістерін салыстыру
Фосфордың негізгі үш аллотропиялық түрі бар: ақ, қызыл, қара фосфор. Олар құрылысы мен қасиеттері бойынша бір-бірінен ерекшеленеді.
![]()
? Салыстырмалы кесте
|
Қасиеттері |
Ақ фосфор |
Қызыл фосфор |
Қара фосфор |
|
Түсі |
Ақ немесе сарғыш |
Қою қызыл |
Қара |
|
Құрылысы |
Молекулалық (P₄) |
Полимерлі |
Қабатты кристалдық |
|
Тұрақтылығы |
Тұрақсыз |
Орташа тұрақты |
Ең тұрақты |
|
Улылығы |
Өте улы |
Усыздау |
Усыз |
|
Ауада жануы |
Өздігінен тұтанады |
Жоғары температурада жанады |
Қиын жанады |
|
Суда ерігіштігі |
Ерімейді (суда сақталады) |
Ерімейді |
Ерімейді |
|
Қолданылуы |
Әскери мақсатта, химияда |
Сіріңке өндірісі |
Жартылай өткізгіш материал |
? Жеке сипаттамасы
1️⃣ Ақ фосфор
-
P₄ молекулаларынан тұрады (тетраэдрлік құрылым)
-
Қараңғыда әлсіз жарық шығарады (хемилюминесценция)
-
Ауада оңай тотығады
-
Суда сақталады
![]()
2️⃣ Қызыл фосфор
-
Ақ фосфорды қыздыру арқылы алынады
-
Қауіпсіздеу және тұрақтырақ
-
Сіріңкенің қорабының жанатын бетінде қолданылады
![]()
3️⃣ Қара фосфор
-
Жоғары қысымда алынады
-
Құрылысы графитке ұқсас
-
Электр тогын өткізеді
-
Ең тұрақты түрі
![]()
? Қорытынды
-
Химиялық белсенділігі бойынша: Ақ > Қызыл > Қара
-
Тұрақтылығы бойынша: Қара > Қызыл > Ақ
-
Қауіптілігі бойынша: Ақ фосфор ең қауіпті
Қаласаңыз, мен осыны сызба түрінде немесе қысқаша шпаргалка форматында дайындап бере аламын.
-фосфор қосылыстарының Қазақстандағы кен орындарын атау
?? Фосфор қосылыстарының Қазақстандағы кен орындары
Қазақстан фосфорит қоры бойынша әлемдегі алдыңғы елдердің бірі. Негізгі кен орындары:
![]()
1️⃣ Қаратау фосфорит алабы
-
? Жамбыл облысында орналасқан
-
Қазақстандағы ең ірі фосфорит бассейні
-
Әлемдік маңызы бар
-
Негізгі кен орындары: Жаңатас, Қаратау
-
Тыңайтқыш өндірісінің негізгі шикізат көзі
![]()
2️⃣ Шилісай фосфорит кен орны
-
? Ақтөбе облысында
-
Батыс Қазақстандағы ірі кен орындарының бірі
-
Фосфор тыңайтқыштарын өндіруге пайдаланылады
![]()
3️⃣ Ақтөбе фосфорит алабы
-
? Ақтөбе өңірінде
-
Фосфориттің шөгінді түрлері кездеседі
![]()
4️⃣ Лисаков фосфорит кен орны
-
? Қостанай облысында
-
Солтүстік Қазақстандағы фосфат шикізат көзі
![]()
? Өндіріс орталығы
Фосфор шикізатын өңдеу орталығы:
-
Тараз
(Минералды тыңайтқыштар өндірісі дамыған)
![]()
? Қорытынды
Қазақстандағы негізгі фосфорит кен орындары:
-
Қаратау
-
Шилісай
-
Ақтөбе
-
Лисаков
Ең ірі және стратегиялық маңыздысы — Қаратау фосфорит алабы.
Қаласаңыз, карта бойынша орналасуын да түсіндіріп бере аламын.
фосфор және оның қосылыстарының жалпы химиялық қасиеттерін түсіндіру
? Фосфор және оның қосылыстарының жалпы химиялық қасиеттері
Фосфор (P) – белсенді бейметалл, тотығу дәрежелері: –3, +3, +5. Осыған байланысты оның қосылыстары да әртүрлі химиялық қасиет көрсетеді.
![]()
? I. Фосфордың химиялық қасиеттері
1️⃣ Оттекпен әрекеттесуі (тотығу)
Фосфор оңай тотығады:
-
Оттек жеткілікті болса:
4P+5O2→2P2O54P + 5O_2 → 2P_2O_54P+5O2→2P2O5
-
Оттек жеткіліксіз болса:
4P+3O2→2P2O34P + 3O_2 → 2P_2O_34P+3O2→2P2O3
? Қышқылдық оксидтер түзеді.
![]()
2️⃣ Металдармен әрекеттесуі
Фосфор металдармен әрекеттесіп фосфидтер түзеді:
3Ca+2P→Ca3P23Ca + 2P → Ca_3P_23Ca+2P→Ca3P2
Фосфидтер суда ыдырап, фосфин түзеді.
![]()
3️⃣ Сутекпен әрекеттесуі
Жанама жолмен Phosphine (PH₃) түзіледі.
-
Өте улы
-
Тотықсыздандырғыш қасиет көрсетеді
![]()
4️⃣ Галогендермен әрекеттесуі
Фосфор галогендермен оңай қосылады:
2P+3Cl2→2PCl32P + 3Cl_2 → 2PCl_32P+3Cl2→2PCl3 2P+5Cl2→2PCl52P + 5Cl_2 → 2PCl_52P+5Cl2→2PCl5
![]()
⚗️ II. Фосфор қосылыстарының химиялық қасиеттері
1️⃣ Оксидтері
Фосфор (V) оксиді – P₂O₅
-
Қышқылдық оксид
-
Сумен әрекеттесіп қышқыл түзеді:
P2O5+3H2O→2H3PO4P_2O_5 + 3H_2O → 2H_3PO_4P2O5+3H2O→2H3PO4
![]()
2️⃣ Қышқылдары
? Phosphoric acid (H₃PO₄)
-
Орташа күшті, үш негізді қышқыл
-
Негіздермен әрекеттесіп тұздар (фосфаттар) түзеді:
H3PO4+3NaOH→Na3PO4+3H2OH_3PO_4 + 3NaOH → Na_3PO_4 + 3H_2OH3PO4+3NaOH→Na3PO4+3H2O
-
Металдармен әрекеттесіп сутек бөледі
![]()
3️⃣ Фосфаттар
-
Қышқылдық, орта және негізгі тұздар түзеді
-
Көпшілігі суда нашар ериді
-
Қыздырғанда ыдырауы мүмкін
![]()
4️⃣ Фосфин (PH₃)
-
Әлсіз негіздік қасиет
-
Күшті тотықсыздандырғыш
-
Ауада тотығып, фосфор қышқылына айналуы мүмкін
![]()
? Тотығу-тотықсыздану қасиеті
Фосфор:
-
? Тотықсыздандырғыш бола алады (O₂, галогендермен)
-
? Тотықтырғыш бола алады (металдарға қатысты)
![]()
? Жалпы қорытынды
Фосфор және оның қосылыстары:
-
Қышқылдық қасиет көрсетеді
-
Тотығу-тотықсыздану реакцияларына оңай түседі
-
Тұздар, оксидтер, гидридтер түзеді
-
Химиялық белсенділігі жоғары
Қаласаңыз, осы тақырыпты қысқаша конспект немесе схема түрінде дайындап бере аламын.
осы тақырыпқа тапсырма жауаппен
? «Фосфор және оның қосылыстары» тақырыбына тапсырмалар (жауаптарымен)
![]()
1-тапсырма. Фосфордың мүмкін болатын тотығу дәрежелерін атаңыз.
Жауабы: –3, +3, +5
![]()
2-тапсырма. Реакция теңдеуін аяқтаңыз:
а) P+O2→?P + O_2 → ?P+O2→?
б) P2O5+H2O→?P_2O_5 + H_2O → ?P2O5+H2O→?
в) Ca+P→?Ca + P → ?Ca+P→?
Жауабы:
а)
4P+5O2→2P2O54P + 5O_2 → 2P_2O_54P+5O2→2P2O5
б)
P2O5+3H2O→2H3PO4P_2O_5 + 3H_2O → 2H_3PO_4P2O5+3H2O→2H3PO4
в)
3Ca+2P→Ca3P23Ca + 2P → Ca_3P_23Ca+2P→Ca3P2
![]()
3-тапсырма. Қай қосылыс қышқылдық оксид болып табылады?
A) PH₃
B) P₂O₅
C) Ca₃P₂
D) Na₃P
Жауабы: B) P₂O₅
![]()
4-тапсырма. Сәйкестендіру
|
Зат |
Қасиеті |
|
1. PH₃ |
а) Үш негізді қышқыл |
|
2. H₃PO₄ |
б) Улы газ |
|
3. P₂O₅ |
в) Қышқылдық оксид |
Жауабы:
1 – б
2 – а
3 – в
![]()
5-тапсырма. Фосфор қышқылы қандай тұздар түзеді?
Жауабы:
-
Орта тұздар (Na₃PO₄)
-
Қышқыл тұздар (NaH₂PO₄, Na₂HPO₄)
![]()
6-тапсырма. Есеп
32 г фосфор толық жанғанда қанша грамм P₂O₅ түзіледі?
3/2/1 әдісі»:
1. Мен білетін үш нәрсе ...
2. Мені таңқалдырған екі нәрсе ...
3. Болашақта тереңірек қарастыратын бір нәрсе....
3/2/1 әдісі»:
1. Мен білетін үш нәрсе ...
2. Мені таңқалдырған екі нәрсе ...
3. Болашақта тереңірек қарастыратын бір нәрсе....
3/2/1 әдісі»:
1. Мен білетін үш нәрсе ...
2. Мені таңқалдырған екі нәрсе ...
3. Болашақта тереңірек қарастыратын бір нәрсе....
3/2/1 әдісі»:
1. Мен білетін үш нәрсе ...
2. Мені таңқалдырған екі нәрсе ...
3. Болашақта тереңірек қарастыратын бір нәрсе....
3/2/1 әдісі»:
1. Мен білетін үш нәрсе ...
2. Мені таңқалдырған екі нәрсе ...
3. Болашақта тереңірек қарастыратын бір нәрсе....

шағым қалдыра аласыз







 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
