
Урок № 7
10"В" класс
|
Неделя |
День |
Урок |
|||||||||||||||||
|
Тема урока |
Периодичность изменения свойств элементов в главных подгруппах и периодах. Периодичность изменения свойств металла и неметалла, высших оксидов и гидроксидов, водородных соединений и их окислительно-восстановительных и кислотно-основных свойств. |
||||||||||||||||||
|
Общая цель |
Повторить и систематизировать информацию о закономерностях периодичности изменения свойств элементов. |
||||||||||||||||||
|
Ожидаемые результаты |
А)Знает периодичность изменения свойств металла и неметалла, высших оксидов и гидроксидов, водородных соединений. Б) Применяют при решении расчетных задач. С)Доказывают и приводят примеры. |
||||||||||||||||||
|
Тип урока |
Комбинированный урок. |
||||||||||||||||||
|
Задания |
1 Составление классификационной таблицы в парах, 2.Блиц-свидание , 3.Эвристическая беседа с просмотром слайдов.4. Контрольное тестирование. |
||||||||||||||||||
|
Необходимые материалы |
учебник, интерактивная доска, электронная презентация, тесты для проверочной работы |
||||||||||||||||||
|
Ход урока: |
|||||||||||||||||||
|
Этапы урока |
Действия учителя |
Действия ученика |
Техники ФО |
||||||||||||||||
|
Вводная часть 5- 10 мин. |
Работая в парах, расставьте следующие факторы в порядке _____________ н-р, их ценности, важности 1.
Что такое валентность? 2. Что такое степень окисления? 3. Чем определяется высшая валентность атомов? 4. Чем определяется низшая валентность атома? Учитель на доске изображает «рыбный скелет», учащиеся переносят его себе в тетради (схема 1). В «голове» рыбы записывается вопрос. На первых «косточках», ближайших к голове, записываются понятия, которые нужно сравнить, на вторых – определения этих понятий. Однако понятие валентности рассматривается уже на более высоком уровне, с точки зрения образования ковалентных связей. На следующих «косточках» учитель записывает примеры веществ N2 и NaCl, учащимся предлагается определить валентности и степень окисления элементов данных соединениях. Затем учащиеся делают вывод о том, в чем состоит отличие рассмотренных понятий. Этот вывод записывается в «хвосте» рыбы. Затем учитель формулирует следующее положение: «Мы обсудили, что валентность атома определяется числом неспаренных электронов. Но тогда, мне бы хотелось знать, чему равна валентность азота в катионе аммония NH4+». Учащиеся с помощью учителя, путем последовательных рассуждений, выводят решение этой проблемы:
|
Самостоятельная работа Ученик составляют схему по теме Фотосинтез , хемосинтез. (10 минут)
|
1Слова поощрения Взаимопроверка.
|
||||||||||||||||
|
Презентация 5-7 мин.
|
2. Презентация Блиц-свидание Сядьте с партнером так, чтобы один из вас смотрел на доску, а второй – в противоположную сторону.
|
У первого участника есть всего 30 секунд, чтобы объяснить ключевое (-ые) слово (-а), приведенное (-ые) ниже, прежде чем он перейдет к следующему партнеру –учитель задает ключевое слово для объяснения |
|
||||||||||||||||
|
Основная часть 15-20 мин.
|
1. Сообщение темы урока.
Периодичность изменения свойств элементов в главных
подгруппах и периодах. Периодичность изменения
свойств металла и
неметалла, высших оксидов и гидроксидов,
водородных соединений и их окислительно-восстановительных и
кислотно-основных свойств. Затем учитель формулирует следующее положение: «Мы обсудили данную тему. Учащиеся с помощью учителя, путем последовательных рассуждений, выводят решение этой проблемы: |
Записывают тему урока Эвристическая беседа с просмотром слайдов. Делают соответствующие записи в тетрадях.
Формулируют выводы |
Измерение температуры Слова поощрения Лист оценивания течении всего урока |
||||||||||||||||
|
Итог Рефлексия 5-8 мин.
|
3. Самостоятельно составьте контрольный тест 1. Подведение итогов урока. 2. Д/з Найти дополнительные сведения |
Самостоятельно составляют тесты по пройденной теме, используя рисунки и текст учебника
Проверка заполнения тестов . Самоконтроль
|
Слова поощрения Лист рефлексии Рефлексия «Все понятно», «Есть вопросы», «Непонятно»
|
||||||||||||||||
Приложение №1
Характеристики химических элементов закономерно изменяются в группах и периодах. (коротко)
В периодах (с увеличением порядкового номера)
-
увеличивается заряд ядра,
-
увеличивается число внешних электронов,
-
уменьшается радиус атомов,
-
увеличивается прочность связи электронов с ядром (энергия ионизации),
-
увеличивается электроотрицательность,
-
усиливаются окислительные свойства простых веществ ("неметалличность"),
-
ослабевают восстановительные свойства простых веществ ("металличность"),
-
ослабевает основный характер гидроксидов и соответствующих оксидов,
-
возрастает кислотный характер гидроксидов и соответствующих оксидов.
В группах (с увеличением порядкового номера)
-
увеличивается заряд ядра,
-
увеличивается радиус атомов (только в А-группах),
-
уменьшается прочность связи электронов с ядром (энергия ионизации; только в А-группах),
-
уменьшается электроотрицательность (только в А-группах),
-
ослабевают окислительные свойства простых веществ ("неметалличность"; только в А-группах),
-
усиливаются восстановительные свойства простых веществ ("металличность"; только в А-группах),
-
возрастает основный характер гидроксидов и соответствующих оксидов (только в А-группах),
-
ослабевает кислотный характер гидроксидов и соответствующих оксидов (только в А-группах),
-
снижается устойчивость водородных соединений (повышается их восстановительная активность; только в А-группах).
Характеристики химических элементов и их соединений (подробнее)
В главных подгруппах сверху вниз металлические свойства усиливаются, а неметаллические ослабевают. Элементы главных и побочных групп сильно отличаются по свойствам.
Номер группы показывает высшую валентность элемента (кроме O, F, элементов подгруппы меди и восьмой группы).
Общими для элементов главных и побочных подгрупп являются формулы высших оксидов (и их гидратов). У высших оксидов и их гидратов элементов I - III групп (кроме бора) преобладают основные свойства, с IV по VIII - кислотные.
|
Группа |
I |
II |
III |
IV |
V |
VI |
VII |
VIII (кроме инертных газов) |
|
Высший оксид |
Э2О |
ЭО |
Э2О3 |
ЭО2 |
Э2О5 |
ЭО3 |
Э2О7 |
ЭО4 |
|
Гидрат высшего оксида |
ЭОН |
Э(ОН)2 |
Э(ОН)3 |
Н2ЭО3 |
Н3ЭО4 |
Н2ЭО4 |
НЭО4 |
Н4ЭО4 |
Для элементов главных подгрупп общими являются формулы водородных соединений. Элементы главных подгрупп I - III групп образуют твердые вещества - гидриды (водород в степени окисления - 1), а IV - VII групп - газообразные. Водородные соединения элементов главных подгрупп IV группы (ЭН4) - нейтральны, V группы (ЭН3) - основания, VI и VII групп (Н2Э и НЭ) - кислоты.
От положения элементов в периодической системе зависят свойства атома, связанные с его электронной конфигурацией: атомный радиус - по периоду слева направо уменьшается, а в подгруппе сверху вниз возрастает; энергия ионизации - по периоду возрастает, а в подгруппе уменьшается; электроотрицательность - по периоду увеличивается, а в подгруппе уменьшается.
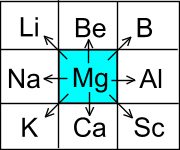
По положению элемента в периодической системе можно прогнозировать его основные свойства как средние всех его соседей:
|
|
Пример
На основании периодической таблицы охарактеризуйте химические элементы с порядковыми номерами 21 и 34.
Для характеристики химического элемента по периодической системе Д.И.Менделеева следует рассмотреть:
1. Положение в периодической таблице (порядковый номер; период, ряд; группа, подгруппа; атомная масса).
2. Строение атома (заряд ядра; состав ядра - количество протонов p11, нейтронов n01 и электронов e; число энергетических уровней и подуровней; написать формулу электронной конфигурации; квантовые ячейки; по числу и характеру валентных электронов определить тип элемента).
3. Формулы и химический характер соединений (высшего оксида и гидроксида; водородных соединений).
4. Сравнить с соседями (по периоду, по группе).
a) Порядковый номер элемента Z = 21 обозначает: заряд ядра атома элемента (скандия): 6521Sc – +21; число протонов p11: 21Sc – 21 p11; число электронов e: 21Sc – 21e; число нейтронов n01 = Ar – Z = 65 – 21 = 44 – 44n10
Формула состава атома
|
6521Sc ( |
21p11; 44n10 |
; 21e) |
|
|
состав ядра |
|
Скандий находится в IV периоде; номер периода обозначает число энергетических уровней - 4.
Скандий расположен в побочной подгруппе. Следовательно, его валентные электроны будут находится на 4s- и 3d-подуровнях.
Электронная формула скандия
|
21Sc |
1s2 2s2 2p6 3s2 3p6 |
3d1 4s2 |
|
|
[Ar] |
|
или в виде сокращенной записи: [Ar] 3d14s2
Электронная формула в виде квантовых ячеек:
|
21Sc [Ar] |
|
Скандий – d- элемент. Электронное строение атома заканчивается s- электронами, поэтому элемент будет проявлять металлические свойства.
Формула высшего оксида – Sc2O3, гидроксида – Sc(OH)3 обладают слабыми основными свойствами. Соединений с водородом не образует.
b) Порядковый номер 34 имеет селен Se. Элемент находится в IV периоде, значит в атоме имеется 4 энергетических уровня. Он находится в главной подгруппе VIгруппы; его валентные электроны распределены на 4s и 4p-подуровнях.
Электронная формула селена:
34Se 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p4
Внешний уровень в виде квантовых ячеек имеет вид:
|
|
Атом селена имеет 6 валентных электронов; поэтому высшая валентность равна 6, что соответствует номеру группы.
Селен - p- элемент, поэтому будет проявлять свойства неметалла.
Высший оксид SeO3, его гидроксид H2SeO4 и газообразное водородное соединение H2Se имеют кислотный характер.
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Периодичность изменения свойств элементов в главных подгруппах и периодах.Периодичность изменения свойств металла и неметалла, выс
Урок № 7
10"В" класс
|
Неделя |
День |
Урок |
|||||||||||||||||
|
Тема урока |
Периодичность изменения свойств элементов в главных подгруппах и периодах. Периодичность изменения свойств металла и неметалла, высших оксидов и гидроксидов, водородных соединений и их окислительно-восстановительных и кислотно-основных свойств. |
||||||||||||||||||
|
Общая цель |
Повторить и систематизировать информацию о закономерностях периодичности изменения свойств элементов. |
||||||||||||||||||
|
Ожидаемые результаты |
А)Знает периодичность изменения свойств металла и неметалла, высших оксидов и гидроксидов, водородных соединений. Б) Применяют при решении расчетных задач. С)Доказывают и приводят примеры. |
||||||||||||||||||
|
Тип урока |
Комбинированный урок. |
||||||||||||||||||
|
Задания |
1 Составление классификационной таблицы в парах, 2.Блиц-свидание , 3.Эвристическая беседа с просмотром слайдов.4. Контрольное тестирование. |
||||||||||||||||||
|
Необходимые материалы |
учебник, интерактивная доска, электронная презентация, тесты для проверочной работы |
||||||||||||||||||
|
Ход урока: |
|||||||||||||||||||
|
Этапы урока |
Действия учителя |
Действия ученика |
Техники ФО |
||||||||||||||||
|
Вводная часть 5- 10 мин. |
Работая в парах, расставьте следующие факторы в порядке _____________ н-р, их ценности, важности 1.
Что такое валентность? 2. Что такое степень окисления? 3. Чем определяется высшая валентность атомов? 4. Чем определяется низшая валентность атома? Учитель на доске изображает «рыбный скелет», учащиеся переносят его себе в тетради (схема 1). В «голове» рыбы записывается вопрос. На первых «косточках», ближайших к голове, записываются понятия, которые нужно сравнить, на вторых – определения этих понятий. Однако понятие валентности рассматривается уже на более высоком уровне, с точки зрения образования ковалентных связей. На следующих «косточках» учитель записывает примеры веществ N2 и NaCl, учащимся предлагается определить валентности и степень окисления элементов данных соединениях. Затем учащиеся делают вывод о том, в чем состоит отличие рассмотренных понятий. Этот вывод записывается в «хвосте» рыбы. Затем учитель формулирует следующее положение: «Мы обсудили, что валентность атома определяется числом неспаренных электронов. Но тогда, мне бы хотелось знать, чему равна валентность азота в катионе аммония NH4+». Учащиеся с помощью учителя, путем последовательных рассуждений, выводят решение этой проблемы:
|
Самостоятельная работа Ученик составляют схему по теме Фотосинтез , хемосинтез. (10 минут)
|
1Слова поощрения Взаимопроверка.
|
||||||||||||||||
|
Презентация 5-7 мин.
|
2. Презентация Блиц-свидание Сядьте с партнером так, чтобы один из вас смотрел на доску, а второй – в противоположную сторону.
|
У первого участника есть всего 30 секунд, чтобы объяснить ключевое (-ые) слово (-а), приведенное (-ые) ниже, прежде чем он перейдет к следующему партнеру –учитель задает ключевое слово для объяснения |
|
||||||||||||||||
|
Основная часть 15-20 мин.
|
1. Сообщение темы урока.
Периодичность изменения свойств элементов в главных
подгруппах и периодах. Периодичность изменения
свойств металла и
неметалла, высших оксидов и гидроксидов,
водородных соединений и их окислительно-восстановительных и
кислотно-основных свойств. Затем учитель формулирует следующее положение: «Мы обсудили данную тему. Учащиеся с помощью учителя, путем последовательных рассуждений, выводят решение этой проблемы: |
Записывают тему урока Эвристическая беседа с просмотром слайдов. Делают соответствующие записи в тетрадях.
Формулируют выводы |
Измерение температуры Слова поощрения Лист оценивания течении всего урока |
||||||||||||||||
|
Итог Рефлексия 5-8 мин.
|
3. Самостоятельно составьте контрольный тест 1. Подведение итогов урока. 2. Д/з Найти дополнительные сведения |
Самостоятельно составляют тесты по пройденной теме, используя рисунки и текст учебника
Проверка заполнения тестов . Самоконтроль
|
Слова поощрения Лист рефлексии Рефлексия «Все понятно», «Есть вопросы», «Непонятно»
|
||||||||||||||||
Приложение №1
Характеристики химических элементов закономерно изменяются в группах и периодах. (коротко)
В периодах (с увеличением порядкового номера)
-
увеличивается заряд ядра,
-
увеличивается число внешних электронов,
-
уменьшается радиус атомов,
-
увеличивается прочность связи электронов с ядром (энергия ионизации),
-
увеличивается электроотрицательность,
-
усиливаются окислительные свойства простых веществ ("неметалличность"),
-
ослабевают восстановительные свойства простых веществ ("металличность"),
-
ослабевает основный характер гидроксидов и соответствующих оксидов,
-
возрастает кислотный характер гидроксидов и соответствующих оксидов.
В группах (с увеличением порядкового номера)
-
увеличивается заряд ядра,
-
увеличивается радиус атомов (только в А-группах),
-
уменьшается прочность связи электронов с ядром (энергия ионизации; только в А-группах),
-
уменьшается электроотрицательность (только в А-группах),
-
ослабевают окислительные свойства простых веществ ("неметалличность"; только в А-группах),
-
усиливаются восстановительные свойства простых веществ ("металличность"; только в А-группах),
-
возрастает основный характер гидроксидов и соответствующих оксидов (только в А-группах),
-
ослабевает кислотный характер гидроксидов и соответствующих оксидов (только в А-группах),
-
снижается устойчивость водородных соединений (повышается их восстановительная активность; только в А-группах).
Характеристики химических элементов и их соединений (подробнее)
В главных подгруппах сверху вниз металлические свойства усиливаются, а неметаллические ослабевают. Элементы главных и побочных групп сильно отличаются по свойствам.
Номер группы показывает высшую валентность элемента (кроме O, F, элементов подгруппы меди и восьмой группы).
Общими для элементов главных и побочных подгрупп являются формулы высших оксидов (и их гидратов). У высших оксидов и их гидратов элементов I - III групп (кроме бора) преобладают основные свойства, с IV по VIII - кислотные.
|
Группа |
I |
II |
III |
IV |
V |
VI |
VII |
VIII (кроме инертных газов) |
|
Высший оксид |
Э2О |
ЭО |
Э2О3 |
ЭО2 |
Э2О5 |
ЭО3 |
Э2О7 |
ЭО4 |
|
Гидрат высшего оксида |
ЭОН |
Э(ОН)2 |
Э(ОН)3 |
Н2ЭО3 |
Н3ЭО4 |
Н2ЭО4 |
НЭО4 |
Н4ЭО4 |
Для элементов главных подгрупп общими являются формулы водородных соединений. Элементы главных подгрупп I - III групп образуют твердые вещества - гидриды (водород в степени окисления - 1), а IV - VII групп - газообразные. Водородные соединения элементов главных подгрупп IV группы (ЭН4) - нейтральны, V группы (ЭН3) - основания, VI и VII групп (Н2Э и НЭ) - кислоты.
От положения элементов в периодической системе зависят свойства атома, связанные с его электронной конфигурацией: атомный радиус - по периоду слева направо уменьшается, а в подгруппе сверху вниз возрастает; энергия ионизации - по периоду возрастает, а в подгруппе уменьшается; электроотрицательность - по периоду увеличивается, а в подгруппе уменьшается.
По положению элемента в периодической системе можно прогнозировать его основные свойства как средние всех его соседей:
|
|
Пример
На основании периодической таблицы охарактеризуйте химические элементы с порядковыми номерами 21 и 34.
Для характеристики химического элемента по периодической системе Д.И.Менделеева следует рассмотреть:
1. Положение в периодической таблице (порядковый номер; период, ряд; группа, подгруппа; атомная масса).
2. Строение атома (заряд ядра; состав ядра - количество протонов p11, нейтронов n01 и электронов e; число энергетических уровней и подуровней; написать формулу электронной конфигурации; квантовые ячейки; по числу и характеру валентных электронов определить тип элемента).
3. Формулы и химический характер соединений (высшего оксида и гидроксида; водородных соединений).
4. Сравнить с соседями (по периоду, по группе).
a) Порядковый номер элемента Z = 21 обозначает: заряд ядра атома элемента (скандия): 6521Sc – +21; число протонов p11: 21Sc – 21 p11; число электронов e: 21Sc – 21e; число нейтронов n01 = Ar – Z = 65 – 21 = 44 – 44n10
Формула состава атома
|
6521Sc ( |
21p11; 44n10 |
; 21e) |
|
|
состав ядра |
|
Скандий находится в IV периоде; номер периода обозначает число энергетических уровней - 4.
Скандий расположен в побочной подгруппе. Следовательно, его валентные электроны будут находится на 4s- и 3d-подуровнях.
Электронная формула скандия
|
21Sc |
1s2 2s2 2p6 3s2 3p6 |
3d1 4s2 |
|
|
[Ar] |
|
или в виде сокращенной записи: [Ar] 3d14s2
Электронная формула в виде квантовых ячеек:
|
21Sc [Ar] |
|
Скандий – d- элемент. Электронное строение атома заканчивается s- электронами, поэтому элемент будет проявлять металлические свойства.
Формула высшего оксида – Sc2O3, гидроксида – Sc(OH)3 обладают слабыми основными свойствами. Соединений с водородом не образует.
b) Порядковый номер 34 имеет селен Se. Элемент находится в IV периоде, значит в атоме имеется 4 энергетических уровня. Он находится в главной подгруппе VIгруппы; его валентные электроны распределены на 4s и 4p-подуровнях.
Электронная формула селена:
34Se 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p4
Внешний уровень в виде квантовых ячеек имеет вид:
|
|
Атом селена имеет 6 валентных электронов; поэтому высшая валентность равна 6, что соответствует номеру группы.
Селен - p- элемент, поэтому будет проявлять свойства неметалла.
Высший оксид SeO3, его гидроксид H2SeO4 и газообразное водородное соединение H2Se имеют кислотный характер.

шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
