
Тексерілді Қысқа мерзімді жоспар Пән мұғалімі Абылайқызы Әзиза
|
Мерзімі: 28.02.2017ж |
Пәні: Химия |
Класы: 9 а, ә |
|||||
|
Сабақтың тақырыбы: |
№3-практикалық жұмыс: «Металдар» тақырыбына эксперименттік есептер шығару» |
||||||
|
Сабақтың мақсаты: |
Оқушылардың металдар тақырыбына есептеулер жүргізіп, оны тәжірибеде көрсете алатындықтарын дәлелдету. |
||||||
|
Табыс критерийі |
|||||||
|
Барлық оқушылар |
Оқушылардың көпшілігі |
Жекелеген оқушылар |
|||||
|
Индикатормен жұмыс жасай отырып, есептеулер жүргізе алады. |
Гидролиздену реакциясын жазып, оны тәжірибеде көрсете алады. Тұздардың ортасын анықтай алады. |
Лакмус қатысында натрий гидроксиді мен күкірт қышқылы арасындағы реакция теңдеуі мен тәжірибені жүргізе алады. |
|||||
|
Пәнаралық байланыс: |
Математика, физика |
||||||
|
Сабақ кезеңдері: |
Сабақ барысы: |
Бағалау |
Ресурстар |
||||
|
Мұғалімнің әрекеті |
Оқушының әрекеті |
||||||
|
І Қызығушылықты ояту |
Ұйымдастыру кезеңі. Оқушылармен амандасып, сабаққа әзірліктерін бақылау. «Өткенге шолу» Оқушылар сабаққа әзірленбес бұрын өткен материалдарын жүйеге салады. Ол үшін топқа бөлініп әзірленеді. 1-топ: Айналулар деген не? Мысал келтір. 2-топ: Индикатор деген не? Қандай индикаторларды білесің? Мысал келтір. 3-топ: Гидролиз деген не? Мысал келтір. 4-топ: КСl, Zn(NO)3 , Na2 SO4 тұздарының ортасын анықта. |
Мұғаліммен амандасып сабаққа әзірленеді. Топ болып аталған анықтамаларға мысалмен қатар дәлелдемелер ұсынады. |
Қошемет сөздер. Формативті бағалау. |
|
|||
|
ІІ Мағынаны тану |
«Мен химикпын!» Бұл жарыста топтар үздік химик топ атағына таласады. 1-топ.Мына айналуларды орындаңдар: А) Темір (III) хлориді ® теміт ( ІІІ) гидроксиді ® темір (ІІІ) оксиді ® темір (ІІІ) нитраты ® Темір (ІІІ) оксиді. 2-топ. Лакмус қатысында натрий гидроксиді мен күкірт қышқылы арасындағы бейтараптану реакциясын жүргізіп, реаксияның толық және қысқартылған иондық теңдеуін жазыңдар. 3 -топ: Төменде берілген тұздардың қай тобында барлық тұздар гидролизге ұшырайды. 1) Na2SO4 , KCI , 2) AI2(SO4)3 , LiNO3 3) K2S , Mg (NO3)2 4) Na2CO3 , BaCI2 4-топ: Мына тұздардың: а) натрий сульфиті; ә) калий сульфаты; б) Мырыш нитраты; в) Темір (III) хлориді; қайсыларының судағы ерітінділері сілтілік орта көрсетеді.Берілген тұздардың гидролиздену реакциясы теңдеулерінің бірінші сатысын жазыңыздар |
Оқушылар топ болып алдарындағы есептерді қорғайды. Ең алғашқы болып аяқтаған топ ең үздік химиктер атағына ие болады. |
Формативті бағалау. |
|
|||
|
ІІІ Ой толғаныс Рефлексия |
«Сізге күміс, маған мыс!!!» Әр топ ойдан қарсы командаға есеп құрайды. Мысалы:
|
Оқушылар топ болып қарсы топқа есеп құрап, оның шығарылу жолын тексереді. |
Формативті бағалау . |
|
|||
|
Қорытынды бағамдау |
Үйге тапсырма. Есептер жинағы № 14,5-14,9 есеп |
||||||
Индикаторлар[1] (латынша: indico – нұсқаймын, анықтаймын) —
-
белгілі бір геологиялық, топырақтық, гидрологиялық, климаттық жағдайларға тән әр-текті табиғи объектілер (өсімдіктер, қазба организмдер, кейбір минералдар және т.б.). Көптеген индикаторлар нақты қарекетте қолданылады (мыс., кейбір өсімдік индикаторлары бойынша грунт суларының жаты тереңдігі мен минералдану дәрежесін білуге болады; бірқатар индикаторлар (өсімдіктер мен минералдар) пайдалы қазбалар қорларын, мыс, мырыш және т.б. кенорындарын іздестіруді жеңілдетеді.
-
Зерттелуші ерітіндіге аз мөлшерде енгізіліп, сол ерітіндіде химиялық әрекеттердің толық аяқталғандығын көрсететін заттар:
-
әрекеттесу аяқталысымен ерітінді түсінің өзгеруі немесе сол ерітіндіге малынған арнаулы қағаз түсінің өзгеруі;
-
мөлдір ерітінділер түбінде тұнбалардың пайда болуы немесе, керісінше, көмескі ерітінділердің мөлдірленуі;
-
түсті тұнбалар қалыптасуы немесе олардың ғайып болуы;
-
әрекет кезінде тұнбаға түскен шөгінді түсінің өзгеруі.
Химические индикаторы
Материал из Википедии — свободной энциклопедии
Индика́тор (лат. indicator — указатель) — соединение, позволяющее визуализировать изменение концентрации какого-либо вещества или компонента, например, в растворе при титровании, или быстро определить pH, еН и др. параметры. Существуют также химические индикаторы для самых различных специальных целей, например, для определения дозы облучения.
Содержание
Применение индикаторов
Индикаторы позволяют быстро и достаточно точно контролировать состав жидких или газообразных сред, следить за изменением их состава, или за протеканием химической реакции.
Широко используются кислотно-основные индикаторы, разбавленные растворы которых обладают способностью заметно изменять цвет, в зависимости от кислотности раствора. Причина изменения цвета — изменения в строении молекул индикатора в кислой и щелочной среде, что приводит к изменению спектра поглощения раствора.
Для определения состава газовых сред используют индикаторные бумажки и индикаторные трубки.
Структура молекул и цвет индикаторов
Трифенилметановые красители-индикаторы
Структура трифенилметановых красителей
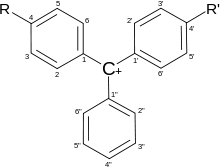
Трифенилметановые красители широко используются в качестве индикаторов. В зависимости от типа заместителей изменения структуры молекулы приводят к широкой гамме цветных соединений, большинство из которых могут служить химическими индикаторами.
|
Название \ Положение |
2" |
2 |
3 |
4 |
5 |
2' |
3' |
4' |
5' |
|
SO3− |
Me |
Br |
OH |
MeEt |
Me |
Br |
OH |
MeEt |
|
|
Бромфеноловый синий |
SO3− |
H |
Br |
OH |
Br |
H |
Br |
OH |
Br |
|
Бромкрезоловый зелёный |
SO3− |
Me |
Br |
OH |
Br |
Me |
Br |
OH |
Br |
|
SO3− |
H |
Me |
OH |
H |
H |
Me |
OH |
H |
|
|
CO2− |
H |
H |
OH |
H |
H |
H |
OH |
H |
|
|
Тимолфталеин |
CO2− |
Me |
H |
OH |
MeEt |
Me |
H |
OH |
MeEt |
|
H |
H |
H |
NMe2 |
H |
H |
H |
NMe2 |
H |
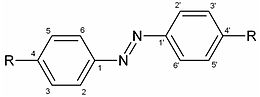
Производные азобензола
Структура производных азобензола
.
Виды индикаторов
-
Редокс-индикаторы, Ох- и Red-формы которых имеют различный цвет
Распространённые кислотно-основные индикаторы
Основная статья: Кислотно-основные индикаторы
|
Индикатор |
Окраска/кислая форма |
Окраска/щелочная форма |
Интервалы pH |
|
жёлтый |
фиолетовый |
10,1—12,1 |
|
|
бесцветный |
синий |
9,4—10,6 |
|
|
бесцветный |
малиновый |
8,2—10,0 |
|
|
жёлтый |
тёмно-красный |
7,0—8,8 |
|
|
красный |
коричневый |
6,8—8,0 |
|
|
жёлтый |
красный |
6,8—8,0 |
|
|
жёлтый |
синий |
6,0—7,6 |
|
|
Лакмус (азолитмин) |
красный |
синий |
5,0—8,0 |
|
красный |
жёлтый |
4,4—6,2 |
|
|
красный |
жёлтый |
3,0—4,4 |
|
|
красный |
синий |
3,0—4,6 |
|
|
Тропеолин 00… |
- |
жёлтый |
1,4—3,2 |
Металлоиндикаторы
Основная статья: Металлоиндикаторы
Окислительно-восстановительные индикаторы
Окислительно-восстановительные индикаторы изменяют цвет в зависимости от присутствия в растворе окислителей или восстановителей. Дифениламин бесцветен в восстановленной форме, но имеет фиолетовый цвет в окисленном состоянии. Метиленовый синий (синька) также бесцветен в восстановленной форме и имеет синий цвет в окисленном состоянии.
Некоторые ярко окрашенные вещества сами могут служить индикатором. Например, при перманганатометрическом определении железа(II)
10FeSO4 + 2KMnO4+ 8H2SO4 = 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
добавляемый в ходе титрования раствор перманганата обесцвечивается, пока не будут окислены все ионы Fe2+, имевшиеся в исследуемом растворе. Точка эквивалентности определяется по розовой окраске раствора, из-за возникшего избытка перманганат-анионов.
Хингидрон также является окислительно-восстановительным индикатором. это смесь хинона и гидрохинона.
Адсорбционные индикаторы
Термоиндикаторы
В качестве термоиндикатора можно использовать бумагу, смоченную хлоридом кобальта(II). При нагревании кристаллогидрат теряет связанную воду и меняет последовательно цвет с розового через красный, фиолетовый и синий на бесцветный.
Химические индикаторы влажности
Смотреть в учебниках химии.
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Практикалық жұмыс №3
Тексерілді Қысқа мерзімді жоспар Пән мұғалімі Абылайқызы Әзиза
|
Мерзімі: 28.02.2017ж |
Пәні: Химия |
Класы: 9 а, ә |
|||||
|
Сабақтың тақырыбы: |
№3-практикалық жұмыс: «Металдар» тақырыбына эксперименттік есептер шығару» |
||||||
|
Сабақтың мақсаты: |
Оқушылардың металдар тақырыбына есептеулер жүргізіп, оны тәжірибеде көрсете алатындықтарын дәлелдету. |
||||||
|
Табыс критерийі |
|||||||
|
Барлық оқушылар |
Оқушылардың көпшілігі |
Жекелеген оқушылар |
|||||
|
Индикатормен жұмыс жасай отырып, есептеулер жүргізе алады. |
Гидролиздену реакциясын жазып, оны тәжірибеде көрсете алады. Тұздардың ортасын анықтай алады. |
Лакмус қатысында натрий гидроксиді мен күкірт қышқылы арасындағы реакция теңдеуі мен тәжірибені жүргізе алады. |
|||||
|
Пәнаралық байланыс: |
Математика, физика |
||||||
|
Сабақ кезеңдері: |
Сабақ барысы: |
Бағалау |
Ресурстар |
||||
|
Мұғалімнің әрекеті |
Оқушының әрекеті |
||||||
|
І Қызығушылықты ояту |
Ұйымдастыру кезеңі. Оқушылармен амандасып, сабаққа әзірліктерін бақылау. «Өткенге шолу» Оқушылар сабаққа әзірленбес бұрын өткен материалдарын жүйеге салады. Ол үшін топқа бөлініп әзірленеді. 1-топ: Айналулар деген не? Мысал келтір. 2-топ: Индикатор деген не? Қандай индикаторларды білесің? Мысал келтір. 3-топ: Гидролиз деген не? Мысал келтір. 4-топ: КСl, Zn(NO)3 , Na2 SO4 тұздарының ортасын анықта. |
Мұғаліммен амандасып сабаққа әзірленеді. Топ болып аталған анықтамаларға мысалмен қатар дәлелдемелер ұсынады. |
Қошемет сөздер. Формативті бағалау. |
|
|||
|
ІІ Мағынаны тану |
«Мен химикпын!» Бұл жарыста топтар үздік химик топ атағына таласады. 1-топ.Мына айналуларды орындаңдар: А) Темір (III) хлориді ® теміт ( ІІІ) гидроксиді ® темір (ІІІ) оксиді ® темір (ІІІ) нитраты ® Темір (ІІІ) оксиді. 2-топ. Лакмус қатысында натрий гидроксиді мен күкірт қышқылы арасындағы бейтараптану реакциясын жүргізіп, реаксияның толық және қысқартылған иондық теңдеуін жазыңдар. 3 -топ: Төменде берілген тұздардың қай тобында барлық тұздар гидролизге ұшырайды. 1) Na2SO4 , KCI , 2) AI2(SO4)3 , LiNO3 3) K2S , Mg (NO3)2 4) Na2CO3 , BaCI2 4-топ: Мына тұздардың: а) натрий сульфиті; ә) калий сульфаты; б) Мырыш нитраты; в) Темір (III) хлориді; қайсыларының судағы ерітінділері сілтілік орта көрсетеді.Берілген тұздардың гидролиздену реакциясы теңдеулерінің бірінші сатысын жазыңыздар |
Оқушылар топ болып алдарындағы есептерді қорғайды. Ең алғашқы болып аяқтаған топ ең үздік химиктер атағына ие болады. |
Формативті бағалау. |
|
|||
|
ІІІ Ой толғаныс Рефлексия |
«Сізге күміс, маған мыс!!!» Әр топ ойдан қарсы командаға есеп құрайды. Мысалы:
|
Оқушылар топ болып қарсы топқа есеп құрап, оның шығарылу жолын тексереді. |
Формативті бағалау . |
|
|||
|
Қорытынды бағамдау |
Үйге тапсырма. Есептер жинағы № 14,5-14,9 есеп |
||||||
Индикаторлар[1] (латынша: indico – нұсқаймын, анықтаймын) —
-
белгілі бір геологиялық, топырақтық, гидрологиялық, климаттық жағдайларға тән әр-текті табиғи объектілер (өсімдіктер, қазба организмдер, кейбір минералдар және т.б.). Көптеген индикаторлар нақты қарекетте қолданылады (мыс., кейбір өсімдік индикаторлары бойынша грунт суларының жаты тереңдігі мен минералдану дәрежесін білуге болады; бірқатар индикаторлар (өсімдіктер мен минералдар) пайдалы қазбалар қорларын, мыс, мырыш және т.б. кенорындарын іздестіруді жеңілдетеді.
-
Зерттелуші ерітіндіге аз мөлшерде енгізіліп, сол ерітіндіде химиялық әрекеттердің толық аяқталғандығын көрсететін заттар:
-
әрекеттесу аяқталысымен ерітінді түсінің өзгеруі немесе сол ерітіндіге малынған арнаулы қағаз түсінің өзгеруі;
-
мөлдір ерітінділер түбінде тұнбалардың пайда болуы немесе, керісінше, көмескі ерітінділердің мөлдірленуі;
-
түсті тұнбалар қалыптасуы немесе олардың ғайып болуы;
-
әрекет кезінде тұнбаға түскен шөгінді түсінің өзгеруі.
Химические индикаторы
Материал из Википедии — свободной энциклопедии
Индика́тор (лат. indicator — указатель) — соединение, позволяющее визуализировать изменение концентрации какого-либо вещества или компонента, например, в растворе при титровании, или быстро определить pH, еН и др. параметры. Существуют также химические индикаторы для самых различных специальных целей, например, для определения дозы облучения.
Содержание
Применение индикаторов
Индикаторы позволяют быстро и достаточно точно контролировать состав жидких или газообразных сред, следить за изменением их состава, или за протеканием химической реакции.
Широко используются кислотно-основные индикаторы, разбавленные растворы которых обладают способностью заметно изменять цвет, в зависимости от кислотности раствора. Причина изменения цвета — изменения в строении молекул индикатора в кислой и щелочной среде, что приводит к изменению спектра поглощения раствора.
Для определения состава газовых сред используют индикаторные бумажки и индикаторные трубки.
Структура молекул и цвет индикаторов
Трифенилметановые красители-индикаторы
Структура трифенилметановых красителей
Трифенилметановые красители широко используются в качестве индикаторов. В зависимости от типа заместителей изменения структуры молекулы приводят к широкой гамме цветных соединений, большинство из которых могут служить химическими индикаторами.
|
Название \ Положение |
2" |
2 |
3 |
4 |
5 |
2' |
3' |
4' |
5' |
|
SO3− |
Me |
Br |
OH |
MeEt |
Me |
Br |
OH |
MeEt |
|
|
Бромфеноловый синий |
SO3− |
H |
Br |
OH |
Br |
H |
Br |
OH |
Br |
|
Бромкрезоловый зелёный |
SO3− |
Me |
Br |
OH |
Br |
Me |
Br |
OH |
Br |
|
SO3− |
H |
Me |
OH |
H |
H |
Me |
OH |
H |
|
|
CO2− |
H |
H |
OH |
H |
H |
H |
OH |
H |
|
|
Тимолфталеин |
CO2− |
Me |
H |
OH |
MeEt |
Me |
H |
OH |
MeEt |
|
H |
H |
H |
NMe2 |
H |
H |
H |
NMe2 |
H |
Производные азобензола
Структура производных азобензола
.
Виды индикаторов
-
Редокс-индикаторы, Ох- и Red-формы которых имеют различный цвет
Распространённые кислотно-основные индикаторы
Основная статья: Кислотно-основные индикаторы
|
Индикатор |
Окраска/кислая форма |
Окраска/щелочная форма |
Интервалы pH |
|
жёлтый |
фиолетовый |
10,1—12,1 |
|
|
бесцветный |
синий |
9,4—10,6 |
|
|
бесцветный |
малиновый |
8,2—10,0 |
|
|
жёлтый |
тёмно-красный |
7,0—8,8 |
|
|
красный |
коричневый |
6,8—8,0 |
|
|
жёлтый |
красный |
6,8—8,0 |
|
|
жёлтый |
синий |
6,0—7,6 |
|
|
Лакмус (азолитмин) |
красный |
синий |
5,0—8,0 |
|
красный |
жёлтый |
4,4—6,2 |
|
|
красный |
жёлтый |
3,0—4,4 |
|
|
красный |
синий |
3,0—4,6 |
|
|
Тропеолин 00… |
- |
жёлтый |
1,4—3,2 |
Металлоиндикаторы
Основная статья: Металлоиндикаторы
Окислительно-восстановительные индикаторы
Окислительно-восстановительные индикаторы изменяют цвет в зависимости от присутствия в растворе окислителей или восстановителей. Дифениламин бесцветен в восстановленной форме, но имеет фиолетовый цвет в окисленном состоянии. Метиленовый синий (синька) также бесцветен в восстановленной форме и имеет синий цвет в окисленном состоянии.
Некоторые ярко окрашенные вещества сами могут служить индикатором. Например, при перманганатометрическом определении железа(II)
10FeSO4 + 2KMnO4+ 8H2SO4 = 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
добавляемый в ходе титрования раствор перманганата обесцвечивается, пока не будут окислены все ионы Fe2+, имевшиеся в исследуемом растворе. Точка эквивалентности определяется по розовой окраске раствора, из-за возникшего избытка перманганат-анионов.
Хингидрон также является окислительно-восстановительным индикатором. это смесь хинона и гидрохинона.
Адсорбционные индикаторы
Термоиндикаторы
В качестве термоиндикатора можно использовать бумагу, смоченную хлоридом кобальта(II). При нагревании кристаллогидрат теряет связанную воду и меняет последовательно цвет с розового через красный, фиолетовый и синий на бесцветный.
Химические индикаторы влажности
Смотреть в учебниках химии.

шағым қалдыра аласыз









 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
