
Наименование: Раздел 1. Периодический закон,
периодическая система химических элементов в свете теории строения атомов
|
ПОУРОЧНЫЙ ПЛАН №1 |
||||||||
|
|
||||||||
|
Курс: |
1 |
Группа: |
ТМ-18-9, Т-18-9, ХТиП-18-9, Д-18-9, ВТиПО-18-9 |
Номер урока (пара) |
|
|||
|
Специальность, квалификация: |
Специальность: 1014000 «Технология машиностроения», 1109000 «Токарное дело и металлообработка (по идам)», 0816000 «Химическая технология и производство», 0402000 «Дизайн (по профилю)», 1304000 «Вычислительная техника и программное обеспечение (по видам)» Квалификация: 1014023 «Техник-механик», 1109113 «Техник - механик»,_ 0816053 «Техник – лаборант», 0402013 «Дизайнер»,1304043 «Техник - программист» |
|||||||
|
Наименование модуля: |
Химия |
|||||||
|
Тема урока: |
Modern theory of the structure of atoms, the movement of electrons in an atom, quantum number. |
|||||||
|
Дата: |
|
Продолжительность: |
2 часа (90 мин) |
|||||
|
Место проведения: |
ЧУ «Политехнический колледж корпорации «Казахмыс», аудитория № |
|||||||
|
Цель урока: |
1)Дать представление учащимся о Периодическом законе и Периодической системе химических элементов Д. И. Менделеева. 2)Закрепить знания учащихся о взаимосвязи между положением элемента в периодической системе и строением атома. 3)Знать определение периодического закона химических элементов. 4)Знать структуру периодической системы химических элементов. 5)Уметь составлять характеристику химическим элементам 6)Способствовать развитию навыков работы в составе малых групп. 7)Способствовать развитию познавательного интереса. 8)Создавать условия для развития логического мышления, творческих способностей, фантазии. 9)Ознакомить с правилами ТБ в кабинете химии и неукоснительно их выполнять. |
|||||||
|
Задачи урока: |
1.Обобщение и углубление знаний о строении атома, объяснение устройства периодической системы элементов с точки зрения строения атома. 2.Развитие познавательной активности учащихся, интереса к предмету, умения сравнивать, анализировать, быстро и четко формулировать и высказывать свои мысли, применять знания на практике. 3.Воспитывать умение работать в коллективе. |
|||||||
|
Ожидаемые результаты: |
correctly give the wording of
the periodic law; |
|||||||
|
Тип урока: |
Урок изучения нового материала |
|||||||
|
Методы обучения, методические приемы, педагогические техники, педагогические технологии: |
||||||||
|
Наглядно-иллюстративный (презентация), методы учебной работы под руководством преподавателя, методы самостоятельной учебной работы. |
||||||||
|
Необходимое оборудование и приборы: |
|
|||||||
|
Дополнительные источники (литература): |
1.Химия.Н.Нұрахметов.Қ.Бекішев.Н.Заграничная Алматы «Мектеп»-2010 2.Артеменко А.И. Органическая химия.- М., 2006 3.Ахметов Н.С. Общая и неорганическая химия.- М., 2003 4.Биологическая химия./Под ред.Ю.Б.Филипповича,Н.И.Ковалевская,Г.А.Севастьяновой . - М., 2005 5.Вольхин В.В. Общая химия. Основной курс. - СПб, М, Краснодар., 2008 6.Гельфман М.И., Юстратов В.П. Химия. - СПб, М, Краснодар., 2008 7.Глинка Н.Л. Общая химия. - М., 2005 8.Говарикер В.Р., Васванатхан Н.В., Шридхар Дж.М. Полимеры. - М., 2000 |
|||||||
ПЛАН-КОНСПЕКТ УРОКА
|
Ход урока |
Время (минуты) |
Действия преподавателя |
|
1 |
2 |
3 |
|
1. Организационный этап |
2 |
Приветствие; сверка присутствующих; запись темы урока. |
|
2. Актуализация знаний |
20 |
Опрос студентов по теме: 1.Периодическая таблица Менделеева? 2.Что такое атом? 3.Как правильно рассчитать протоны? |
|
3. Формирование новых знаний и способов деятельности |
35 |
1.Формулировка периодического закона, данная Д.И.Менделеевым. Отклонения от порядка возрастания атомных масс, причина. Современная формулировка. 2.Характеристика частиц, входящих в состав атома. 3.Сходства и различия иона натрия и атома неона, иона хлора и атома аргона. 4.Связь между строением атома и положением элемента в периодической системе. |
|
4. Закрепление
|
10 |
Закрепить знания с помощью тестов |
|
5. Контроль или самоконтроль
усвоения знаний |
10 |
Выявление качества и уровня усвоения знаний сначала работаем по фронтальнлму опросу , потом тесты |
|
6. Выдача домашнего задания |
5 |
Преподаватель проводит инструктаж о выполнении домашнего задания: §2.1 №2,3,6 [1] §2.2 №1-5 [1]
|
|
7. Summarizing |
10 |
Summing up the lessons. We do it in the form of tests. We estimate |
формировать представление о гражданской войне как битве приверженцев
альтернативных путей возрождения России;
Ø уяснить причины Гражданской войны;
Ø раскрыть цели противоборствующих сторон, определить их социальный состав
формировать представление о гражданской войне как битве приверженцев
альтернативных путей возрождения России;
Ø уяснить причины Гражданской войны;
Ø раскрыть цели противоборствующих сторон, определить их социальный состав
Планируемые результаты обучения:
-
Новые знания: понятия – ядро, протон, нейтрон, электрон.
-
Обобщение представлений об атоме.
-
Умение определять количество р+ , no, е– .
-
Развитие навыков: работы с инструментами, самостоятельное принятие решений, коммуникативные умения и навыки, умение самостоятельной мыслительной деятельности.
-
Развитие навыка самоконтроля.
-
Воспитание толерантности.
-
Расширение кругозора.
Ход урока
Здравствуйте, ребята!
Сегодня мы начинаем изучать новую тему “Атомы химических элементов”. На изучение этой темы отводится 7 часов. Сегодня мы познакомимся со строением атома, а на следующих уроках вы будете знакомиться со строением электронных орбиталей, ионами, видами химической связи. Напишите 2 тематических учета знаний и 1 контрольную работу.
А сейчас мы отправимся в дальнейшее путешествие по удивительной стране “Химия”. План нашего урока перед вами. Пожалуйста, с ним познакомьтесь. Обратите внимание, у нас с вами с/р, где вы покажите на сколько хорошо усвоили материал. Посмотрите на меня внимательно. Главное, что вы должны запомнить на сегодняшнем уроке: как устроен атом, состав атомного ядра. Научиться определять заряд ядра, количество протонов, нейтронов, электронов.
Откройте тетради, запишите число, тему урока: “Строение атома”. И так, мы начинаем.
ВИДЕО
(После просмотра) Давайте хором назовем химические элементы.
СЛАЙД № 1
Вы знаете, что вещества состоят из молекул, а молекулы из атомов. Ребята, атом тоже имеет сложное строение. Об этом говорят многочисленные опыты, с которыми вы будете знакомиться на уроках физики и при дальнейшем изучении химии. Атом имеет ядро и электроны, которые движутся вокруг ядра. Если применить образное сравнение, то весь объем атома можно уподобить стадиону в Лужниках, а ядро – футбольному мячу, положенному в центр поля. Атом любого химического элемента – как бы крохотная Солнечная система. Поэтому такую модель атома, предложенную Резерфордом, назвали планетарной. Но оказывается, что крохотное атомное ядро, в котором сосредоточена вся масса атома, состоит из частиц двух видов – протонов и нейтронов.
СХЕМА № 1 Возьми на своих столах схему № 1.
Рассмотрите ее внимательно: атом состоит из ядра и электронной оболочки, которая состоит из электронов. В центре атома находится ядро. Ядро состоит из протонов и нейтронов, которые называются нуклонами.
СЛАЙД № 2 Задание – заполнить пропуски в тексте, используя данные слова.
“В центре атома находится ядро, которое состоит из протонов и нейтронов. Вокруг ядра с большой скоростью движутся электроны”.
Повернитесь друг к другу в полоборота, сядьте ровно. Сейчас вы работаете в парах и друг другу проговорите еще раз шепотом строение атома, используя данную схему(рис.1).
Познакомимся с основными характеристиками элементарных частиц. Заполним вместе таблицу.
|
Масса |
Заряд |
|
|
Протон р+ |
1 |
+1 |
|
Нейтрон n0 |
1 |
0 |
|
Электрон е– |
0 |
-1 |
СЛАЙД № 3
-
Посмотрим в схему 1. Какие частицы находятся в ядре?
-
Какие из них имеют заряд?
-
А ядро будет иметь заряд?
-
За счет каких частиц?
-
Атом имеет массу?
-
За счет каких частиц?
-
Электроны вносят вклад в массу атома?
-
Значит в какой части атома сосредоточена его масса?
Мы знакомы с ПСХЭ. Сегодня мы научимся характеризовать элемент с т.з. строения атома.
СЛАЙД № 4 Химический элемент представляет собой совокупность атомов, имеющих одинаковый атомный номер.
Запишем в тетрадь: Число протонов в ядре атома соответствует его атомному номеру и обозначается символом Z.
Работа по закреплению у ПСХЭ.
Гимнастика для глаз
Познакомимся с атомным номером. Возьмите в руки ПСХЭ Д.И.Менделеева. Вам необходимо определить атомный номер элемента и число протонов для следующих элементов: Al S // Переверните ПС на 180о O H
Мы узнали, что число протонов определяется по порядковому номеру элемента.
СЛАЙД № 5 Сейчас наша задача научиться определять число нейтронов. Т.к. вся масса атома сосредоточена в ядре, то число нейтронов можно определить по следующей формуле:
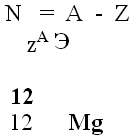
Запишите в тетрадь атомный номер и массовое число следующих элементов:
Фосфора и кислорода.
Обратная сторона доски: Проверьте.
СЛАЙД № 6 Кол-во нейтронов вычисляется по формуле: N=A-Z.
Например: ядро атома магния содержит 12 нейтронов. 24 – 12 = 12.
Гимнастика для глаз: Возьмите в руки ПСХЭ Д.И.Менделеева на расстоянии вытянутой руки. Молча определите кол-во протонов и нейтронов для атомов: С, Si.
Обратная сторона доски: Проверьте. Правильно? Запишите это в тетрадь.
Учимся определять число электронов. Число электронов определяется по порядковому номеру. Допишите в тетради число электронов у С и Si.
Ребята, кто был из вас внимателен в начале урока? Скажите мне, с какими новыми понятиями вы сегодня познакомились? ………….
У нас с вами творческая работа. Работать вы будете в группах по 4 человека. Вам предстоит создать модель атома гелия. Посмотрите внимательно, как может выглядеть атом. Для работы используйте наборы, которые лежат на столах. На выполнение работы вам дается 4 минуты. И так, время пошло. Кто первый завершит конструирование своей модели атома гелия, тот вывешивает свою работу на доску.
Давайте посмотрим ваши работы. Выбрать правильную. Расскажите как вы выполняли. Молодцы.
Сейчас посмотрите в свои тетрадочки с самого начала урока. Вспомните то, что мы сегодня записали. Подошло время Испытать себя. Записали в тетрадях “Самостоятельная работа”. (Инструкция)
СЛАЙД № 7 Время на выполнение работы – 3 минуты. Самопроверка по образцу.
Встаньте те, кто не допустил ни одной ошибки. Продолжайте стоять. Встаньте те, кто допустил 1 ошибку. Похлопаем. Молодцы. Садитесь.
Самой распространенной ошибкой в этой работе было нахождение числа нейтронов. Еще раз, скажите мне, как мы находим кол-во нейтронов?
Домашнее задание.
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Современная теория строения атомов, движение электронов в атоме, квантовое число.
Наименование: Раздел 1. Периодический закон,
периодическая система химических элементов в свете теории строения атомов
|
ПОУРОЧНЫЙ ПЛАН №1 |
||||||||
|
|
||||||||
|
Курс: |
1 |
Группа: |
ТМ-18-9, Т-18-9, ХТиП-18-9, Д-18-9, ВТиПО-18-9 |
Номер урока (пара) |
|
|||
|
Специальность, квалификация: |
Специальность: 1014000 «Технология машиностроения», 1109000 «Токарное дело и металлообработка (по идам)», 0816000 «Химическая технология и производство», 0402000 «Дизайн (по профилю)», 1304000 «Вычислительная техника и программное обеспечение (по видам)» Квалификация: 1014023 «Техник-механик», 1109113 «Техник - механик»,_ 0816053 «Техник – лаборант», 0402013 «Дизайнер»,1304043 «Техник - программист» |
|||||||
|
Наименование модуля: |
Химия |
|||||||
|
Тема урока: |
Modern theory of the structure of atoms, the movement of electrons in an atom, quantum number. |
|||||||
|
Дата: |
|
Продолжительность: |
2 часа (90 мин) |
|||||
|
Место проведения: |
ЧУ «Политехнический колледж корпорации «Казахмыс», аудитория № |
|||||||
|
Цель урока: |
1)Дать представление учащимся о Периодическом законе и Периодической системе химических элементов Д. И. Менделеева. 2)Закрепить знания учащихся о взаимосвязи между положением элемента в периодической системе и строением атома. 3)Знать определение периодического закона химических элементов. 4)Знать структуру периодической системы химических элементов. 5)Уметь составлять характеристику химическим элементам 6)Способствовать развитию навыков работы в составе малых групп. 7)Способствовать развитию познавательного интереса. 8)Создавать условия для развития логического мышления, творческих способностей, фантазии. 9)Ознакомить с правилами ТБ в кабинете химии и неукоснительно их выполнять. |
|||||||
|
Задачи урока: |
1.Обобщение и углубление знаний о строении атома, объяснение устройства периодической системы элементов с точки зрения строения атома. 2.Развитие познавательной активности учащихся, интереса к предмету, умения сравнивать, анализировать, быстро и четко формулировать и высказывать свои мысли, применять знания на практике. 3.Воспитывать умение работать в коллективе. |
|||||||
|
Ожидаемые результаты: |
correctly give the wording of
the periodic law; |
|||||||
|
Тип урока: |
Урок изучения нового материала |
|||||||
|
Методы обучения, методические приемы, педагогические техники, педагогические технологии: |
||||||||
|
Наглядно-иллюстративный (презентация), методы учебной работы под руководством преподавателя, методы самостоятельной учебной работы. |
||||||||
|
Необходимое оборудование и приборы: |
|
|||||||
|
Дополнительные источники (литература): |
1.Химия.Н.Нұрахметов.Қ.Бекішев.Н.Заграничная Алматы «Мектеп»-2010 2.Артеменко А.И. Органическая химия.- М., 2006 3.Ахметов Н.С. Общая и неорганическая химия.- М., 2003 4.Биологическая химия./Под ред.Ю.Б.Филипповича,Н.И.Ковалевская,Г.А.Севастьяновой . - М., 2005 5.Вольхин В.В. Общая химия. Основной курс. - СПб, М, Краснодар., 2008 6.Гельфман М.И., Юстратов В.П. Химия. - СПб, М, Краснодар., 2008 7.Глинка Н.Л. Общая химия. - М., 2005 8.Говарикер В.Р., Васванатхан Н.В., Шридхар Дж.М. Полимеры. - М., 2000 |
|||||||
ПЛАН-КОНСПЕКТ УРОКА
|
Ход урока |
Время (минуты) |
Действия преподавателя |
|
1 |
2 |
3 |
|
1. Организационный этап |
2 |
Приветствие; сверка присутствующих; запись темы урока. |
|
2. Актуализация знаний |
20 |
Опрос студентов по теме: 1.Периодическая таблица Менделеева? 2.Что такое атом? 3.Как правильно рассчитать протоны? |
|
3. Формирование новых знаний и способов деятельности |
35 |
1.Формулировка периодического закона, данная Д.И.Менделеевым. Отклонения от порядка возрастания атомных масс, причина. Современная формулировка. 2.Характеристика частиц, входящих в состав атома. 3.Сходства и различия иона натрия и атома неона, иона хлора и атома аргона. 4.Связь между строением атома и положением элемента в периодической системе. |
|
4. Закрепление
|
10 |
Закрепить знания с помощью тестов |
|
5. Контроль или самоконтроль
усвоения знаний |
10 |
Выявление качества и уровня усвоения знаний сначала работаем по фронтальнлму опросу , потом тесты |
|
6. Выдача домашнего задания |
5 |
Преподаватель проводит инструктаж о выполнении домашнего задания: §2.1 №2,3,6 [1] §2.2 №1-5 [1]
|
|
7. Summarizing |
10 |
Summing up the lessons. We do it in the form of tests. We estimate |
формировать представление о гражданской войне как битве приверженцев
альтернативных путей возрождения России;
Ø уяснить причины Гражданской войны;
Ø раскрыть цели противоборствующих сторон, определить их социальный состав
формировать представление о гражданской войне как битве приверженцев
альтернативных путей возрождения России;
Ø уяснить причины Гражданской войны;
Ø раскрыть цели противоборствующих сторон, определить их социальный состав
Планируемые результаты обучения:
-
Новые знания: понятия – ядро, протон, нейтрон, электрон.
-
Обобщение представлений об атоме.
-
Умение определять количество р+ , no, е– .
-
Развитие навыков: работы с инструментами, самостоятельное принятие решений, коммуникативные умения и навыки, умение самостоятельной мыслительной деятельности.
-
Развитие навыка самоконтроля.
-
Воспитание толерантности.
-
Расширение кругозора.
Ход урока
Здравствуйте, ребята!
Сегодня мы начинаем изучать новую тему “Атомы химических элементов”. На изучение этой темы отводится 7 часов. Сегодня мы познакомимся со строением атома, а на следующих уроках вы будете знакомиться со строением электронных орбиталей, ионами, видами химической связи. Напишите 2 тематических учета знаний и 1 контрольную работу.
А сейчас мы отправимся в дальнейшее путешествие по удивительной стране “Химия”. План нашего урока перед вами. Пожалуйста, с ним познакомьтесь. Обратите внимание, у нас с вами с/р, где вы покажите на сколько хорошо усвоили материал. Посмотрите на меня внимательно. Главное, что вы должны запомнить на сегодняшнем уроке: как устроен атом, состав атомного ядра. Научиться определять заряд ядра, количество протонов, нейтронов, электронов.
Откройте тетради, запишите число, тему урока: “Строение атома”. И так, мы начинаем.
ВИДЕО
(После просмотра) Давайте хором назовем химические элементы.
СЛАЙД № 1
Вы знаете, что вещества состоят из молекул, а молекулы из атомов. Ребята, атом тоже имеет сложное строение. Об этом говорят многочисленные опыты, с которыми вы будете знакомиться на уроках физики и при дальнейшем изучении химии. Атом имеет ядро и электроны, которые движутся вокруг ядра. Если применить образное сравнение, то весь объем атома можно уподобить стадиону в Лужниках, а ядро – футбольному мячу, положенному в центр поля. Атом любого химического элемента – как бы крохотная Солнечная система. Поэтому такую модель атома, предложенную Резерфордом, назвали планетарной. Но оказывается, что крохотное атомное ядро, в котором сосредоточена вся масса атома, состоит из частиц двух видов – протонов и нейтронов.
СХЕМА № 1 Возьми на своих столах схему № 1.
Рассмотрите ее внимательно: атом состоит из ядра и электронной оболочки, которая состоит из электронов. В центре атома находится ядро. Ядро состоит из протонов и нейтронов, которые называются нуклонами.
СЛАЙД № 2 Задание – заполнить пропуски в тексте, используя данные слова.
“В центре атома находится ядро, которое состоит из протонов и нейтронов. Вокруг ядра с большой скоростью движутся электроны”.
Повернитесь друг к другу в полоборота, сядьте ровно. Сейчас вы работаете в парах и друг другу проговорите еще раз шепотом строение атома, используя данную схему(рис.1).
Познакомимся с основными характеристиками элементарных частиц. Заполним вместе таблицу.
|
Масса |
Заряд |
|
|
Протон р+ |
1 |
+1 |
|
Нейтрон n0 |
1 |
0 |
|
Электрон е– |
0 |
-1 |
СЛАЙД № 3
-
Посмотрим в схему 1. Какие частицы находятся в ядре?
-
Какие из них имеют заряд?
-
А ядро будет иметь заряд?
-
За счет каких частиц?
-
Атом имеет массу?
-
За счет каких частиц?
-
Электроны вносят вклад в массу атома?
-
Значит в какой части атома сосредоточена его масса?
Мы знакомы с ПСХЭ. Сегодня мы научимся характеризовать элемент с т.з. строения атома.
СЛАЙД № 4 Химический элемент представляет собой совокупность атомов, имеющих одинаковый атомный номер.
Запишем в тетрадь: Число протонов в ядре атома соответствует его атомному номеру и обозначается символом Z.
Работа по закреплению у ПСХЭ.
Гимнастика для глаз
Познакомимся с атомным номером. Возьмите в руки ПСХЭ Д.И.Менделеева. Вам необходимо определить атомный номер элемента и число протонов для следующих элементов: Al S // Переверните ПС на 180о O H
Мы узнали, что число протонов определяется по порядковому номеру элемента.
СЛАЙД № 5 Сейчас наша задача научиться определять число нейтронов. Т.к. вся масса атома сосредоточена в ядре, то число нейтронов можно определить по следующей формуле:
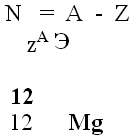
Запишите в тетрадь атомный номер и массовое число следующих элементов:
Фосфора и кислорода.
Обратная сторона доски: Проверьте.
СЛАЙД № 6 Кол-во нейтронов вычисляется по формуле: N=A-Z.
Например: ядро атома магния содержит 12 нейтронов. 24 – 12 = 12.
Гимнастика для глаз: Возьмите в руки ПСХЭ Д.И.Менделеева на расстоянии вытянутой руки. Молча определите кол-во протонов и нейтронов для атомов: С, Si.
Обратная сторона доски: Проверьте. Правильно? Запишите это в тетрадь.
Учимся определять число электронов. Число электронов определяется по порядковому номеру. Допишите в тетради число электронов у С и Si.
Ребята, кто был из вас внимателен в начале урока? Скажите мне, с какими новыми понятиями вы сегодня познакомились? ………….
У нас с вами творческая работа. Работать вы будете в группах по 4 человека. Вам предстоит создать модель атома гелия. Посмотрите внимательно, как может выглядеть атом. Для работы используйте наборы, которые лежат на столах. На выполнение работы вам дается 4 минуты. И так, время пошло. Кто первый завершит конструирование своей модели атома гелия, тот вывешивает свою работу на доску.
Давайте посмотрим ваши работы. Выбрать правильную. Расскажите как вы выполняли. Молодцы.
Сейчас посмотрите в свои тетрадочки с самого начала урока. Вспомните то, что мы сегодня записали. Подошло время Испытать себя. Записали в тетрадях “Самостоятельная работа”. (Инструкция)
СЛАЙД № 7 Время на выполнение работы – 3 минуты. Самопроверка по образцу.
Встаньте те, кто не допустил ни одной ошибки. Продолжайте стоять. Встаньте те, кто допустил 1 ошибку. Похлопаем. Молодцы. Садитесь.
Самой распространенной ошибкой в этой работе было нахождение числа нейтронов. Еще раз, скажите мне, как мы находим кол-во нейтронов?
Домашнее задание.

шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
