
Сыныбы: 11
Cабақтытың тақырыбы: Спирттер, құрамы мен жіктелуі
Сабақтың мақсаты: 1. Спирттердің формуласы гомологтық қатары, изомер түзілуі туралы түсініктер беру.
2. Спирттерді атау және изомерлерін жазу.
Сабақтың түрі: ұжымдық ойлау.
Сабақтың әдісі: Сұрақ жауап, баяндау, кітаппен жұмыс. .
Сабақтың барысы: І. Ұйымдастыру бөлімі.
ІІ. Жаңа сабақты түсіндіру.
ІІІ. Бекіту
ІV. Үйге тапсырма беру.
ІІ. СПИРТТЕР
Спирттер мен фенолдар. Функционалдық топ (- ОН).
Спирттердің жіктелуі:біріншілік;екіншілік;үшіншілік;
біратомды;көпатомды.
"Спирт" сөзі латынның "шараптың рухы" деген сөзінен шыққан көрінеді. этил спирті формуласы — С2Н5ОН. Жүзімнің, қанттың, крахмалдың ферменттік ашуы нәтижесінде түзілетін бұл затты тұрмыста жай ғана спирт деп атайды. Ал XVIII гасырдан бастап "спирт" деген сөзбен қатар "алкоголь" (араб, "эл-кугул") деген сөз .
Кұрамында гидроксил тобы бар органикалык косылыстар
Спирттер мен фенолдар.
Фенол молекуласында гидроксил тобы бензол сақинасымен тікелей байланысқан (С6Н5 — ОН) және оған ерекше касиет береді.
Спирттер — молекуласындаеы бір немесе бірнеше сутек атомдары гидроксил тобына алмасқан көмірсутектердің туындылары.
Спирттердін жалпы формуласы: R(OH)х.
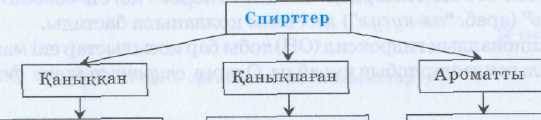
Спирттердің жіктелуі. Спирттерді жіктеудің бірнеше түрі бар (14, а, ә, б-сызбанұскалар):
1. Спирттер кұрамындағы гидроксил тобьшың санына байланысты біратомды және көпатомды болып бөлінеді.

СН3-ОН метил спирті(метанол) СН2-ОН - СН2-ОН
2. Гидроксил тобымен
байланыскан көмірсутек радикалына
сэйкес 
СН2- ОН
СН3 - СН2 - ОН СН2 = СН - ОН винил спирті этил спирті
3. Гидроксил тобымен байланыскан көміртек атомының таби-ғатына байланысты спирттер біріншілік, екіншілік және цшішиілік болып бөлінеді:
R - СН2 - ОН сн3 - сн2 - сн2 - он
біріншілік пропанол-1(біріншілік пропил спирті
R-CН —ОН СН3 - СН - СН3
| он
R
Қаньгқкан біратомды спирттерді бір сутек атомы гидроксил тобына алмасқан алкандардың туындылары ретінде карастыруға болады. Олардың жалпы формуласы: СяН2л+1ОН. Басқа органикалық косылыстар сиякты спирттерді де әр түрлі атаулармен атайды.
Атауы. ИЮПАК халыкаралық атаулар жүйесі бойынша спирт-терді көмірсутектердің атына ол деген жұрнақ косып атайды. Функ-ционалдық ОН тобы байланыскан ең үзын тізбек таңдап алынып, көміртек атомдарын гидроксил тобы жакьін орналаскдн жағынан бастап нөмірлейді:
сн3 - сн -сн — сн3
сн3 он
Изомерлері. Спирттердің изомерлері: а) көміртек каңқасының қүрылысына; ә) көмірсутек тізбегіндегі гидроксил тобының орнына байланысты жөне б) класаралық изомерлену болады. Гомологтык қатардың алғашкы екі мүшесінде метил СН3ОН және этил спирттер-ң С2Н5ОН изомерлері жоқ. Келесі мүшесі — пропил спиртінің С3Н7ОН үш изомері бар:
ІІІ. 4,5-жаттығу.
ІV § оқу. 8.1. 6,7- жаттығу. 157 бет.
V.Қазақстанда мұнай кен орындары қай жерлерде орналасқан?
Мұнай өндіру кезінде қандай зиянды жақтары бар?
Бекітемін:
Сыныбы: 11
Cабақтытың тақырыбы: Спирттердің қасиеттері.
Сабақтың мақсаты: 1.Спирттердің физикалық, химиялдық қасиеттері туралы түсініктер беру.
2. Спирттердің қасиеттерін сипатауда химиялық реакцияларды қатесіз жазу.
3. Салауатты өмір сүруге тәрбиелеу.
Сабақтың түрі: Шығармашылық.
Сабақтың пәнаралық байланысы: математика
Сабақтың әдісі: Сұрақ жауап,баяндау, түсіндіру, .
Сабақтың барысы: І. Ұйымдастыру бөлімі.
ІІ. Жаңа сабақты түсіндіру.
ІІІ. Бекіту
ІV. Үйге тапсырма беру.
V. Үй тапсырмасын тексеру.
ІІ. Спирттте С10-дейін сұйық, С11-ден бастан қатты Мол-қ массасының артуына бай-тықайнау температурасынан жоғары болады. Себебі спирттерде молекулааралык сутектік байланыс түзіледі. Спирт молекуласында электртерістігі жоғары оттек атомы сутектін электрондарын өзіне тартып, оларда ішінара теріс және оң зарядтар пайда болады:R —О —Н
Осы зарядтардың әсерінен оттек атомы мен спирттін екінші молекуласындағы гидроксилдің сутек атомының арасында сутектік байланыс түзіледі:
R — О... Н — О... Н — О...
Н R R
Кейбір біратомды спирттердің физикалық қасиегтері
|
Формула |
Атаулары |
Температурасы, °С |
|
|
балқу |
қайнау |
||
|
СН3ОН |
метил спирті (метанол) |
-97,8 |
64,7 |
|
с2н5он |
этил спирті (этанол) |
-117,3 |
78,4 |
|
снасн3сн2он |
н-пропил спирті (пропанол-1) |
-127,0 |
97,2 |
Химияльщ қасиеттері. Спирттердің химиялық цасиеттерін анъщтайтын гидроксил тобы және ол байланысқан радикалдардың
Спирттер (алканолдар) полюсті қосылыстар, көміртек пен оттек және оттек пен сутек атомдарының арасында екі полюсті байланысы бар: C+ ~* 0- жене О- <— Н+ О <— Н байланысының полюстігі С → О байланысының полюстігіне қарағанда жоғары..
Гидроксил тобындагы сутек арқылы жүретін реакциялар. Гидроксил тобындағы сутек атомы әлсіз қышкылдық қасиет көрсетеді, қозгалғыш келеді, орынбасу реакциясына түседі. Сутектің қозғалғыш болу себебі, оттектің электр-терістігі жоғары болғандықтан, оттек электрон тығыздығын өзіне қарай тартады, осыдан О—Н байланысы полюстенеді: R — О <— Н.
1. Спирттің гидроксил тобындагы сутек атомыпың орнын бел-сенді металдар баса алады:
2R — OH + 2Na -> 2R — ONa + H2t
Этанол натриймен әрекеттескенде, натрий этилаты мен сутек түзіледі:
2Na +2С2НЭОН→2 C2H5ONa+ Н2↑
натрий этилаты
Спирттің мүндай металл туындыларын алкоголяттар деп атайды. Алкоголяттар кдтты заттар, гидролизге оңай үшырайды:
C2H5ONa+H — ОН -» C2H5OH + NaOH
Этил спиртінің қышқылдығы судан төмен, ацетиленнен 1010 еседей жоғары. Сумен салыстырғанда, спирттердің қышқыпдық қасиеті әлсіз, әсіресе екіншілік, содан кейін үшіншілік спирттерде төмен болады. Үшіншілік спирттердің қышқылдығының төмен болатын себебі, алкил топтарының оң индуктивті эффектіне байланысты сольваттануға кедергі жасайды:
сн3
СН, -> С→ О <- Н үшіншілік бутил спирті
сн3
Сонымен спирттерді қышқылдық қасиеттеріне байланысты, яғни сутек атомын протон түрінде бөліп жіберетін қатарын былай орнапастыруға болады: біріншілік > екіншіпік > үшіншілік.
Егер радикапға электронакцепторлы топ енгізсе, ондә спирттің қышқылдығы артады. Мысалы, СІ—СН2—СН2ОН, бұл спиртте хлордың электрондарды тартуынан спирттің қышқылдығы күшейеді.
Органикалық қосылыстардың қышқылдығы мына қатар бойынша өзгереді:
Н2О > R - ОН > СН = СН > NH3 > CH2 = CH2 > R – Н
2. Этерификация ОН тобының орнын карб.қыш-ғы
с2н5он + ноос - сн3 → с2н5О - ОС — СН3+ н2о
сірке қышңылынын этил эфирі (этилацетат)
Гидроксил тобында жцрепин реакциялар.С—ОН байланысының үзілуі арқылы
3. Спирттер галогенсутектермен әрекеттеседі
Н2SO4
R - ОН + НВг → R — Вг+ н2о
4. Дегидратация реакциялары. Спирттерге су тарткыш заттар (концентрлі күкірт кышкылы, фосфор кышкылы жене т.б.)
4, а. Егер дегидратация реакциясын төменірек температурада жүргізсе, онда реакция молекулааралық өтеді де, жай эфир түзіледі:
н2sо4,
С2Н5 - ОН + НО - С3Н5→ С2Н5 - О - — С2Н5 +н2о диэтил эфирі
4, ә. Жоғарырак температурада t > 140"С дегидратациялағанда, реакция молекула ішінде отеді, нәтижесінде, алкен түзіледі:
н2sо4,t
СН3-СН2ОН → СН2=СН2+Н2О
Үшіншілік, екіншілік спирттер суды жеңіл бөледі. Мысалы:
сн3сн2сн3снсн3→ СН3СН2СН = СНСН3+ Н2О пентен-2
|
ОН
Зайцев ережесі бойынша мүндай спирттерде сутек атомы сутегі аз көміртек атомынан бөлінеді.
5. Тотыгу реакциялары. Тотықтыртыштардың әсерінен (СиО, хром-ды коспа К2Сг207 + H2SO4) біріншілік спирттер альдегидке дейін тотығады:
[О]
СН3СН2ОН→ СН3 - С = 0 сірке альдегиді
этил спирті|
Н
ал екіншілік спирттер тотыкканда, кетонға айналады:
сн3 - сн – сн3 [01 сн3 - со - сн3 ацетон (пропанон)
OH
изопропил спирті
6. Мыс (II) оксидімен тотыгып, альдегид тузуі біріншілік спирт-тердін сапалық реакциясы;
сн3- СН2ОН + СuО →сн3-сон+ н2о+Сu қара түсті мыс (II) оксиді тотықсызданып, қызгылт түсті мыс түзіледі жөне альдегидтің өткір иісі сезіледі.
Егер біріншілік спирттерді концентрлі азот кышқылымен немесе калий перманганатының сілтілік ерітіндісімен тотықтырса, ол карбон қышкылына айналады:
RCH2OH
KM"°''OH),RCOOH
7.. Этанол кегілдір жалынмен жанады:
С2Н5ОН + ЗО2 -> 2СО2 + ЗН2О + Q
Қолданывлуы: Спирттерді мотор отыны ретінде колданғанда осы реакцияны пайдаланады.
Спирттердің жеке өкілдері және олардың қолданылуы.
Метил спирті (метанол). СН3ОН — түссіз сүйықтық, спиртке тән иісі бар. Қайнау температурасы 64,7С Оны жоғары температурада катализатор катысында коміртек (IV) оксиді мен сутекті әрекеттестіріп а лады:
со2 + зн2 →сн3он + н2о
Метанолды өнеркөсіпте су газьшан синтездеп алады:
СО
+ 2Н2 Cu'ZnO'P'S СН3ОН
Бастапкы кезде метил спиртін ағашты құрғақ айдау арқылы алған, "ағаш спирті" деген атау содан шыккан.
Метанол өндірісте формальдегид, полимерлер, бояғыш заттар, фармацевтік препараттар алу үшін, бояулар мен лактарды ерітетін еріткіш ретінде және т.б. заттар алуда кең түрде қолданылады. Метил спиртімен жұмыс істегенде, оның өте улы екенін үмытпау керек. Бірнеше грамынан адам сокыр болады, одан көбірек болса, уланып өледі.
Этилспирті (этанол). С.,Н5ОН — езіне тән иісі бар түссіз сүйықтық. Қайнау температурасы — 78,3°С. Сумен барлық мөлшерде араласады. Егер спирттің күрамында 4—4,5% су болса, оны ректификат,ал сусыз спиртті абсолютті спирт дейді. Сусыз спиртті су тартқыш заттар (CaO, CuSO4) қосып қайнатып алады. Этил спиртін әр түрлі жолдармен алады. Соның бірі — глюкозадан (жүзім канты) ашытқы катысында мына жалпы реакция бойынша алады:
С6Н12О6→ 2С2Н5ОН+ 2СО2
Мұндай жолмен алынған спирт таза болады, тамак өнеркөсібінде және медицинада пайдаланылады. Целлюлозаны гидролиздеп алын-ған спиртті гидролиз спирті деп атайды:(С6Н10О5)п + пН2О -> 2СО2
Бұл әдіс өте тиімді, себебі тамақ өнімдері, картоп, бидай пайдаланбайды. Бірақ гидролиз спиртінде басқа қосымша өнімдер болады, соның бірі — метанол, сондықтан мұндай спирт кебіне техникада колданылады, тамақ өнімдері үшін пайдалануға болмайды.Синтездік жолмен этил спиртін этиленді гидратациялап алады.
Этанол дәрі-дәрмек жасауда, зарарсыздандырғыш зат ретінде медицинада пайдаланылады. Этил спирті химия өндірісінде сірке кьішкылын, бояу, синтездік каучук, диэтил эфирін және т.б. заттар алуда қолданылады. Ен арзан еріткіштердің бірі этил спирті адам организміне есірткілік эсер етеді. Спирт мига эсер етіп, жүйке клеткаларын уландырады. Осыдан адамнын ақыл-ойы, сөйлеу, ойлау қабілеттері, кимыл үйлесімділігі бұзылады. Спиртті ішімдіктер ішкен адамның мінез-кұлкында желөкпелік, әделсіздік, дөрекілік пайда болып, оны айналасындағыларға жеккөрінішті етеді.
ІІІ. № 10,12 – жаттығу 170 бет
V § оқу. 3.2 17,18- жаттығу. Тапсырма жинағы 93 бет.
Бекітемін:
Сыныбы:
Cабақтытың тақырыбы: Көп атомды спирттер..
Сабақтың мақсаты: 1. Көп атомды спирттердің физикалық,химиялдық қасиеттері және қолданылуы туралы түсініктер беру.
2. Спирттедің қаиеттерін ғылыми тұрғыда негіздей алу..
3. Еңбекке мамандық таңдауға тәрбиелеу.
Сабақтың көрнекілігі: кесте, реавтивтер.
Сабақтың пәнаралық байланысы: математика
Сабақтың әдісі: Сұрақ жауап,баяндау, түсіндіру, .
Сабақтың барысы: І. Ұйымдастыру бөлімі.
ІІ. Жаңа сабақты түсіндіру.
ІІІ. Бекіту
ІV. Үйге тапсырма беру.
V. Үй тапсырмасын тексеру
Диолдар,триолдар: этиленгликопь; глицерин.
Көп атомды спирттер көмірсутектердің құрамында бірнеше гидроксил тобы бар туындылары. Көпатомды спирттерге этилен-гликоль С2Н4(ОН)2, глицерин С3Н5 (ОН)3, ксилит С5Н7(ОН)5 сорбит C6H8 (OH)6, т.б. жатады.
Екі гидроксил тобы бар спирттерді гликольдер немесе алкандиолдар деп атайды. Жалпы формуласы: Cn H2n(OH)2.
Аталуы. Х.а. атаулар жүйесі бойынша сәйкес қаныққан көмірсутек атына диол немесе триол жұрнағын қосып, гидроксил тобы байланысып тұрған көміртек атомының немірі корсетіледі:сн2-сн2 сн3 -сн – сн2 сн2 - сн - сн2
| | | | | | |
он он он он он он он
этандиол пропандиол-1,2 пропантриол-1,2,
(этиленгликоль) (глицерин)
Алу әдістері.. Мысалы, екіатомды спирттерді көмірсутектердің дигалогентуындыларын гидролиздеп алады:
сн2 –СІ сн2 –ОН
| + Н2О → | +2НСІ
сн2 -СІ сн2 —ОН
Глицеринді 1,2,3-трихлорпропанды гидролиздеп алуға болады. 2. Этиленгликольді этилен к\с тотықтырып алады.
3. Этиленгликольді этилен оксидін гидратациялап алады:
4. Глицеринді өсімдік немесе жануар майларынан сілті қатысындә гидролиздеп алады:
Көпатомды спирттердің химиялық қасиеттері.
1. Көпатомды спирттер химиялық қасиеттері біратомды спирттерге ұқсас. Олармен белсенді металдар әрекеттесіп, гидроксил тобындағы сутекті ығыстырады, галогенсутектермен орынбасу реакциясына түседі, спирттермен әрекеттесіп, жай эфирлер, карбон қышкылдарымен әрекеттесіп, күрделі эфирлер түзіледі. Реакцияға бір гидроксил тобы:немесе бірнеше гидроксил топтары түсуі мүмкін:
СН2ОН CH2ONa
| +2Na→ |
сн2он CH2ONa
Глицериннің кышқылдығы алканолдар мен гликольден жоғары.
2. Глицераттар тузілуі. Глицериндегі гидроксил тобының сутек атомдары сілтілік металдарға жене ауыр металдардың (Fe, Cu, Ba) гидроксидтеріндегі металдарға оңай алмаса алады. Мысалы, глицерин мыс (П) гидроксидімен өрекеттесіп, ашьщ көк түсті ерітінді түзеді:
СН2ОН СН2 - О - Н О - СН2
2СНОН + Си(ОН)2 → СН - О - Сu <- О - СН +2Н2О
СН2ОН СН2 — ОН |
мыс (II) глицераты он - сн2
Бұл көпатомды спирттердің сапалық реакциясы.
3.Гидроксил тобын галогенмен алмастыру. Гликольдер хлорсутекпен әрекеттесіп, дихлорэтан түзеді:этиленхлоргидрин
4. Көпатомды спирттер алканолдармен әрекеттесіп, жай эфир тузеді:
5. Көпатомды спирттер минералды және органикалық қышқылдармен әрекеттесіп, күрделі эфирлер түзеді: нитроглицерин (глицериннің тринитраты)
Нитроглицерин — төттілеу дәмі бар ауыр майлы сұйықтық. Сілкудің және қыздырудың әсерінен оңай қопарылады. Қопарылғыш заттар жасауға колданылады.
Жеке өкілдері және олардың қолданылуы. Этиленгликолъ СН2ОН — СН2ОН — түссіз, тәтті коймалжың зат. Екіатомды спирт-тердің ішіндегі маңыздысы. Қайнау температурасы біратомды спирттердін кайнау температурасынан едәуір жоғары. 197,6°С, тығыздығы d410 = 1,13, сумен кез келген мөлшерде араласады. Сусыз гликоль су тартқыш келеді. Әр түрлі бейорганикалық тотыктыргыштардың әсерінен гликоль оңай тотығады. Кышкыл қосып қыздырса, түйык эфир түзіледі, күшті кьгшкьіддардьщ әсерінен қайта топтасады. Орг. қышқылдармен және олардың туындыларымен күрделі эфир түзеді. Этиленгликольді антифриз дайындау үшін пайдаланады. Этилен-гликольдің судағы 36%-тік ерітіндісі -20" С-та, 66%-тік ерітіндісі -60"С-та қатады. Этиленгликольді типографияда және косметикалык препараттар дайындауда колданады.
Глицерин СН2ОН — СНОН — СН2ОН — тәтті дөмі бар түссіз, қоймалжың сұйықтыкқ. Суды жақсы сіңіретін, гигроскопиялық зат. Сумен кез келген мөлшерде араласады. Атмосфералык қысымда 290°С-та кайнап, ыдырай бастайды, сондьщтан оны белгілі бір кысымда айдайды. Глицеринді өнеркәсіпте пропиленнен алады. Көп мөлшерде химия жөне тамақ өнеркәсібінде колданылады. Глицерин гигроскопиялык зат болғандықтан, теріні жұмсартатын қасиетіне байланысты парфюмерияда, былғары ө\к пайдаланады. Сонымен катар глицерин копарылғыш заттар және дәрі-дәрмектер ендіруде медицинада колданылады. Дикарбон қышкылдары және олардың туындыларымен глицеринді әрекеттестіріп, полимерлі қосылыс — полиэфир алады.
ІІІ. № 5,6 – жаттығу 173 бет
ІV. 1.Метанолдың физикалык қасиеттері мен адам организміне физиологиялык әсері туралы айтыңдар.
2. Этанолдын физикалык касиеттері мен адам организміне әсері туралы не білесіңдер? .
3. Этил спиртіндегі сутектік байланыс калай түзіледі?
4. Пропанол тольщ тотыкканда (жанғанда) не түзіледі? Жану реакциясының теңдеуін .
5. Этанолдан сірке альдегидін калай алуға болады? Сәйкес реакция теңдеулерін жаз.
4. Спирттердің реакцияға түсу қабілетін қалай түсіндіруге болады?
V § 3.4. оқу 17,18- жаттығу. Тапсырма жинағы 93 бет.
Бекітемін:
Сыныбы: 11-сынып.
Cабақтытың тақырыбы: Фенолдар
Сабақтың мақсаты: 1. Оқушыларға фенолдардың құрьпысы, аталуы, изомериясы, алынуы, химиялык қасиеттері. колданьпуы жөнінде түсінік беру.
2.Оқушылардың ой-өрісін дамыты отырып,оқу материалдарын меңгерту қабілетін дамыту.
![]() Тәрбиелік: Қоршаған ортаны қорғауға
тәрбиелеу.
Тәрбиелік: Қоршаған ортаны қорғауға
тәрбиелеу.
Сабақтың көрнекілігі: Сызба -нұсқалар
Сабақтың пәнаралық байланысы: Физика,
Сабақтың әдісі: .химиялық реакцияларды мысал келтіре отырып түсіндіру
Сабақтың барысы: І. Ұйымдастыру бөлімі.
ІІ. Жаңа сабақты түсіндіру.
ІІІ. Бекіту.
ІV. Үй тапсырмасын сұрау .Тест.
V. Үйге тапсырма
ІІ. Фенолдар- бензол сақинасындағы бір н/е бірнеше сутек атомдарының орнын ОН басқан ароматты көмірсутектердің туындылары.
С 6Н5ОН
ОН
6Н5ОН
ОН
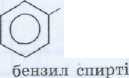
Ароматты көмірсутектердің бүйір тізбектеріндегі сутек атом-дарының орнын гидроксотоп басқан өнімдер ароматты спирттер деп аталады:

сн2сн2он
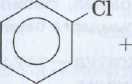
А![]() лынуы. Фенолды көбіне тас көмір
шайырын өндеу арқылы алады. Сондай-ак. ароматты көмірсутектерінің
галогентуындыларын сілтімен әрекеттестіріп те
алады:
лынуы. Фенолды көбіне тас көмір
шайырын өндеу арқылы алады. Сондай-ак. ароматты көмірсутектерінің
галогентуындыларын сілтімен әрекеттестіріп те
алады:
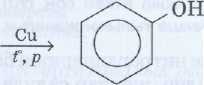 NaOH ерт.
+NaCl
NaOH ерт.
+NaCl
хлорбензол фенол
Ө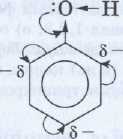 ндірісте
бастапқы шикізаттар ретінде бензол мен пропиленді
пайдаланып, кумолъді
әдіспен фенол алу іске
асырылған.Физикалық қасиеттері. Фенол — түссіз кристалдық зат.
43'С-та балқиды. Ауада ашнық қалғанда тотығатындыктан, қызғылт
түсті болады. Бөлме температурасында аздап қана ериді, ал
60°С-тан жогары кыздырғанда, суда шексіз ериді. Фенол — улы зат,
теріні күйдіреді. Ерітіндісі антисептик ретінде
колданылады.
ндірісте
бастапқы шикізаттар ретінде бензол мен пропиленді
пайдаланып, кумолъді
әдіспен фенол алу іске
асырылған.Физикалық қасиеттері. Фенол — түссіз кристалдық зат.
43'С-та балқиды. Ауада ашнық қалғанда тотығатындыктан, қызғылт
түсті болады. Бөлме температурасында аздап қана ериді, ал
60°С-тан жогары кыздырғанда, суда шексіз ериді. Фенол — улы зат,
теріні күйдіреді. Ерітіндісі антисептик ретінде
колданылады.
Химиялык қасиеттері. Фенол молекуласьшдагы атомдар бір-біріне өзара эсер ететіндіктен, полярлы қосылыс болады:
Молекуладағы гидроксотоптың оттек атомының бөліспеген электрон жұптары ығысуы әсерінен сақинадағы Пи-электрондар жүйесінің біркелкілігі бұзылып, сақинаның үш жерінде (2,4,6) электрон тығыздығы артады. Сондыктан өз кезегінде гидроксотоптагы сутек атомы козғалғыш болады. Бұл жағдай фенолдың судағы ерітшдісінде кышкыл сиякты диссоциациялануына себеп болады. Сол себепті, фенолдың 1 %-тік ерітіндісін карбол қышцылы деп атайды. Диссоциациялап6-
-
 ОН
ОН
+
↔ + н+
С6Н5ОН+2К→ 2 С6Н5ОК+Н2↑
С6Н5ОН+ NaOH→ С6Н5О Na+ Н2О
С6Н5О Na+СО2+ Н2О→ С6Н5ОН+ NaНСО3
Фенол молекуласының полярлы болуына байланысты (жоғарыда айтылған) орынбасу реакциялары өте жеңіл жүреді екен.
С6Н5ОН+3Вr2→ С6Н2 Вr3ОН↓+3НВr 2,4,6-трибромфенол ақ тұнба
Фенол+ҒеСІ3- сапалық реакция күлгін түсті комплексті қосылыс түзіледі.
ІІІ, Тест.
1. Фенолдын формуласы:
А) С6Н18ОН B) С6Н5СН2 ОН C) С6Н11ОН D) C6Н5OH
2. Фенол дегеніміз:
A) өзіне тән иісі бар жене суда қиын еритін тұткыр зат;
B) суда жақсы еритін, иісі жок, кристалдық зат;
C) өзіне тән иісі бар, ыстык суда жақсы еритін, улы кристалдык зат;
D) суық суда нашар еритін, ыстык суда жақсы еритін, иісі жоқ кристалдық зат.
3. Пикрин кышкылы:
A) C6H5-COOH B) CfiH5—ОН C) С6Н5Вг3-ОН D) С6Н2 (NO)3-ОН
4. Фенолдын сулы ерітіндісін глицериннің сулы ерітіндісінен ажыратуға болатын реактив:
A) Na В) СиО С) FeCL D) CH2СO0H
5. Күшті антисептик ретінде колданылатын зат:
A) этанол; B) диэтил эфирі; С) фенол; D) нитроглицерин.
6. Өндіріс қалдыктарының құрамында болып, қоршаған ортаға зиянды әсерін тигізетін зат:
A) этанол; B) диэтил эфирі; С) фенол; D) нитроглицерин.
ІV. Үйге § 3.5 оқу. 10-12жат 89 бет.
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Спирттер, құрамы мен жіктелуі
Сыныбы: 11
Cабақтытың тақырыбы: Спирттер, құрамы мен жіктелуі
Сабақтың мақсаты: 1. Спирттердің формуласы гомологтық қатары, изомер түзілуі туралы түсініктер беру.
2. Спирттерді атау және изомерлерін жазу.
Сабақтың түрі: ұжымдық ойлау.
Сабақтың әдісі: Сұрақ жауап, баяндау, кітаппен жұмыс. .
Сабақтың барысы: І. Ұйымдастыру бөлімі.
ІІ. Жаңа сабақты түсіндіру.
ІІІ. Бекіту
ІV. Үйге тапсырма беру.
ІІ. СПИРТТЕР
Спирттер мен фенолдар. Функционалдық топ (- ОН).
Спирттердің жіктелуі:біріншілік;екіншілік;үшіншілік;
біратомды;көпатомды.
"Спирт" сөзі латынның "шараптың рухы" деген сөзінен шыққан көрінеді. этил спирті формуласы — С2Н5ОН. Жүзімнің, қанттың, крахмалдың ферменттік ашуы нәтижесінде түзілетін бұл затты тұрмыста жай ғана спирт деп атайды. Ал XVIII гасырдан бастап "спирт" деген сөзбен қатар "алкоголь" (араб, "эл-кугул") деген сөз .
Кұрамында гидроксил тобы бар органикалык косылыстар
Спирттер мен фенолдар.
Фенол молекуласында гидроксил тобы бензол сақинасымен тікелей байланысқан (С6Н5 — ОН) және оған ерекше касиет береді.
Спирттер — молекуласындаеы бір немесе бірнеше сутек атомдары гидроксил тобына алмасқан көмірсутектердің туындылары.
Спирттердін жалпы формуласы: R(OH)х.
Спирттердің жіктелуі. Спирттерді жіктеудің бірнеше түрі бар (14, а, ә, б-сызбанұскалар):
1. Спирттер кұрамындағы гидроксил тобьшың санына байланысты біратомды және көпатомды болып бөлінеді.

СН3-ОН метил спирті(метанол) СН2-ОН - СН2-ОН
2. Гидроксил тобымен
байланыскан көмірсутек радикалына
сэйкес 


СН2- ОН
СН3 - СН2 - ОН СН2 = СН - ОН винил спирті этил спирті
3. Гидроксил тобымен байланыскан көміртек атомының таби-ғатына байланысты спирттер біріншілік, екіншілік және цшішиілік болып бөлінеді:
R - СН2 - ОН сн3 - сн2 - сн2 - он
біріншілік пропанол-1(біріншілік пропил спирті
R-CН —ОН СН3 - СН - СН3
| он
R
Қаньгқкан біратомды спирттерді бір сутек атомы гидроксил тобына алмасқан алкандардың туындылары ретінде карастыруға болады. Олардың жалпы формуласы: СяН2л+1ОН. Басқа органикалық косылыстар сиякты спирттерді де әр түрлі атаулармен атайды.
Атауы. ИЮПАК халыкаралық атаулар жүйесі бойынша спирт-терді көмірсутектердің атына ол деген жұрнақ косып атайды. Функ-ционалдық ОН тобы байланыскан ең үзын тізбек таңдап алынып, көміртек атомдарын гидроксил тобы жакьін орналаскдн жағынан бастап нөмірлейді:
сн3 - сн -сн — сн3
сн3 он
Изомерлері. Спирттердің изомерлері: а) көміртек каңқасының қүрылысына; ә) көмірсутек тізбегіндегі гидроксил тобының орнына байланысты жөне б) класаралық изомерлену болады. Гомологтык қатардың алғашкы екі мүшесінде метил СН3ОН және этил спирттер-ң С2Н5ОН изомерлері жоқ. Келесі мүшесі — пропил спиртінің С3Н7ОН үш изомері бар:
ІІІ. 4,5-жаттығу.
ІV § оқу. 8.1. 6,7- жаттығу. 157 бет.
V.Қазақстанда мұнай кен орындары қай жерлерде орналасқан?
Мұнай өндіру кезінде қандай зиянды жақтары бар?
Бекітемін:
Сыныбы: 11
Cабақтытың тақырыбы: Спирттердің қасиеттері.
Сабақтың мақсаты: 1.Спирттердің физикалық, химиялдық қасиеттері туралы түсініктер беру.
2. Спирттердің қасиеттерін сипатауда химиялық реакцияларды қатесіз жазу.
3. Салауатты өмір сүруге тәрбиелеу.
Сабақтың түрі: Шығармашылық.
Сабақтың пәнаралық байланысы: математика
Сабақтың әдісі: Сұрақ жауап,баяндау, түсіндіру, .
Сабақтың барысы: І. Ұйымдастыру бөлімі.
ІІ. Жаңа сабақты түсіндіру.
ІІІ. Бекіту
ІV. Үйге тапсырма беру.
V. Үй тапсырмасын тексеру.
ІІ. Спирттте С10-дейін сұйық, С11-ден бастан қатты Мол-қ массасының артуына бай-тықайнау температурасынан жоғары болады. Себебі спирттерде молекулааралык сутектік байланыс түзіледі. Спирт молекуласында электртерістігі жоғары оттек атомы сутектін электрондарын өзіне тартып, оларда ішінара теріс және оң зарядтар пайда болады:R —О —Н
Осы зарядтардың әсерінен оттек атомы мен спирттін екінші молекуласындағы гидроксилдің сутек атомының арасында сутектік байланыс түзіледі:
R — О... Н — О... Н — О...
Н R R
Кейбір біратомды спирттердің физикалық қасиегтері
|
Формула |
Атаулары |
Температурасы, °С |
|
|
балқу |
қайнау |
||
|
СН3ОН |
метил спирті (метанол) |
-97,8 |
64,7 |
|
с2н5он |
этил спирті (этанол) |
-117,3 |
78,4 |
|
снасн3сн2он |
н-пропил спирті (пропанол-1) |
-127,0 |
97,2 |
Химияльщ қасиеттері. Спирттердің химиялық цасиеттерін анъщтайтын гидроксил тобы және ол байланысқан радикалдардың
Спирттер (алканолдар) полюсті қосылыстар, көміртек пен оттек және оттек пен сутек атомдарының арасында екі полюсті байланысы бар: C+ ~* 0- жене О- <— Н+ О <— Н байланысының полюстігі С → О байланысының полюстігіне қарағанда жоғары..
Гидроксил тобындагы сутек арқылы жүретін реакциялар. Гидроксил тобындағы сутек атомы әлсіз қышкылдық қасиет көрсетеді, қозгалғыш келеді, орынбасу реакциясына түседі. Сутектің қозғалғыш болу себебі, оттектің электр-терістігі жоғары болғандықтан, оттек электрон тығыздығын өзіне қарай тартады, осыдан О—Н байланысы полюстенеді: R — О <— Н.
1. Спирттің гидроксил тобындагы сутек атомыпың орнын бел-сенді металдар баса алады:
2R — OH + 2Na -> 2R — ONa + H2t
Этанол натриймен әрекеттескенде, натрий этилаты мен сутек түзіледі:
2Na +2С2НЭОН→2 C2H5ONa+ Н2↑
натрий этилаты
Спирттің мүндай металл туындыларын алкоголяттар деп атайды. Алкоголяттар кдтты заттар, гидролизге оңай үшырайды:
C2H5ONa+H — ОН -» C2H5OH + NaOH
Этил спиртінің қышқылдығы судан төмен, ацетиленнен 1010 еседей жоғары. Сумен салыстырғанда, спирттердің қышқыпдық қасиеті әлсіз, әсіресе екіншілік, содан кейін үшіншілік спирттерде төмен болады. Үшіншілік спирттердің қышқылдығының төмен болатын себебі, алкил топтарының оң индуктивті эффектіне байланысты сольваттануға кедергі жасайды:
сн3
СН, -> С→ О <- Н үшіншілік бутил спирті
сн3
Сонымен спирттерді қышқылдық қасиеттеріне байланысты, яғни сутек атомын протон түрінде бөліп жіберетін қатарын былай орнапастыруға болады: біріншілік > екіншіпік > үшіншілік.
Егер радикапға электронакцепторлы топ енгізсе, ондә спирттің қышқылдығы артады. Мысалы, СІ—СН2—СН2ОН, бұл спиртте хлордың электрондарды тартуынан спирттің қышқылдығы күшейеді.
Органикалық қосылыстардың қышқылдығы мына қатар бойынша өзгереді:
Н2О > R - ОН > СН = СН > NH3 > CH2 = CH2 > R – Н
2. Этерификация ОН тобының орнын карб.қыш-ғы
с2н5он + ноос - сн3 → с2н5О - ОС — СН3+ н2о
сірке қышңылынын этил эфирі (этилацетат)
Гидроксил тобында жцрепин реакциялар.С—ОН байланысының үзілуі арқылы
3. Спирттер галогенсутектермен әрекеттеседі
Н2SO4
R - ОН + НВг → R — Вг+ н2о
4. Дегидратация реакциялары. Спирттерге су тарткыш заттар (концентрлі күкірт кышкылы, фосфор кышкылы жене т.б.)
4, а. Егер дегидратация реакциясын төменірек температурада жүргізсе, онда реакция молекулааралық өтеді де, жай эфир түзіледі:
н2sо4,
С2Н5 - ОН + НО - С3Н5→ С2Н5 - О - — С2Н5 +н2о диэтил эфирі
4, ә. Жоғарырак температурада t > 140"С дегидратациялағанда, реакция молекула ішінде отеді, нәтижесінде, алкен түзіледі:
н2sо4,t
СН3-СН2ОН → СН2=СН2+Н2О
Үшіншілік, екіншілік спирттер суды жеңіл бөледі. Мысалы:
сн3сн2сн3снсн3→ СН3СН2СН = СНСН3+ Н2О пентен-2
|
ОН
Зайцев ережесі бойынша мүндай спирттерде сутек атомы сутегі аз көміртек атомынан бөлінеді.
5. Тотыгу реакциялары. Тотықтыртыштардың әсерінен (СиО, хром-ды коспа К2Сг207 + H2SO4) біріншілік спирттер альдегидке дейін тотығады:
[О]
СН3СН2ОН→ СН3 - С = 0 сірке альдегиді
этил спирті|
Н
ал екіншілік спирттер тотыкканда, кетонға айналады:
сн3 - сн – сн3 [01 сн3 - со - сн3 ацетон (пропанон)
OH
изопропил спирті
6. Мыс (II) оксидімен тотыгып, альдегид тузуі біріншілік спирт-тердін сапалық реакциясы;
сн3- СН2ОН + СuО →сн3-сон+ н2о+Сu қара түсті мыс (II) оксиді тотықсызданып, қызгылт түсті мыс түзіледі жөне альдегидтің өткір иісі сезіледі.
Егер біріншілік спирттерді концентрлі азот кышқылымен немесе калий перманганатының сілтілік ерітіндісімен тотықтырса, ол карбон қышкылына айналады:
RCH2OH
KM"°''OH),RCOOH
7.. Этанол кегілдір жалынмен жанады:
С2Н5ОН + ЗО2 -> 2СО2 + ЗН2О + Q
Қолданывлуы: Спирттерді мотор отыны ретінде колданғанда осы реакцияны пайдаланады.
Спирттердің жеке өкілдері және олардың қолданылуы.
Метил спирті (метанол). СН3ОН — түссіз сүйықтық, спиртке тән иісі бар. Қайнау температурасы 64,7С Оны жоғары температурада катализатор катысында коміртек (IV) оксиді мен сутекті әрекеттестіріп а лады:
со2 + зн2 →сн3он + н2о
Метанолды өнеркөсіпте су газьшан синтездеп алады:
СО
+ 2Н2 Cu'ZnO'P'S СН3ОН
Бастапкы кезде метил спиртін ағашты құрғақ айдау арқылы алған, "ағаш спирті" деген атау содан шыккан.
Метанол өндірісте формальдегид, полимерлер, бояғыш заттар, фармацевтік препараттар алу үшін, бояулар мен лактарды ерітетін еріткіш ретінде және т.б. заттар алуда кең түрде қолданылады. Метил спиртімен жұмыс істегенде, оның өте улы екенін үмытпау керек. Бірнеше грамынан адам сокыр болады, одан көбірек болса, уланып өледі.
Этилспирті (этанол). С.,Н5ОН — езіне тән иісі бар түссіз сүйықтық. Қайнау температурасы — 78,3°С. Сумен барлық мөлшерде араласады. Егер спирттің күрамында 4—4,5% су болса, оны ректификат,ал сусыз спиртті абсолютті спирт дейді. Сусыз спиртті су тартқыш заттар (CaO, CuSO4) қосып қайнатып алады. Этил спиртін әр түрлі жолдармен алады. Соның бірі — глюкозадан (жүзім канты) ашытқы катысында мына жалпы реакция бойынша алады:
С6Н12О6→ 2С2Н5ОН+ 2СО2
Мұндай жолмен алынған спирт таза болады, тамак өнеркөсібінде және медицинада пайдаланылады. Целлюлозаны гидролиздеп алын-ған спиртті гидролиз спирті деп атайды:(С6Н10О5)п + пН2О -> 2СО2
Бұл әдіс өте тиімді, себебі тамақ өнімдері, картоп, бидай пайдаланбайды. Бірақ гидролиз спиртінде басқа қосымша өнімдер болады, соның бірі — метанол, сондықтан мұндай спирт кебіне техникада колданылады, тамақ өнімдері үшін пайдалануға болмайды.Синтездік жолмен этил спиртін этиленді гидратациялап алады.
Этанол дәрі-дәрмек жасауда, зарарсыздандырғыш зат ретінде медицинада пайдаланылады. Этил спирті химия өндірісінде сірке кьішкылын, бояу, синтездік каучук, диэтил эфирін және т.б. заттар алуда қолданылады. Ен арзан еріткіштердің бірі этил спирті адам организміне есірткілік эсер етеді. Спирт мига эсер етіп, жүйке клеткаларын уландырады. Осыдан адамнын ақыл-ойы, сөйлеу, ойлау қабілеттері, кимыл үйлесімділігі бұзылады. Спиртті ішімдіктер ішкен адамның мінез-кұлкында желөкпелік, әделсіздік, дөрекілік пайда болып, оны айналасындағыларға жеккөрінішті етеді.
ІІІ. № 10,12 – жаттығу 170 бет
V § оқу. 3.2 17,18- жаттығу. Тапсырма жинағы 93 бет.
Бекітемін:
Сыныбы:
Cабақтытың тақырыбы: Көп атомды спирттер..
Сабақтың мақсаты: 1. Көп атомды спирттердің физикалық,химиялдық қасиеттері және қолданылуы туралы түсініктер беру.
2. Спирттедің қаиеттерін ғылыми тұрғыда негіздей алу..
3. Еңбекке мамандық таңдауға тәрбиелеу.
Сабақтың көрнекілігі: кесте, реавтивтер.
Сабақтың пәнаралық байланысы: математика
Сабақтың әдісі: Сұрақ жауап,баяндау, түсіндіру, .
Сабақтың барысы: І. Ұйымдастыру бөлімі.
ІІ. Жаңа сабақты түсіндіру.
ІІІ. Бекіту
ІV. Үйге тапсырма беру.
V. Үй тапсырмасын тексеру
Диолдар,триолдар: этиленгликопь; глицерин.
Көп атомды спирттер көмірсутектердің құрамында бірнеше гидроксил тобы бар туындылары. Көпатомды спирттерге этилен-гликоль С2Н4(ОН)2, глицерин С3Н5 (ОН)3, ксилит С5Н7(ОН)5 сорбит C6H8 (OH)6, т.б. жатады.
Екі гидроксил тобы бар спирттерді гликольдер немесе алкандиолдар деп атайды. Жалпы формуласы: Cn H2n(OH)2.
Аталуы. Х.а. атаулар жүйесі бойынша сәйкес қаныққан көмірсутек атына диол немесе триол жұрнағын қосып, гидроксил тобы байланысып тұрған көміртек атомының немірі корсетіледі:сн2-сн2 сн3 -сн – сн2 сн2 - сн - сн2
| | | | | | |
он он он он он он он
этандиол пропандиол-1,2 пропантриол-1,2,
(этиленгликоль) (глицерин)
Алу әдістері.. Мысалы, екіатомды спирттерді көмірсутектердің дигалогентуындыларын гидролиздеп алады:
сн2 –СІ сн2 –ОН
| + Н2О → | +2НСІ
сн2 -СІ сн2 —ОН
Глицеринді 1,2,3-трихлорпропанды гидролиздеп алуға болады. 2. Этиленгликольді этилен к\с тотықтырып алады.
3. Этиленгликольді этилен оксидін гидратациялап алады:
4. Глицеринді өсімдік немесе жануар майларынан сілті қатысындә гидролиздеп алады:
Көпатомды спирттердің химиялық қасиеттері.
1. Көпатомды спирттер химиялық қасиеттері біратомды спирттерге ұқсас. Олармен белсенді металдар әрекеттесіп, гидроксил тобындағы сутекті ығыстырады, галогенсутектермен орынбасу реакциясына түседі, спирттермен әрекеттесіп, жай эфирлер, карбон қышкылдарымен әрекеттесіп, күрделі эфирлер түзіледі. Реакцияға бір гидроксил тобы:немесе бірнеше гидроксил топтары түсуі мүмкін:
СН2ОН CH2ONa
| +2Na→ |
сн2он CH2ONa
Глицериннің кышқылдығы алканолдар мен гликольден жоғары.
2. Глицераттар тузілуі. Глицериндегі гидроксил тобының сутек атомдары сілтілік металдарға жене ауыр металдардың (Fe, Cu, Ba) гидроксидтеріндегі металдарға оңай алмаса алады. Мысалы, глицерин мыс (П) гидроксидімен өрекеттесіп, ашьщ көк түсті ерітінді түзеді:
СН2ОН СН2 - О - Н О - СН2
2СНОН + Си(ОН)2 → СН - О - Сu <- О - СН +2Н2О
СН2ОН СН2 — ОН |
мыс (II) глицераты он - сн2
Бұл көпатомды спирттердің сапалық реакциясы.
3.Гидроксил тобын галогенмен алмастыру. Гликольдер хлорсутекпен әрекеттесіп, дихлорэтан түзеді:этиленхлоргидрин
4. Көпатомды спирттер алканолдармен әрекеттесіп, жай эфир тузеді:
5. Көпатомды спирттер минералды және органикалық қышқылдармен әрекеттесіп, күрделі эфирлер түзеді: нитроглицерин (глицериннің тринитраты)
Нитроглицерин — төттілеу дәмі бар ауыр майлы сұйықтық. Сілкудің және қыздырудың әсерінен оңай қопарылады. Қопарылғыш заттар жасауға колданылады.
Жеке өкілдері және олардың қолданылуы. Этиленгликолъ СН2ОН — СН2ОН — түссіз, тәтті коймалжың зат. Екіатомды спирт-тердің ішіндегі маңыздысы. Қайнау температурасы біратомды спирттердін кайнау температурасынан едәуір жоғары. 197,6°С, тығыздығы d410 = 1,13, сумен кез келген мөлшерде араласады. Сусыз гликоль су тартқыш келеді. Әр түрлі бейорганикалық тотыктыргыштардың әсерінен гликоль оңай тотығады. Кышкыл қосып қыздырса, түйык эфир түзіледі, күшті кьгшкьіддардьщ әсерінен қайта топтасады. Орг. қышқылдармен және олардың туындыларымен күрделі эфир түзеді. Этиленгликольді антифриз дайындау үшін пайдаланады. Этилен-гликольдің судағы 36%-тік ерітіндісі -20" С-та, 66%-тік ерітіндісі -60"С-та қатады. Этиленгликольді типографияда және косметикалык препараттар дайындауда колданады.
Глицерин СН2ОН — СНОН — СН2ОН — тәтті дөмі бар түссіз, қоймалжың сұйықтыкқ. Суды жақсы сіңіретін, гигроскопиялық зат. Сумен кез келген мөлшерде араласады. Атмосфералык қысымда 290°С-та кайнап, ыдырай бастайды, сондьщтан оны белгілі бір кысымда айдайды. Глицеринді өнеркәсіпте пропиленнен алады. Көп мөлшерде химия жөне тамақ өнеркәсібінде колданылады. Глицерин гигроскопиялык зат болғандықтан, теріні жұмсартатын қасиетіне байланысты парфюмерияда, былғары ө\к пайдаланады. Сонымен катар глицерин копарылғыш заттар және дәрі-дәрмектер ендіруде медицинада колданылады. Дикарбон қышкылдары және олардың туындыларымен глицеринді әрекеттестіріп, полимерлі қосылыс — полиэфир алады.
ІІІ. № 5,6 – жаттығу 173 бет
ІV. 1.Метанолдың физикалык қасиеттері мен адам организміне физиологиялык әсері туралы айтыңдар.
2. Этанолдын физикалык касиеттері мен адам организміне әсері туралы не білесіңдер? .
3. Этил спиртіндегі сутектік байланыс калай түзіледі?
4. Пропанол тольщ тотыкканда (жанғанда) не түзіледі? Жану реакциясының теңдеуін .
5. Этанолдан сірке альдегидін калай алуға болады? Сәйкес реакция теңдеулерін жаз.
4. Спирттердің реакцияға түсу қабілетін қалай түсіндіруге болады?
V § 3.4. оқу 17,18- жаттығу. Тапсырма жинағы 93 бет.
Бекітемін:
Сыныбы: 11-сынып.
Cабақтытың тақырыбы: Фенолдар
Сабақтың мақсаты: 1. Оқушыларға фенолдардың құрьпысы, аталуы, изомериясы, алынуы, химиялык қасиеттері. колданьпуы жөнінде түсінік беру.
2.Оқушылардың ой-өрісін дамыты отырып,оқу материалдарын меңгерту қабілетін дамыту.
![]() Тәрбиелік: Қоршаған ортаны қорғауға
тәрбиелеу.
Тәрбиелік: Қоршаған ортаны қорғауға
тәрбиелеу.
Сабақтың көрнекілігі: Сызба -нұсқалар
Сабақтың пәнаралық байланысы: Физика,
Сабақтың әдісі: .химиялық реакцияларды мысал келтіре отырып түсіндіру
Сабақтың барысы: І. Ұйымдастыру бөлімі.
ІІ. Жаңа сабақты түсіндіру.
ІІІ. Бекіту.
ІV. Үй тапсырмасын сұрау .Тест.
V. Үйге тапсырма
ІІ. Фенолдар- бензол сақинасындағы бір н/е бірнеше сутек атомдарының орнын ОН басқан ароматты көмірсутектердің туындылары.
С 6Н5ОН
ОН
6Н5ОН
ОН
Ароматты көмірсутектердің бүйір тізбектеріндегі сутек атом-дарының орнын гидроксотоп басқан өнімдер ароматты спирттер деп аталады:

сн2сн2он
А![]() лынуы. Фенолды көбіне тас көмір
шайырын өндеу арқылы алады. Сондай-ак. ароматты көмірсутектерінің
галогентуындыларын сілтімен әрекеттестіріп те
алады:
лынуы. Фенолды көбіне тас көмір
шайырын өндеу арқылы алады. Сондай-ак. ароматты көмірсутектерінің
галогентуындыларын сілтімен әрекеттестіріп те
алады:

 NaOH ерт.
+NaCl
NaOH ерт.
+NaCl
хлорбензол фенол
Ө ндірісте
бастапқы шикізаттар ретінде бензол мен пропиленді
пайдаланып, кумолъді
әдіспен фенол алу іске
асырылған.Физикалық қасиеттері. Фенол — түссіз кристалдық зат.
43'С-та балқиды. Ауада ашнық қалғанда тотығатындыктан, қызғылт
түсті болады. Бөлме температурасында аздап қана ериді, ал
60°С-тан жогары кыздырғанда, суда шексіз ериді. Фенол — улы зат,
теріні күйдіреді. Ерітіндісі антисептик ретінде
колданылады.
ндірісте
бастапқы шикізаттар ретінде бензол мен пропиленді
пайдаланып, кумолъді
әдіспен фенол алу іске
асырылған.Физикалық қасиеттері. Фенол — түссіз кристалдық зат.
43'С-та балқиды. Ауада ашнық қалғанда тотығатындыктан, қызғылт
түсті болады. Бөлме температурасында аздап қана ериді, ал
60°С-тан жогары кыздырғанда, суда шексіз ериді. Фенол — улы зат,
теріні күйдіреді. Ерітіндісі антисептик ретінде
колданылады.
Химиялык қасиеттері. Фенол молекуласьшдагы атомдар бір-біріне өзара эсер ететіндіктен, полярлы қосылыс болады:
Молекуладағы гидроксотоптың оттек атомының бөліспеген электрон жұптары ығысуы әсерінен сақинадағы Пи-электрондар жүйесінің біркелкілігі бұзылып, сақинаның үш жерінде (2,4,6) электрон тығыздығы артады. Сондыктан өз кезегінде гидроксотоптагы сутек атомы козғалғыш болады. Бұл жағдай фенолдың судағы ерітшдісінде кышкыл сиякты диссоциациялануына себеп болады. Сол себепті, фенолдың 1 %-тік ерітіндісін карбол қышцылы деп атайды. Диссоциациялап6-
-
 ОН
ОН
+
↔ + н+
С6Н5ОН+2К→ 2 С6Н5ОК+Н2↑
С6Н5ОН+ NaOH→ С6Н5О Na+ Н2О
С6Н5О Na+СО2+ Н2О→ С6Н5ОН+ NaНСО3
Фенол молекуласының полярлы болуына байланысты (жоғарыда айтылған) орынбасу реакциялары өте жеңіл жүреді екен.
С6Н5ОН+3Вr2→ С6Н2 Вr3ОН↓+3НВr 2,4,6-трибромфенол ақ тұнба
Фенол+ҒеСІ3- сапалық реакция күлгін түсті комплексті қосылыс түзіледі.
ІІІ, Тест.
1. Фенолдын формуласы:
А) С6Н18ОН B) С6Н5СН2 ОН C) С6Н11ОН D) C6Н5OH
2. Фенол дегеніміз:
A) өзіне тән иісі бар жене суда қиын еритін тұткыр зат;
B) суда жақсы еритін, иісі жок, кристалдық зат;
C) өзіне тән иісі бар, ыстык суда жақсы еритін, улы кристалдык зат;
D) суық суда нашар еритін, ыстык суда жақсы еритін, иісі жоқ кристалдық зат.
3. Пикрин кышкылы:
A) C6H5-COOH B) CfiH5—ОН C) С6Н5Вг3-ОН D) С6Н2 (NO)3-ОН
4. Фенолдын сулы ерітіндісін глицериннің сулы ерітіндісінен ажыратуға болатын реактив:
A) Na В) СиО С) FeCL D) CH2СO0H
5. Күшті антисептик ретінде колданылатын зат:
A) этанол; B) диэтил эфирі; С) фенол; D) нитроглицерин.
6. Өндіріс қалдыктарының құрамында болып, қоршаған ортаға зиянды әсерін тигізетін зат:
A) этанол; B) диэтил эфирі; С) фенол; D) нитроглицерин.
ІV. Үйге § 3.5 оқу. 10-12жат 89 бет.

шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
