
10 «___» класс Фамилия имя:__________________________
Суммативное оценивание за разделы 10.3С Химическое равновесие
Задание.1
Большая часть получаемого в промышленности аммиака производится в процессе Габера
А)Напишите уравнение реакции процесса Габера
_____________________________________________________________________________
В)Заполните таблицу:Влияние изменения температуры и давления на выход аммиака.
|
Изменение условий |
Выход(увеличивается/уменшается) |
|
Повышение температуры |
|
|
Понижение температуры |
|
|
Повышение давления |
|
|
Понижение давления |
|
С)Объясните роль смещение химического равновесия для увеличения выхода аммиака.
__________________________________________________________________________________________________________________________________________________________
Задание.2
А) Показана обратимая реакция: 2NO2(г) ⇌N2O4 (г) Н=-58 кДж/моль Выберите верное утверждение о равновесной смеси NO2 и N2O4

в) Азот, водород и газообразный аммиак помещены внутри контейнера. Контейнер запечатывается. Через некоторое время наступает равновесие:
N2(r) + 3H2 (r) → 2NH3(r) Н= -92 кДж/моль
Какое утверждение описывает равновесие в этом контейнере?

Задание.3
а) При некоторой температуре равновесные концентрации в системе:
2SO2(г)+O2(г)⇌2SO3(г)
составляли: [SO₂] = 0,10 моль/л, [O₂] = 0,16 моль/л, [SO₃] = 0,08 моль/л.
Вычислите константу равновесия и исходные концентрации SO₂ и O₂.

Задание.4
а. Аммиак может быть получен при разложении карбоната аммония:
(NH4)2CO3(s)= 2NH3(g) + H₂O(g) + CO₂(g)
Реакция обратима и может достичь состояния равновесия.
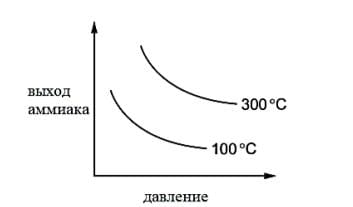
График показывает, как выход аммиака при равновесии изменяется с температурой и
Давлением
В. (а) Что понимается под термином химическое равновесие? Почему его называют динамическим?
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________
(b) Используя информацию из графика, объясните, является ли реакция эндотермической или экзотермической.
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________
(с) Установите и объясните влияние увеличения давления на выход аммиака в этой реакции.
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Суммативное оценивание за разделы 10.3С Химическое равновесие
10 «___» класс Фамилия имя:__________________________
Суммативное оценивание за разделы 10.3С Химическое равновесие
Задание.1
Большая часть получаемого в промышленности аммиака производится в процессе Габера
А)Напишите уравнение реакции процесса Габера
_____________________________________________________________________________
В)Заполните таблицу:Влияние изменения температуры и давления на выход аммиака.
|
Изменение условий |
Выход(увеличивается/уменшается) |
|
Повышение температуры |
|
|
Понижение температуры |
|
|
Повышение давления |
|
|
Понижение давления |
|
С)Объясните роль смещение химического равновесия для увеличения выхода аммиака.
__________________________________________________________________________________________________________________________________________________________
Задание.2
А) Показана обратимая реакция: 2NO2(г) ⇌N2O4 (г) Н=-58 кДж/моль Выберите верное утверждение о равновесной смеси NO2 и N2O4

в) Азот, водород и газообразный аммиак помещены внутри контейнера. Контейнер запечатывается. Через некоторое время наступает равновесие:
N2(r) + 3H2 (r) → 2NH3(r) Н= -92 кДж/моль
Какое утверждение описывает равновесие в этом контейнере?

Задание.3
а) При некоторой температуре равновесные концентрации в системе:
2SO2(г)+O2(г)⇌2SO3(г)
составляли: [SO₂] = 0,10 моль/л, [O₂] = 0,16 моль/л, [SO₃] = 0,08 моль/л.
Вычислите константу равновесия и исходные концентрации SO₂ и O₂.

Задание.4
а. Аммиак может быть получен при разложении карбоната аммония:
(NH4)2CO3(s)= 2NH3(g) + H₂O(g) + CO₂(g)
Реакция обратима и может достичь состояния равновесия.
График показывает, как выход аммиака при равновесии изменяется с температурой и
Давлением

В. (а) Что понимается под термином химическое равновесие? Почему его называют динамическим?
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________
(b) Используя информацию из графика, объясните, является ли реакция эндотермической или экзотермической.
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________
(с) Установите и объясните влияние увеличения давления на выход аммиака в этой реакции.
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________

шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
