
Химия
1-нұсқа
-
Атом-молекулалық ілімді ұсынған ғалым
А) Д.И.Менделеев
В) Э.Франкленд
С) Ж.Л.Пруст
D)* М.В.Ломоносов
Е) А.Лавуазье
2. Р-элемент болатын
А) Li
В) Mg
C) Sr
D)* Si
E) Rb
3. Жай заттардың тотығу дәрежелері
А) Атомдағы электрон санына тең
В) протон санына тең
С)* Нольге тең
D) Жұптаспаған электрон санына тең
Е) Валенттік электрон санына тең
4 .
Zn2+
+
2OH-
= Zn(OH)2 қысқартылған иондық
теңдеуіне сәйкес келетін
.
Zn2+
+
2OH-
= Zn(OH)2 қысқартылған иондық
теңдеуіне сәйкес келетін
молекулалық теңдеу
А)* Zn(NO3)2 + 2KOH= Zn(OH)2 + 2KNO3
В) ZnCI2 + K2S = ZnS + 2 KCI
С) ZnO + 2HNO3 = Zn(NO3)2 + H2O
D) ZnO + H2SO4 = ZnSO4 + H2O
E) ZnS + 2HCI = ZnCI2 + H2S
5. Сутек газын ашқан ғалым
А) А.Беккерель
В) Дж. Прустли
С)* Г.Кавендиш
D) Р.Бойль
Е) М.В.Ломоносов
6. Сумен әрекеттеспейтін оксид
А) Күкірт (ҮІ) оксиді
В) Фосфор (Ү) оксиді
С)* Кремний оксиді
D) Натрий оксиді
Е) Барий оксиді
7. Алюминийдің темір (ІІ) оксидімен реакциясы теңдеуінде
тотықсыздандырғыштың алдына қойылатын коэффициент
А) 1
В)* 2
С) 3
D) 4
Е) 5
8. Орыс ғалымы А.М.Бутлеров алғаш рет синтездеген зат
А) Мочевина
В) Май
С)* Қантты заттар
Д) Қымыздық қышқылы
Е) Сірке қышқылы
9. Полимерлер-
А) Жеке атомдардан тұрады
В) Иондардан тұрады
С)* макромолекуладан тұрады
D) Жеке молекулалардан тұрады
Е) Радикалдардан тұрады
10. Егер температураны 50 С-қа төмендеткенде, реакция жылдамдығының
(y =3) кемуі:
А) 3
В) 81
С) 27
D)* 243
Е) 9
11. Азот қышқылының 2 литр 20%-тік ерітіндісіндегі (p=1.6 г/мл) судың көлемі
А) 2,0л
В) 2,42л
С)*2,56л
D) 3,24л
Е) 2,81л
12. Құрамында 32 г мыс бар CuSO4 ·5H2O мыс купоросының массасы:
А)* 125г
В) 100г
С) 65г
D) 80г
Е) 44г
13. Құрамында 9,8г фосфор қышқылы және 12г кальций гидроксиді бар
ерітінділерді араластырғанда түзілетін тұнба массасы:
А)* 15,5г
В) 16,5г
С) 17,5г
D) 18,5г
Е) 20,5г
14. Кальций гидрокарботындағы ковалентті байланыстардың саны
А) 9
В) 4
С)* 10
D) 8
Е) 12
15. Концентрлі азот қышқылымен әрекеттеспейтін металл:
А) мыс
В) күміс
С)* хром
D) мырыш
Е) сынап
16. Домна пешінде жүретін реакциялардың бірі:
Fe2O3 +3CO → Fe + 3CO2
Осы теңдеу бойынша 32г тотықтырғыш пен әрекеттесетін
тотықсыздандырғыш мөлшері:
А) 2 моль
В) 0,4 моль
С)*0,6 моль
D) 3 моль
Е) 1 моль
17. 2,5г натриймен 2,3г этил спиртіне әсер еткенде сутектің (қ.ж.) көлемі:
А) 0,85 мл
В) 5,6 мл
С)* 560 мл
D) 0,65 мл
Е) 0,5 мл
18. Тығыздығы 0,8 г/мл 110 мл сірке қышқылының этил эфирін алу үшін қажет
сірке қышқылының массасы:
А) 44г
В) 40г
С)* 60г
D) 88г
Е) 30г
19. Өзгерістердің нәтижесінде түзілетін «А» затының аталуы:
C2H6 +Br2__ X1 +HOH X2 [O] X3 [O] A
А)* Сірке қышқылы
В) Бромды этил
С) Этанол
D) Ацетальдегид
Е) Сүт қышқылы
20. Сілтінің артық мөлшері қажет болатын стадия
2 AI(OH)3 4AI3+
AI 1 AI3+
3 [AI(OH)4] ____5____AI3+
A) 1
В)* 3
C) 5
D) 4
Е) 2
21. Хлор (І) оксиді мына қышқылдың ангидриді:
А) Хлор қышқылының
В)* Хлорлылау қышқылдың
С) Тұз қышқылының
D) Хлорлау қышқылдың
Е) Хлорлы қышқылдың
22. 500л пентанды дегидрлегенде алынған циклопентанды жағуға жұмсалған
оттектің (қ.ж.) көлемі:
А) 3360л
В) 3270л
С) 3460л
D)* 3750л
Е) 3520л
23. Құрамында көлемдік үлесі бойынша 44,8% этилен 32,8% метан бар этилен,
ацетилен және метаннан тұратын 5л қоспа қосып алатын бромның массасы:
А)* 32г
В) 20г
С) 48г.
D) 16г
Е) 30г
24. 34,2г сахароза гидролизденгенде алынған глюкоза спирттік ашығанда
түзілген этанолдың массасы:
А) 5,2г
В) 6,2г
С)* 9,2г
D) 8,2г
Е) 7,2г
25. Сутек бойынша тығыздығы 15,5- ке (қ.ж.) тең аминнің 5,6 литрін жағуға
жұмсалатын оттектің көлемі:
А) 11,2л
В) 22,4л
С)* 12,6л
D) 14,4л
Е) 16,8л
2-нұсқа
-
Химиялық құбылысқа жататыны:
А) шайқау
В)* крекингілеу
С) хромотографиялау
D) дистилдеу
Е) буландыру
2. Атомның электрон саны
А)* протон санына тең
В) салыстырмалы атомдық массаға тең
С) протон санынан көп
D) нейтрон санына тең
Е) нейтрон санынан аз
3. NaF – фтордың тотығу дәрежесі
А)* -1
В) -2
С) +2
D) +3
Е) +1
4. Электролиттік диссоциация дегеніміз:
А)* заттардың суда ерігенде немесе балқығанда иондарға ыдырау процесі
В) заттардың өз бетімен жеке молекулаларға ыдырауы
С) иондар және атомдар түзілу процесі
D) иондардың қосылып молекула түзу процесі
Е) электролиттердің жеке атомдарға ыдырауға процесі
5. Сутектің табиғи изотоптарының массалық сандары
А) 1
В) 1, 2
С)* 1, 2, 3
D) 2, 3
Е) 1, 3
6. Сілтіні зертханада алу әдісі:
А) негіз бен тұзды әрекеттестіру
В)* белсенді металды сумен әрекеттестіру
С) металды тұзбен әрекеттестіру
D) мыс (ІІ) оксидін сумен әрекеттестіру
Е) металл мен қышқылды әрекеттестіру
7. Сілтілік жер металдарға жатады:
А)* Mg
B) K
C) Na
D) Cs
E) Li
8. Органикалық заттың құрамына міндетті түрде кіретін элемент
А) кремний
В) азот
С) сутек
D)* көміртек
Е) оттек
9. Полимерлену реакциясы
А)* пH2C=CH2 → (-H2C- CH2-)n
B) H2C=CH2 + H2→CH3—CH3
C) H2C=CH2 +Cl2 →ClH2C-CH2Cl
D) H2C=CH2+ 3O2→ 2CO2-2H2O
E) H2C=CH2+ HCI→ CH3-CH2CI
10. Н2 + СІ2= 2HCI реакциядағы сутектің концентрациясын 4 есе азайтқанда
реакция жылдамдығы...
А) 8 есе артады
В) 2 есе артады
С) 2 есе кемиді
D)* 4 есе кемиді
Е) 8 есе кемиді
11. Натрий нитратының 450г 20%-ті ерітіндісіндегі судың массасы
А)* 360г
В) 418г
С) 370г
D) 402г
Е) 434г
12. Күкірт қышқылына тән емес қасиет:
А)* Тотықсыздандарғыш қасиет көрсетеді
В) Суда жақсы ериді
С) Концентрлі күкірт қышқылы күшті тотықтырғыш
D) Суға қосқанда жылу бөлінеді
Е) Ауыр май тәрізді сұйық зат
13. Қалыпты температурада концентрлі азот қышқылымен әрекеттеспейтін
металл:
А) Mg
B) Cu
C)* AI
D) K
E) Na
14. 5,6г көміртегі (ІІ) оксиді алатын көлем:\
А) 0,71л
В)* 4,48л
С) 2,24л
D) 5,6л
Е) 3,6л
15. Домна пешіне салуға дайындалған шахтаның құрамы:
А)* Руда, флюс, кокс
В) Кокс, кремний оксиді, флюс
С) Көмір, темір, кремний оксиді
D) Көмір, ізбес тас, темір
Е) Флюс, көмір, темір
16. Ерітіндіде темір (ІІІ) ионының бар екендігін анықтайтын реактивтер
А) NaOH, H2S
B) BaSO4, KCI
C) K3[Fe(CN)6], KCI
D)* KCNS, NaOH
E) KOH, NaCI
17. Іс жүзінде жүруі мүмкін реакция:
А) CH4 + Na →
B)* CH3OH + HCI→
C) CH3OH + NaBr→
D) CH3OH + Br2→
E) CH3OH + NaCI→
18. 0,8 моль пропан қышқылы 0,5 моль натриймен әрекеттескенде түзілетін
сутектің (қ.ж.) көлемі:
А) 89,6л
В) 11,2л
С)* 5,6л
D) 44,8л
Е) 22,4л
19. СaO +C→Х +Н2О С2Н2 +У С2Н2Вr2. Өзгерістер схемасындағы Х
және У заттары:
А) Х- Ca(OH)2, У- Br2
В) Х- CaCI2, У-HBr
С)* Х- CaC2, У- Br2
D) Х- Ca(OH)2, У- HBr
Е) Х- CaC2, У- HBr
20. Өзгерістер тізбегіндегі этаналь қатысатын стадия
Cu 1→ Cu(NO3)3 2→ Cu(OH)2 3→ Cu2O 4→Cu
А) 1
В)* 3
С) 1,4
D) 2
Е) 4
21. Реакция теңдеуіндегі барлық коэффициенттердің қосындысы
K2Cr2O7 + KJ + H2SO4 → Cr2(SO4)3 +J2+K2SO4 +H2O
А) 27
В)* 29
С) 23
D) 31
Е) 25
22. Зат құрамында 80% көміртегі бар, ал сутгеі бойынша салыстырмалы тығыздығы 15-ке тең. Көмірсутектің молекулалық формуласы
А) C2H5
B)* C2H6
C) C2H2
D) C2H4
E) C2H5OH
23. Нитрлеу реакциясы кезінде 78г бензолдан 98,4 г нитробензол алынды. Нитробензолдың шығымы (%-пен):
А) 40%
В) 70%
С)* 80%
D) 50%
Е) 60%
24. 16г метил спиртін толық жаққанда түзілетіндей газ алу үщін спирттік ашитын глюкозаның массасы:
А) 4,5г
В)* 45г
С) 4,6г
D) 47г
Е) 46г
25. Шығымы 92% болатын 42,8г анилин алынғанда жұмсалатын нитробензолдың массасы:
А) 58,8г
В) 57г
С)* 61,5г
D) 56,8г
Е) 57,8г
3 – нұсқа
1![]() . Cu+HgCl2
CuCl2+Hg теңдеулермен
өрнектелген реакция типі
. Cu+HgCl2
CuCl2+Hg теңдеулермен
өрнектелген реакция типі
А) алмасу
В) қосылу
C) айрылу
D) * орын басу
E) бейтараптану
2. S – орбаталдың сыйымдылығы
А) 1е
В) 5е
C) 2е
D) 4е
E) 3е
3. Берілген теңдеудің тотықтырғыш болатын зат
4![]() NH3+3O2
2N2+6H2O
NH3+3O2
2N2+6H2O
А) Азот
В) Күкірт
C) * Оттек
D)Аммиак
E) Сутек
4. Алюминий сульфаты ерітіндісінде лакмус индикаторының түсі
А) * қызыл
В) көк
C) таңқурай түсті
D) сары
E) түссіз
5. Күкірт оксиді (VI) қалыпты жғдайда
А) қатты зат
В) түссіз газ
C) сары түсті ұнтақ
D) * сұйықтық
E) қоңыр кристалдар
6. Кальций оксидін пайдаланатын жағдай
А) көмір қышқыл газын анықтау үшін
В) * сөндірірілген әкті алу үшін
C) мұнайды тазарту үшін
D) аккумуляторда қолдану үшін
E) бордосс қоспасын дайындау үшін
7. Судың кермектігін жою әдісі
А) Қайнату арқылы
В) Тұндыру арқылы
C) Тазартылған суды қосу арқылы
D) * Дистелдеу арқылы
E) Сүзу арқылы
8. Алкандар қатарына жататын көмірсутек
А) C8H14
В) * C10H22
C) C5H10
D) C6H12
E) C8H16
9. Химиялық полимерге жатпайды:
А) Полиэтилен
В) Полистирол
C) Капрон
D) * Белок
E) Лавсан
10. Осы реакцияда сутек концетрациясын арттыру тепе – теңдікті солға ығыстырады:
А) * Аммиакты жай заттарға айыру
В) Сутектің хлормен әрекеттсуі
C) Жай заттардан су буының түзілуі
D) Темір (II) оксидін сутекпен тотықсыздандырғанда
E) Жай заттардан аммиакты синтездеу
11. 100г кристалдық содадағы судың массалық үлесі (%)
А) 11
В) 89
C) *63
D) 37
E) 74
12. Массасы 442г күкіртсутектің моль саны:
А) 14
В) *13
C) 12
D) 11
E) 15
13. Азот қышқылы төмендегі затпен әрекеттескенде барлық қышқылдарға ортақ қасиет көрсетеді:
А) C
В) Cu
C) CO2
D) *BaCO3
E) CH4
14. 2000г кальций корбанаты ыдырағанда бөлінген көмірқышқыл газының қалыпты жағдайдағы көлемі:
А) *448л
В) 336л
C) 560л
D) 672л
E) 224л
15. 800г мыс (II) оксидін сутекпен тотықсыздандырғанда түзілетін мыстың массасы:
А) *640г
В) 6,4г
C) 320г
D) 32г
E) 64г
16. Гидролизденетін тұздар жұбы:
А) * FeCl2, CrSO4
В) MgSO4, K2SO4
C) FeCl3, NaNO3
D) Na2SO4, Ba(NO3)2
E) BaCl2, MgSO4
17. 3м3 этиленнен (қ.ж.) шығымы 70% болса, алынатын массасы:
А) 8,3кг
В) *4,3кг
C) 6,3кг
D) 7,3кг
E) 5,3кг
18. Құмырсқа қышқылын зертханада алу әдісі:
А) Көміртегі және сутегіден
В) Көмірсутек (II) оксиді мен су буынан
C) *Формиат және концентрлі күкәрт қышқылынан
D) Көміртегі (IV) оксиді және судан
E) Көміртек (II) оксиді мен натрий гидроксидінен
19. 2,3 – димитилгексан қышқылының құрылым формуласы
А![]()
![]() ) * H3C – CH2
- CH2 – CH – CH –
COOH
) * H3C – CH2
- CH2 – CH – CH –
COOH
CH3 CH3
В) H3C – CH – CH – COOH
![]()
![]()
CH3 CH3
C) CH3 CH3
![]()
![]()
CH3 – C – C – COOH
![]()
![]()
CH3 CH3
D) H3C – CH – CH2 – COOH
![]()
CH3
E![]()
![]() ) H3C – CH – CH –
CH2 – CH2
– COOH
) H3C – CH – CH –
CH2 – CH2
– COOH
CH3 CH3
20. Тізбекті орындау үшін дұрыс ретімен жазылған реагенттер қатары
K


 1 KOH 2
KHCO3 3
KCl 4 KNO3
1 KOH 2
KHCO3 3
KCl 4 KNO3
А) H2O, CO2, HCl, HNO3
В) NaOH, CO2, HCl, HNO3
C) *H2O, CO2, HCl, AgNO3
D) H2O, CO, HCl, AgNO3
E) H2O, H2CO3, HCl, HNO3
21. 1л хлор мен 2л сутегі (қ.ж.) газдарын араластырды, осы қоспадан алынатын хлорсутектің массасы мен көлемі
А) 1,63г HCl және 3л
В) 2,24г HCl және 6л
C) *3,26 HCl және 2л
D) 6,66г HCl және 3л
E) 1,5г HCl және 2л
22. 11,2л метан мен 56л хлордан шығымы 70% - тік тетрахлорметан алынды. Тетрахлорметанның массасы:
А) 55г
В) 58г
C) 50,5г
D) *53,9г
E) 57,5г
23. Көмірсутек буының ауа бойынша тығыздығы 1,862, көмірсутектің формуласы. Көмірсутектің массалық үлесі 88,9% болса, онда оның формуласы:
А) C6H10
В) *C4H6
C) C7H12
D) C5H8
E) C3H4
24. Егер практикалық шығымы 80% болса, 200г глюкозадан алынатын сүт қышқылының массасы:
А) 140г
В) 180г
C) *160г
D) 150г
E) 170г
25. Комплементарлық жұп -
А) *пурин мен пиримидин негіздері арасында түзіледі
В) тимин мен урацил арасында түзіледі
C) ДНК мен РНК арасында түзіледі
D) амин қышқылдары мен нуклеин қышқылдары арасында түзіледі
E) сұйық пен газ арасында түзіледі.
4 – нұсқа
1. Орынбасу реакциясы
А) Zn (OH)2+2HCl
В![]() ) *Zn + 2HCl
) *Zn + 2HCl
C![]() ) Cu (OH)2
) Cu (OH)2
D![]() ) Fe + S
) Fe + S
E![]() ) ZnO + H2SO4
) ZnO + H2SO4
2![]() . Атомының сыртқы энергетикалық деңгейінде төрт электроны
элемент
. Атомының сыртқы энергетикалық деңгейінде төрт электроны
элемент
А) He
В) Be
C) O
D) *C
E) S
3. Полярлығы күшті қосылыс:
А) CH4
В) PH3
C) *HCl
D) H2S
E) HBr
4. Диссоциациаланғанда OH ионын түзетін зат
А) Cr(OH)3
В) *NaOH
C) KNO3
D) H2S2O3
E) Li2CO3
5. Күкіртті газ сумен әрекеттескенде түзілетін зат
А) сілті
В) суда ерімейтін негіз
C) *қышқыл
D) қышқыл тұз
E) тұз
6. Берілген заттардың арасында иондық қосылыс
А) *NaCl
В) H2
C) Ca
D) OF2
E) Cl2
7. Ерітіндісі жалынды күлгін түске бояйтын тұз
А) NaCl
В) AgCl
C) MgCl2
D) *KCl
E) CaCl2
8. Органикалық қосылыстардың химиялық құрылыс теориясының негізін қалаған ғалым...
А) А.Кекуле
В) *А.Бутлеров
C) Д.И.Менделеев
D) С.Аррениус
E) А.Кольбе
9. Табиғи полимерге жатпайды
А) Целлюлоза
В) *Капрон
C) Ақуыз
D) Нуклеин қышқылдары
E) Крахмал
10. 2Na+O2=2NO2 азот (II) оксидінің (NO) концетрациясын екі есе арттырғанда, химиялық реакциясын жылдамдығының артуы
А) 2 есе
В) *4 есе
C) 6 есе
D) 8 есе
E) 7 есе
11. Су электр тогының әсерінен сутек пен оттекке айрылады. Түзілген газдардың көлемдік қатынастары:
А) H2:O2=3:2
В) H2:O2=1:2
C) H2:O2=2:3
D) * H2:O2=2:1
E) H2:O2=1:1
12. Тотықсыздандыру үрдісінің сызбанұсқасы
А![]() ) Br BrO2
) Br BrO2
В![]() ) BrO2 BrO4
) BrO2 BrO4
C![]() ) BrO BrO2
) BrO BrO2
D![]() ) * BrO2 Br
) * BrO2 Br
E![]() ) Br2 BrO
) Br2 BrO
13. 200г мыс (II) оксиді мен 200г күкірт қышқылын қыздырғанда түзілетін тұздың массасы:
А) *326,5г
В) 326,6г
C) 326,8г
D) 326,7г
E) 326,4г
14. 170г натрий нитратынан алынатын 63% - тік азот қышқылы ерітіндісінің массасы:
А) *200г
В) 205г
C) 190г
D) 210г
E) 195г
15. Жүруі мүмкін емес реакциясының теңдеуі:
А![]() ) CO2+CaO …
) CO2+CaO …
В![]() ) CO2+NaOH …
) CO2+NaOH …
C![]() ) CO2+H2O …
) CO2+H2O …
D![]() ) CO2+SO2 …
) CO2+SO2 …
E![]() ) O2+CH4
…
) O2+CH4
…
16. Массасы 2,6г темір мен 2,8г күкірт әрекеттескенде түзілетін темір (II) сульфидінің массасы (г):
А) 2,04
В) 6,6
C) *4,08
D) 7,7
E) 8,8
1![]()
![]() 7. Zn x
Zn(NO3)2 y
ZnCO3 өзгерісіндегі “X” және
“Y” заттарының формуласы:
7. Zn x
Zn(NO3)2 y
ZnCO3 өзгерісіндегі “X” және
“Y” заттарының формуласы:
А) X – NO; Y – H2O
В) X – HNO2; Y – CH4
C) *X – HNO3; Y – K2CO3
D) X – NH3; Y - C
E) X – NH3; Y – CO
18. Ароматты спиртке жататын заттың формуласы:
А) C6H13OH
В) C2H5 - CH2 - OH
C) C6H5OH
D) * CH2 - OH
![]()
![]()
E) C6H4(OH)2
19. Халықаралық номенклатура бойынша заттың аталуы:
CH3
![]()
CH3 – CH – CH – C = O
![]()
![]()
C3H7 H
А) *2 – метил – 3 - пропилбутаналь
В) 2,3 - диметилгексаналь
C) гексаналь
D) гептаналь
E) 3 – метилгексаналь – 2
20. Схеманы пайдаланып А, В, С заттары
N![]()
![]()
![]() O ? HNO3
Cu(OH)2? қызд.
А
O ? HNO3
Cu(OH)2? қызд.
А
H![]()
![]()
![]() 2S +O
? +O
2S +O
? +O![]() SO3+H2O
B
SO3+H2O
B
A+B=C
А![]() ) A – N2O5,
B-SO3, C - H2SO4
) A – N2O5,
B-SO3, C - H2SO4
В) A – NO2, B-H2SO4, C - NO
C) *A – CuO, B-H2SO4, C – CuSO4
D) A – O2, B-H2SO3, C – H2SO4
E) A – Cu(NO3)2, B-H2SO4, C – CuSO4
21. 5,6л метанды 33,6л хлормен (қ.ж.) хлорланғанда түзілген трихлорметанның массасы:
А) *29,8г
В) 32,8г
C) 30,8г
D) 31,8г
E) 28,8г
22. 39г бензол және 39г азот қышқылы өзара әрекеттескенде түзілген нитробензолдың массасы:
А) 78г
В) 62,5г
C) 58,5г
D) *61,5г
E) 74г
23. Егер шығымы 75% болса, 1620г крахмалды гидлиздегенде түзілген, глюкозаның спирттік ашуынан түзілетін этанол массасы:
А) 630г
В) *690г
C) 700г
D) 650г
E) 720г
24. 150г 5% - тік аминосірке қышқылының ерітіндісіне 150г 5% - тік калий гидроксиді ерітіндісін қосқандағы, алынған ерітіндідегі әр заттың массалық үлестері:
А) 0,45% КОН және 2,36% H2NCH2COOK
В) 0,25% КОН және 3,15% H2NCH2COOK
C) 0,51% H2NCH2COOK және 2,56% H2NCH2COOK
D) *0,32% H2NCH2COOK және 4,04% H2NCH2COOK
E) 2,5% H2NCH2COOK және 3,75% H2NCH2COOK
2![]()
![]()
![]()
![]() 5. Тізбек арқылы: крахмал 1глюкоза
2этанол 3көміртек (IV) оксиді
крахмал. 243г крахмалдан, үшінші стадияда бөлінетін көміртек (IV)
оксидінің зат мөлшері:
5. Тізбек арқылы: крахмал 1глюкоза
2этанол 3көміртек (IV) оксиді
крахмал. 243г крахмалдан, үшінші стадияда бөлінетін көміртек (IV)
оксидінің зат мөлшері:
А) 9 моль
В) 15 моль
C) 12 моль
D) *6 моль
E) 3 моль
5-нұсқа
1. Мольдік массаны анықтау формуласы:
А)
![]()
B) ![]()
C) *![]()
D) ![]()
E) ![]()
2. Қосымша топша элементі
А) Be
В) Mg
С) Sr
D) * Ғе
Е) Са
3.СІ ₂ молекуласындағы химиялық байланыстың түрі
А) иондық
В) металдық
С)* ковалентті полюсcіз
D) Сутектік
Е) Ковалентті полюсті
4) Күшті электролиттің формуласы
А) Ag 4SO4
B)BaSO4
C) *K2 SO4
D) PbSO4
E) CaSO4
5.Cутек теріс тотығу дәрежесін көрсететін зат
А) *КН
В) НСІ
С) Н 2 S
D) H2 O
E) NH3
6.Салыстырмалы молекулалық массасы -40 болатын негіздің формуласы-
A) Ca (OH)2
B) KOH
C)* NaOH
D) Ba (OH)2
E) NH4 OH
7.Алюминий хлормен әрекеттескенде түзілетін заттың формуласы:
А) АІНСІ2
В) АІ(ОН)3
С) АІ2О3
D)*AICI3
E) AIJ3
8.Жалпы формуласы СпН 2п-6 болатын заттың атауы
А) гексан
В) октан
С)* бензол
D) ацетилен
Е) циклогексан
9.Фенолформальдегид смоласын алу үшін қолданылатын зат:
А)С6Н 4(NO 2) 2
В) С6Н5 - NO 2
C)* C6H5OH
D) C6H5-NH2
E) C6H5 –CH3
10.S+O2=SO2+297кДЖ термохимиялық теңдеуі бойынша 59,4 кДж жылу бөлінген болса,жанған күкірттің массасы (г(
А) 10
В)* 6,4
С) 7,2
D) 9,4
Е) 8
11.Массасы 200г NaОН ерітіндісі арқылы көміртек (ІҮ) оксидін жібергенде массасы 53г орта түзіледі. Бастапқы ерітіндідегі натрий гидроксидінің массалық үлесі:
А) 0,1
В)* 0,2
С) 0,3
D) 0,4
Е) 0,5
12.Бертолле тұзы КСІО3-тегі хлордың тотығу дәрежесі:
А) -1
В) +1
С) 0
D)* +5
Е) +7
13.Молекуладағы байланыстарының полярлығы кемитін заттар қатары:
А) H2S ,K2S,SO2
B) H2S,SO2, K2S
C) S8,H2S ,K2S
D)*K2S, H2S, S8
E) H2S, S8, ,K2S
14.Тотығу-тотықсыздану теңдеуіндегі HNO3→H2O+NO2+O2
Барлық коэффициенттердің қосындысы
А)5
В) 7
С) 15
D) *11
Е) 13
15.Көміртектің иіссіз,түссіз ауадан 1,5 есе ауыр,судағы ерітіндісі қышқыл болатын газ түріндегі қосылысы:
А)карболен
В)* көміртек (ІҮ) оксиді
С) карборунд
D) көмірқышқылы
Е) көміртек (ІІ) оксиді
16.Сынап (ІІ) нитратының ерітіндісін электролиздеу теңдеуіндегі барлық коэффициенттердің қосындысы
А)10
В)12
С)*11
D)9
Е)8
17.Темір алынбайтын үрдіс:
А)Ғе2О3-ті сутекпен тотықсыздандыру
В) Ғе3О4-ті алюминотермиялау
С) ҒеSО4-ті элекролиздеу
D)*Темір (ІІІ) гидроксидін айыру
Е) ҒеСІ2-ерітіндісін электролиздеу
18.Құрамы С7Н8О болатын фенолдың барлық изомерлерінің саны:
А) 2
В) 1
С) 5
D)*3
Е) 4
19.Іс жүзінде жүрмейтін реакцияның схемасы:
А) СН3СООН +Na→
В)*СН3СООН+Сu→
С) СН3СООН +K2O→
D) СН3СООН+НОС2Н5→
Е) СН3СООН+Са →
20.А және Е заттары
Электролизі +H2SiO3 +HNO3 t0
К


 СІ А Б С Е
СІ А Б С Е
А) К және КNO3
B) KOH және К2О
С) К және КNО2
D)*КОН және КNO2
E) К2О және КNO2
21.Циклопентанның тұйық тізбекті изомерлерлерінің саны:
А)*4
В) 1
С) 3
D) 2
Е) 5
22.Этилбензолды нитрлегендегі өнімнің 1 молінің массасы:
А)*241 г
В) 244 г
С) 240 г
D) 238 г
Е) 239 г
23.Егер шығымы 75% болса, онда 18 г глбкозаны тотықтырғанда түзілетін күмістің массасы:
А) 13,2 г
В)*16,2 г
С) 15,2 г
D) 17,2 г
Е) 14,2 г
24. Құрамында бір қос байланыс бар көмірсутектер
А) *Алкендер
В) Арендер
С) Алкиндер
D) Алкадиендер
Е) Алкандар
25.Құрамы 40% метан,60% этаннан тұратын 10 л газ қоспасын жағуға жұмсалатын (қ.ж) оттектің көлемі:
А)*29 л
В) 30 л
С) 31 л
D) 32 л
Е) 33 л
6-нұсқа
1.Электрондар доноры-
А)*N
B) Mg
C) H
D) K
E) Na
2.Кіші период элементтерінде атом радиусы бірінші элементтен соңғы элементке қарай өзгеруі
А) Артады
В) Минимум арқылы өтеді
С)*Кемиді
D) Максимум арқылы өтеді
Е) өзгермейді
3.Теріс электрлігі аз ажыратылатын элементтер атомдарының арасындағы байланыс:
А) иондық
В) сутектік
С)*Ковалентті полюсті
D) Ковалентті полюссіз
Е) донорлы-акцепторлы механизм
4.MgCI2 диссоциацияланғанда түзілетін иондар
А)*Мg2+ +CI-
В) Мg +2CI
С) диссоциацияланғанда түзілетін иондық
D) Мg2+ +CI-
Е) Мg2+ +CI2
5. ҮІ топтың А топшасындағы элементтердің ұшқыш сутекті қосылыстарының жалпы формуласы
А) НR
B) НRО3
С)*Н2R
D) Н4 R
Е) Н3 R
6.Негіздік оксидтің формуласы
А) N2O5
B) SiO2
C)*Na2O
D) SO2
E) NO
7.Алюминий электрондарының энергетикалық деңгейлерге бөлінгенін көрсететін сызба-нұсқа
А)* 2е 8е 3е
В) 2е 8е 8е
С) 2е 8е 8е 3е
D) 2е 7е
Е) 2е 8е 1е
8. .Лабораторияда метан алудың әдісі
А) 2СН4→С2Н2+3Н3
В)*СН3СООNa+NaOH →CH4↑+Na2CO3
C) табиғи газдан бөліп алу арқылы
D) С+2Н2→СН4
Е) 2СН3СІ + 2Na→СН3-СН3+2NaСІ
9.Полимерлену дәрежесі ....... көрсетеді.
А)*Политердің макромолекуласында неше мономер молекулалары біріккенін
В) Негізгі элементтің индексін
С)Балқу температурасын
D) қайнау температурасын
Е) Макромолекула санын
10.СО(r)+ 2Н2(r) →СН3ОН(r)+Q
Үрдісіндегі тепе-теңдікті солға ығыстыратын жағдай
А) қысымды жоғарылату
В) Н2концентрациясын арттыру
С)*СО концентрациясын төмендету
D) CH3OH концентрациясын төмендету
Е) температураның төмендеуі
11. 480 г 20 %-ті ерітінді дайындау үшін қажет калий гидроксидінің массасы:
А) 48 г
В) 40 г
С) 56 г
D)*96 г
Е) 20 г
12. Хлорлылау қышқылдың формуласы:
А) НСІ
В) НСІО2
С) НСІО3
D)*НСІО
Е) НСІО4
13. 3моль оттекпен әректтесетін натрийдің зат мөлшері (моль)
А) 15
В) 12
С) 9
D)*6
Е) 3
14.Күміс нитраты мен натрий фосфаты әрекеттескенде 41,9 г күміс фосфаты түзілген.Реакцияға түскен натрий фосфатының массасы (г) және зат мөлшері (моль)
А) 11,2 және 0,2
В) 21,6 және 0,3
С)*16,4 және 0,1
D) 36,2 және 0,2
Е) 46,1 және 0,1
15.Графит және алмаз бір элемент атомы-көміртектен – тұратынын дәлелдейтін әдіс:
А)*Екі затты жаққанда СО2 түзілуі
В) Сілтімен әрекеттесуі
С) Азотпен әректтесуі
D) Күкірпен әрекеттесуі
Е) Қышқылмен әрекеттесуі
16. Ғе2О3+С →Ғе +Со реакция үрдісі бойынша 280 г қызыл теміртастағы
(Ғе2О3) темірді тотықсыздандыру үшін қажет кокс массасы:
А) 68 г
В)*63 г
С) 56 г
D) 59 г
Е) 65 г
17.Екі сатыдан кейін фенол алуға болатын зат:
А) СН4
В) С2Н 2
С) С2Н 6
D)* С6Н6
Е) циклогексан
18.Х,Ү қосылыстары
СН4 →Х → С6Н12О 6 → Ү →СН3СООС2Н5
А)СО2,СН3СООН
В) СН2О,С2Н5ОН
С)*СО2, С2Н5ОН
D) СН3СООН, С2Н5ОН
Е) СН2О, СО2
19. Өзгерістер нәтижесінде алынатын «А» өнімнің аталуы:
+Br2 H2O +O Ag2O
C


 H3- CH3
X1
X2
X3
A
H3- CH3
X1
X2
X3
A
А) Формальдегид
В) Сірке альдегиді
С)*Сірке қышқылы
D) Күміс ацетаты
Е) Құмырысқа қышқылы
20. Газ толтырылған пластик
А) силикон
В) полиэтилен
С) *пенопластар
D) целлулоид
Е) аминопластар
21.Құрамында мырыштың массалық үлесі 37% болатын қосылыс
А) ZпО
В) ZпS
C)*K2ZnO2
D) ZnSiO3
E) Zn (OH)2
22.80 г 1,2% бром суын 200 мл (қ.ж) метан этилен қоспасы түссіздендіреді.Қоспадағы метанның көлемдік үлесі (%)
А) 3,32
В) 30,3
С)*32,3
D) 38,9
Е) 3,84
23.Массасы 9,9 г дихлорэтан алу үшін хлорсутекпен әрекеттесетін ацетиленнің (қ.ж) көлемі
А) 5,60
В) 4,48 л
С)*2,24 л
D) 22,40 л
Е) 1,12 л
24.85,5г сахароза гидролизденгенде алынған глюкозаны тотықтырғанда түзілген күмістің массасы
А) 46 г
В)*54 г
С) 48 г
D) 52 г
Е) 64 г
25. Егер белоктың мономері глицилаланин болып және одан гидролиздегенде 222,5 г аланин түзілсе,белоктың массасы
А)*365 г
В) 250 г
С) 290 г
D) 300 г
Е) 270 г
7-нұсқа
1. Қосылу реакциясы
A) ![]() .
.
B) ![]() .
.
C) ![]() .
.
D)* ![]() .
.
E) ![]() .
.
2. ![]() атомы ядросының құрамында:
атомы ядросының құрамында:
A) 80p және 36n.
B) 36p және 36n.
C) 36p және 44e.
D)* 36p және 44n.
E) 80p және 44n.
3.Ортақ электрон жұбы арқылы түзілетін химиялық байланыс.
A) иондық.
B)* ковалентті.
C) металдық.
D) сутекті.
E) молекулалық.
4. Диссоцияциясы сатылы жүретін қосылыс...
A) калий гидроксиді.
B) натрий хлориді.
C)* күкіртсутек қышқылы.
D) аммоний нитраты.
E) азот қышқылы.
5. Жану реакциясының белгісі -
A) қысым пайда болуы.
B) тұнба түзілі.
C)* жылу мен жарық бөлінуі.
D) ток пайда болуы.
E) заттардың сұйылуы.
6. Н3ВО3 осы қышқылға сәйкес келетін оксидтің формуласы
A)* В2О3.
B) Ве2О3.
C) ВО3.
D) ВО.
E) ВеО.
7. Натрий атомының электрондық конфигурациясы
A) 1s22s22p1.
B) 1s22s22p63s2.
C)* 1s22s22p63s1.
D) 1s22s22p3.
E) 1s22s22p4.
8. Құрамында бір қос байланыс бар көмірсутектер
A)* Алкендер.
B) Арендер.
C) Алкиндер.
D) Алкадиендер.
E) Алкандар.
9. Полимерлену дәрежесін көрсететін сан
A) Макромолекула саны.
B) Негізгі элементтің индексі.
C)* Полимердің макромолекуласында құрылымдық буын саны.
D) Қайнау температурасы.
E) Балқу температурасы.
10. Температура 30 С-қа төмендеп ,жылдамдық 27 есе азайғанда, температуралық коэффицент
A) 2.
B)* 3 .
C) 3,5.
D) 2,5.
E) 4.
11. 160 грамм ерітіндіні суалатқанда 40 құрғақ тұз қалды,ерітіндідегі еріген заттың массалық үлесі
A)* 25%.
B) 20%.
C) 30%.
D) 10%.
E) 15%.
12. 9,8 г күкірт қышқылы ерітіндісін натрий гидроксиді ерітіндісінің артық мөлшерімен бейтараптағанда,түзілетін тұздың зат мөлшері:
A) 0,05 моль.
B) 0,01 моль.
C) 1 моль.
D)* 0,1 моль.
E) 0,2 моль.
13. Фосфор қышқылы түзілетін реакция:
A) P2O3+H2O=
B) Na3PO4+H2O=
C) P2O5+H2O=
D)* Na2SO4+P2O5=
E) Na2O+K3PO4=
14. Алюминийдің гидроксиликатындағы байланыстардың жалпы саны
A)12.
B) 14.
C) 18.
D)* 19.
E) 15.
15. Ең активті металдардың (Na, K, Ca, Mg) өнеркәсіпте алыну әдісі
A) тұздар ерітінділердің электролизі.
B) көміртек (II) оксидімен оксидтерден тотықсыздандыру.
C) тұздар балқымаларының электролизі.
D)* көміртекпен оксидтерден тотықсыздандыру
E) алюминотеропия.
16.Өзгерістер сызба- нұсқасындағы FeCl2→X1→X2→Fe2O3 X1 және X2 заттары:
A) X1 – FeCO3, X2 – FeCl3.
B) X1 – Fe2(CO3)3, X2 – FeSO4.
C) X1 – Fe2(NO3)3, X2 – Fe2SO4.
D)* X1 – Fe(OH)2, X2 – Fe(OH)3.
E) X1 – FeO, X2 – FeCl2.
17. 230г этил спиртімен толық жағу үшін қажет оттектің (қ.ж.) көлемі
A)168 л.
B)112 л.
C)*336 л.
D) 224 л.
E) 210 л.
18. Фенол, натрий ацетатын ажыратады:
A)* Темір (III) хлоридінің ерітіндісі және фенолфталеин ерітіндісі.
B) лакмус ерітіндісі ,су.
C) сыртқы түрінен.
D) лакмус ерітіндісі,сілті ерітіндісі.
E) қорғасын нитраты,натрий гидроксиді.
19. Детонация дегеніміз-бензиннің ...
A) крекингіленуі.
B)* қопарылыс түзіп жануы.
C) пиролизденуі.
D) дегенерациялануы.
E) дегидрленуі.
20. 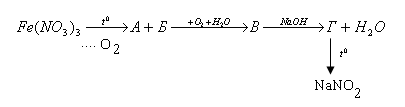
Тізбегіндегі А,В,Г заттары.
А) темір(II) оксиді, азот (IV) оксиді, натрий нитриты.
В)* темір(III) оксиді, азот қышқылы, натрий нитриты.
C) темір(II) оксиді, азот қышқылы, натрий нитриты.
D) темір(III) оксиді, азот қышқылы, натрий нитриты.
E) азот (II) оксиді, азот (IV) оксиді, натрий нитриты.
21. SiCl4 – тің толық гидролизі кезіндегі түзілетін екі зат.
A) Si және HCl.
B) SiO2 және HClO.
C) SiO2 және HCl.
D)* H2SiO3 және HCl.
E) H2SiO3 және Cl2.
22. 142 г. Йодметан мен 50г. Натрий әрекеттескенде түзілген этанның (қ.ж.) көлемі.
A) 44,8 л.
B)* 11,2 л.
C) 67,2 л.
D) 33,6 л.
E) 22,4 л.
23. 9,2 г. толуол толық жану үшін қажет ауаның көлемі (ауадағы оттектің көлемдік үлесі 20 %);
A) 103 л.
B) 105 л.
C)* 101 л.
D) 112 л.
E) 104 л.
24. картоптағы крахмалдың массалық үлесі 20 %, өнім шығыны 50 %, сыйымдылығы 50 кг. 5 қап картоптан алынған глюкозаның массасы.
A) 27,28 кг.
B)* 27,78 кг.
C) 27,38 кг.
D) 27,48 кг.
E) 27,18 кг.
25. Егер шығыны 70 % болса, 6,2 г метиламин алу үшін қажет нитрометанның масса:
A) 17,32 г.
B)* 17,43 г.
C) 19,21 г.
D) 18,12 г.
E) 17,78 г.
8-нұсқа
1. А+В = С+Д типті реакцияда 5 г. А заты мен 6г. В заты әрекеттесіп 3г. Д заты түзілген болса, С затының массасы:
A) 5 г.
B) 5 г.
C) 7 г.
D)* 8 г.
E) 9 г.
2. Атомның энергетикалық деңгейлеріндегі электрон
A) Al.
B) N.
C) As.
D)* P.
E) Cl.
3. Бір периодтағы элементтердің электр терістігі.
A) бірінші өсіп, сонан соң кемиді.
B) оңнан солға қарай өседі.
C)* солдан оңға қарай өседі.
D) солдан оңға қарай кемиді.
E) өзгермейді.
4. Үш сатылы диссоциацияланатын қосылыс.
A) мыс (ІІ) гидроксиді.
B) натрий хлориді.
C)* ортофосфор қышқылы.
D) күкірт қышқылы.
E) хром (ІІ) гидроксиді.
5. Атмосферадағы оттектің массалық үлесі (%).
A) 40.
B) 25.
C)* 21.
D) 35.
E) 30.
6. Суда жақсы еритің негіз:
A) Zn(OH)2.
B) Fe(OH)3
C) Cu(OH)2.
D)* LiOH.
E) Ca(OH)2.
7. Өзгерістер тізбегіндегі қышқыл тұз түзетін реакция
![]()
A) 1,4.
B) 2,4.
C)* 2,3.
D) 1,2.
E) 1,3.
8. sp - гибридтенген көміртек атомына сәйкес келетін валенттік бұрышы:
A)* 1800.
B) 1200.
C) 450.
D) 1080.
E) 1090.
9. Полимерлену реакциясы дегеніміз бұл -
A) екі заттың қосылу процесі.
B) тұздардың айырылуы.
C)* қос байланыстардын үзілуі есебінен мономердің бірдей молекулаларрының макромалекулаға бірігу процессі.
D) мономер қатысып, кіші молекулалы қосылыс бөліне жүретін полимер түзілу реакциясы.
E) каталитикалық гидрлеу процессі.
10. Термохимиялық теңдеуі S+O2=SO2 + 297 кДж болса, 16г. күкірт жаңғанда бөлінетін жылу мөлшері (кДж)
A) 135,5
B) 175,5
C)* 148,5
D) 182,5
E) 124,5
11. Күкір қышқылының 320 г. 10% - ті ертіндісіне 80г. су қосқанда алынған ерітіндегі Н2SO4 – тің массалық үлесі:
A) 6%
B)* 8%
C) 10%
D) 7%
E) 9%
12. Сутектің хлормен әрекеттесу механизімі осы заттың хлормен әрекеттесуіне ұқсайды:
A) анилиннің.
B)* алкандардың.
C) алкиндердің.
D) арендердің.
E) алкендердің.
13. 49 г. натрий гидрооксиді мен 49 г. күкір қышқылының ерітінділерін араластырғанда түзілетін тұздың массасы.
A) 51г.
B)* 71г.
C) 61г.
D) 91г.
E) 81 г.
14. Фосфор тотықтырғыш болатын химиялық теңдеу.
A) 4P+5O2 = 2P2O5.
B)* 2P+3Ba = Ba3P2.
C) 2P+3Cl2= 2PCl3.
D) 6P+5KClO3 = 5KCl+3P2O5.
E) 4P+3O2 = 2P2O3.
15. 8,4 г. көміртек (ІІ) оксидінің қалыпты жағдайдағы көлемі (л.).
A) 16,2 л.
B) 6,2 л.
C) 7,5 л.
D)* 6,72 л.
E) 5,8 л.
16. Магний хлоридінің ерітіндіс электролизге ұшырағанда катодта түзілген заттың салыстырмалы молекулалық массасы.
A) 4.
B) 24.
C)* 2.
D) 32.
E) 71.
17. Табиғатта темір формуласы төменде берілген заттар түрінде кездеседі, темірдің мөлшері көп зат.
A) FeS2
B) Fe2O3
C) Fe3O4
D)* FeO
E) FeCO3
18. Тотықтырғанда құмырсқа альдегидін түзетін сприттің құрамындағы көміртегі атомының саны:
A)* 1.
B) 2.
C) 3.
D) 4.
E) 5.
19. Мына өзгерістерде түзілетін A, B, C, қосылыстарына төмендегі заттардың сәйкестігі:
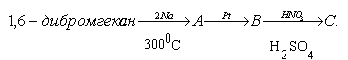
Жауапты А, В, С қосылыстарының түзілу ретімен қосылыстар белгіленге нөмірлер арқылы көрсетіңіз.
1. 2-нитрогексан. 2. гексан. 3. циклогексан. 4. 1,5 – гексадиен. 5. бензол. 6. нитробензол.
A)* 3, 5, 6.
B) 2, 3, 1.
C) 4, 5, 6.
D) 3, 4, 5.
E) 2, 3, 5.
20. Натрий концентрациялы тұз қышқылымен әрекеттескенде көлемі 5,6 л газ бөлінеді. (қ.ж.). Түзілген тұздың массасы.
А) 30,40 г.
В) 40,25 г.
C) 30,01 г.
D)* 29,25 г.
E) 25,16 г.
21. Азот бойынша тығыздығы 2,5 – ке тең 35 г. циклоалканды жаққанда жұмсалатын ауаның көлемі (ауадағы оттектің үлесі – 20%).
A) 460 л.
B) 430 л.
C)* 420 л.
D) 450 л.
E) 440 л.
22. 132 г. CH3COH ацетальдегид (шығымы 70%) алу үшін жұмсалатын құрамындағы 28 % қоспасы бар кальций карбидінің массасы.
A)* 265,5.
B) 325,5.
C) 235,5.
D) 355,5.
E) 255,5
23. 340 г. хлор бензол мен 220 г. натрий гидрооксиді әрекеттескенде түзілетін фенолдың массасы.
A) 244 г.
B) 274 г.
C)* 284 г.
D) 254 г.
E) 264 г.
24. 40,5 г. целлюлозаны нитрлегенде түзілген денитроцеллюлозаның массасы:
A)* 63 г.
B) 62 г.
C) 59 г.
D) 61 г.
E) 58 г.
25. Массасы 78 г. бензолды нитрлегенде іс жүзінде 105 г. нитробензол алынады. Нитробензолдың шығыны:
A) 4,27 %.
B) 8,54 %.
C) 42,7 %.
D)* 85,4 %.
E) 0,427 %.
9 –нұсқа
1. О химиялық таңбасы… көрсетеді.
A) бір молекуланы
B) мольдік массаны
C) бір атомды
D)* жай заттың бір молін
E) салыстырмалы молекулалық массаны
2. 20 протон 20 нейтрон және 20 электроны бар элементтің салыстырмалы атомдық массасы
A)* 20
B) 40
C) 68
D) 60
E) 78
3. Алмаздың кристалдық торы
A) молекулалық
B) иондық
C)* атомдық
D) атомдық, молекулалық
E) металдық
4. ![]() реакциясының ақырына дейін жүру себебі, нәтижесінде түзілетін
заттардың бірі -
реакциясының ақырына дейін жүру себебі, нәтижесінде түзілетін
заттардың бірі -
A) ерімейтін тұз
B) су
C) ерімейтін негіз
D)* тұнба
E) газ
5. Оттек газы
A)* суда жақсы ериді
B) дәмді
C) түссіз
D) өткір иісті
E) ауадан жеңіл
6. «Органикалық химия» деген атауды ұсынған ғалым...
A) Г.Кольбе
B) Ф.Велер
C) И.Берцелиус
D) Н.Зинин
E)* М.Бертло
7. Металл пісіру жұмысы кезінде көзді қорғау үшін арнайы маска киеді, себебі
A) ацетилен жанбайды
B) ацетилен көгілдір түсті жалынмен жанады
C) ацетилен бықсып жанады
D) ацетилен баяу жанады
E)* ацетилен өте жарқырап жанады
8. Қарапайым спирттің формуласы:
A) ![]()
B) ![]()
![]()
C) ![]()
D) *![]()
E) ![]()
9. Ең қарапайым карбон қышқылының аталуы:
A) Акрил қышқылы.
B) Сірке қышқылы.
C) Стеарин қышқылы.
D) Құмырсқа қышқылы.
E)* Май қышқылы.
10. Температураны
500С-тан 90 0С-қа көтергендегі ![]() реакция жылдамдығының артуы
реакция жылдамдығының артуы
A)* 8 есе
B) 10 есе
C) 16 есе
D) 12 есе
E) 4 есе
11. 80г ерітіндіні буландырған соң, ыдыста 20г тұз қалды. Ерітіндідегі еріген заттың массалық үлесі
A) 22 %
B) 30 %
C)*25 %
D) 35 %
E) 20 %
12. Тұз түзбейтін оксидтерге көбірек тән болатын қасиеттер
A) Гидролизге бейімділік
B)* Тотықсыздануға бейімділік
C) Тотығуға бейімділік
D) Этерификацияға бейімділік
E) Орынбасуға бейімділік
13. 1,5 моль күкіртсутек толық жанғанда түзілетін күкірт(IV) оксидінің массасы:
A) 64г
B) 9,6г
C) 3,2г
D) 96г
E) *32г
14. Сутегі бойынша тығыздығы 62-ге ақ фосфор молекуласындағы фосфор атом саны:
A) 2
B) 5
C) 1
D) 4
E)* 3
15. Реакцияда осы заттармен кремний- тотықсыздандырғыш болады
A) ![]()
B) ![]()
C) ![]()
D)*![]()
E) ![]()
16. Сілтілік металдарды тек қана тұздарының балқымаларын электролиздеу арқылы алуға болады. Оған себеп:
A) сілтілік металдардың белсенділігі төмен
B)* сілтілік металдар- ең белсенді металдар, сондықтан басқа әдістермен алу мүмкін емес
C) сілтілік металдар табиғатта бос түрінде кездеседі
D) сілтілік металдардың белсенділігі орташа
E) кернеу қатарында сілтілік металдар сутектен кейін орналасқан
17.III топ элементі хлоридінде жоғары валенттілік көрсетеді.Егер осы зат құрамында 79,77% хлор болса, металдың химиялық таңбасы және салыстырмалы атомдық массасы:
A)*45 Sc
B) 56 Fe
C) 70 Ga
D) 11 B
E) 27 Al
18. Темір тақташаны мыс (II) сульфаты ерітіндісіне батырғанда, 40г мыс бөлінді. Тақташаның массасы
A) *28г
B) 40г
C) 10г
D) 35г
E) 39г
19. Детонация дегеніміз
A)* Бензиннің қозғалтқышта қопарылыс түзіп жануы
B) мұнай өнімдерін айдау
C) Жоғары температурада бөлшектенуі
D) Жоғары қысымда мұнай өнімдерінің бөлшектенуі
E) Мұнайдың өнімдерін тазарту
20. Схеманы пайдаланып А, В, С заттары
![]()
![]()
![]()
A)
![]() ,
, ![]() ,
, ![]()
B)
![]() ,
, ![]() ,
, ![]()
C)
*![]()
![]() ,
, ![]()
D)
![]()
![]() ,
, ![]()
E)
![]()
![]()
![]() .
.
21.Әрқайсысы екі мольден: тұз, бромсутек, фторсутек, иодсутек қышқылдарының қоспасына күміс нитратымен әсер еткенде түзілген тұнбаның зат мөлшері:
A)* 2 моль
B) 8 моль
C) 6 моль
D) 4 моль
E) 10 моль
22. 250г гептан бір мезгілде циклденгенде және дегидрленгенде бензолдың гомологы түзіледі. Осы кезде түзілген газдың көлемі (қ.ж.литрмен)
A) 112
B)* 224
C) 198
D) 148
E) 168
23.Массалық үлесі 20 %-тті 90г глюкоза ерітіндісі күміс оксидінің аммиактағы ерітіндісімен әрекеттескенде массасы 2г күміс бөлінсе, күмістің шығымы (%)
A) 9,3
B) 9,5
C) 10,2
D) *10,5
E) 9,4
24. Құрамында 15,73 % -азот бар моноамин қышқылының күрделі эфирінің құрылысы:
A)* ![]()
B) ![]()
C) ![]()
D) ![]()
E) ![]()
25. Нитрон талшығының мономері акрилонитрилді пропеннен алады:
Құрамына пропеннің көлемдік
үлесі – 15 %табиғи газдың ![]() -нан (қ.ж) алынатын
акронитрилдің массасы (г) :
-нан (қ.ж) алынатын
акронитрилдің массасы (г) :
A)* 2842
B) 2840
C) 2835
D) 2839
E) 2830
10- нұсқа
1. Химиялық құбылысқа жататыны
A) крекингілеу.
B) шайқау.
C) буландыру.
D)* хромотографиялау
E) дистилдеу.
2. Элементтің реттік нөмірі көрсетеді:
A) протон және нейтрон санын
B) протон және изотоп санын
C)* протон және нуклон санын
D) протон және электрон санын
E) нейтрон және электрон санын
3. Калий хлориды түзілетін кристалдық тордың түрі
A) *молекулалық
B) молекулалық, атомдық
C) металдық
D) атомдық
E.)иондық
4. Диссоциация кезінде катион ретінде сутек пен металл иондары түзілетін заттардың аты:
A) қышқыл тұздар
B) қышқылдар
C)негізгі тұздар
D)* сілтілер
E) орта тұздар
5. Оттегінің латынша аталуы
A) оксигениум
B) силициум
C) гидрогениум
D) гидраргирум
E.)*феррум
6. ![]() - гибридизация кезінде
валенттік бұрыш тең
- гибридизация кезінде
валенттік бұрыш тең
A) ![]()
B) *![]()
C) ![]()
D) ![]()
E) ![]()
7. Көміртек қаңқасы бойынша пентадиен-1,2-нің изомері:
A)* пентин-1
B) пентадиен-1,3
C) пентин-2
D) 2-метилбутадиен-1,3
E)3-метилбутадиен-1,2
8. Сірке қышқылының молекулаларының арасындағы байланыс
A) сутектік
B) иондық
C) *ковалентті полюсті
D) металдық
E) ковалентті полюссіз
9. Синтетикалық талшық
A) мақта
B)жүн
C) ацетатты талшық
D)* жібек
E) капрон
10. Егер температураны
400C-қа көтерсе, реакция
жылдамдығы ![]() ... есе
артады
... есе
артады
A)16
B)* 4
C) 2,5
D) 5
E)14
11. Сумен орын басу реакциясына түсетін зат
A) ![]()
B) ![]()
C) *![]()
D) ![]()
E) ![]()
12. 4 моль күкірт қышқылының массасы:
A )490 г
B) 196 г
C) 441 г
D)* 392 г
E.)98 г
13. Күкірт(VI) оксиді мен калий гидроксиді әрекеттескендегі (орта тұз түзілсе) толық иондық теңдеудегі барлық коэффициенттер қосындысы
A) 5
B) 7
C) *9
D) 8
E) 6
14. ![]() қыздырғанда пайда болатын
заттар
қыздырғанда пайда болатын
заттар
A)сынап оксиді, оттек, азот (II) оксиді
B) сынап, азот (IV) оксиді, оттек
C) сынап, азот (II) оксиді, оттек
D) *сынап оксиді, оттек, азот (IV) оксиді
E)сынап (I) нитраты және оттек
15. Қысқартылған иондық теңдеу бойынша әрекеттесетін заттардың жұбы:
![]()
A) магний карбонаты мен натрий гидроксиді
B) калий карбонаты мен су
C) көмір қышқыл газы мен су
D)* көмір қышқыл газы мен натрий гидроксиді
E)натрий карбонаты мен тұз қышқылы
16. Металдардың жалпы химиялық қасиеттерін көрсететін реакциялар үрдісінің жұбы
A)* ![]()
![]()
B) ![]()
![]()
C) ![]()
![]()
D) ![]()
![]()
E) ![]()
![]()
17. ![]() және
және ![]() иондарындағы протондарының
жалпы саны
иондарындағы протондарының
жалпы саны
A) 31
B) 33
C) 32
D)* 30
E) 28
18. ![]() өзгерісінде Х заты
өзгерісінде Х заты
A) ![]()
B) ![]()
C) *![]()
D) ![]()
E) ![]()
19. Мына затты анықтау үшін мыс (ІІ) гидроксидін қолданады
A) пропанол
B) циклогексан
C)* бензол
D) глюкоза
E) фенол
20. 7,8 г алюминий гидроксидін еріту үшін қажет 10% -ті натрий гидроксиді ерітіндісінің массасы:
A) 30 г
B) 60 г
C) 40 г
D)* 20 г
E) 50 г
21. ![]()
Реакция теңдеуіндегі жалпы коэффициент саны
A) 7
B) * 3
C) 10
D) 5
E) 14
22. 60 г этан мен 240 г бром әрекеттескенде түзілген бромэтанның массасы :
A) 143,3 г
B) 133,6 г
C) 163,5 г
D)* 173,5 г
E) 153.6 г
23. 25 г 94 % -тік фенол ерітіндісі мен 75 г1 % бром суын араластырғанда түзілетін реакция өнімінің массасы:
A) 0,52 г
B) 0,63 г
C) 0,47 г
D)*0,35 г
E) 0,59 г
24. 0,5 моль целлюлоза азот қышқылымен әрекеттескенде түзілетін тринитроцеллюлозаның массасы:
A) 148,4 г
B) 148,2 г
C) 148,3 г
D)* 148,5 г
E) 148,1 г
25. Құрамында элементтердің массалық қатынастары
m(C) :m(O) :m(N) :m(H) = 12 :16:7:2,5 болатын зат:
A![]() )
) ![]()
![]()
![]()
B![]() )
) ![]()
![]()
C![]() )
) ![]()
![]()
D![]() )
) ![]()
![]()
E![]() ) *
) * ![]()
![]()
Исабаева Гүлбаршын Тұрсынғалиқызы, т.35-28-23
11 нұсқа
1. Егер химиялық реакцияның кескіні төмендегідей болса
∆ + О → ∆О
Онда реакцияның типі
A) айырылу
B) қосылу
C) *орын басу
D) алмасу
E) бейтараптану
2. Электрондық формуласы 3s23p4 элементтің реттік нөмірі
A) * 16
B) 10
C) 14
D) 6
E) 12
3. Тотығу-тотықсыздану реакцияларына жататын реакцияның сипаттамасы
A) ерімейтін заттар түзіле жүретін реакциялар
B) * әрекеттесуші заттар элементтерінің тотығу дәрежесі өзгеретін реакциялар
C) әлсіз электролиттер
түзіле жүретін реакциялар
D) әрекеттесуші заттар иондары арасындағы алмасу реакциялары
E) газ түзіле жүретін реакциялар
4. Катион болып есептелетін бөлшек
A) Cr2O72-
B) * NH4+
C)
Cl-
D) SO42-
E) NO3-
5. Металдарды оксидтерінен тотықсыздандыруға қолданылытын газ
A) хлор
B) озон
C) * сутек
D) фтор
E) оттек
6. Алкиндердің жалпы формуласы
A) * СnH2n-2
B) СnH2n
C)
СnH2n-+
2
D) СnH2n-6
E) СnH2n+1
7. Диен көмірсутектеріне тән емес реакция
A) гидрлену
B) полимерлену
C) * гидролиз
D) жану
реакциясы
E) галогендермен
әрекеттесу
8. Эфирлену реакциясы
A) СН3ОН + СН3ОН → СН3 ─ О ─ СН3 + Н2О
B) 2СН3ОН + О2 → 2СО2 + 4 Н2О
C) НСОН +Ag2O → НСООН + 2Ag↓
D) *
НСООН + СН3ОН → НСОО СН3
+ Н2О
E) 2С2Н5ОН + 2 Na → 2С2Н5ОNa + Н2↑
9. Кремнийорганикалық полимерлер
A) * силикондар
B) фенопластар
C) пенопластар
D) каучуктер
E) аминопластар
10. Катализатор ретінде Н2 SO4 (конц.) қолданылатын реакция
A) С6H6 + О2 →
B) С6H6 + Br2 →
C) * С6H6 + HNО3
→
D) С6H6 + H2 →
E) С6H6 + Cl2 →
11. Массасы 40 г сусыз мыс (ІІ) сульфатын алу үшін кристаллогидраттың
СuSO4∙∙5 Н2О қажет массасы
A) 91,5 г
B) * 62,5 г
C) 52,5 г
D) 31,5 г
E) 41,5 г
12. Берілген қосылыстардан: Na2О, HCl, SO3, Ca(OH)2, H3PO4 калий гидроксидімен әрекеттесін қосылыстар саны
A) * 3
B) 1
C) 2
D) 4
E) 5
13. Егер калий бромидінің 200 г ерітіндісінен хлормен 16 г бром ығыстырылған болса, оның проценттік концентрациясы
A) 15,4%
B) 10,2%
C) * 11,9%
D) 6,2 %
E) 14,0%
14. 320 г мысты концентрлі күкірт қышқылында еріткенде түзілген мыс (ІІ) сульфатының моль саны
A) * 5
B) 3
C) 1
D) 4
E) 2
15. Аммиактың сутекпен салыстырғанда тығыздығы
A) 6,5
B) 4,0
C) * 8,5
D)
0,117
E) 17,0
16. Магний сульфаты ерітіндісін электролиздегенде катодта бөлінетін жай заттың молекулалық массасы
A) 26
B) 24
C) 16
D) * 2
E) 32
17. ІІ топтағы металдың 20 грамы судан 11,2 л сутекті қ.ж. ығыстырады. Осы металл
A) * Са
B) Ва
C)
Sr
D) Be
E) Mg
18. Мыс пластинкасын қара ұнтаққа, одан кейін көк ерітіндіге айналдыру процесін көрсететін реакциялар жұбы
A) * Сu + O2 →
CuO + HCl →
B) Cu + Н2О →
CuCl2 + NaOH →
C) Cu + O2 →
CuO + Н2О →
D) Cu + Cl2 →
Cu + HgCl2 →
E) Cu + O2 →
CuO + Cu(OH)2 →
19. Схемадағы Х заттың формуласы
to, Ni, (+H2) HNO3 (H2SO4 конц.)
С2Н4 → С2Н6 → Х
A) С2Н4 NO2
B) С2Н2 NO2
C) С2Н5NO3
D) * С2Н5 NO2
E) С2Н5N
20. 31 г кальций фосфатын алу үшін жұмсалатын негіз бен қышқылдың массалары (г)
A) 28,2 ; 22,6
B) 31,2; 15,6
C) 15,2; 33,6
D) 25,2; 39,6
E) * 22,2; 19,6
21. 2,5 кг кальций карбонатын күйдіргенде бөлінген көмірқышқыл газының көлемі 448 л (қ.ж.). Ыдырауға жұмсалған кальций карбонатының массалық үлесі
A) 85%
B) * 80%
C) 75%
D) 90%
E) 100%
22. Азот бойынша тығыздығы 2,5-ке тең циклоалканның 14 грамын жаққанда түзілетін көмірқышқыл газының көлемі (қ.ж.)
A) 4408 л
B) * 22,4 л
C) 179,2 л
D) 11,2 л
E) 89,6л
23. 30 г пропанол мен 20 г калий әрекеттескенде шығымы 60% болса, түзілетін сутектің көлемі (қ.ж.)
A) * 5,6 л
B) 4,48 л
C) 1,12 л
D) 2,24 л
E) 3,36 л
24. Егер шығымы 75%, 620 г крахмалды гидролиздегенде түзілген глюкозаның спирттік ашуынан түзілетін этанол массасы (г)
A) 650
B) 630
C) * 690
D) 700
E) 720
25. 88 г триброманилин алу үшін 35%-ті бром суының
(ρ= 1,02 г/см3) қажет көлемі (мл)
A) 415,3
B) 425,5
C) * 358,5
D) 325,5
E) 375,5
12 нұсқа
1. Күрделі зат
A) вольфрам
B) алтын
C) * күкіртсутек
D) күкірт
E) алюминий
2. Атомның электрондық формуласы 1s22s22p63s 23p63d74s 2 болатын элемент
A) мыс
B) көміртек
C) калий
D) *
кобальт
E) кальций
3. Ковалентті полюссіз байланысқа жататын зат
A) SO3
B) * Cl2
C)
Na2О
D) Fe(OH)3
E) Al
4. Диссоциацияланғанда Н+ ионын түзетін зат
A) CrOH)3
B) Ca(OH)2
C)
Na2SiO3
D) K2CO3
E) * H2SO3
5. Мырыш сульфатын түзетін заттар жұбы
A) ZnO және Н2S
B) Zn және S
C) *
Zn(OH)2 және Н2SO4
D) Zn және SO3
E) Zn және SO2
6. Органикалық қосылыстардың химиялық құрылыс теориясын ашкан
A) Бертло М.
B) Лебедев С.В.
C) Марковников В.В.
D) Менделеев
Д.И.
E) * Бутлеров
А.М.
7. Көп атомды спиртке жататын зат
A) ROH
B) (СН3)3C─OH
C)
CH3─
СН2─
СН2OH
D) C6H5OH
E) * СН2ОН─ СН2──
СН2ОН
8. Өндірісте сірке қышқылын алатын реакция теңдеуі
A) +[O]
НСОН → HCOOH
+[O]
B) * СН3─ СН2── СН2─CH3 → 2 CH3COOH
- Н2О
C) С2Н4 +[O] → CH3COOH
+ Н2О [O]
D) С2Н4 → CH3COH
→ CH3COOH
+ Н2О
E) С2Н2 → CH3COOH
9. Жоғары молекулалық қосылыстар мынадай болып бөлінеді
A) оксидтер және тұздар
B) қышқылдар және негіздер
C) оттекті және
оттексіз
D) қаныққан және қанықпаған
E) * табиғи және химиялық
10. 1 моль суйық судың түзілу жылуы 286 кДж тең болса, 7,2 г су түзілгенде жұмсалатые жылу мөлшері
A) 104,4 кДж
B) * 114,4 кДж
C) 102,2 кДж
D) 103,4 кДж
E) 110,4 кДж
11. Іс жүзінде суда ерімейтін зат
A) мыс купоросы
B) калий хлориді
C) қант
D) * күміс хлориді
E) кальций гидкроксиді
12. Күкірт қышқылы мен темір (ІІ) гидроксиді әрекеттескенде (егер негіздік тұз түзілсе) барлық қойылатын коэффициент саны
A) 8
B) 3
C) 2
D) 4
E) * 6
13. Бертолле тұзындағы ( KClO3) хлордың тотығу дәрежесі
A) +1
B) -1
C) * +5
D) 0
E) +7
14. 568 г фосфор (V) оксидін алу үшін жұмсалатын оттектің (қ.ж.) көлемі (л)
A) 56
B) 100
C) 112
D) 448
E) * 224
15. 2 г әктасты күйдіргенде 336 мл (қ.ж.) көмірқышқыл газы түзілді. Әктастағы қоспаның массалық үлесі
A) 30%
B) 75%
C) * 25%
D) 50%
E) 35%
16. Мыстың массалық үлесі көп қосылыс
A) CuS
B) CuO
C)
CuSO4
D) CuCl2
E) * Сu2О
17. Натрий гидроксидімен әрекеттесетін заттар қатары
A) Ag2S, BaSO4, PbSO4,
B) * СО2, CuCl2. HCl
C) SO2, BaSO4, H3PO4
D)
P2O5, HNO3,
K2SO4
E) Cl2, KCl, H2SO4
18. 2-метилбутадиен-1,3 молекуласындағы σ-байланыстың саны
A) 7
B) 11
C) 8
D) * 12
Е) 9
19. Химиялық өзгерістер тізбегіндегі Y заты
+ HBr
С2Н4 → X → Y → С2Н5 ─ O ─ С2Н5
A) ацетальдегид
B) бромэтан
C) диметил эфирі
D) * этанол
Е) этан
20. + Н2О +HJ t
Mg3N2 → A↑ → B → A↑ тізбегіндегі В затының молекулалық массасы
A) 278
B) 129
C) 17
D) * 145
E) 127
21. Массасы 10,3 г натрий бромидіне концентрлі күкірт қышқылымен әсер еткенде 0,896 л күкірт (ІV) оксиді бөлінді. Өнімнің шығымы
2 Н2SO4 + 2 NaBr → SO2 ↑ + Na2SO4 + Br2 + 2 Н2О
A) 60%
B) 90%
C) 75%
D) 78%
E) * 80%
22. Калий карбонаты мен темір (ІІІ) хлоридінің ерітінділері арасындағы реакция нәтижесінде түзілген темір қосылысының құрамы
A) Fe2(CO3)3
B) FeOHCO3
C)
FeCl3
D) * Fe(OH)3
E) Fe(OH)2
23. 14 г циклопентан 12 л хлормен (қ.ж.) әрекеттескенде, шығымы 70% болса, түзілген хлорциклопентанның массасы (г)
A) 15,6
B) 20,9
C) * 14,6
D) 11,9
E) 17,2
24. 5%-ті 200г глюкоза ерітіндісінен спирттік ашығанда түзілетін көмірқышқыл газының көлемі (л)
A) 2,89
B) 2,69
C) 2,09
D) * 2,49
E) 3,69
25. Мына заттың атауы
СН3
│
СН3 ─ С ─ СН── СН2 ─ СН2 ─ COOH
│
СН3 NH2
A) α-амино-ε,ε - диметилвалериан қышқылы
B) α,α -диамино - β -метилкапрон қышқылы
C) * γ-амино- δ,δ -
диметилкапрон қышқылы
D) δ - амино – α,α -диметилвалериан қышқылы
E) β- амино – δ,δ -диметилкапрон қышқылы
13-нұсқа
1. Құрамында 82% - азот және 18% сутегі бар белгісіз заттың формуласы
А) *NH3
В) N2O3
С) N2O5
D) NO
Е) NH4NO3
2. Реттік нөмірі 17-ші элементтің электрондық конфигурациясы
А) 3s23p2
В) 3s23p1
С) *3s23p5
D) 3s23p3
Е) 3s23p4
3. Концентрациялы азот қышқылы
А) тотықсыздандырғыш
В) *өте күшті тотықтырғыш
С) алтын мен платинаны ерітеді
D) металдармен әрекеттеспейді
Е) барлық металдарды пассивтендіреді
4. Сулы ерітіндіде тек анион бойынша гидролизденетін натрий тұзы
А) бромид
В) хлорид
С) *силикат
D) нитрат
Е) сульфат
5. Оттек газы
А) *түссіз
В) суда жақсы ериді
С) дәмді
D) өткір иісті
Е) ауада жеңіл
6. Электролиттерге жатады
А) спирт
В) металдар
С) бейметалдар
D) *тұздардың судағы ерітінділері
Е) қант
7. Сілтілік металдарға жатады
А) Na, Zn, Cu
В) Ca, Mg, Se
С) *К, Na, Li
D) Fe, Ca, Ni
Е) K, Ca, Mg
8. Органикалық қосылыстардағы көміртек атомдарының арасындағы химиялық байланысының түрі ....
А) иондық
В) * ковалентті полюссіз
С) сутектік
D) металдық
Е) ковалентті полюсті
9. Макромолекулаларда –CH2-HC=CH-CH2- қарапайым буыны бар зат:
А) *Бутадиен каучугі
В) Полипропилен
С) Полистирол
D) Хлоропренді каучук
Е) Полиэтилен
10. Кальцийдің сумен әрекеттесуінен түзілген күрделі заттың мольдік массасы:
А) 70 г/моль.
В) 80 г/моль.
С) 76 г/моль.
D) *74 г/моль.
Е) 78 г/моль.
11. Гидролизденетін тұз
А) NaCl
В) Na2O
С) *NaF
D) NaJ
Е) NaBr
12. Күкіртсутек толық жанбағанда түзілетін өнімдер:
А) * S, H2O
В) SO2, H2O
С) H2, SO2
D) SO3, H2O
Е) SO3, H2
13. 16,8 л аммиак синтездеу үшін (қ.ж) қажет сутектің көлемі
А) 72, 0 л
В) 30, 6 л
С) 33,6 л
D) *25,2 л
Е) 36,2 л
14. 200 г ізбестас ыдырағанда түзілетін көмірқышқыл газдың көлемі
А) 22,4 л
В) *44,8 л
С) 33,6 л
D) 5,6 л
Е) 11,2 л
15. Тұздар ерітіндісінен хромның ығыстырып шығаратын металы
А) марганец
В) * мыс
С) кальций
D) алюминий
Е) мырыш
16. Калий дихроматындағы хромның массалық үлесі (%)
А) 25
В) 65
С) *35
D) 55
Е) 45
17. Бензолдан бромбензол алу реакциясы
А) қосылу реакциясына жатады
В) *орын басу реакциясына жатады
С) ыдырау реакциясына жатады
D) жану реакциясына жатады
Е) тотығу реакциясына жатады
18. Массасы 60 г суда 1 моль формальдегидті ерітті. Ерітіндідегі формальдегидтің массалық үлесі:
А) 30,3 %
В) 50,3 %
С) *33,3 %
D) 40,3 %
Е) 32,3 %
19. Бензолдан, толуолдан, пентаннан, ксилолдан крекинг-бензинді ажырату жолы
А) *Қанықпаған көмірсутектерінің реактивтерімен (KМnO4, бром суы) қолдану.
В) Күміс нитратымен қолдану.
С) Күкірт қышқылының ерітіндісімен қолдану.
D) Ізбес суымен қолдану.
Е) Жағып, жалын арқылы.
20. Ацетиленнің жануының термохимиялық теңдеуі
2C2H2+5O24CO2+2H2O+2600 кДж.
Егер көлемі бойынша 20 % қоспасы бар, 25л ацетиленді (қ.ж.) жақса бөлініп шығатын жылу
А) 116,0 кДж.
В) 58 кДж.
С) 290 кДж.
D) *1160,7 кДж.
Е) 13,0 кДж.
21.
![]() өзгерістер тізбегінде
іске аспайтын стадиялар
өзгерістер тізбегінде
іске аспайтын стадиялар
А) 1,2
В) 2,3
С) 3,4
D) *1,3
Е) 1,4
22. 41 г натрий ацетатын 30 г натрий гидроксидімен әрекеттестіргенде (қ.ж.) түзілген метанның көлемі
А) *11,2 л
В) 1,4 л
С) 5,6 л
D) 2,8 л
Е) 22,4 л
23. Өзара әрекеттескенде үшіншілік бутил спиртін түзетін заттар жұбы:
А) * (CH3)2C=CH2 және H2O
В) (CH3)2CH2 және CH3Br
С) (CH3)3CCl және CH3Br
D) (CH3)3CH және NaOH
Е) (CH3)3CH және H2O
24. Техникада глюкозаны крахмалды гидролиздеу арқылы алады. Егер реакция өнімінің шығымы теориямен салыстырғанда 75 % болатын болса, 81 кг крахмалдан алынатын глюкозаның массасын есепте.
А) 36,5 кг
В) 69,5 кг
С) 48,5 кг
D) *67,5
Е) 56,5 кг
25. 10,3 г этиламиноацетатты алуға жұмсалатын аминосірке қышқылы мен этанолдың массасы
А) 7,8 г; 2,5 г
В) 6,8 г; 3,8 г
С) *7,5 г; 4,6 г
D) 6,2 г; 3,7 г
Е) 5,7 г; 2,5 г
14-нұсқа
1. Алмасу реакциясы
А) 2H2+O22H2O
В) 2KClO32KCl+3O3
С) *CuO+2HClCuCl2+ H2O
D) N2+3H22NH3
Е) Fe+CuCl2 FeCl2 +Cu
2. Ядродағы протон саны ...
А) топ нөмірін көрсетеді
В) период нөмірін көрсетеді
С) *рет нөмірін көрсетеді
D) ұшқыш сутекті қосылыстардың жалпы фомуласын көрсетеді
Е) жоғарғы оксид формуласын көрсетеді.
3. Алмаздың кристалл тор түйіндерінде орналасқан бөлшектер
А) аниондар
В) *атомдар
С) атомдар және молекулалар
D) катиондар
Е) молекулалар
4. Катион болып есептелетін бөлшек
А) SO42-
В) Cr2O72-
С) *NH4+
D) NO3-
Е) Сl-
5. Өнеркәсіпте оттегін алу әдісі
А) Ауаны ығыстыру әдісі
В) Суды ығыстыру әдісі
С) *Ауаны қысып, сұйылтуып, айдау
D) Электр тогы әсерімен суды айыру
Е) Сынап оксидін қыздырғанда
6. Қышқыл тұз
А) Na3PO4
В) *NaH2PO4
С) CuOHCl
D) K2NaPO4
Е) Ca3(PO4)2
7. Натрий атомының электрондық конфигурациясы:
А) *1s22s22p63s1
В) 1s22s22p63s23p63d104s1
С) 1s22s22p63s23p63d54s1
D) 1s22s22p1
Е) 2s22s1
8. Жалпы формуласы CnH2n-6 болатын қатардың мүшесі
А) нафталин
В) тротил
С) *бензол
D) бензин
Е) фенол
9. Метанальдің судағы 40%-тік ерітіндісі:
А) Алколят
В) Фенолят
С) *Формалин
D) Ацетат
Е) Этиленгликолят
10. Натрий нитратының 500 г 7 %-ті ерітіндісіне 200 г су қосқанда алынған ерітіндідегі NaNO3-тің массалық үлесі:
А) 1%
В) 2%
С) *5%
D) 4%
Е) 3%
11.
![]() тізбегіндегі Х, Ү
заттары
тізбегіндегі Х, Ү
заттары
А) MgO, Mg(OH)2
В) * MgOHCl, Mg(OH)2
С) MgOHCl, MgO
D) MgO, MgOHCІ
Е) Mg(OH)2, MgO
12. Лабораторияда HCl-ды алу үшін қажет H2SO4 мен NaCl–дың жағдайлары:
А)* NaCl(кат.)+H2SO4(конц.)![]()
В) NaCl(балқыма)+H2SO4(сұйт.)
С) NaCl(ертін)+H2SO4(сұйт.)
D) NaCl(ертін)+H2SO4(конц.)
Е) NaCl(кат.)+H2SO4(сұйт.)
13. H2O- H2S- H2Sе- H2Те – қатарында қышқылдар күшінің өзгеруі:
А) Кемиді
В) Артады, соңынан кемиді
С) Өзгермей қалады
D) *Артады
Е) Кемиді, соңынан артады
14. Азоттың ауа бойынша тығыздығы:
А) 0,25
В) *0,96
С) 0,74
D) 0,53
Е) 0,82
15. Оттектің массалық үлесі көп зат
А) PbO2
В) *CO2
С) SnO2
D) GeO2
Е) SiO2
16. Электролиз кезінде анодта жүретін процесс:
А) Айырылу
В) Орын басу
С) Тотықсыздану
D) *Тотығу
Е) Алмасу
17. Таза никель алуға болатын тәсіл
А) *Электрометаллургия
В) Көміртектітермия
С) Алюмотермия
D) Сутектітермия
Е) Металлотермия
18. 4,4 демителгексен-2 құрамына сәйкес заттың жалпы формуласы.
А) CnH2n+2
В) *CnH2n
С) CnH2n-6
D) CnH2n-4
Е) CnH2n-2
19. Мына өзгерістер схемасындағы А заты:
(C6H10O5)n C6H12O6A С2 H5OC2H5
А) * C2H5OH
В) CO2
С) CH3OH
D)
CH3 - CH – COOH
|
OH
Е) CH3COOH
20. 2NO+O22NO2+Q теңдеудегі тепе-теңдікті оңға ығыстыратын факторлар нөмірлері.
1. Оттектің концентрациясын көбейту
2. Азот (ІІ) оксидінің концентрациясын кеміту
3. Температураны арттыру
4. Қысымды азайту
5. Температураны төмендету
6. Қысымды арттыру
7. Катализатор қолдану.
А) *1 5 6.
В) 2 4 6
С) 1 4 6
D) 2 5 6
Е) 1 3 5
21. Егер дегидрлегенде 56 л сутек бөленетін болса, жұмсалған циклогексанның, түзілген бензолдың массалары
А) 30 г, 25 г,
В) *70 г, 65 г
С) 50 г, 45 г
D) 40 г, 35 г
Е) 60 г, 55 г
22. 35 г метил спиртінен 12 г диметил эфирі алынған болса, диметил эфирдің шығымы:
А) 88 %
В) 58 %
С) 68 %
D) *48 %
Е) 78 %
23. Массасы 360 кг глюкоза ашығанда, 300кг этил спиртінің ерітіндісі алынған. Осы ерітіндідегі спирттің массалық үлесі
А) 61,2
В) 61,4
С) *61,3
D) 60,0
Е) 61,1
24. Егер бірінші және екінші сатысында түзілген заттың шығымы 50%, ал соңғы сатысында 100 % болса, 33 г 2,4,6-триброманилин алу үшін қажет бензолдың массасы
А) 30,0 г
В) *31,2 г
С) 32,0 г
D) 29,2 г
Е) 32,8 г
25. 50 г полипропиленді толық жағу үшін қажет (қ.ж.) ауаның көлемі (Ауадағы оттектің көлемдік үлесі – 0,2.)
А) 400 л
В) 500 л
С) * 600 л
D) 700 л
Е) 300 л
16 нұсқа
-
Күрделі зат
А) Графит
В) *Су
С) Күкірт
D) Сутек
Е) Алмаз
-
VІ – топтың негізгі топшасы элементтерінің атомдарының электрондық конфигурациясының жалпы формуласы
А) ns2 np6
В) *ns2 np4
С) ns2 np5
D) ns2 np2
Е) ns2 np3
-
Ковалентті полюссіз байланысы бар қосылыс
А) натрий хлориді
В) хлорлы сутек
С) су
D) *оттек
Е) сутек пероксиді
-
Ион алмасу реакциясы
А) NH3+ H2O = NH4OH
В) *CaCl2+Na 2CO3=CaCO3+2NaCl
С) Zn+SnCl2=ZnCl2+Sn
D) NH3+HCl=NH4Cl
Е) Zn+Cl2=ZnCl2
-
Оттек жай зат түрінде... құрамында кездеседі
А) *атмосфера
В) дистилденген су
С) құм
D) гранит
Е) әктас
-
Алюминий гидроксидімен тұз қышқылы әрекеттескенде түзілетін орта тұз
А) Al (OH)3
В) *Al Cl3
С) AlOHCl2
D) Al2O3
Е) Al(OH)2Cl
-
Ерітіндісі жалынды кірпіш қызыл түске бояйтын қосылыс
А) ерігіш шыны
В) *ғаныш
С) кір сабын
D) сильвинит
Е) ас содасы
-
Циклопентанға тән жалпы формула
А) CnH 2n+2
В) CnH2n-2
С) CnH2n-6
D)* CnH2n
Е) CnH2n-1
-
Табиғи жоғары молекулалық қосылыстарға жататын зат:
А) глюкоза
В) *целюлоза
С) мальтоза
D) сахароза
Е) полиэтилен
-
Al2O3 +6HCl = 2AlCl3+3H2O +Q үрдісінің сипаты
А) *қайтымсыз және гетерогенді
В) қайтымсыз және гомогенді
С) қайтымды және экзотермиялық
D) қайтымсыз және эндотермиялық
Е) қайтымды және гетерогенді
-
250г 2% -ті ерітінді дайындау үшін қажет натрий хлоридінің массасы
А) *5г
В) 2г
С) 4г
D) 1г
Е) 3г
-
Егер күкірттің молярлық массасы 256г/моль болса, ондағы күкірттің атомдарының саны
А)* 8
В) 4
С) 7
D) 2
Е) 6
-
49г фосфор қышқылын алу үшін қажет фосфор (Ү) оксидінің массасы (г) және зат мөлшері (моль)
А) 14,8 және 0,15
В) 54,3 және 0,55
С)* 35,5 және 0,25
D) 48,2 және 0,45
Е) 32,8 және 0,35
-
Қозған күйіндегі конфигурациясы ... 3s13p33d0 болатын элемент
А) Sn
В) *Si
С) C
D) Al
Е) N
-
49г фосфор қышқылын алу үшін қажет фосфор (Ү) оксидінің массасы (г) және зат мөлшері (моль)
А) 14,8 және 0,15
В) 54,3 және 0,55
С)* 35,5 және 0,25
D) 48,2 және 0,45
Е) 32,8 және 0,35
-
Өзгерістер сызба-нұсқасында
+Cl2 +NaOH +HNO3 t0
Fe X1 X2 X3 X4
X1 және X4 заттары
А) Fe Cl2 және Fe2О3
В) Fe Cl2 және Fe
С) Fe Cl2 және FeО
D)* Fe Cl3 және Fe2О3
Е) Fe Cl3 және Fe(NО2)2
-
Этил спиртінен бутадиенді алғаш алған ғалым
А) В.В. Марковников
В) Н.Н. Семенов
С) М.В. Ломоносов
D)* С.В.Лебедев
Е) Н.Д.Зелинский
-
Этанол мен реакцияға түсетін зат:
А)* HBr
В) KBr
С) Ba (OH)2
D) NaOH
Е) H2O
-
22г этанальды гидрлегенде түзілген спиртті 177 мг суда ерітілді, ерітіндідегі спирттің массалық үлесі:
А) 11%
В) 10%
С) 14%
D)* 11,5%
Е) 13%
-
16г темір (ІІІ) оксидін толық тотықсыздандыру үшін қажет сутегінің мөлшері тең
А) 0,1 моль
В) 5 моль
С)* 0,3 моль
D) 3 моль
Е) 2 моль
-
20л 36,5% -ті тұз қышқылы ерітіндісін (р= 1,18г/мл) даярлау үшін (қ.ж.) қажет хлордың көлемі
А) 7,92м3
В)* 2,64 м3
С) 1,32м3
D) 5,28м3
Е) 4,44м3
-
13г пропенмен қосылу реакциясына түсетін бромның массасы:
А) 52,4г
В) 48г
С)* 49,5г
D) 32г
Е) 45,6г
-
575мл спирт (р= 0,8г/мл) алу үшін жұмсалатын глюкозаның массасы
А) 950г
В) 850г
С)* 900г
D) 970г
Е) 800г
-
Көлемі 8л метиламинді жағуға қажет ауаның (оттекті ң ауадағы көлемдік үлесі 0,2) (қ.ж.) көлемі:
А) 18л
В) 56л
С)* 90л
D) 8л
Е) 45л
-
Сызбанұсқадағы С заты:
+Н2О + NaOH NaOH, t0
Глицилглицин А В С
А)* CH3NH2
В) CH3COONa
С) C6H6
D) C2H6
Е) CH3COOH
17 нұсқа
-
Алмасу реакцияларында газдың түзілуі.
А) Қайтылымдықтың белгісі
В)* Қайтымсыздықтың белгісі
С) Экзотермиялықтың белгісі
D) Эндотермиялықтың белгісі
Е) Айырылудың белгісі
-
Химиялық қасиеттері ұқсас элементтер
А) Li және Be
В) Be және Ba
С) Na және Ag
D)* Li және Na
Е) Be және B
-
Беймолекулалық құрылысты зат
А)*NaH
В) CH4
С) H2O
D) NH3
Е) HNO3
-
Диссоциацияланғанда NO3- түзетін зат
А) KNO2
В) K2SO3
С) *NaNO3
D) H3PO4
Е) Fe (OH)3
-
Агрегаттық күйі сутекпен бірдей зат
А) Na
В) Ca
С) Al
D) *He
Е) S
-
Амфотерлі оксидтің қасиеті
А) сумен және қышқылмен әрекеттесуі
В) қышқылмен және қышқылдық оксидтермен әрекеттесуі
С) тұзбен және қышқылмен әрекеттесуі
D)* қышқылмен және негізбен де әрекеттесуі
Е) тұзбен және негізбен әрекеттесуі
-
Оттекті қышқыл -
А) *HNO3
В) HCl
С) CaO
D) CO2
Е) Zn (OH)2
-
Молекула құрамы бірдей болғанымен, құрылымы өзгеше болғандықтан, қасиеттері де өзгеше болатын органикалық заттар атауы
А) гомологтар
В) дальтонидтер
С) изотоптар
D) *изомерлер
Е) бертоллидтер
-
Химиялық синтез арқылы және өсімдіктерден алынатын жоғарғы молекулалы полимер
А) целюлоза
В) гликоген
С) резеңке
D) *каучук
Е) крахмал
-
Термохимиялық теңдеу бойынша: 4Р + 5О2 = 2Р2О5 + 3010кДж 62г фосфор жанғанда бөлінетін жылу мөлшері
А) 1485кДж
В) 1450кДж
С) 1350кДж
D)* 1505кДж
Е) 1400кДж
-
290г 20%-ті ерітінді дайындау үшін қажет натрий бромидінің массасы:
А) 48г
В) *58г
С) 29г
D) 14г
Е) 43г
-
Бөлшектердің саны көп зат:
А)* 224л Cl2
В) 254г J2
С) 38г F2
D) 160г Br2
Е) 160г O2
-
Аниондардың тотықсыздандырғыш қасиеттерінің арту қатары
А) *O 2-S 2-Se2-
В) Te2- Se2- S2-
С) Se2- Te2- S2-
D) S2-O2- Te2-
Е) Se2- Te2- Se2-
-
Қосылыстардағы азотттың ең көп массалық үлесі бар зат:
А) HNO3
В) Ca(NO3)2
С) N2O5
D)*NO
Е) KNO3
-
100л көміртек (ІІ) оксиді жанғанда қажет болатын оттектің көлемі (қ.ж.):
А) 100 л
В)* 50 л
С) 75 л
D) 150 л
Е) 125 л
-
32 г мыс ұнтағы 11,2 л оттек (қ.ж) бар ыдыста қатты қыздырылды. Түзілген оксидтің массасы:
А) *40 г
В) 20 г
С) 60 г
D) 2 г
Е) 0,4 г
-
102 г пентадиен – 1,3 зат мөлшері (моль)
А) 5,4
В) 2,3
С) 3,1
D)* 1,5
Е) 4,2
-
1,2,3-трихлорпропаннан глицерин алу үшін қажет зат:
А) С3Н6
В) СН3СООН
С) НВr
D) *H2O
Е) Na
-
22% 150г құмырсқа қышқылын бейтараптауға жұмсалатын натрий гидроксидінің массасы
А) 25,6г
В)* 28,7г
С) 22,3г
D) 26,3г
Е) 21,6г
-
40г мыс (ІІ) сульфаты бар ерітіндіге 16г темір ұнтағын қосқанда бөлінген мыстың массасы:
А) 40г
В) 24г
С) 28г
D)* 16г
Е) 32г
1 2 3 4
-
ККОНКCl KNO3 KNO2 өзгерістер тізбегіндегі әрекеттесетін реагенттердің дұрыс реті
А) O2,HCl, HNO3, O2
В) H2O, HCl, HNO3, O2
С)* H2O, CuCl2, AgNO3, t0
D) O2, CuCl2, AgNO3, O2
Е) H2O, HCl, AgNO3, H2O
-
Циклопарафиндердегі көміртектің массалық үлесі (%)
А) 95,7
В) 55,7
С)* 85,7
D) 65,7
Е) 75,7
-
Массасы 64,8г крахмалдан алынған глюкозаның шығымы 80% болса , осы глюкозаны күміс оксидінің аммиактағы ерітіндісімен тотықтырғанда тұнбаға түскен күмістің массасы
А) 69,18г
В) 69,16г
С)* 69,12г
D) 68,13г
Е) 69,95г
-
10,53г метиламинбутилат алу үшін шығымдылығы 90% болса, жұмсалатын амин қышқылы мен спирттің маасалары
А) 10,8г; 5,2г
В 1,5г ; 3,7г
С)* 10,3г; 3,2г
D) 8,7г ; 4,5г
Е) 9,5г ; 4,2г
-
11,2л (қ.ж.) сутек бөліну үшін натрий мен әрекеттесетін фенол және метанолдың массалары
А) 188г, 64г
В) 128г, 56г
С) 142г, 60г
D) *94г, 32г
Е) 150г, 30г
18 нұсқа
1.Химиялық реакцияның белгісі
А) балқуы
В) ұнтақталуы
С)* түс өзгеруі
Д) жылтырауы
Е) еруі
2.Электрондық конфигурациясы 1s2 2s2 2p6 болатын элемент
А) O
В) F
С)* Ne
Д) Ca
Е) C
3.Бромсутек молекуласында химиялық байланысты түзуге қатысатын электрон саны
А) 4
В) *2
С) 6
Д) 18
Е) 3
4.Сl- анионына реактив болатын зат
А) *Күміс нитраты
В) Натрий оксиді
С) Алюминий гидроксиді
Д) Калий нитраты
Е) индикатор
5.Қыздырғанда оттегімен әрекеттеспейді
А) темір
В) күкірт
С) фосфор
Д)* алтын
Е) мыс
6.Іс жүзінде жүрмейтін реакцияның схемасы
А![]() ) BaO
+H2O
) BaO
+H2O
В![]() ) SO2 +
H2O
) SO2 +
H2O
С![]() )* CuO+ H2O
)* CuO+ H2O
Д![]() ) P2O5 + H2O
) P2O5 + H2O
Е![]() )CaO +
H2O
)CaO +
H2O
7.Алкендер класының сипаттамасына жатпайды
А) кеңістікте молекуланаң құрылысы жазықтық
В) *гибридтену түрі sp3
С) валенттілік бұрышы 1200
Д) 1п байланыс
Е) С=С байланысының ұзындығы 0,134нм
8.Күрделі эфирлердің жалпы формуласы
А) R- NH2
В) ROR1
С) R-OH
Д)* RCOOR1
Е) NH2-R-COOH
9.Полиэтилен- ... полимер болады
А) әрі табиғи, әрі химиялық
В)* химиялық, синтетикалық
С) табиғи, өсімдік текті
Д) табиғи, жануар текті
Е) химиялық жасанды
1![]() 0.2HgO (қ) 2Hg (қ) + O2(г) –Q
0.2HgO (қ) 2Hg (қ) + O2(г) –Q
т![]() еңдеуінде
тепе-теңдікті оңға ығыстыратын жағдай
еңдеуінде
тепе-теңдікті оңға ығыстыратын жағдай
А) қысымды көтеру
В) температураны төмендету
С)* қысымды төмендету
Д) катализатор енгізу
Е) О2 концентрациясын арттыру
11.Гидроксоний ионындағы оттектің валенттілігі
А) *3
В) 1
4С)
Д0)
Е) 2
12.168г калий гидроксиді 63г азот қышқылымен әрекеттескенде түзілетін тұздың мөлшері (моль)
А) 4
В) 3
С) 0,5
Д) *1
Е) 2
13.Хлордың жалпы қасиетіне сай емес тұжырымдама:
А) Сары жасыл түсті,өткір иісті газ
В)* Тек тотықтырғыштық қасиеттері болады
С) Суда еріп,хлор суын түзеді
Д) Исі бар
Е) Ауадан 2,5 есе ауыр
14.6,12 мл суда 44,8 (қ.ж) күкіртсутек ерітілген. Ертіндідегі H2S- тің (%)
Массалық үлесі:
А)2,6%
В)*10%
С) 5,2%
Д) 12%
Е) 10,6% Fe
15.Аммиактың зертханада алыну реакциясы
А![]() ) NH4OH
+HNO3 NH4NO3+H2O
) NH4OH
+HNO3 NH4NO3+H2O
В![]() ) N2 +3H2
2NH3
) N2 +3H2
2NH3
С![]()
![]() ) *2NH4Cl+Ca(OH)2
CaCl2+2NH3
+2H2O
) *2NH4Cl+Ca(OH)2
CaCl2+2NH3
+2H2O
Д![]()
![]() ) 3NH3+H3PO4 (NH4)3PO4
) 3NH3+H3PO4 (NH4)3PO4
Е![]() ) NH4NO3 N2O
+2H2O
) NH4NO3 N2O
+2H2O
16.Көміртекпен қосылысы этинді алуға қолданатын металл:
А)Ba
В) Mg
С) K
Д) *Ca
Е) Na
17.Магниймен барлығы әрекеттесетін заттар тобы
А)*HCl , CO2 , FeSO4
В) HBr , H2O ,MgCl2
С) HNO3 ,KOH ,O2
Д) H2SO4 , H2O ,KCl
Е) H2SO4 , NaOH , H2O
18.Тек екіатомды спирттерге жататын зат:
А) *CH3 – CHOH- CHOH- C2H5
В)CH3-CH-CH3
![]()
CH2OH
С) CH3CH2OH
Д) CH2OH-CHOH-CH2-OH
Е) CH2OH-CHOH-CH-CH3
![]()
OH
19.Заттардың барлығы сутекті қосып ала алмайтын топ:
А) C2H4 , C6H6
В) C2H2 , CH3OH
С)*C3H8 , CH3NH2
![]()
![]() O
O
Д) CH3-C , C6H6
![]() H
H
Е)C2H2 , C3H4
20.Массасы 12г алюминий мен мыс(II) оксидтерінің қоспасы натрий гидроксидімен әрекеттескенде 11,25г натрий металюминаты түзілді.
Қоспадағы мыс оксидінің массасы:
А)9г
В) *5г
С) 7г
Д)6г
Е) 18г
21.Тотығу үрдісінің сызба-нұсқасы
А![]() )CrO4-2 Cr +3
)CrO4-2 Cr +3
В![]() )* Fe+3
FeO4-2
)* Fe+3
FeO4-2
С![]() ) Cr2O7-2
Cr0
) Cr2O7-2
Cr0
Д![]() ) MnO4-2
Mn+2
) MnO4-2
Mn+2
Е![]() ) MnO4-
MnO4-2
) MnO4-
MnO4-2
22.Құрамы 90% метан, 5%этан, 3%көміртек диоксиді және 2% азот газдарынан тұратын қоспанвң 50м3 көлемін жағу үшін қажет ауаның
көлемі (м3)
А)465
В) 486
С)* 497
Д)470
Е) 473
23.4г кальций карбидінен алынған ацетиленді толық гидрлегенде шығымы
75 % болса, алынатын этанның көлемі (қ.ж)
А)*1.05
В) 2.05
С) 3.05
Д)4.05
Е) 5.05
24.Егер шығымы 90%, ал картоптағы крахмалдың массалық үлесі 20% болса, 100кг картоптан алынатын глюкозаның массасы
А)21
В) 22
С) 24
Д)*20
Е) 23
25.Дипептид глицилглициндегі көміртектің массалық үлесі
А)8,36%
В) 21,36%
С) 40,36%
Д)*36,36%
Е) 35,36%
19- нұсқа
1. Fe3O4+Al арасындағы реакцияның типі.
А) Қосылу
В) Айырылу
С) * Орын басу
D) Алмасу
E) Бейтараптану
2.Сыртқы энергетикалық деңгейіндегі электрондық формуласы 4s24p4 болатын элемент атом.
А) Cr
В) Ti
С) * Se
D) Ge
E) S
3. Терісэлектрлігі өте алшақ атомдардың арасында болатын байланыс.
А) ковалентті полюсті
В) донор акцепторлы
С)* иондық
D) сутектік
E) ковалентті полюссіз
4.Ең күшті қышқыл.
А)* H2SO4
В) H2SiO3
С) H2SO3
D) H3PO4
E) H2CO3
5. Периодтық жүйедегі күкірттің орны.
А) 5-ші период VI B тобы
В) 2-ші период VI A тобы
С)* 3-ші период VI A тобы
D) 6-шы период II B тобы
E) 4-ші период VI A тобы
6. Қышқыл оксидтің формуласы.
А) ZnO
В) CaO
С)* Cl2O7
D) Na2O
E) Fe2O3
7. Пропеннің гомологы болмайтын зат.
А)* C4H6
В) C7H14
С) C5H10
D) C6H12
E) C2H4
8. 2,3,3- триметилпентан қышқылының формуласы.
А![]() ) CH3
) CH3
H3C –C – CH2 – CH2 – COOH
![]()
CH3
В) C2H5
![]() H3C – C – CH2
– CH2 - COOH
H3C – C – CH2
– CH2 - COOH
![]()
CH3
CH3
![]()
С) * H3C – CH2 – C – CH – COOH
![]()
![]()
CH3 CH3
D) H3C – CH2 – CH2 – CH – COOH
![]()
C2H5
E![]() ) H3C – CH – CH – CH2 – COOH
) H3C – CH – CH – CH2 – COOH
![]()
CH3 CH3
9. Ашық тізбекті глюкоза молекуласындағы гидроксил тобының саны.
А) 1
B)* 5
C) 3
D) 4
E) 2
10. 2 моль метан жанғанда 1604 кДж жылу бөлінетін болса, химиялық реакцияның жылу эффектісі CH4( r ) +2O2( r )= CO2 ( r )+2H2O + Q
А) 803 кДж
B)* 802 кДж
C) 804 кДж
D) 816 кДж
E) 798 кДж
11. Калий хлоридінің 400г 10%-ті және 100г 5%-ті ерітінділерін қосқанда алынған ерітіндідегі KCl – дың массалық үлесі.
А)* 9%
B) 7%
C) 8%
D) 10%
E) 6%
12. Өзгерістер тізбегінің осы стадиясында қышқыл қатысады.
N


 2 1
NH3 2 NH4Cl 3
NH3 4 N2
2 1
NH3 2 NH4Cl 3
NH3 4 N2
A) 1
B)* 2
C) 3
D) 4
E) 1,4
13. KClO3 – тегі барлық ковалентті байланыстардың саны.
A) 6
B) 2
C) 3
D)* 5
E) 4
14. 8 моль азот қышқылы айырылғанда бөлінетін оттектің мөлшері.
A) 1 моль
B) 8 моль
C)* 2 моль
D) 4 моль
E) 3 моль
15. Ерітінділері сілтілік орта көрсететін заттар.
A) Na2SO3 , K2SO4
B) Na2CO3 , K2SO4
C)* Na2CO3 , K2SiO3
D) Na2SiO3 , KNO3
E) NaNO3 , K2CO3
16. Катодта жүретін процесс.
A) Айырылу
B)* Тотықсыздану
C) Диссоциация
D) Тотығу
E) Бейтараптану
17. Өзгерістер тізбегіндегі тұнба түзілетін реакциялар.
C


![]() uO 1 CuCl2
2 Cu(OH)2 3
CuSO4 4 Cu3(PO4)2
uO 1 CuCl2
2 Cu(OH)2 3
CuSO4 4 Cu3(PO4)2
A)* 2.4
B) 1.3
C) 3.4
D) 2.3
E) 1.2
18. Орташа молекулалық массасы 100000 – ға тең полипропиленнің полимерлену дәрежесі және бір макромолекуласын синтездеуге жұмсалатын пропиленнің ( қ.ж ) көлемі.
A)* 2381;53,4 м3
B) 2431;49,4 м3
C) 2452;48,5 м3
D) 2331;52,5 м3
E) 2385;46,7 м3
19. Ацептиленнен тікелей алынатын заттар.
A) глицерин, фенол
B) глюкоза, метаналь
C)* этаналь, бензол
D) толуол, бутаналь
E) крахмал, этаналь
20. Құрамында 45% күкірті бар 1т пириттен шығымы 98% болса, түзілетін күкіртті газдың массасы (г)
A) 0,68
B) 0,78
C)* 0,47
D) 0,98
E) 0,88
21. Өзгерістер тізбегіндегі.
N


 a +O2 A t0 B
HNO3 C t0
D
a +O2 A t0 B
HNO3 C t0
D
A және D заттары:
A) Na2O және NaOH
B)* Na2O2 және NaNO2
C) Na2O2 және NaNO3
D) Na2O және Na2N
E) Na2O және NaNO3
22. Құрылысы төмендегідей заттың дұрыс аты:
CH3 C2H5 Br CH3
![]()
![]()
![]()
![]()
![]() Br – CH2
– CH – C – C – CH – CH3
Br – CH2
– CH – C – C – CH – CH3
![]()
Br Br
A) Тетрабром – диметил – этилгексан.
B) 2- метил -3,3- дибром -4-бром -4-этил – 5-метил – 6-бром.
C)* 1,3,4,4- тетрабром -2,5- диметил – 3-этил гексан.
D) Триметил – этил – бромметил – трибромбутан.
E) 5- метил – 3 – этил -4,4- дибром –пентан.
23. 39 г бензолды хлорлағанда 0,25 моль хлорбензол алынса, түзілген заттың шығымы (%-пен )
A) 30%
B) 40%
C) 70%
D)* 50%
E) 60%
24. Егер шығымы 55% болса, онда 30кг көміртек (II) оксиді бар синтез газдан түзілетін метанолдың массасы.
A)* 18,9кг
B) 23,9кг
C) 19,9кг
D) 21,9кг
E) 15,9кг
25. 15г сірке қышқылынан (әр сатысының шығымы 75% болса) алынатын 15% - тік аминсірке қышқылының массасы.
A) 75,3г
B) 67,8г
C)* 70,3г
D) 65,8г
E) 71,5г
20-нұсқа
1. 3 моль магний жанатын болса,түзілетін магний оксидінің зат мөлшері
а) 2,5 моль
в)* 3 моль
с) 2 моль
d) 1.5 моль
е) 4 моль
2. периодтық жүйенің үшіншісі периодын аяқтайтын элементтің сыртқы электрон қабатындағы электрондар саны
а)* 8
в) 6
с) 18
d) 14
e) 2
3. oң және теріс зарядталған бөлшектер
а) протон
в)* иондар
с) ядро заряды
d) атомдық масса
e) нейтрон
4. бейэлектролиттер деп... заттарды айтамыз
а) электр тоғын өткізетін
в) металдар
с) өзгеріссіз
d)* элект тоғын өткізбейтін
e) өзгеретін
5.тек қышқылдық қасиет көрсететін оксидтер
а)* so2
b) al2o2
c) mgo
d) cao
e) na2o
6. тек амфотерлі оксидтердің қатары
а)*al2o3 zno
b) beo2
c) zno, mgo
d)feo, no
e) zno, cao
7. кальций гидроксидімен әрекеттесетін зат
а)*co2
b)na 2
c)nacl
d)naoh
e)na2so4
8. молекуладағы атомдардың орналасу реті ... қарай анықталады .
а) атомдардың санына
b) тотығу дәрежесіне
c)* валенттілігіне
d)атомдардың түріне
e)салыстырмалы атомдық массасына
9. «көмірсулар»деп аталу себебі
а)алғашқы өкілдері хош иісті болған
b)*алғашқы зерттелген өкілдері көміртегі мен судан тұрған
c)құрамында гидроксил тобының болуына байланысты
d)құрамында карбонил тобының болуына байланысты
e)құрамында карбоксил тобының болуына байланысты.
10. этиленнің жану реакциясының термохимиялық теңдеуі: с2н4+3о 2=2со2+2н2о +1400 кдж, егер реакцияға 336л оттегі кірісетін болса, бөлінген жылудың мөлшері.
а) 5000 кдж
b) 8000кдж
c) 4000кдж
d)* 7000кдж
e) 6000кдж
11. судың молекуласының құрылысы
а) сызықтық
b)*бұрыштық
c) тетраэдрлік
d) жазықтық
e)зигзаг тәрізді
12. натрий гидроксидінің ерітіндісімен әрекеттесетін оксидтер қатары.
а) cro мен p2o 5
b)* ai2 o3 пен р2 о5
c) со мен р2 о5
d) al2 о3 мен со
e) сro мен со
13. натрий хлоридінің балқымасын электролиздегенде түзілетін заттар.
а) оттек пен хлор
b) оттек пен натрий гидроксиді
c)* хлор мен натрий
d) хлор мен натрий гидроксиді
e) натрий мен оттек
14. азот қосылыстарының формулалары берілген:
1.nh3; 2.n 2o5; 3. нno2 ; 4. n2o; 5. no. олардың азот атомының тотығу дәрежесінің кему ретімен орналасуы.
а) 5 4 3 2 1
b) 1 2 3 4 5
c)* 2 3 5 4 1
d) 2 4 3 5 1
e) 3 2 5 4 1
15. кальций оксидіне көмір қосып қатты қыздырғанда түзілетін газ
а)*со
b)со2
c)о2
d)н2
e)n2
16. мыс (ii) сульфаты ерітіндісін электролиздегенде түзілетін заттар:
(электродтар инертті)
а)*сu,o2
b)cu,so3
c)h2,o2
d)cu,so2
e)cu,h2
17. егер реакция нәтижесінде тек темір (iii) гидроксиді түзілген болса, онда реакцияға қатысатын заттар:
а)fe2o3 және h2o
b)fe және h2o2
c)*fe(oh)2 және h2o2
d)fe3o4 және h2o
e)feo және h2o
18.390г бензолды гидрлегенде 336г циклогексан алынған.реакция өнімінің шығымы
а)100%
b)95%
c)*80%
d)85%
e)90%
19. реакция өнімінің шығымы 70% болса, 330г ацетальдегидтен алынатын сірке қышқылының массасы(г)
а)*315
b)405
c)360
d)270
e)450
20. 79,2г темір (ii) сульфидіне артық мөлшерде тұз қышқылын қосып, түзілген газды натрий гидроксидінің 15-%-тік 240г ерітіндісі арқылы өткізгенде түзілген тұздың формуласы және массасы:
а)nahso4 , 40,4г
b)na2s, 50,4г
c)*nahs, 50,4г
d)na2so4 , 50,4г
e)na2so3, 44,4г
21.егер реакцияның шығымы 80% болса, 40 грамм метанды толық хлорлағанда түзілетін тетрахлорметанның массасы:
а)279г
b)285г
c)*308г
d)315г
e)320г
22. егер пропанол-1 дегидрациялап, алынған қосылысқа хлорсутекпен әсер етсек түзілетін өнім
а)1,2-дихлорпропан
b)*2-хлорпропан
c)хлорлы этил
d)винилхлорид
e)пропилхлорид
23. 190г 2% аминсірке қышқылының ерітіндісімен әрекеттесетін пропанолдың массасы
а)*3г
b)9г
c)18г
d)15г
e)6г
24. құрамында 45% этилен бар 500л этиленнің (қ.ж.)
этанмен қоспасынан алынатын полиэтилен массасы
а)320,38г
b)250,65г
c)380,25г
d)*281,25г
e)311,25г
25. өзгерістердің нәтижесінде түзілетін "d" заттың аталуы
+hono2 +[h]
c
 h4→c2h2→c6h6 a d
h4→c2h2→c6h6 a d
a)нитробензол
b)нитрозобензол
c)нитрофенол
d)*анилин
e)фенол
21-нұсқа
1.Орынбасу реакциясы:
А) Fe +S→
В) Cu (OH)2 →
С) ZnO +H2 SO4 →
D)* Zn + 2 HCl →
Е)Ca (OH)2 + 2 HCl →
2.Алтыншы периодтағы барлық элементтер саны
А) 2
В)* 32
С) 1
D) 23
Е) 8
3.Тотығу процесі
А) Заттың агрегаттық күйінің өзгеруі
В) элементтің валенттілігінің өзгеруі
С) электронды қосып алу
D)* электронды беру
Е) иондарды қосып алу
4)Иондық алмасу реакциясының нәтижесінде көміртек(IV)оксидің түзетің заттар:
А) Fe(NO3) 2 және NaCl
В)* Na2CO3 және H2SO4
С) K2SO4 және BaCl2
D) CuCl2 және KOH
Е) HCl және Al(OH)3
5. Сутек изотопы-протийдің таңбалануы
А)* 1H
В) 2H
С) 2H
D) 3H
Е) 1H
6.Сөндірілген ізбестің формуласы
А) CaO
В)* Ca(OH)2
С) Ca(HCO3)2
D) CaCO3
Е) CaHCO3
7.Қаныққан көмірсутектерді халықаралық номенклатура бойынша атағанда алдымен молекуладағы көміртек қанқасының…табады:
А) ацилді тізбегін
В) ең қысқа тізбегін
С)* ең ұзын тізбегін
D) цикілді тізбегін
Е) тармақты тізбегін анықтап алады
8.Альдегидтердің молекулалық массалары өсуіменбірге
А) суда ерігіштігі артады
В)* суда ерігіштігі кемиді
С) қайнау температуралары кемиді
D) қайнау температуралары өзгермейді
Е) тығыздығы кемиді
9.Жоғары молекулалық қосылыс-
А)* малекуласы қайталанып отыратын атомдар тобынан тұратын молекулалық массасы өте үлкен заттар.
В) 2 атомнан тұратын зат.
С) қайнау температурасы төмен заттар.
D) тек тірі организмдерде кездесетін зат.
Е) массасы өте үлкен зат.
10.Азот(II) оксиді тотыққанда азот(IV) оксидіне айналып,жылу бөлінеді.
Осы реакция типі және қысымды арттырғанда тепе-теңдіктің ығысуы
А) Эндотермиялық,тура жүретін реакция жағына.
В)* Экзотермиялық,тура реакция жағына.
С) Экзотермиялық, тепе-теңдік ауыспайды.
D) Эндотермиялық, тепе-теңдік ауыспайды.
Е) Экзотермиялық,кері реакция жағына.
11.Калий хлоридінің 250 г 6%-рітіндісіне 50 г су қосқанда алынған ерітіндідегі KCl-дың массалық үлесі…
А)* 5%
В) 2%
С) 3%
D) 4%
Е) 1%
12.Тұз қышқылмен әрекеттесетін зат.
А)* Темір(III) оксиді
В) Кремний(IV) оксиді
С) Фосфор (V) оксиді
D) Хром (VI) оксиді
Е) Темір (III) хлориді
13. 130 г ұнталған мырыш 100 г күкіртпен әрекеттескенде алынған мырыш сульфидінің моль саны.
А) 5
В) 3
С) 4
D)* 2
Е) 1
14.Өзгерістер сызбанұсқасы берілген:
1 2 3 4
N2→ NH3→(NH4)2SO4→NH4Cl→NH3 1 және 3 станцияларға қолданылатын реактивтер.
А) H2; HCl
В)* H2; BaCl2
С) H2; KCl
D) H2; NH4Cl
Е) H2; BaCl2
15.Метандағы көміртектің массалық үлесі.
А) 70%
В) 90%
С)* 75%
D) 85%
Е) 80%
16.Fe3O4-ті тұз қышқылында еріткенде түзілетін заттар
А)* FeCl2,FeCl3 және H2O
В) FeCl3; және H2O
С) FeCl2; және H2
D) FeCl3; және H2
Е) FeCl2; және H2O
17.Бутадиенді каучуктің монометрінің құрамы
А) 4 атом көміртек және 8 атом сутек
В) 6 атом көміртек және 4 атом сутек
С)* 4 атом көміртек және 6 атом сутек
D) 6 атом көміртек және 8 атом сутек
Е) 4 атом көміртек және 10 атом сутек
18.4,7 г фенол бром суының артық мөлшерімен әрекеттескенде шығымы 90% болса,түзілген өнім массасы.
А) 10,2 г
В) 22,7 г
С) 27,5 г
D)* 14,9 г
Е) 31,7 г
19.Төмендегі өзгерістерге А,В,С заттарының реттік нөмірлері
HCl NaOH CH3COOH
C2H4 → A → B → C
1) Винилхлорид. 2) Этаналь.
3) Этихлорид. 4) Этан қышқылы.
5) Этанол. 6) Екіэтил эфирі.
7) Этилацетат.
А) 2,4,7
В) 1,5,6
С) 2,4,6
D)* 3,5,7
Е) 2,4,5
20.Өзгерістер схемасы берілген
1 2 3 4
H2O→O2→Fe3O4→Fe→FeCl3
Фторды қолдануға болатын стадия:
А)* 1
В) 2
С) 3
D) 4
Е) 3,4
21. 230 г натрий 780 мл сумен әрекеттесетін болса,ерітіндіде түзілген сілтіні(%) массалық үлесі
А) 42,0
В)* 40,0
С) 41,0
D) 38,5
Е) 39,0
22. BaCl2-нің 260 г 4%-тік ерітіндісіне әзірлеу үшін қажет BaCl2·2 H2O кристаллогидратының массасы(г)
А) 10,4
В) 14,2
С) 21
D)* 12,2
E) 65
23. 14 г циклопентанның 12 л хлормен (қ.ж.) әрекеттескенде,шығымы 70% болса,түзілген хлорциклопентанның массасы
А) 15,6 г
В) 11,9 г
С) 17,2 г
D)* 14,6 г
E) 20,9 г
24.Шығымы 60% болып,54 г сүт қышқылын алуға жұмсалатын глюкозаның массасы
A) 89 г
B) 94 г
C)* 90 г
D) 85 г
E) 96 г
25.15,6 г бензолды нитрлегенде шығымы 90% нитробензол алынды.Оны әрі қарай тотықсыздандырғанда шығымы 75% аналин алынды.Алынған аналиннің массасы.
A) 12,8 г
B) 11,5 г
C) 10,5 г
D)* 12,6 г
E) 11,0 г
22-нұсқа
1.Гидрлену реакциясы:
А) Fe2O3 + 3H2 →2Fe +3H2O
В) ZnO +2HCl→ZnCl2 +H2O
С)* C3H6 +H2→ C3H8
D) H2 +Cl2→2HCl
Е) C2H4 +H2O→ C2H5OH
2.S-электрон бұлтының пішіні
А) гантель тәрізді
В) пирамида
С) тетраэдр
D)* шар
Е) сызықтық
3.Элементтердің терісэлектрлігі өсетін қатары:
А) Si-Al-Mg-Na
В) P-As-Sb-Bi
С) O-N-C-B
D)* Si-P-S-Cl
Е) Cr-Se-Mo-Te
4.Күшті электролит:
А) көмір ышқылының қаныққан ерітіндісі
В)* күкірт қышқылының ерітіндісі
С) су
D) әктіленген су
Е) күкіртсутектің қаныққан ерітіндісі
5.Қыздырған кезде сутекпен әрекеттеспейтін зат:
А) қалайы(ІІ)
В) қорғасын(ІІ) оксиді
С) мыс(ІІ) оксиді
D)* күкірт қышқылы
Е) калий оксиді
6. P2O5 +BaO→Ba3 (PO4 )2
А)* 5
В) 4
С) 7
D) 6
Е) 3
7.Құрамында 20 сутек атомы бар қаныққан көмірсутектің молярлық массасы:
А) 72 г/моль
В) 86 г/моль
С)* 128 г/моль
D) 114 г/моль
Е) 100 г/моль
8. Ақуыз денатурациясы
А)* Белоктардың екінші, үшінші, төртінші реттік құрылымының бүзылуы
В) Белок молекулалардың аминқышқылдарға ыдырауы
С) Белоктар құрамына кіретін аминқышқылдарының тотығуы.
D) Аминқышқылдарының полимерленуі.
Е) Аминоқышқылдарының дигиддрогенденуі.
9. Жоғары молекулалық қосылыстарды алатын реакция
А) Тотықтыру
В) Изомерлеу.
С)* Полимерлеу.
D) Гидролиздеу.
Е) Бейтараптау.
10. Температураны жоғарылатқанда тепе-теңдіқ күйдегі жүйенің тепе-теңдігі
...
А) газ молекулалары санының көбею реакциясы жағына ығысады
В) өрекеттесуші заттар реакциясы жағына ығысады
С)* жылу сіңіре жүретін реакция жағына ығысады
D) жылу боле жүретін реакция жағына ығысады
Е) газ молекулалары санының азаю реакциясы жағына ығысады
11. Екеуі де сумен өрекеттесетін заттар қатары
А)* СО2, Р2О3
В) NО2, С2Н6
С) Si O2,, C2H4
D)`NO2,, SiH4
E) SO2 , CH4
12.Мыс өрекеттессссспейтін қышқылдар жүбы
А) H3 PO4 ; HNO3 сұй
В) H2 SO4 конц; HNO конц.
С)* HCI ; H 2CO3
D) HNO3; өте сұй HNO3
E ) HNО3; өте сұй. HNO3
13.Реакция нәтижесінде күкірт тотықсыздандырғыш болатын реакция үрдісі:
А) C +S→
В)* S +O2 →
С) Cu +S→
D) Ca +S→
Е) P +S→
14.Найзағайдан кейінгі жаңбырдың «қышқыл» болуының себебі:
А)* N2 → NO →NO2→ HNO3
В) N2 →NH3→ N2 →Ca3N2
С) N2→ Mg3N3→NH3 →NH4OH
D) N2→Na3N →NaOH→NaNO3
Е) N2→ NO →NO2 →Mg (NO3 )2
15.Калий силикаты мен фосфор қышқылы арасындағы реакцияның толық иондық теңдеуіндегі барлық коэффициенттердің қосындысы:
А)* 28
В) 27
С) 25
D) 26
Е) 24
16.Al +O2 →Al 2O3 реакциясы теңдеуінде алюминийдің алдына қойылатын коэффициент:
А) 5
В)* 4
С) 3
D) 2
Е) 1
17.Егер іс жүзіндегі шығым 80 екені белгілі болса, 44,8 л (қ.ж) этиленді тікелей гидратациялау арқылы алынған этанолдың массасы:
А) 74,6 г
В)* 74 г
С) 73,8 г
D) 73,6 г
Е) 74,2 г
18.Қосылыстардың ішіндегі күрделі эфир:
А)
Н3С-С-О-С-СН3
║ ║
О О
В) Н3С-СН2-О-СН2-СН3
С)*
Н3С-С-О-СН3
║
О
D) СН3ОН
Е) Н3С-С-СН3
║
О
19.Изомерлерге жататын заттар жұбы:
А) Формальдегид және құмырсқа қышқылы
В)* Пентан және диметрилпропан
С) Бензол және фенол
D) Гексан және циклогексан
Е) Этанол және сірке қышқылы
20. 58,5 г натрий хлоридінің судағы ерітіндісін электролизденгенде анодта калий бромидінен бромды ығыстыратын газ түзілді.Түзілген бромның мөлшері:
А) 5 моль
В)* 0,5 моль
С) 3 моль
D) 4 моль
Е) 2 моль
21.Литий өте сұйылтылған азот қышқылымен әрекеттескенде азоттың тотықсыздану өнімі NH4NO3 болса, теңдеудегі коэффициенттердің жалпы саны:
А) 28
В) 26
С) 29
D)* 30
Е) 31
22.Темірдің массалық үлесі 0, 95 болатын металдан жасалған 3,54 г бұйым бөлшегін ерітуге қажет 14,6 % -тті тұз қышқылы еріндісінің массасы:
А)* 30 г
В) 49 г
С) 50 г
D) 25 г
Е) 45 г
23.Ауа бойынша тығыздығы 2,414-ке тең, құрамындағы көміртектің массалық үлесі 0,857 болатын циклоалканның формуласы:
А)* С 5Н10
В) С 4Н8
С) С 7Н14
D) С 6Н12
Е) С 3Н6
24.Толуолдың жақын гомологтарының саны:
А)* 5
В) 4
С) 3
D) 0
Е) 1
25.Картопта 20 % крахмал бар.Егер шығымы 75 % болса, онда 1620 кг картоптан алынатын глюкозаның массасы:
А)* 270 кг
В) 360 кг
С) 180 кг
D) 220 кг
Е) 300 кг
23-нұсқа
1. Аммоний ионы
A)* NH+4
B) AI3+
C) Hg2+
D) Sn2+
E) Ca2+
2. 2-ші энергетикалық деңгейдегі электрон саны
A) 1e
B) 32e
C) 18e
D)* 8e
E) 2e
3. Гептан молекуласындағы гибридтену типі
A) sp2
B)* sp3
C) sp2, sp3
D) sp
E) sp2, sp
4. Электролиттік диссоциациялану процесі
A) электр тогын өткізу
B)* электролиттердердің иондарға ыдырауы
C) иондарға мүлдем ыдырамауы
D) гидроксид ионының түзілуі
E) электр тогын өткізбеуі
5. Сілтілік жер металдар гидридтерінің жалпы формуласы
A)* MeH2
B) MeH3
C) MeH4
D) Me2H3
E) MeH
6. Аз еритін негіз:
A) мыс гидроксиді (ІІ)
B) мырыш гидроксиді
C)* кальций гидроксиді
D) калий гидроксиді
E) натрий гидроксиді
7. Тұздардың жіктелу қатары
A) қышқылдық, орта, еритін
B) *орта, қышқылдық, негіздік, қостұз
C) орта, сілтілер, қышқылдық
D) суда ерімейтін, амфотерлі, орта
E) амфотерлі, қышқылдық, орта
8. Бос радикалдың ең негізгі белгісі
A) Бос электрон жұбының болуында
B) Бос атомның болуында
C) Иондық байланыстың болуында
D)* Жұптаспаған электронның болуында
E) Атомдар арасында екі жұп электрондардың болуында
9. Пластмассалар құрамына кірмейтін зат
A) толықтырғыштар
B)* еріткіштер
C) тұрақтандырғыштар
D) бояғыш заттар
E) жұмсартқыштар
10. Термохимиялық теңдеуі С6Н12О6 + 6О2 = 6СО2 + 6Н2О + 2820кДж болса, 18г глюкоза тотыққанда бөлінетін жылу мөлшері:
A) 258кДж
B)* 282 кДж
C) 228 кДж
D) 248 кДж
E) 148 кДж
11. Иондардың тотықсыздану қасиеттері өсу ретімен орналасқан қатар
A) CI-, J-, Br-
B)* CI-, Br-, J-
C) Br-, J-, CI-
D) Br-, J-, Br-
E) J-, Br-, CI-
12. Күкірт (VІ) оксиді мен натрий гидроксиді әрекеттескендегі (орта тұз түзілсе) толық иондық теңдеудегі барлық коэффициенттер қосындысы
A) 6
B)* 9
C) 8
D) 7
E) 5
13. Бейтарап орта көрсететін тұз ерітіндісі
A)* натрий нитраты
B) мыс (ІІ) нитраты
C) алюминий нитраты
D) күміс нитраты
E) аммоний нитраты
14. 96г күйені жандырғанда түзілген көміртегі (ІV) оксидінің (қ.ж.) көлемі (л)
A) 177,2
B) 178,2
C)* 179,2
D) 175,2
E) 176,2
15. NаОН балқымасын электролиздегенде түзілетін заттар
A) Na2O, H2
B) Na, H2
C) H2, O2
D)* Na, O2
E) Na2O, O2
16. Алюминий қосылысы қышқылдық қасиет көрсететін реакцияның схемасы
A)* AI(OH)3 + OH- →
B) AI2(SO4)3 + H+ →
C) AI(OH)3 + H+ →
D) AI2O3 + H+ →
E) AIPO4 + H+ →
17. Мына өзгерістегі «Х» заты
СН4 → С2Н2 → Х→ С6Н5NО2
A)* бензол
B) циклогексан
C) хлорбензол
D) толуол
E) этилен
18. А және Б заттары
А + Н2О → пропанол-2 ← Б + NаОН
A) пропан-1, хлорпропан
B) пропаналь, 2-хлорпропан
C) 2-аминопропан, 1,2-дихлорпропан
D)* пропен, 2-хлорпропан
E) ацетилен, пропан қышқылы
19. Құрамында 54,54% көміртек, 9,1% сутек, 36,36% оттек бар альдегид
A) құмырсқа
B) валериан
C)* сірке
D) май
E) пропаналь
20. Көлемі 200мл, молярлық концентрациясы С(Nа2СО3) = 0,25моль/л ерітіндідегі натрий карбонатының массасы
A) 53г
B) 7,3г
C)* 5,3г
D) 10,6г
E) 106г
21. Темір (ІІ) хлоридінің гидролизінің 2 сатысының толық иондық теңдеуіндегі коэффициенттер қосындысы
A) 2
B) 4
C)* 6
D) 7
E) 5
22. Жартысы метаннан, жартысы этаннан тұратын көлемі 1м3 газ қоспасын жағу үшін қажет оттектің көлемі
A) 2,5м3
B)* 2,75м3
C) 3м3
D) 2,1м3
E) 2м3
23. 45кг глюкоза сүт қышқылды ашығын кезінде 40кг сүт қышқылы түзілді. Теориямен салыстырғанда реакция өнімінің шығымын есепте
A) 74%
B) 69%
C) 59%
D)* 88,9%
E) 42,6%
24. 32г кальций карбидінен алынған глицинмен әрекеттесуге жұмсалатын 10 натрий гидроксиді ерітіндісінің (тығыздығы 1,1г/мл) көлемі
A) 110мл
B)* 182мл
C) 136мл
D) 162мл
E) 190мл
25.Өзгерістерді жүззеге асыру үшін реагенттерді қосудың дұрыс реті
C
4, катал.
3
t
2
1

5
4H10 → C4H9CI → C8H18 → CO2 C6H12O6 → C6H12O7
A) HCI, Na, O2, O2, O2
B)* CI2, Na, O2, H2O, Ag2O
C) CI2, Na, O2, O2, KMnO4
D) HCI, Na, H2O, O2, KMnO4
E) CI2, Na, O2, O2, Ag2O
24-нұсқа
1. Химиялық реакцияға кіріскен заттардың массасы түзілген заттардың массасына тең
A)* Зат массасының сақталу заңы
B) Газдар заңы
C) Периодтық заңы
D) Авогадро заңы
E) Құрам тұрақтылық заңы
2. 19 протоны, 20 нейтроны және 19 электроны бар элементтің атом ядросының заряды
A)* 19
B) 26
C) 39
D) 40
E) 20
3. Электролит бола алмайтын қосылыс
A) Na3PO4
B)* Cu3(PO4)2
C) AI(NO3)3
D) Ba(CH3COO)2
E) KCI
4. Лабораторияда сутек алатын құралғы
A) ректификациялық қондырғы
B)* Кипп аппараты
C) Вюрц құтысы
D) Антицеклон
E) Циклон
5. Конфигурациясы ...6s2 болатын элемент
A) Po
B)* Ba
C) Mo
D) Ag
E) At
6. Қосымша топтың металдары –
A) s және p- элементтер
B) p және d- элементтер
C)* d және f- элементтер
D) p және f- элементтер
E) s және d- элементтер
7. Фенол натрий гидроксидімен әрекеттескенде түзілетін қосылыс
A)* натрий феноляты
B) бензол
C) ароматты спирт
D) фенол
E) гексан
8. Нәтижесінде глюкоза түзілетін реакция
A)* крахмал гидролизі
B) майдың гидролизі
C) жай эфир гидролизі
D) мононуклеотидтердің гидролизі
E) белок гидролизі
9. Белок денатурациясы –
A) оның суда еруі
B)* оның ІІ, ІІІ реттік құрылымдарының сыртқы әсерлерден бұзылуы
C) оның ерітіндіден бөлінуі
D) оның коллоид ерітінді түзуі
E) оның ауада тотығуы
10. 1 моль сұйық судың түзілу жылуы 286кДж тең болса, 7,2г су түзілгенде жұмсалатын жылу мөлшері
A) 110,4 кДж
B)* 114,4 кДж
C) 103,4 кДж
D) 104,4 кДж
E) 102,2 кДж
11. Cr2O3 + HNO3 → орта тұз + ...
теңдеуіндегі барлық коэффициенттердің қосындысы
A) 10
B) 13
C)* 12
D) 9
E) 11
12. Калий гидроксиді ерітіндісінде еритін қосылыс
A) NaOH
B) CsOH
C)* Be(OH)2
D) Ni(OH)2
E) Fe(OH)2
13. Натрий хлоратындағы химиялық байланыс
A) ковалентті полюссіз және полюсті
B) ковалентті полюсті және металдық
C)* ковалентті полюсті және иондық
D) иондық және металдық
E) иондық және сутектік
14. Eгер реакция нәтижесінде Mg(NO3)2 + N2 + H2O түзілген болса, онда әрекеттесуші заттар:
A) MgO және HNO3 (конц)
B) Mg(OH)2 және NO2
C)* Mg және HNO3 (сұйық)
D) MgO және HNO3 (сұйық)
E) Mg және N2O5
15. Қысқартылған иондық теңдей бойынша әрекеттесетін заттардың жұбы:
2H+ + CO32- → H2O + CO2↑
A) көмірқышқыл газы мен натрий гидроксиді
B)* натрий карбонаты мен тұз қышқылы
C) магний карбонаты мен натрий гидроксиді
D) көмірқышқыл газы мен су
E) калий карбонаты мен су
16. Бір-біріне изомер заттар:
а. CH2 = C – CH3
│
CH3
б. CH2 – CH – CH3
│ │
CH2 – CH2
в. CH3 – CH = CH – CH2 – C2H5
г. CH2 = CH – CH = CH2
д. CH2 – CH2
│ │
CH2 – CH2
е. CH3 – CH = CH – CH3
A) а, г
B) б, д
C)* а, д, е
D) а, г, е
E) в,б
17. Бутен -1 бромсутектен әрекеттескенде түзілетін зат:
A) 1- бормбутен-1
B) 1- бормбутен-2
C) 1- бромбутан
D)* 2- бромбутан
E) 2- бромбутен-2
18. Сірке альдегиді әрекеттесетін заттар жұбы:
A) сутекпен және сумен.
B) мыс(ІІ) гидроксидімен және кальций оксидімен
C) тұз қышқылымен және күміспен
D)* Ag2O-нің аммиактағы ерітіндісімен және оттекпен
E) натрий гидроксидімен және сутекпен
19. Поликонденсация реакциясы нәтижесінде алынатын зат:
A)*Фенолформальдегид смоласы
B) Полистирол
C) Бутадиенстирол
D) Полиэтилен
E) Полипропилен
20. Егер реакция өнімдері ретінде KCI + KCO3 + H2O түзілген болса, онда әрекеттесуші заттар:
A) HCI және KOH
B)* CI2 және KOH жоғары температурада
C) CI2 және H2O
D) HCIO4 және K
E) CI2 және KOH (қ.ж.)
21.Егер күкірт қышқылының молярлық концентрациясы 5 моль/л болса (ρ = 1,9г/мл), онда ерітіндегі қышқылдың массалық үлесі
A)* 26%
B) 25%
C) 27%
D) 28%
E) 29%
22. Озонатордан 100л (қ.ж.) оттек өткізіп, оның 20%-і озонға айналады. Реакциядан кейінгі газ қоспасының көлемі
A) 80,0л
B)* 93,3л
C) 13,3л
D) 90,3л
E) 18,3л
23. Калийдің 6,02·1022 бөлшектері концентрлі азот қышқылының 12,04·1023 молекуласымен әрекеттеседі. Реакцияға қатыспаған бөлшектердің саны (газ түрінде бөлінеді):
A) 6,02 · 1021
B) 4,1 · 1023
C)* 1,1 · 1024
D) 5,1 · 1022
E) 4,5 ·1023
24.6,72 л(қ.ж) пропанды толық жаққанда алынған өнімді ізбес суының артық мөлшерімен өндеді.Сол кезде 80 г тұңба түзілді. Тұздың шығымы
A) 87%
B)* 88,9%
C) 82%
D) 84%
E) 80,9%
25.Өзгерістер тізбегіндегі соңғы өнім Х5 –
C




H2SO4 (k)
t › 140ºC
Br2
KOH, спирт, tº
H2O, Hg2+
H2, Ni
2H5OH X1 X2 X3 X4 X5A) пропанол
B) сірке қышқылы
C)*этанол
D) этилен
E) этан
25–нұсқа
-
2 период элементтерінің сыртқы денгейде болатын
А) s – және d – электрондар
В) s – және f – электрондар
С)* s – және p – электрондар
D) p – және d – электрондар
E) p – және f – электрондар
2. Тұрақты тотығу дәрежесі + 2 болатын элемент…
А) Марганец
В)* Бериллий
С) Титан
D) Темiр
Е) Хром
3. Әлсіз электролиттерге жататын қосылыс...
А) * H2S
B) HCI
C) H2SO4
D) HI
E) HNO3
4. Kәдімгі жағдайда жай зат - сутектің агрегаттық күйі
А) сұйық
В) плазма
С)* газ
D) кристалл зат
Е) аморфты зат
5. Диссоциация кезінде хлорит-ион түзетін зат
A) HCIO4
B)* KCIO2
C) KCIO
D) KCI
E) HCIO
6. Бокситтің негізгі құрам бөлігі –
А) *AI2O3
B) CrO
C) P2O3
D) CaO
E) WO3
7. Сірке қышқылы қолданылады
А) пластмасса
В) бояулар алуда
С)* тамақ өнеркәсібінде
D) хош иісті заттар алуда
Е) отын ретінде
8. (С6 Н10О5)n формуласымен өрнектеледі:
A)* крахмал
В) рибоза
С) глицерин
D) фруктоза
Е) сахароза
9. Жоғары молекулалық қосылыстар қасиеті және қолданылуы бойынша мынадай болып бөлінеді:
А) полимерлер және мономерлер
В)* пластмассалар, эластомерлер және талшықтар
С) жасанды және табиғи
D) Өсімдік және жануар текті
Е) синтетикалық және табиғи
10. Құрамында 18,06 ∙1023 молекуласы бар судың (4 οС және 1 атм қысымдағы) көлемі
А) 67,2 л
В)* 54 мл
С) 22,4 л
D) 540 мл
Е) 44,8 л
11. Егер температура мен қысымды бір мезгілде арттырса, онда қай реакцияның тепе-тендігі оң жаққа қарай ығысытын реакция теңдеуі
А) Fe + C ↔ Fe + CO - Q
B) 2CO + O2 ↔ 2CO2 + Q
C)* 2N2 + O2 ↔ 2N2O - Q
D) 2NO + O2 ↔ 2NO2
E) 2H2O ↔ 2H2 + O2 - Q
12. Берілген сызба- нұсқадағы А, В элементтері
![]()
![]()
![]() А
А2О АОН
А
А2О АОН
![]() А2ВО3
А2ВО3
![]()
![]()
![]() В
ВО2 Н2ВО3
В
ВО2 Н2ВО3
А) * A – K, B - S
B) A – Fe, B – B
С) A – Cu, B -N
D) A – Na, В – Cr
E) A – AI, B – P
13. Құрамында 98 г ортофосфор қышқылы бар ерітіндіден 44,8 л аммиак жібергенде пайда болған тұз:
А) аммоний дигидрофосфаты
В) аммоний метафосфаты
С) аммоний ортофосфаты
D)* аммоний гидрофосфаты
Е) аммоний пирофосфаты
14. Темірдің (II) гидрокарбонатындағы π- байланыстардың жалпы саны
А) 3
В) 4
С) *2
D) 8
Е) 6
15. Іс жүзінде жүруі мүмкін реакция:
![]()
![]() А) *Na + H2O
А) *Na + H2O
![]() B) Cu + FeSO4
B) Cu + FeSO4
![]() C) ZnCI2 + Cu
C) ZnCI2 + Cu
![]() D) Hg + H2O
D) Hg + H2O
![]() E) Ag + HCI
E) Ag + HCI
16. Сыртқы электрондық денгейінің формуласы ... 3 d10 4s2 болатын элемент
А) Cr
B)* Zn
C) V
D) W
E) Cu
17. Құрамында 18 атом сутек бар алкеннің салыстырмалы молекулалық массасы
А) 132
В) *126
C) 142
D) 164
E) 108
18. 552 г этил спирті дегидратацияланғанда 333 г диэтил эфирі алынған. Реакция өнімінің массалық шығымы:
А) 100%
B) * 75%
C) 85%
D) 95%
E) 80%
19. 1,2 – диметилбензолдың толық жану теңдеуіндегі өнімдерінің формуласының алдындағы коэффициенттердің қосындысы
А) *26
В) 13
С) 15
D) 18
E) 10
20. 135 мл суда 25 г мыс купоросы СuSO4 ∙ 5H2O ерітілген. Алынған ерітіндідегі мыс ( ІІ) сульфатының массалық үлесі ( %)
А) *10
В) 16,7
С) 9
D) 7.5
E) 12
21. 2 мольден мыс (ІІ) нитратын айырғанда түзілетін оттектің көлемі
А) 44,8 л
B) 89,6 л
C)* 22,4 л
D) 112 л
E) 133,6 л
22. Концентрлі күкірт қышқылы мырышпен ережеге сай күкірт (ІҮ) оксидіне дейін тотықсызданады. 245 грамнан тұратын күкірт қышқылы мырышпен толық әрекеттескенде түзілетін күкірт (ІҮ) оксидінің массасы:
А) 64,0 г
В) 240 г
С) 128 г
D)* 80,0 г
Е) 160 г
23. 8,4 г циклогександы дегидрлегенде және 5,2 г ацетиленді тримерлегенде алынатын бензол массаларының қатынасы
А) 5:3
B) 3:1
C) 4:3
D)* 3:2
E) 4:1
24. Тығыздығы ρ = 0,88 г/мл , 65 мл бензол жарық қатысында хлормен әрекеттескенде түзілген гексахлоранның массасы
А) 253,4 г
В) 223,4 г
С)* 213,4 г
D) 243,4 г
Е) 233,4 г
25. 15 г сірке қышқылынынан алынатын құрамы С4Н8О3N2 дипептидтің массасы
А) 10,5 г
В) 12,5 г
С)* 16,5 г
D) 18,5 г
Е) 14,5 г
Тестовый материал взят из книжки-вопросника пробного тестирования Национального Центра тестирования МОН РК
Вариант 0106
ХИМИЯ
1. Берілген теңдеудің (... Fe + … Cl2 → … FeCl3) коэффициенттері
A) 1, 2, 3
B)* 2, 3, 2
C) 2, 2, 2
D) 2, 3 ,1
E) 1, 1, 1
2. Натрий атомының құрамындағы протон саны
A) 23
B)* 11
C) 12
D) 13
E) 15
3. Формуласы S8 болатын зат молекуласындағы химиялық байланыстың түрі
A) донорлы-акцепторлық
B) сутектік
C) коваленттік полюсті
D)* коваленттік полюссіз
E) иондық
4. Электрөткізгіштікті анықтайтын құралдың лампасы электродты осы затқа батырғанда жарқырап жанады
A) қант (қатты)
B) қант (ерітіндісі)
C) натрий хлориді (қатты)
D)* натрий хлориді (ерітіндісі)
E) спирт (ерітіндісі)
5. Оттектің адам ағзасындағы мөлшері (%)
A) 21,0
B) 32
C)* 65
D) 1,43
E) 49,13
6. Жалпы формуласы CnH2n-6 болатын заттың атауы
A) гексан
B)* бензол
C) циклогексан
D) ацетилен
E) октен
7. Иодсутектің бутен-1-мен әрекеттесуі ... жатады.
A) галогендену реакциясына
B)* қосып алу реакциясына
C) тотықсыздану реакциясына
D) гидрлену реакциясына
E) орын басу реакциясына
8. Нуклеин қышқылдарының белоктар ұқсастығы –
A) екеуі де полинуклеотидтер.
B) екеуінің мономерлері бірдей.
C) екеуі де полипептидтер.
D) екеуі де тек клетка ядросында болады.
E)* екеуі де биополимерлер.
9. Полиэтилен –
A) әрі табиғи, әрі химиялық полимер болады.
B)* химиялық, синтетикалық.
C) табиғи, өсімдік текті.
D) табиғи жануар текті.
E) химиялық, жасанды.
10. 5,6 литр (қ.ж.) метан жанғанда 401 кДж жылу бөлінетін жағдайда реакцияның жылу эффектісі CH4(r) + 2O2(r) = CO2(r) + 2H2O + Q
A) 1602 кДж
B) 1590 кДж
C) 1601 кДж
D) 1600 кДж
E)* 1604 кДж
11. Массалық үлесі 56% ерітінді түзе алатын зат:
A) әк тас.
B) гипс.
C) бор.
D) мәрмәр.
E)* калий перманганаты.
12. Натрий тетрагидроксоцинкатының формуласы
A) Zn(OH)Cl
B) ZN(OH)2SO4
C) Na2ZnO2
D)* Na2[Zn(OH)4]
E) Zn(OH)2
13. Аммоний гидрофосфаты түзілгенде, аммиак пен ортофосфор қышқылы арасындағы реакция теңдеуіндегі коэффициенттер қосындысы:
A)
2.![]()
B) 3.
C) 6.
D)* 4.
E) 5.
14. СО2, СО, СН4 қосылыстарындағы көміртектің валенттіліктерін көрсететін қатар
A) 2, 1, 4
B)* 4, 2, 4
C) 1, 1, 1
D) 4, 2 ,2
E) 2, 2, 4
15. Ізбесті сөндіру реакциясының нөмірі:
Ca ![]() CaCl2
CaCl2
![]() CaCO3
CaCO3 ![]() CaO
CaO![]() Ca(OH)2
Ca(OH)2
![]() CaCO3
CaCO3
A)* 4.
B) 2.
C) 3.
D) 5.
E) 1.
16. 1,5 моль октанның массасы:
A) 175 г.
B)* 171 г.
C) 180 г.
D) 232 г.
E) 86,5 г.
17. Тек екіатомды спирттерге жататын зат:
A)* CH3 – CHOH – CHOH – C2H5
CH3 – CH – CH3
B![]() )
)
CH2OH![]()
C) CH3CH2OH
D) CH2OH – CHOH - CH2 - OH
CH2OH – CHOH- CH – CH3
E![]() )
)
OH
18. Құрамында төрт сутек атомы бар күрделі эфирдің салыстырмалы молекулалық массасы
A)* 60
B) 102
C) 88
D) 74
E) 116
19. Мына заттардың ішінен 2-хлорпропанның формуласын анықта
A) CH3 - CH2 - CH2Cl
B) CH3Cl
C) CH3 - CH2 - CH2Br
D) H3C - CH - CH2Cl
![]()
CH3
E)* CH3 - CH – CH3
![]()
Cl
20.
NH3 ![]() X1
X1 ![]() X2
X2 ![]() X3
X3 ![]()
![]() X4
X4
тізбегі бойынша 224 л аммиактан алынатын Х4 затының массасы (қ.ж.)
A) 17 г
B)* 800 г
C) 80 г
D) 160 г
E) 85 г
21. Өзгерістер схемасы берілген:
H2O ![]() O2
O2 ![]() Fe3O4
Fe3O4 ![]() Fe
Fe![]() FeCl3.
FeCl3.
Фторды қолдануға болатын стадия:
A) 3, 4.
B) 2.
C) 3.
D) 4.
E)* 1.
22. Көлемі 2,8 л күкірт сутекті (қ.ж.) мыс (ІІ) сульфатының артық мөлшеріне жібергенде массасы 11,4 г тұнба алынды. Реакция өнімінің практикалық шығымы:
A) 55%.
B) 85%.
C) 75%.
D)* 95%.
E) 65%.
23. Темір (ІІ) оксиді мен темір (ІІІ) оксидінің қоспасының 37 грамын сутегімен тотықсыздандырғанда темірдің 28 грамы алынды. Қоспадағы оксидтердің массалық үлестерін анықтаңыз.
A) 68% FeО және 32% Fe2О3
B) 83% FeО және 17% Fe2О3
C) 90% FeО және 10% Fe2О3
D)* 73% FeО және 27% Fe2О3
E) 65% FeО және 35% Fe2О3
24. 0,1 моль темір 75г 20%-ті мыс (ІІ) сульфаты ерітіндісімен әрекеттескенде түзілетін мыстың массасы (г)
A) 8
B) 5
C) 7
D)* 6
E) 9
25. Картопта 20% крахмал бар. Егер шығымы 75% болса, онда 1620 кг картоптан алынатын глюкозаның массасы:
A) 300 кг
B)* 270 кг
C) 180 кг
D) 220 кг
E) 360 кг
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Тест Химия сабақтан
Химия
1-нұсқа
-
Атом-молекулалық ілімді ұсынған ғалым
А) Д.И.Менделеев
В) Э.Франкленд
С) Ж.Л.Пруст
D)* М.В.Ломоносов
Е) А.Лавуазье
2. Р-элемент болатын
А) Li
В) Mg
C) Sr
D)* Si
E) Rb
3. Жай заттардың тотығу дәрежелері
А) Атомдағы электрон санына тең
В) протон санына тең
С)* Нольге тең
D) Жұптаспаған электрон санына тең
Е) Валенттік электрон санына тең
4 .
Zn2+
+
2OH-
= Zn(OH)2 қысқартылған иондық
теңдеуіне сәйкес келетін
.
Zn2+
+
2OH-
= Zn(OH)2 қысқартылған иондық
теңдеуіне сәйкес келетін
молекулалық теңдеу
А)* Zn(NO3)2 + 2KOH= Zn(OH)2 + 2KNO3
В) ZnCI2 + K2S = ZnS + 2 KCI
С) ZnO + 2HNO3 = Zn(NO3)2 + H2O
D) ZnO + H2SO4 = ZnSO4 + H2O
E) ZnS + 2HCI = ZnCI2 + H2S
5. Сутек газын ашқан ғалым
А) А.Беккерель
В) Дж. Прустли
С)* Г.Кавендиш
D) Р.Бойль
Е) М.В.Ломоносов
6. Сумен әрекеттеспейтін оксид
А) Күкірт (ҮІ) оксиді
В) Фосфор (Ү) оксиді
С)* Кремний оксиді
D) Натрий оксиді
Е) Барий оксиді
7. Алюминийдің темір (ІІ) оксидімен реакциясы теңдеуінде
тотықсыздандырғыштың алдына қойылатын коэффициент
А) 1
В)* 2
С) 3
D) 4
Е) 5
8. Орыс ғалымы А.М.Бутлеров алғаш рет синтездеген зат
А) Мочевина
В) Май
С)* Қантты заттар
Д) Қымыздық қышқылы
Е) Сірке қышқылы
9. Полимерлер-
А) Жеке атомдардан тұрады
В) Иондардан тұрады
С)* макромолекуладан тұрады
D) Жеке молекулалардан тұрады
Е) Радикалдардан тұрады
10. Егер температураны 50 С-қа төмендеткенде, реакция жылдамдығының
(y =3) кемуі:
А) 3
В) 81
С) 27
D)* 243
Е) 9
11. Азот қышқылының 2 литр 20%-тік ерітіндісіндегі (p=1.6 г/мл) судың көлемі
А) 2,0л
В) 2,42л
С)*2,56л
D) 3,24л
Е) 2,81л
12. Құрамында 32 г мыс бар CuSO4 ·5H2O мыс купоросының массасы:
А)* 125г
В) 100г
С) 65г
D) 80г
Е) 44г
13. Құрамында 9,8г фосфор қышқылы және 12г кальций гидроксиді бар
ерітінділерді араластырғанда түзілетін тұнба массасы:
А)* 15,5г
В) 16,5г
С) 17,5г
D) 18,5г
Е) 20,5г
14. Кальций гидрокарботындағы ковалентті байланыстардың саны
А) 9
В) 4
С)* 10
D) 8
Е) 12
15. Концентрлі азот қышқылымен әрекеттеспейтін металл:
А) мыс
В) күміс
С)* хром
D) мырыш
Е) сынап
16. Домна пешінде жүретін реакциялардың бірі:
Fe2O3 +3CO → Fe + 3CO2
Осы теңдеу бойынша 32г тотықтырғыш пен әрекеттесетін
тотықсыздандырғыш мөлшері:
А) 2 моль
В) 0,4 моль
С)*0,6 моль
D) 3 моль
Е) 1 моль
17. 2,5г натриймен 2,3г этил спиртіне әсер еткенде сутектің (қ.ж.) көлемі:
А) 0,85 мл
В) 5,6 мл
С)* 560 мл
D) 0,65 мл
Е) 0,5 мл
18. Тығыздығы 0,8 г/мл 110 мл сірке қышқылының этил эфирін алу үшін қажет
сірке қышқылының массасы:
А) 44г
В) 40г
С)* 60г
D) 88г
Е) 30г
19. Өзгерістердің нәтижесінде түзілетін «А» затының аталуы:
C2H6 +Br2__ X1 +HOH X2 [O] X3 [O] A
А)* Сірке қышқылы
В) Бромды этил
С) Этанол
D) Ацетальдегид
Е) Сүт қышқылы
20. Сілтінің артық мөлшері қажет болатын стадия
2 AI(OH)3 4AI3+
AI 1 AI3+
3 [AI(OH)4] ____5____AI3+
A) 1
В)* 3
C) 5
D) 4
Е) 2
21. Хлор (І) оксиді мына қышқылдың ангидриді:
А) Хлор қышқылының
В)* Хлорлылау қышқылдың
С) Тұз қышқылының
D) Хлорлау қышқылдың
Е) Хлорлы қышқылдың
22. 500л пентанды дегидрлегенде алынған циклопентанды жағуға жұмсалған
оттектің (қ.ж.) көлемі:
А) 3360л
В) 3270л
С) 3460л
D)* 3750л
Е) 3520л
23. Құрамында көлемдік үлесі бойынша 44,8% этилен 32,8% метан бар этилен,
ацетилен және метаннан тұратын 5л қоспа қосып алатын бромның массасы:
А)* 32г
В) 20г
С) 48г.
D) 16г
Е) 30г
24. 34,2г сахароза гидролизденгенде алынған глюкоза спирттік ашығанда
түзілген этанолдың массасы:
А) 5,2г
В) 6,2г
С)* 9,2г
D) 8,2г
Е) 7,2г
25. Сутек бойынша тығыздығы 15,5- ке (қ.ж.) тең аминнің 5,6 литрін жағуға
жұмсалатын оттектің көлемі:
А) 11,2л
В) 22,4л
С)* 12,6л
D) 14,4л
Е) 16,8л
2-нұсқа
-
Химиялық құбылысқа жататыны:
А) шайқау
В)* крекингілеу
С) хромотографиялау
D) дистилдеу
Е) буландыру
2. Атомның электрон саны
А)* протон санына тең
В) салыстырмалы атомдық массаға тең
С) протон санынан көп
D) нейтрон санына тең
Е) нейтрон санынан аз
3. NaF – фтордың тотығу дәрежесі
А)* -1
В) -2
С) +2
D) +3
Е) +1
4. Электролиттік диссоциация дегеніміз:
А)* заттардың суда ерігенде немесе балқығанда иондарға ыдырау процесі
В) заттардың өз бетімен жеке молекулаларға ыдырауы
С) иондар және атомдар түзілу процесі
D) иондардың қосылып молекула түзу процесі
Е) электролиттердің жеке атомдарға ыдырауға процесі
5. Сутектің табиғи изотоптарының массалық сандары
А) 1
В) 1, 2
С)* 1, 2, 3
D) 2, 3
Е) 1, 3
6. Сілтіні зертханада алу әдісі:
А) негіз бен тұзды әрекеттестіру
В)* белсенді металды сумен әрекеттестіру
С) металды тұзбен әрекеттестіру
D) мыс (ІІ) оксидін сумен әрекеттестіру
Е) металл мен қышқылды әрекеттестіру
7. Сілтілік жер металдарға жатады:
А)* Mg
B) K
C) Na
D) Cs
E) Li
8. Органикалық заттың құрамына міндетті түрде кіретін элемент
А) кремний
В) азот
С) сутек
D)* көміртек
Е) оттек
9. Полимерлену реакциясы
А)* пH2C=CH2 → (-H2C- CH2-)n
B) H2C=CH2 + H2→CH3—CH3
C) H2C=CH2 +Cl2 →ClH2C-CH2Cl
D) H2C=CH2+ 3O2→ 2CO2-2H2O
E) H2C=CH2+ HCI→ CH3-CH2CI
10. Н2 + СІ2= 2HCI реакциядағы сутектің концентрациясын 4 есе азайтқанда
реакция жылдамдығы...
А) 8 есе артады
В) 2 есе артады
С) 2 есе кемиді
D)* 4 есе кемиді
Е) 8 есе кемиді
11. Натрий нитратының 450г 20%-ті ерітіндісіндегі судың массасы
А)* 360г
В) 418г
С) 370г
D) 402г
Е) 434г
12. Күкірт қышқылына тән емес қасиет:
А)* Тотықсыздандарғыш қасиет көрсетеді
В) Суда жақсы ериді
С) Концентрлі күкірт қышқылы күшті тотықтырғыш
D) Суға қосқанда жылу бөлінеді
Е) Ауыр май тәрізді сұйық зат
13. Қалыпты температурада концентрлі азот қышқылымен әрекеттеспейтін
металл:
А) Mg
B) Cu
C)* AI
D) K
E) Na
14. 5,6г көміртегі (ІІ) оксиді алатын көлем:\
А) 0,71л
В)* 4,48л
С) 2,24л
D) 5,6л
Е) 3,6л
15. Домна пешіне салуға дайындалған шахтаның құрамы:
А)* Руда, флюс, кокс
В) Кокс, кремний оксиді, флюс
С) Көмір, темір, кремний оксиді
D) Көмір, ізбес тас, темір
Е) Флюс, көмір, темір
16. Ерітіндіде темір (ІІІ) ионының бар екендігін анықтайтын реактивтер
А) NaOH, H2S
B) BaSO4, KCI
C) K3[Fe(CN)6], KCI
D)* KCNS, NaOH
E) KOH, NaCI
17. Іс жүзінде жүруі мүмкін реакция:
А) CH4 + Na →
B)* CH3OH + HCI→
C) CH3OH + NaBr→
D) CH3OH + Br2→
E) CH3OH + NaCI→
18. 0,8 моль пропан қышқылы 0,5 моль натриймен әрекеттескенде түзілетін
сутектің (қ.ж.) көлемі:
А) 89,6л
В) 11,2л
С)* 5,6л
D) 44,8л
Е) 22,4л
19. СaO +C→Х +Н2О С2Н2 +У С2Н2Вr2. Өзгерістер схемасындағы Х
және У заттары:
А) Х- Ca(OH)2, У- Br2
В) Х- CaCI2, У-HBr
С)* Х- CaC2, У- Br2
D) Х- Ca(OH)2, У- HBr
Е) Х- CaC2, У- HBr
20. Өзгерістер тізбегіндегі этаналь қатысатын стадия
Cu 1→ Cu(NO3)3 2→ Cu(OH)2 3→ Cu2O 4→Cu
А) 1
В)* 3
С) 1,4
D) 2
Е) 4
21. Реакция теңдеуіндегі барлық коэффициенттердің қосындысы
K2Cr2O7 + KJ + H2SO4 → Cr2(SO4)3 +J2+K2SO4 +H2O
А) 27
В)* 29
С) 23
D) 31
Е) 25
22. Зат құрамында 80% көміртегі бар, ал сутгеі бойынша салыстырмалы тығыздығы 15-ке тең. Көмірсутектің молекулалық формуласы
А) C2H5
B)* C2H6
C) C2H2
D) C2H4
E) C2H5OH
23. Нитрлеу реакциясы кезінде 78г бензолдан 98,4 г нитробензол алынды. Нитробензолдың шығымы (%-пен):
А) 40%
В) 70%
С)* 80%
D) 50%
Е) 60%
24. 16г метил спиртін толық жаққанда түзілетіндей газ алу үщін спирттік ашитын глюкозаның массасы:
А) 4,5г
В)* 45г
С) 4,6г
D) 47г
Е) 46г
25. Шығымы 92% болатын 42,8г анилин алынғанда жұмсалатын нитробензолдың массасы:
А) 58,8г
В) 57г
С)* 61,5г
D) 56,8г
Е) 57,8г
3 – нұсқа
1![]() . Cu+HgCl2
CuCl2+Hg теңдеулермен
өрнектелген реакция типі
. Cu+HgCl2
CuCl2+Hg теңдеулермен
өрнектелген реакция типі
А) алмасу
В) қосылу
C) айрылу
D) * орын басу
E) бейтараптану
2. S – орбаталдың сыйымдылығы
А) 1е
В) 5е
C) 2е
D) 4е
E) 3е
3. Берілген теңдеудің тотықтырғыш болатын зат
4![]() NH3+3O2
2N2+6H2O
NH3+3O2
2N2+6H2O
А) Азот
В) Күкірт
C) * Оттек
D)Аммиак
E) Сутек
4. Алюминий сульфаты ерітіндісінде лакмус индикаторының түсі
А) * қызыл
В) көк
C) таңқурай түсті
D) сары
E) түссіз
5. Күкірт оксиді (VI) қалыпты жғдайда
А) қатты зат
В) түссіз газ
C) сары түсті ұнтақ
D) * сұйықтық
E) қоңыр кристалдар
6. Кальций оксидін пайдаланатын жағдай
А) көмір қышқыл газын анықтау үшін
В) * сөндірірілген әкті алу үшін
C) мұнайды тазарту үшін
D) аккумуляторда қолдану үшін
E) бордосс қоспасын дайындау үшін
7. Судың кермектігін жою әдісі
А) Қайнату арқылы
В) Тұндыру арқылы
C) Тазартылған суды қосу арқылы
D) * Дистелдеу арқылы
E) Сүзу арқылы
8. Алкандар қатарына жататын көмірсутек
А) C8H14
В) * C10H22
C) C5H10
D) C6H12
E) C8H16
9. Химиялық полимерге жатпайды:
А) Полиэтилен
В) Полистирол
C) Капрон
D) * Белок
E) Лавсан
10. Осы реакцияда сутек концетрациясын арттыру тепе – теңдікті солға ығыстырады:
А) * Аммиакты жай заттарға айыру
В) Сутектің хлормен әрекеттсуі
C) Жай заттардан су буының түзілуі
D) Темір (II) оксидін сутекпен тотықсыздандырғанда
E) Жай заттардан аммиакты синтездеу
11. 100г кристалдық содадағы судың массалық үлесі (%)
А) 11
В) 89
C) *63
D) 37
E) 74
12. Массасы 442г күкіртсутектің моль саны:
А) 14
В) *13
C) 12
D) 11
E) 15
13. Азот қышқылы төмендегі затпен әрекеттескенде барлық қышқылдарға ортақ қасиет көрсетеді:
А) C
В) Cu
C) CO2
D) *BaCO3
E) CH4
14. 2000г кальций корбанаты ыдырағанда бөлінген көмірқышқыл газының қалыпты жағдайдағы көлемі:
А) *448л
В) 336л
C) 560л
D) 672л
E) 224л
15. 800г мыс (II) оксидін сутекпен тотықсыздандырғанда түзілетін мыстың массасы:
А) *640г
В) 6,4г
C) 320г
D) 32г
E) 64г
16. Гидролизденетін тұздар жұбы:
А) * FeCl2, CrSO4
В) MgSO4, K2SO4
C) FeCl3, NaNO3
D) Na2SO4, Ba(NO3)2
E) BaCl2, MgSO4
17. 3м3 этиленнен (қ.ж.) шығымы 70% болса, алынатын массасы:
А) 8,3кг
В) *4,3кг
C) 6,3кг
D) 7,3кг
E) 5,3кг
18. Құмырсқа қышқылын зертханада алу әдісі:
А) Көміртегі және сутегіден
В) Көмірсутек (II) оксиді мен су буынан
C) *Формиат және концентрлі күкәрт қышқылынан
D) Көміртегі (IV) оксиді және судан
E) Көміртек (II) оксиді мен натрий гидроксидінен
19. 2,3 – димитилгексан қышқылының құрылым формуласы
А![]()
![]() ) * H3C – CH2
- CH2 – CH – CH –
COOH
) * H3C – CH2
- CH2 – CH – CH –
COOH
CH3 CH3
В) H3C – CH – CH – COOH
![]()
![]()
CH3 CH3
C) CH3 CH3
![]()
![]()
CH3 – C – C – COOH
![]()
![]()
CH3 CH3
D) H3C – CH – CH2 – COOH
![]()
CH3
E![]()
![]() ) H3C – CH – CH –
CH2 – CH2
– COOH
) H3C – CH – CH –
CH2 – CH2
– COOH
CH3 CH3
20. Тізбекті орындау үшін дұрыс ретімен жазылған реагенттер қатары
K


 1 KOH 2
KHCO3 3
KCl 4 KNO3
1 KOH 2
KHCO3 3
KCl 4 KNO3
А) H2O, CO2, HCl, HNO3
В) NaOH, CO2, HCl, HNO3
C) *H2O, CO2, HCl, AgNO3
D) H2O, CO, HCl, AgNO3
E) H2O, H2CO3, HCl, HNO3
21. 1л хлор мен 2л сутегі (қ.ж.) газдарын араластырды, осы қоспадан алынатын хлорсутектің массасы мен көлемі
А) 1,63г HCl және 3л
В) 2,24г HCl және 6л
C) *3,26 HCl және 2л
D) 6,66г HCl және 3л
E) 1,5г HCl және 2л
22. 11,2л метан мен 56л хлордан шығымы 70% - тік тетрахлорметан алынды. Тетрахлорметанның массасы:
А) 55г
В) 58г
C) 50,5г
D) *53,9г
E) 57,5г
23. Көмірсутек буының ауа бойынша тығыздығы 1,862, көмірсутектің формуласы. Көмірсутектің массалық үлесі 88,9% болса, онда оның формуласы:
А) C6H10
В) *C4H6
C) C7H12
D) C5H8
E) C3H4
24. Егер практикалық шығымы 80% болса, 200г глюкозадан алынатын сүт қышқылының массасы:
А) 140г
В) 180г
C) *160г
D) 150г
E) 170г
25. Комплементарлық жұп -
А) *пурин мен пиримидин негіздері арасында түзіледі
В) тимин мен урацил арасында түзіледі
C) ДНК мен РНК арасында түзіледі
D) амин қышқылдары мен нуклеин қышқылдары арасында түзіледі
E) сұйық пен газ арасында түзіледі.
4 – нұсқа
1. Орынбасу реакциясы
А) Zn (OH)2+2HCl
В![]() ) *Zn + 2HCl
) *Zn + 2HCl
C![]() ) Cu (OH)2
) Cu (OH)2
D![]() ) Fe + S
) Fe + S
E![]() ) ZnO + H2SO4
) ZnO + H2SO4
2![]() . Атомының сыртқы энергетикалық деңгейінде төрт электроны
элемент
. Атомының сыртқы энергетикалық деңгейінде төрт электроны
элемент
А) He
В) Be
C) O
D) *C
E) S
3. Полярлығы күшті қосылыс:
А) CH4
В) PH3
C) *HCl
D) H2S
E) HBr
4. Диссоциациаланғанда OH ионын түзетін зат
А) Cr(OH)3
В) *NaOH
C) KNO3
D) H2S2O3
E) Li2CO3
5. Күкіртті газ сумен әрекеттескенде түзілетін зат
А) сілті
В) суда ерімейтін негіз
C) *қышқыл
D) қышқыл тұз
E) тұз
6. Берілген заттардың арасында иондық қосылыс
А) *NaCl
В) H2
C) Ca
D) OF2
E) Cl2
7. Ерітіндісі жалынды күлгін түске бояйтын тұз
А) NaCl
В) AgCl
C) MgCl2
D) *KCl
E) CaCl2
8. Органикалық қосылыстардың химиялық құрылыс теориясының негізін қалаған ғалым...
А) А.Кекуле
В) *А.Бутлеров
C) Д.И.Менделеев
D) С.Аррениус
E) А.Кольбе
9. Табиғи полимерге жатпайды
А) Целлюлоза
В) *Капрон
C) Ақуыз
D) Нуклеин қышқылдары
E) Крахмал
10. 2Na+O2=2NO2 азот (II) оксидінің (NO) концетрациясын екі есе арттырғанда, химиялық реакциясын жылдамдығының артуы
А) 2 есе
В) *4 есе
C) 6 есе
D) 8 есе
E) 7 есе
11. Су электр тогының әсерінен сутек пен оттекке айрылады. Түзілген газдардың көлемдік қатынастары:
А) H2:O2=3:2
В) H2:O2=1:2
C) H2:O2=2:3
D) * H2:O2=2:1
E) H2:O2=1:1
12. Тотықсыздандыру үрдісінің сызбанұсқасы
А![]() ) Br BrO2
) Br BrO2
В![]() ) BrO2 BrO4
) BrO2 BrO4
C![]() ) BrO BrO2
) BrO BrO2
D![]() ) * BrO2 Br
) * BrO2 Br
E![]() ) Br2 BrO
) Br2 BrO
13. 200г мыс (II) оксиді мен 200г күкірт қышқылын қыздырғанда түзілетін тұздың массасы:
А) *326,5г
В) 326,6г
C) 326,8г
D) 326,7г
E) 326,4г
14. 170г натрий нитратынан алынатын 63% - тік азот қышқылы ерітіндісінің массасы:
А) *200г
В) 205г
C) 190г
D) 210г
E) 195г
15. Жүруі мүмкін емес реакциясының теңдеуі:
А![]() ) CO2+CaO …
) CO2+CaO …
В![]() ) CO2+NaOH …
) CO2+NaOH …
C![]() ) CO2+H2O …
) CO2+H2O …
D![]() ) CO2+SO2 …
) CO2+SO2 …
E![]() ) O2+CH4
…
) O2+CH4
…
16. Массасы 2,6г темір мен 2,8г күкірт әрекеттескенде түзілетін темір (II) сульфидінің массасы (г):
А) 2,04
В) 6,6
C) *4,08
D) 7,7
E) 8,8
1![]()
![]() 7. Zn x
Zn(NO3)2 y
ZnCO3 өзгерісіндегі “X” және
“Y” заттарының формуласы:
7. Zn x
Zn(NO3)2 y
ZnCO3 өзгерісіндегі “X” және
“Y” заттарының формуласы:
А) X – NO; Y – H2O
В) X – HNO2; Y – CH4
C) *X – HNO3; Y – K2CO3
D) X – NH3; Y - C
E) X – NH3; Y – CO
18. Ароматты спиртке жататын заттың формуласы:
А) C6H13OH
В) C2H5 - CH2 - OH
C) C6H5OH
D) * CH2 - OH
![]()
![]()
E) C6H4(OH)2
19. Халықаралық номенклатура бойынша заттың аталуы:
CH3
![]()
CH3 – CH – CH – C = O
![]()
![]()
C3H7 H
А) *2 – метил – 3 - пропилбутаналь
В) 2,3 - диметилгексаналь
C) гексаналь
D) гептаналь
E) 3 – метилгексаналь – 2
20. Схеманы пайдаланып А, В, С заттары
N![]()
![]()
![]() O ? HNO3
Cu(OH)2? қызд.
А
O ? HNO3
Cu(OH)2? қызд.
А
H![]()
![]()
![]() 2S +O
? +O
2S +O
? +O![]() SO3+H2O
B
SO3+H2O
B
A+B=C
А![]() ) A – N2O5,
B-SO3, C - H2SO4
) A – N2O5,
B-SO3, C - H2SO4
В) A – NO2, B-H2SO4, C - NO
C) *A – CuO, B-H2SO4, C – CuSO4
D) A – O2, B-H2SO3, C – H2SO4
E) A – Cu(NO3)2, B-H2SO4, C – CuSO4
21. 5,6л метанды 33,6л хлормен (қ.ж.) хлорланғанда түзілген трихлорметанның массасы:
А) *29,8г
В) 32,8г
C) 30,8г
D) 31,8г
E) 28,8г
22. 39г бензол және 39г азот қышқылы өзара әрекеттескенде түзілген нитробензолдың массасы:
А) 78г
В) 62,5г
C) 58,5г
D) *61,5г
E) 74г
23. Егер шығымы 75% болса, 1620г крахмалды гидлиздегенде түзілген, глюкозаның спирттік ашуынан түзілетін этанол массасы:
А) 630г
В) *690г
C) 700г
D) 650г
E) 720г
24. 150г 5% - тік аминосірке қышқылының ерітіндісіне 150г 5% - тік калий гидроксиді ерітіндісін қосқандағы, алынған ерітіндідегі әр заттың массалық үлестері:
А) 0,45% КОН және 2,36% H2NCH2COOK
В) 0,25% КОН және 3,15% H2NCH2COOK
C) 0,51% H2NCH2COOK және 2,56% H2NCH2COOK
D) *0,32% H2NCH2COOK және 4,04% H2NCH2COOK
E) 2,5% H2NCH2COOK және 3,75% H2NCH2COOK
2![]()
![]()
![]()
![]() 5. Тізбек арқылы: крахмал 1глюкоза
2этанол 3көміртек (IV) оксиді
крахмал. 243г крахмалдан, үшінші стадияда бөлінетін көміртек (IV)
оксидінің зат мөлшері:
5. Тізбек арқылы: крахмал 1глюкоза
2этанол 3көміртек (IV) оксиді
крахмал. 243г крахмалдан, үшінші стадияда бөлінетін көміртек (IV)
оксидінің зат мөлшері:
А) 9 моль
В) 15 моль
C) 12 моль
D) *6 моль
E) 3 моль
5-нұсқа
1. Мольдік массаны анықтау формуласы:
А)
![]()
B) ![]()
C) *![]()
D) ![]()
E) ![]()
2. Қосымша топша элементі
А) Be
В) Mg
С) Sr
D) * Ғе
Е) Са
3.СІ ₂ молекуласындағы химиялық байланыстың түрі
А) иондық
В) металдық
С)* ковалентті полюсcіз
D) Сутектік
Е) Ковалентті полюсті
4) Күшті электролиттің формуласы
А) Ag 4SO4
B)BaSO4
C) *K2 SO4
D) PbSO4
E) CaSO4
5.Cутек теріс тотығу дәрежесін көрсететін зат
А) *КН
В) НСІ
С) Н 2 S
D) H2 O
E) NH3
6.Салыстырмалы молекулалық массасы -40 болатын негіздің формуласы-
A) Ca (OH)2
B) KOH
C)* NaOH
D) Ba (OH)2
E) NH4 OH
7.Алюминий хлормен әрекеттескенде түзілетін заттың формуласы:
А) АІНСІ2
В) АІ(ОН)3
С) АІ2О3
D)*AICI3
E) AIJ3
8.Жалпы формуласы СпН 2п-6 болатын заттың атауы
А) гексан
В) октан
С)* бензол
D) ацетилен
Е) циклогексан
9.Фенолформальдегид смоласын алу үшін қолданылатын зат:
А)С6Н 4(NO 2) 2
В) С6Н5 - NO 2
C)* C6H5OH
D) C6H5-NH2
E) C6H5 –CH3
10.S+O2=SO2+297кДЖ термохимиялық теңдеуі бойынша 59,4 кДж жылу бөлінген болса,жанған күкірттің массасы (г(
А) 10
В)* 6,4
С) 7,2
D) 9,4
Е) 8
11.Массасы 200г NaОН ерітіндісі арқылы көміртек (ІҮ) оксидін жібергенде массасы 53г орта түзіледі. Бастапқы ерітіндідегі натрий гидроксидінің массалық үлесі:
А) 0,1
В)* 0,2
С) 0,3
D) 0,4
Е) 0,5
12.Бертолле тұзы КСІО3-тегі хлордың тотығу дәрежесі:
А) -1
В) +1
С) 0
D)* +5
Е) +7
13.Молекуладағы байланыстарының полярлығы кемитін заттар қатары:
А) H2S ,K2S,SO2
B) H2S,SO2, K2S
C) S8,H2S ,K2S
D)*K2S, H2S, S8
E) H2S, S8, ,K2S
14.Тотығу-тотықсыздану теңдеуіндегі HNO3→H2O+NO2+O2
Барлық коэффициенттердің қосындысы
А)5
В) 7
С) 15
D) *11
Е) 13
15.Көміртектің иіссіз,түссіз ауадан 1,5 есе ауыр,судағы ерітіндісі қышқыл болатын газ түріндегі қосылысы:
А)карболен
В)* көміртек (ІҮ) оксиді
С) карборунд
D) көмірқышқылы
Е) көміртек (ІІ) оксиді
16.Сынап (ІІ) нитратының ерітіндісін электролиздеу теңдеуіндегі барлық коэффициенттердің қосындысы
А)10
В)12
С)*11
D)9
Е)8
17.Темір алынбайтын үрдіс:
А)Ғе2О3-ті сутекпен тотықсыздандыру
В) Ғе3О4-ті алюминотермиялау
С) ҒеSО4-ті элекролиздеу
D)*Темір (ІІІ) гидроксидін айыру
Е) ҒеСІ2-ерітіндісін электролиздеу
18.Құрамы С7Н8О болатын фенолдың барлық изомерлерінің саны:
А) 2
В) 1
С) 5
D)*3
Е) 4
19.Іс жүзінде жүрмейтін реакцияның схемасы:
А) СН3СООН +Na→
В)*СН3СООН+Сu→
С) СН3СООН +K2O→
D) СН3СООН+НОС2Н5→
Е) СН3СООН+Са →
20.А және Е заттары
Электролизі +H2SiO3 +HNO3 t0
К


 СІ А Б С Е
СІ А Б С Е
А) К және КNO3
B) KOH және К2О
С) К және КNО2
D)*КОН және КNO2
E) К2О және КNO2
21.Циклопентанның тұйық тізбекті изомерлерлерінің саны:
А)*4
В) 1
С) 3
D) 2
Е) 5
22.Этилбензолды нитрлегендегі өнімнің 1 молінің массасы:
А)*241 г
В) 244 г
С) 240 г
D) 238 г
Е) 239 г
23.Егер шығымы 75% болса, онда 18 г глбкозаны тотықтырғанда түзілетін күмістің массасы:
А) 13,2 г
В)*16,2 г
С) 15,2 г
D) 17,2 г
Е) 14,2 г
24. Құрамында бір қос байланыс бар көмірсутектер
А) *Алкендер
В) Арендер
С) Алкиндер
D) Алкадиендер
Е) Алкандар
25.Құрамы 40% метан,60% этаннан тұратын 10 л газ қоспасын жағуға жұмсалатын (қ.ж) оттектің көлемі:
А)*29 л
В) 30 л
С) 31 л
D) 32 л
Е) 33 л
6-нұсқа
1.Электрондар доноры-
А)*N
B) Mg
C) H
D) K
E) Na
2.Кіші период элементтерінде атом радиусы бірінші элементтен соңғы элементке қарай өзгеруі
А) Артады
В) Минимум арқылы өтеді
С)*Кемиді
D) Максимум арқылы өтеді
Е) өзгермейді
3.Теріс электрлігі аз ажыратылатын элементтер атомдарының арасындағы байланыс:
А) иондық
В) сутектік
С)*Ковалентті полюсті
D) Ковалентті полюссіз
Е) донорлы-акцепторлы механизм
4.MgCI2 диссоциацияланғанда түзілетін иондар
А)*Мg2+ +CI-
В) Мg +2CI
С) диссоциацияланғанда түзілетін иондық
D) Мg2+ +CI-
Е) Мg2+ +CI2
5. ҮІ топтың А топшасындағы элементтердің ұшқыш сутекті қосылыстарының жалпы формуласы
А) НR
B) НRО3
С)*Н2R
D) Н4 R
Е) Н3 R
6.Негіздік оксидтің формуласы
А) N2O5
B) SiO2
C)*Na2O
D) SO2
E) NO
7.Алюминий электрондарының энергетикалық деңгейлерге бөлінгенін көрсететін сызба-нұсқа
А)* 2е 8е 3е
В) 2е 8е 8е
С) 2е 8е 8е 3е
D) 2е 7е
Е) 2е 8е 1е
8. .Лабораторияда метан алудың әдісі
А) 2СН4→С2Н2+3Н3
В)*СН3СООNa+NaOH →CH4↑+Na2CO3
C) табиғи газдан бөліп алу арқылы
D) С+2Н2→СН4
Е) 2СН3СІ + 2Na→СН3-СН3+2NaСІ
9.Полимерлену дәрежесі ....... көрсетеді.
А)*Политердің макромолекуласында неше мономер молекулалары біріккенін
В) Негізгі элементтің индексін
С)Балқу температурасын
D) қайнау температурасын
Е) Макромолекула санын
10.СО(r)+ 2Н2(r) →СН3ОН(r)+Q
Үрдісіндегі тепе-теңдікті солға ығыстыратын жағдай
А) қысымды жоғарылату
В) Н2концентрациясын арттыру
С)*СО концентрациясын төмендету
D) CH3OH концентрациясын төмендету
Е) температураның төмендеуі
11. 480 г 20 %-ті ерітінді дайындау үшін қажет калий гидроксидінің массасы:
А) 48 г
В) 40 г
С) 56 г
D)*96 г
Е) 20 г
12. Хлорлылау қышқылдың формуласы:
А) НСІ
В) НСІО2
С) НСІО3
D)*НСІО
Е) НСІО4
13. 3моль оттекпен әректтесетін натрийдің зат мөлшері (моль)
А) 15
В) 12
С) 9
D)*6
Е) 3
14.Күміс нитраты мен натрий фосфаты әрекеттескенде 41,9 г күміс фосфаты түзілген.Реакцияға түскен натрий фосфатының массасы (г) және зат мөлшері (моль)
А) 11,2 және 0,2
В) 21,6 және 0,3
С)*16,4 және 0,1
D) 36,2 және 0,2
Е) 46,1 және 0,1
15.Графит және алмаз бір элемент атомы-көміртектен – тұратынын дәлелдейтін әдіс:
А)*Екі затты жаққанда СО2 түзілуі
В) Сілтімен әрекеттесуі
С) Азотпен әректтесуі
D) Күкірпен әрекеттесуі
Е) Қышқылмен әрекеттесуі
16. Ғе2О3+С →Ғе +Со реакция үрдісі бойынша 280 г қызыл теміртастағы
(Ғе2О3) темірді тотықсыздандыру үшін қажет кокс массасы:
А) 68 г
В)*63 г
С) 56 г
D) 59 г
Е) 65 г
17.Екі сатыдан кейін фенол алуға болатын зат:
А) СН4
В) С2Н 2
С) С2Н 6
D)* С6Н6
Е) циклогексан
18.Х,Ү қосылыстары
СН4 →Х → С6Н12О 6 → Ү →СН3СООС2Н5
А)СО2,СН3СООН
В) СН2О,С2Н5ОН
С)*СО2, С2Н5ОН
D) СН3СООН, С2Н5ОН
Е) СН2О, СО2
19. Өзгерістер нәтижесінде алынатын «А» өнімнің аталуы:
+Br2 H2O +O Ag2O
C


 H3- CH3
X1
X2
X3
A
H3- CH3
X1
X2
X3
A
А) Формальдегид
В) Сірке альдегиді
С)*Сірке қышқылы
D) Күміс ацетаты
Е) Құмырысқа қышқылы
20. Газ толтырылған пластик
А) силикон
В) полиэтилен
С) *пенопластар
D) целлулоид
Е) аминопластар
21.Құрамында мырыштың массалық үлесі 37% болатын қосылыс
А) ZпО
В) ZпS
C)*K2ZnO2
D) ZnSiO3
E) Zn (OH)2
22.80 г 1,2% бром суын 200 мл (қ.ж) метан этилен қоспасы түссіздендіреді.Қоспадағы метанның көлемдік үлесі (%)
А) 3,32
В) 30,3
С)*32,3
D) 38,9
Е) 3,84
23.Массасы 9,9 г дихлорэтан алу үшін хлорсутекпен әрекеттесетін ацетиленнің (қ.ж) көлемі
А) 5,60
В) 4,48 л
С)*2,24 л
D) 22,40 л
Е) 1,12 л
24.85,5г сахароза гидролизденгенде алынған глюкозаны тотықтырғанда түзілген күмістің массасы
А) 46 г
В)*54 г
С) 48 г
D) 52 г
Е) 64 г
25. Егер белоктың мономері глицилаланин болып және одан гидролиздегенде 222,5 г аланин түзілсе,белоктың массасы
А)*365 г
В) 250 г
С) 290 г
D) 300 г
Е) 270 г
7-нұсқа
1. Қосылу реакциясы
A) ![]() .
.
B) ![]() .
.
C) ![]() .
.
D)* ![]() .
.
E) ![]() .
.
2. ![]() атомы ядросының құрамында:
атомы ядросының құрамында:
A) 80p және 36n.
B) 36p және 36n.
C) 36p және 44e.
D)* 36p және 44n.
E) 80p және 44n.
3.Ортақ электрон жұбы арқылы түзілетін химиялық байланыс.
A) иондық.
B)* ковалентті.
C) металдық.
D) сутекті.
E) молекулалық.
4. Диссоцияциясы сатылы жүретін қосылыс...
A) калий гидроксиді.
B) натрий хлориді.
C)* күкіртсутек қышқылы.
D) аммоний нитраты.
E) азот қышқылы.
5. Жану реакциясының белгісі -
A) қысым пайда болуы.
B) тұнба түзілі.
C)* жылу мен жарық бөлінуі.
D) ток пайда болуы.
E) заттардың сұйылуы.
6. Н3ВО3 осы қышқылға сәйкес келетін оксидтің формуласы
A)* В2О3.
B) Ве2О3.
C) ВО3.
D) ВО.
E) ВеО.
7. Натрий атомының электрондық конфигурациясы
A) 1s22s22p1.
B) 1s22s22p63s2.
C)* 1s22s22p63s1.
D) 1s22s22p3.
E) 1s22s22p4.
8. Құрамында бір қос байланыс бар көмірсутектер
A)* Алкендер.
B) Арендер.
C) Алкиндер.
D) Алкадиендер.
E) Алкандар.
9. Полимерлену дәрежесін көрсететін сан
A) Макромолекула саны.
B) Негізгі элементтің индексі.
C)* Полимердің макромолекуласында құрылымдық буын саны.
D) Қайнау температурасы.
E) Балқу температурасы.
10. Температура 30 С-қа төмендеп ,жылдамдық 27 есе азайғанда, температуралық коэффицент
A) 2.
B)* 3 .
C) 3,5.
D) 2,5.
E) 4.
11. 160 грамм ерітіндіні суалатқанда 40 құрғақ тұз қалды,ерітіндідегі еріген заттың массалық үлесі
A)* 25%.
B) 20%.
C) 30%.
D) 10%.
E) 15%.
12. 9,8 г күкірт қышқылы ерітіндісін натрий гидроксиді ерітіндісінің артық мөлшерімен бейтараптағанда,түзілетін тұздың зат мөлшері:
A) 0,05 моль.
B) 0,01 моль.
C) 1 моль.
D)* 0,1 моль.
E) 0,2 моль.
13. Фосфор қышқылы түзілетін реакция:
A) P2O3+H2O=
B) Na3PO4+H2O=
C) P2O5+H2O=
D)* Na2SO4+P2O5=
E) Na2O+K3PO4=
14. Алюминийдің гидроксиликатындағы байланыстардың жалпы саны
A)12.
B) 14.
C) 18.
D)* 19.
E) 15.
15. Ең активті металдардың (Na, K, Ca, Mg) өнеркәсіпте алыну әдісі
A) тұздар ерітінділердің электролизі.
B) көміртек (II) оксидімен оксидтерден тотықсыздандыру.
C) тұздар балқымаларының электролизі.
D)* көміртекпен оксидтерден тотықсыздандыру
E) алюминотеропия.
16.Өзгерістер сызба- нұсқасындағы FeCl2→X1→X2→Fe2O3 X1 және X2 заттары:
A) X1 – FeCO3, X2 – FeCl3.
B) X1 – Fe2(CO3)3, X2 – FeSO4.
C) X1 – Fe2(NO3)3, X2 – Fe2SO4.
D)* X1 – Fe(OH)2, X2 – Fe(OH)3.
E) X1 – FeO, X2 – FeCl2.
17. 230г этил спиртімен толық жағу үшін қажет оттектің (қ.ж.) көлемі
A)168 л.
B)112 л.
C)*336 л.
D) 224 л.
E) 210 л.
18. Фенол, натрий ацетатын ажыратады:
A)* Темір (III) хлоридінің ерітіндісі және фенолфталеин ерітіндісі.
B) лакмус ерітіндісі ,су.
C) сыртқы түрінен.
D) лакмус ерітіндісі,сілті ерітіндісі.
E) қорғасын нитраты,натрий гидроксиді.
19. Детонация дегеніміз-бензиннің ...
A) крекингіленуі.
B)* қопарылыс түзіп жануы.
C) пиролизденуі.
D) дегенерациялануы.
E) дегидрленуі.
20. 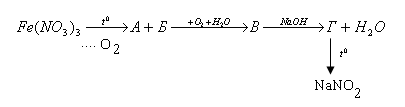
Тізбегіндегі А,В,Г заттары.
А) темір(II) оксиді, азот (IV) оксиді, натрий нитриты.
В)* темір(III) оксиді, азот қышқылы, натрий нитриты.
C) темір(II) оксиді, азот қышқылы, натрий нитриты.
D) темір(III) оксиді, азот қышқылы, натрий нитриты.
E) азот (II) оксиді, азот (IV) оксиді, натрий нитриты.
21. SiCl4 – тің толық гидролизі кезіндегі түзілетін екі зат.
A) Si және HCl.
B) SiO2 және HClO.
C) SiO2 және HCl.
D)* H2SiO3 және HCl.
E) H2SiO3 және Cl2.
22. 142 г. Йодметан мен 50г. Натрий әрекеттескенде түзілген этанның (қ.ж.) көлемі.
A) 44,8 л.
B)* 11,2 л.
C) 67,2 л.
D) 33,6 л.
E) 22,4 л.
23. 9,2 г. толуол толық жану үшін қажет ауаның көлемі (ауадағы оттектің көлемдік үлесі 20 %);
A) 103 л.
B) 105 л.
C)* 101 л.
D) 112 л.
E) 104 л.
24. картоптағы крахмалдың массалық үлесі 20 %, өнім шығыны 50 %, сыйымдылығы 50 кг. 5 қап картоптан алынған глюкозаның массасы.
A) 27,28 кг.
B)* 27,78 кг.
C) 27,38 кг.
D) 27,48 кг.
E) 27,18 кг.
25. Егер шығыны 70 % болса, 6,2 г метиламин алу үшін қажет нитрометанның масса:
A) 17,32 г.
B)* 17,43 г.
C) 19,21 г.
D) 18,12 г.
E) 17,78 г.
8-нұсқа
1. А+В = С+Д типті реакцияда 5 г. А заты мен 6г. В заты әрекеттесіп 3г. Д заты түзілген болса, С затының массасы:
A) 5 г.
B) 5 г.
C) 7 г.
D)* 8 г.
E) 9 г.
2. Атомның энергетикалық деңгейлеріндегі электрон
A) Al.
B) N.
C) As.
D)* P.
E) Cl.
3. Бір периодтағы элементтердің электр терістігі.
A) бірінші өсіп, сонан соң кемиді.
B) оңнан солға қарай өседі.
C)* солдан оңға қарай өседі.
D) солдан оңға қарай кемиді.
E) өзгермейді.
4. Үш сатылы диссоциацияланатын қосылыс.
A) мыс (ІІ) гидроксиді.
B) натрий хлориді.
C)* ортофосфор қышқылы.
D) күкірт қышқылы.
E) хром (ІІ) гидроксиді.
5. Атмосферадағы оттектің массалық үлесі (%).
A) 40.
B) 25.
C)* 21.
D) 35.
E) 30.
6. Суда жақсы еритің негіз:
A) Zn(OH)2.
B) Fe(OH)3
C) Cu(OH)2.
D)* LiOH.
E) Ca(OH)2.
7. Өзгерістер тізбегіндегі қышқыл тұз түзетін реакция
![]()
A) 1,4.
B) 2,4.
C)* 2,3.
D) 1,2.
E) 1,3.
8. sp - гибридтенген көміртек атомына сәйкес келетін валенттік бұрышы:
A)* 1800.
B) 1200.
C) 450.
D) 1080.
E) 1090.
9. Полимерлену реакциясы дегеніміз бұл -
A) екі заттың қосылу процесі.
B) тұздардың айырылуы.
C)* қос байланыстардын үзілуі есебінен мономердің бірдей молекулаларрының макромалекулаға бірігу процессі.
D) мономер қатысып, кіші молекулалы қосылыс бөліне жүретін полимер түзілу реакциясы.
E) каталитикалық гидрлеу процессі.
10. Термохимиялық теңдеуі S+O2=SO2 + 297 кДж болса, 16г. күкірт жаңғанда бөлінетін жылу мөлшері (кДж)
A) 135,5
B) 175,5
C)* 148,5
D) 182,5
E) 124,5
11. Күкір қышқылының 320 г. 10% - ті ертіндісіне 80г. су қосқанда алынған ерітіндегі Н2SO4 – тің массалық үлесі:
A) 6%
B)* 8%
C) 10%
D) 7%
E) 9%
12. Сутектің хлормен әрекеттесу механизімі осы заттың хлормен әрекеттесуіне ұқсайды:
A) анилиннің.
B)* алкандардың.
C) алкиндердің.
D) арендердің.
E) алкендердің.
13. 49 г. натрий гидрооксиді мен 49 г. күкір қышқылының ерітінділерін араластырғанда түзілетін тұздың массасы.
A) 51г.
B)* 71г.
C) 61г.
D) 91г.
E) 81 г.
14. Фосфор тотықтырғыш болатын химиялық теңдеу.
A) 4P+5O2 = 2P2O5.
B)* 2P+3Ba = Ba3P2.
C) 2P+3Cl2= 2PCl3.
D) 6P+5KClO3 = 5KCl+3P2O5.
E) 4P+3O2 = 2P2O3.
15. 8,4 г. көміртек (ІІ) оксидінің қалыпты жағдайдағы көлемі (л.).
A) 16,2 л.
B) 6,2 л.
C) 7,5 л.
D)* 6,72 л.
E) 5,8 л.
16. Магний хлоридінің ерітіндіс электролизге ұшырағанда катодта түзілген заттың салыстырмалы молекулалық массасы.
A) 4.
B) 24.
C)* 2.
D) 32.
E) 71.
17. Табиғатта темір формуласы төменде берілген заттар түрінде кездеседі, темірдің мөлшері көп зат.
A) FeS2
B) Fe2O3
C) Fe3O4
D)* FeO
E) FeCO3
18. Тотықтырғанда құмырсқа альдегидін түзетін сприттің құрамындағы көміртегі атомының саны:
A)* 1.
B) 2.
C) 3.
D) 4.
E) 5.
19. Мына өзгерістерде түзілетін A, B, C, қосылыстарына төмендегі заттардың сәйкестігі:
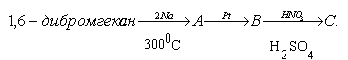
Жауапты А, В, С қосылыстарының түзілу ретімен қосылыстар белгіленге нөмірлер арқылы көрсетіңіз.
1. 2-нитрогексан. 2. гексан. 3. циклогексан. 4. 1,5 – гексадиен. 5. бензол. 6. нитробензол.
A)* 3, 5, 6.
B) 2, 3, 1.
C) 4, 5, 6.
D) 3, 4, 5.
E) 2, 3, 5.
20. Натрий концентрациялы тұз қышқылымен әрекеттескенде көлемі 5,6 л газ бөлінеді. (қ.ж.). Түзілген тұздың массасы.
А) 30,40 г.
В) 40,25 г.
C) 30,01 г.
D)* 29,25 г.
E) 25,16 г.
21. Азот бойынша тығыздығы 2,5 – ке тең 35 г. циклоалканды жаққанда жұмсалатын ауаның көлемі (ауадағы оттектің үлесі – 20%).
A) 460 л.
B) 430 л.
C)* 420 л.
D) 450 л.
E) 440 л.
22. 132 г. CH3COH ацетальдегид (шығымы 70%) алу үшін жұмсалатын құрамындағы 28 % қоспасы бар кальций карбидінің массасы.
A)* 265,5.
B) 325,5.
C) 235,5.
D) 355,5.
E) 255,5
23. 340 г. хлор бензол мен 220 г. натрий гидрооксиді әрекеттескенде түзілетін фенолдың массасы.
A) 244 г.
B) 274 г.
C)* 284 г.
D) 254 г.
E) 264 г.
24. 40,5 г. целлюлозаны нитрлегенде түзілген денитроцеллюлозаның массасы:
A)* 63 г.
B) 62 г.
C) 59 г.
D) 61 г.
E) 58 г.
25. Массасы 78 г. бензолды нитрлегенде іс жүзінде 105 г. нитробензол алынады. Нитробензолдың шығыны:
A) 4,27 %.
B) 8,54 %.
C) 42,7 %.
D)* 85,4 %.
E) 0,427 %.
9 –нұсқа
1. О химиялық таңбасы… көрсетеді.
A) бір молекуланы
B) мольдік массаны
C) бір атомды
D)* жай заттың бір молін
E) салыстырмалы молекулалық массаны
2. 20 протон 20 нейтрон және 20 электроны бар элементтің салыстырмалы атомдық массасы
A)* 20
B) 40
C) 68
D) 60
E) 78
3. Алмаздың кристалдық торы
A) молекулалық
B) иондық
C)* атомдық
D) атомдық, молекулалық
E) металдық
4. ![]() реакциясының ақырына дейін жүру себебі, нәтижесінде түзілетін
заттардың бірі -
реакциясының ақырына дейін жүру себебі, нәтижесінде түзілетін
заттардың бірі -
A) ерімейтін тұз
B) су
C) ерімейтін негіз
D)* тұнба
E) газ
5. Оттек газы
A)* суда жақсы ериді
B) дәмді
C) түссіз
D) өткір иісті
E) ауадан жеңіл
6. «Органикалық химия» деген атауды ұсынған ғалым...
A) Г.Кольбе
B) Ф.Велер
C) И.Берцелиус
D) Н.Зинин
E)* М.Бертло
7. Металл пісіру жұмысы кезінде көзді қорғау үшін арнайы маска киеді, себебі
A) ацетилен жанбайды
B) ацетилен көгілдір түсті жалынмен жанады
C) ацетилен бықсып жанады
D) ацетилен баяу жанады
E)* ацетилен өте жарқырап жанады
8. Қарапайым спирттің формуласы:
A) ![]()
B) ![]()
![]()
C) ![]()
D) *![]()
E) ![]()
9. Ең қарапайым карбон қышқылының аталуы:
A) Акрил қышқылы.
B) Сірке қышқылы.
C) Стеарин қышқылы.
D) Құмырсқа қышқылы.
E)* Май қышқылы.
10. Температураны
500С-тан 90 0С-қа көтергендегі ![]() реакция жылдамдығының артуы
реакция жылдамдығының артуы
A)* 8 есе
B) 10 есе
C) 16 есе
D) 12 есе
E) 4 есе
11. 80г ерітіндіні буландырған соң, ыдыста 20г тұз қалды. Ерітіндідегі еріген заттың массалық үлесі
A) 22 %
B) 30 %
C)*25 %
D) 35 %
E) 20 %
12. Тұз түзбейтін оксидтерге көбірек тән болатын қасиеттер
A) Гидролизге бейімділік
B)* Тотықсыздануға бейімділік
C) Тотығуға бейімділік
D) Этерификацияға бейімділік
E) Орынбасуға бейімділік
13. 1,5 моль күкіртсутек толық жанғанда түзілетін күкірт(IV) оксидінің массасы:
A) 64г
B) 9,6г
C) 3,2г
D) 96г
E) *32г
14. Сутегі бойынша тығыздығы 62-ге ақ фосфор молекуласындағы фосфор атом саны:
A) 2
B) 5
C) 1
D) 4
E)* 3
15. Реакцияда осы заттармен кремний- тотықсыздандырғыш болады
A) ![]()
B) ![]()
C) ![]()
D)*![]()
E) ![]()
16. Сілтілік металдарды тек қана тұздарының балқымаларын электролиздеу арқылы алуға болады. Оған себеп:
A) сілтілік металдардың белсенділігі төмен
B)* сілтілік металдар- ең белсенді металдар, сондықтан басқа әдістермен алу мүмкін емес
C) сілтілік металдар табиғатта бос түрінде кездеседі
D) сілтілік металдардың белсенділігі орташа
E) кернеу қатарында сілтілік металдар сутектен кейін орналасқан
17.III топ элементі хлоридінде жоғары валенттілік көрсетеді.Егер осы зат құрамында 79,77% хлор болса, металдың химиялық таңбасы және салыстырмалы атомдық массасы:
A)*45 Sc
B) 56 Fe
C) 70 Ga
D) 11 B
E) 27 Al
18. Темір тақташаны мыс (II) сульфаты ерітіндісіне батырғанда, 40г мыс бөлінді. Тақташаның массасы
A) *28г
B) 40г
C) 10г
D) 35г
E) 39г
19. Детонация дегеніміз
A)* Бензиннің қозғалтқышта қопарылыс түзіп жануы
B) мұнай өнімдерін айдау
C) Жоғары температурада бөлшектенуі
D) Жоғары қысымда мұнай өнімдерінің бөлшектенуі
E) Мұнайдың өнімдерін тазарту
20. Схеманы пайдаланып А, В, С заттары
![]()
![]()
![]()
A)
![]() ,
, ![]() ,
, ![]()
B)
![]() ,
, ![]() ,
, ![]()
C)
*![]()
![]() ,
, ![]()
D)
![]()
![]() ,
, ![]()
E)
![]()
![]()
![]() .
.
21.Әрқайсысы екі мольден: тұз, бромсутек, фторсутек, иодсутек қышқылдарының қоспасына күміс нитратымен әсер еткенде түзілген тұнбаның зат мөлшері:
A)* 2 моль
B) 8 моль
C) 6 моль
D) 4 моль
E) 10 моль
22. 250г гептан бір мезгілде циклденгенде және дегидрленгенде бензолдың гомологы түзіледі. Осы кезде түзілген газдың көлемі (қ.ж.литрмен)
A) 112
B)* 224
C) 198
D) 148
E) 168
23.Массалық үлесі 20 %-тті 90г глюкоза ерітіндісі күміс оксидінің аммиактағы ерітіндісімен әрекеттескенде массасы 2г күміс бөлінсе, күмістің шығымы (%)
A) 9,3
B) 9,5
C) 10,2
D) *10,5
E) 9,4
24. Құрамында 15,73 % -азот бар моноамин қышқылының күрделі эфирінің құрылысы:
A)* ![]()
B) ![]()
C) ![]()
D) ![]()
E) ![]()
25. Нитрон талшығының мономері акрилонитрилді пропеннен алады:
Құрамына пропеннің көлемдік
үлесі – 15 %табиғи газдың ![]() -нан (қ.ж) алынатын
акронитрилдің массасы (г) :
-нан (қ.ж) алынатын
акронитрилдің массасы (г) :
A)* 2842
B) 2840
C) 2835
D) 2839
E) 2830
10- нұсқа
1. Химиялық құбылысқа жататыны
A) крекингілеу.
B) шайқау.
C) буландыру.
D)* хромотографиялау
E) дистилдеу.
2. Элементтің реттік нөмірі көрсетеді:
A) протон және нейтрон санын
B) протон және изотоп санын
C)* протон және нуклон санын
D) протон және электрон санын
E) нейтрон және электрон санын
3. Калий хлориды түзілетін кристалдық тордың түрі
A) *молекулалық
B) молекулалық, атомдық
C) металдық
D) атомдық
E.)иондық
4. Диссоциация кезінде катион ретінде сутек пен металл иондары түзілетін заттардың аты:
A) қышқыл тұздар
B) қышқылдар
C)негізгі тұздар
D)* сілтілер
E) орта тұздар
5. Оттегінің латынша аталуы
A) оксигениум
B) силициум
C) гидрогениум
D) гидраргирум
E.)*феррум
6. ![]() - гибридизация кезінде
валенттік бұрыш тең
- гибридизация кезінде
валенттік бұрыш тең
A) ![]()
B) *![]()
C) ![]()
D) ![]()
E) ![]()
7. Көміртек қаңқасы бойынша пентадиен-1,2-нің изомері:
A)* пентин-1
B) пентадиен-1,3
C) пентин-2
D) 2-метилбутадиен-1,3
E)3-метилбутадиен-1,2
8. Сірке қышқылының молекулаларының арасындағы байланыс
A) сутектік
B) иондық
C) *ковалентті полюсті
D) металдық
E) ковалентті полюссіз
9. Синтетикалық талшық
A) мақта
B)жүн
C) ацетатты талшық
D)* жібек
E) капрон
10. Егер температураны
400C-қа көтерсе, реакция
жылдамдығы ![]() ... есе
артады
... есе
артады
A)16
B)* 4
C) 2,5
D) 5
E)14
11. Сумен орын басу реакциясына түсетін зат
A) ![]()
B) ![]()
C) *![]()
D) ![]()
E) ![]()
12. 4 моль күкірт қышқылының массасы:
A )490 г
B) 196 г
C) 441 г
D)* 392 г
E.)98 г
13. Күкірт(VI) оксиді мен калий гидроксиді әрекеттескендегі (орта тұз түзілсе) толық иондық теңдеудегі барлық коэффициенттер қосындысы
A) 5
B) 7
C) *9
D) 8
E) 6
14. ![]() қыздырғанда пайда болатын
заттар
қыздырғанда пайда болатын
заттар
A)сынап оксиді, оттек, азот (II) оксиді
B) сынап, азот (IV) оксиді, оттек
C) сынап, азот (II) оксиді, оттек
D) *сынап оксиді, оттек, азот (IV) оксиді
E)сынап (I) нитраты және оттек
15. Қысқартылған иондық теңдеу бойынша әрекеттесетін заттардың жұбы:
![]()
A) магний карбонаты мен натрий гидроксиді
B) калий карбонаты мен су
C) көмір қышқыл газы мен су
D)* көмір қышқыл газы мен натрий гидроксиді
E)натрий карбонаты мен тұз қышқылы
16. Металдардың жалпы химиялық қасиеттерін көрсететін реакциялар үрдісінің жұбы
A)* ![]()
![]()
B) ![]()
![]()
C) ![]()
![]()
D) ![]()
![]()
E) ![]()
![]()
17. ![]() және
және ![]() иондарындағы протондарының
жалпы саны
иондарындағы протондарының
жалпы саны
A) 31
B) 33
C) 32
D)* 30
E) 28
18. ![]() өзгерісінде Х заты
өзгерісінде Х заты
A) ![]()
B) ![]()
C) *![]()
D) ![]()
E) ![]()
19. Мына затты анықтау үшін мыс (ІІ) гидроксидін қолданады
A) пропанол
B) циклогексан
C)* бензол
D) глюкоза
E) фенол
20. 7,8 г алюминий гидроксидін еріту үшін қажет 10% -ті натрий гидроксиді ерітіндісінің массасы:
A) 30 г
B) 60 г
C) 40 г
D)* 20 г
E) 50 г
21. ![]()
Реакция теңдеуіндегі жалпы коэффициент саны
A) 7
B) * 3
C) 10
D) 5
E) 14
22. 60 г этан мен 240 г бром әрекеттескенде түзілген бромэтанның массасы :
A) 143,3 г
B) 133,6 г
C) 163,5 г
D)* 173,5 г
E) 153.6 г
23. 25 г 94 % -тік фенол ерітіндісі мен 75 г1 % бром суын араластырғанда түзілетін реакция өнімінің массасы:
A) 0,52 г
B) 0,63 г
C) 0,47 г
D)*0,35 г
E) 0,59 г
24. 0,5 моль целлюлоза азот қышқылымен әрекеттескенде түзілетін тринитроцеллюлозаның массасы:
A) 148,4 г
B) 148,2 г
C) 148,3 г
D)* 148,5 г
E) 148,1 г
25. Құрамында элементтердің массалық қатынастары
m(C) :m(O) :m(N) :m(H) = 12 :16:7:2,5 болатын зат:
A![]() )
) ![]()
![]()
![]()
B![]() )
) ![]()
![]()
C![]() )
) ![]()
![]()
D![]() )
) ![]()
![]()
E![]() ) *
) * ![]()
![]()
Исабаева Гүлбаршын Тұрсынғалиқызы, т.35-28-23
11 нұсқа
1. Егер химиялық реакцияның кескіні төмендегідей болса
∆ + О → ∆О
Онда реакцияның типі
A) айырылу
B) қосылу
C) *орын басу
D) алмасу
E) бейтараптану
2. Электрондық формуласы 3s23p4 элементтің реттік нөмірі
A) * 16
B) 10
C) 14
D) 6
E) 12
3. Тотығу-тотықсыздану реакцияларына жататын реакцияның сипаттамасы
A) ерімейтін заттар түзіле жүретін реакциялар
B) * әрекеттесуші заттар элементтерінің тотығу дәрежесі өзгеретін реакциялар
C) әлсіз электролиттер
түзіле жүретін реакциялар
D) әрекеттесуші заттар иондары арасындағы алмасу реакциялары
E) газ түзіле жүретін реакциялар
4. Катион болып есептелетін бөлшек
A) Cr2O72-
B) * NH4+
C)
Cl-
D) SO42-
E) NO3-
5. Металдарды оксидтерінен тотықсыздандыруға қолданылытын газ
A) хлор
B) озон
C) * сутек
D) фтор
E) оттек
6. Алкиндердің жалпы формуласы
A) * СnH2n-2
B) СnH2n
C)
СnH2n-+
2
D) СnH2n-6
E) СnH2n+1
7. Диен көмірсутектеріне тән емес реакция
A) гидрлену
B) полимерлену
C) * гидролиз
D) жану
реакциясы
E) галогендермен
әрекеттесу
8. Эфирлену реакциясы
A) СН3ОН + СН3ОН → СН3 ─ О ─ СН3 + Н2О
B) 2СН3ОН + О2 → 2СО2 + 4 Н2О
C) НСОН +Ag2O → НСООН + 2Ag↓
D) *
НСООН + СН3ОН → НСОО СН3
+ Н2О
E) 2С2Н5ОН + 2 Na → 2С2Н5ОNa + Н2↑
9. Кремнийорганикалық полимерлер
A) * силикондар
B) фенопластар
C) пенопластар
D) каучуктер
E) аминопластар
10. Катализатор ретінде Н2 SO4 (конц.) қолданылатын реакция
A) С6H6 + О2 →
B) С6H6 + Br2 →
C) * С6H6 + HNО3
→
D) С6H6 + H2 →
E) С6H6 + Cl2 →
11. Массасы 40 г сусыз мыс (ІІ) сульфатын алу үшін кристаллогидраттың
СuSO4∙∙5 Н2О қажет массасы
A) 91,5 г
B) * 62,5 г
C) 52,5 г
D) 31,5 г
E) 41,5 г
12. Берілген қосылыстардан: Na2О, HCl, SO3, Ca(OH)2, H3PO4 калий гидроксидімен әрекеттесін қосылыстар саны
A) * 3
B) 1
C) 2
D) 4
E) 5
13. Егер калий бромидінің 200 г ерітіндісінен хлормен 16 г бром ығыстырылған болса, оның проценттік концентрациясы
A) 15,4%
B) 10,2%
C) * 11,9%
D) 6,2 %
E) 14,0%
14. 320 г мысты концентрлі күкірт қышқылында еріткенде түзілген мыс (ІІ) сульфатының моль саны
A) * 5
B) 3
C) 1
D) 4
E) 2
15. Аммиактың сутекпен салыстырғанда тығыздығы
A) 6,5
B) 4,0
C) * 8,5
D)
0,117
E) 17,0
16. Магний сульфаты ерітіндісін электролиздегенде катодта бөлінетін жай заттың молекулалық массасы
A) 26
B) 24
C) 16
D) * 2
E) 32
17. ІІ топтағы металдың 20 грамы судан 11,2 л сутекті қ.ж. ығыстырады. Осы металл
A) * Са
B) Ва
C)
Sr
D) Be
E) Mg
18. Мыс пластинкасын қара ұнтаққа, одан кейін көк ерітіндіге айналдыру процесін көрсететін реакциялар жұбы
A) * Сu + O2 →
CuO + HCl →
B) Cu + Н2О →
CuCl2 + NaOH →
C) Cu + O2 →
CuO + Н2О →
D) Cu + Cl2 →
Cu + HgCl2 →
E) Cu + O2 →
CuO + Cu(OH)2 →
19. Схемадағы Х заттың формуласы
to, Ni, (+H2) HNO3 (H2SO4 конц.)
С2Н4 → С2Н6 → Х
A) С2Н4 NO2
B) С2Н2 NO2
C) С2Н5NO3
D) * С2Н5 NO2
E) С2Н5N
20. 31 г кальций фосфатын алу үшін жұмсалатын негіз бен қышқылдың массалары (г)
A) 28,2 ; 22,6
B) 31,2; 15,6
C) 15,2; 33,6
D) 25,2; 39,6
E) * 22,2; 19,6
21. 2,5 кг кальций карбонатын күйдіргенде бөлінген көмірқышқыл газының көлемі 448 л (қ.ж.). Ыдырауға жұмсалған кальций карбонатының массалық үлесі
A) 85%
B) * 80%
C) 75%
D) 90%
E) 100%
22. Азот бойынша тығыздығы 2,5-ке тең циклоалканның 14 грамын жаққанда түзілетін көмірқышқыл газының көлемі (қ.ж.)
A) 4408 л
B) * 22,4 л
C) 179,2 л
D) 11,2 л
E) 89,6л
23. 30 г пропанол мен 20 г калий әрекеттескенде шығымы 60% болса, түзілетін сутектің көлемі (қ.ж.)
A) * 5,6 л
B) 4,48 л
C) 1,12 л
D) 2,24 л
E) 3,36 л
24. Егер шығымы 75%, 620 г крахмалды гидролиздегенде түзілген глюкозаның спирттік ашуынан түзілетін этанол массасы (г)
A) 650
B) 630
C) * 690
D) 700
E) 720
25. 88 г триброманилин алу үшін 35%-ті бром суының
(ρ= 1,02 г/см3) қажет көлемі (мл)
A) 415,3
B) 425,5
C) * 358,5
D) 325,5
E) 375,5
12 нұсқа
1. Күрделі зат
A) вольфрам
B) алтын
C) * күкіртсутек
D) күкірт
E) алюминий
2. Атомның электрондық формуласы 1s22s22p63s 23p63d74s 2 болатын элемент
A) мыс
B) көміртек
C) калий
D) *
кобальт
E) кальций
3. Ковалентті полюссіз байланысқа жататын зат
A) SO3
B) * Cl2
C)
Na2О
D) Fe(OH)3
E) Al
4. Диссоциацияланғанда Н+ ионын түзетін зат
A) CrOH)3
B) Ca(OH)2
C)
Na2SiO3
D) K2CO3
E) * H2SO3
5. Мырыш сульфатын түзетін заттар жұбы
A) ZnO және Н2S
B) Zn және S
C) *
Zn(OH)2 және Н2SO4
D) Zn және SO3
E) Zn және SO2
6. Органикалық қосылыстардың химиялық құрылыс теориясын ашкан
A) Бертло М.
B) Лебедев С.В.
C) Марковников В.В.
D) Менделеев
Д.И.
E) * Бутлеров
А.М.
7. Көп атомды спиртке жататын зат
A) ROH
B) (СН3)3C─OH
C)
CH3─
СН2─
СН2OH
D) C6H5OH
E) * СН2ОН─ СН2──
СН2ОН
8. Өндірісте сірке қышқылын алатын реакция теңдеуі
A) +[O]
НСОН → HCOOH
+[O]
B) * СН3─ СН2── СН2─CH3 → 2 CH3COOH
- Н2О
C) С2Н4 +[O] → CH3COOH
+ Н2О [O]
D) С2Н4 → CH3COH
→ CH3COOH
+ Н2О
E) С2Н2 → CH3COOH
9. Жоғары молекулалық қосылыстар мынадай болып бөлінеді
A) оксидтер және тұздар
B) қышқылдар және негіздер
C) оттекті және
оттексіз
D) қаныққан және қанықпаған
E) * табиғи және химиялық
10. 1 моль суйық судың түзілу жылуы 286 кДж тең болса, 7,2 г су түзілгенде жұмсалатые жылу мөлшері
A) 104,4 кДж
B) * 114,4 кДж
C) 102,2 кДж
D) 103,4 кДж
E) 110,4 кДж
11. Іс жүзінде суда ерімейтін зат
A) мыс купоросы
B) калий хлориді
C) қант
D) * күміс хлориді
E) кальций гидкроксиді
12. Күкірт қышқылы мен темір (ІІ) гидроксиді әрекеттескенде (егер негіздік тұз түзілсе) барлық қойылатын коэффициент саны
A) 8
B) 3
C) 2
D) 4
E) * 6
13. Бертолле тұзындағы ( KClO3) хлордың тотығу дәрежесі
A) +1
B) -1
C) * +5
D) 0
E) +7
14. 568 г фосфор (V) оксидін алу үшін жұмсалатын оттектің (қ.ж.) көлемі (л)
A) 56
B) 100
C) 112
D) 448
E) * 224
15. 2 г әктасты күйдіргенде 336 мл (қ.ж.) көмірқышқыл газы түзілді. Әктастағы қоспаның массалық үлесі
A) 30%
B) 75%
C) * 25%
D) 50%
E) 35%
16. Мыстың массалық үлесі көп қосылыс
A) CuS
B) CuO
C)
CuSO4
D) CuCl2
E) * Сu2О
17. Натрий гидроксидімен әрекеттесетін заттар қатары
A) Ag2S, BaSO4, PbSO4,
B) * СО2, CuCl2. HCl
C) SO2, BaSO4, H3PO4
D)
P2O5, HNO3,
K2SO4
E) Cl2, KCl, H2SO4
18. 2-метилбутадиен-1,3 молекуласындағы σ-байланыстың саны
A) 7
B) 11
C) 8
D) * 12
Е) 9
19. Химиялық өзгерістер тізбегіндегі Y заты
+ HBr
С2Н4 → X → Y → С2Н5 ─ O ─ С2Н5
A) ацетальдегид
B) бромэтан
C) диметил эфирі
D) * этанол
Е) этан
20. + Н2О +HJ t
Mg3N2 → A↑ → B → A↑ тізбегіндегі В затының молекулалық массасы
A) 278
B) 129
C) 17
D) * 145
E) 127
21. Массасы 10,3 г натрий бромидіне концентрлі күкірт қышқылымен әсер еткенде 0,896 л күкірт (ІV) оксиді бөлінді. Өнімнің шығымы
2 Н2SO4 + 2 NaBr → SO2 ↑ + Na2SO4 + Br2 + 2 Н2О
A) 60%
B) 90%
C) 75%
D) 78%
E) * 80%
22. Калий карбонаты мен темір (ІІІ) хлоридінің ерітінділері арасындағы реакция нәтижесінде түзілген темір қосылысының құрамы
A) Fe2(CO3)3
B) FeOHCO3
C)
FeCl3
D) * Fe(OH)3
E) Fe(OH)2
23. 14 г циклопентан 12 л хлормен (қ.ж.) әрекеттескенде, шығымы 70% болса, түзілген хлорциклопентанның массасы (г)
A) 15,6
B) 20,9
C) * 14,6
D) 11,9
E) 17,2
24. 5%-ті 200г глюкоза ерітіндісінен спирттік ашығанда түзілетін көмірқышқыл газының көлемі (л)
A) 2,89
B) 2,69
C) 2,09
D) * 2,49
E) 3,69
25. Мына заттың атауы
СН3
│
СН3 ─ С ─ СН── СН2 ─ СН2 ─ COOH
│
СН3 NH2
A) α-амино-ε,ε - диметилвалериан қышқылы
B) α,α -диамино - β -метилкапрон қышқылы
C) * γ-амино- δ,δ -
диметилкапрон қышқылы
D) δ - амино – α,α -диметилвалериан қышқылы
E) β- амино – δ,δ -диметилкапрон қышқылы
13-нұсқа
1. Құрамында 82% - азот және 18% сутегі бар белгісіз заттың формуласы
А) *NH3
В) N2O3
С) N2O5
D) NO
Е) NH4NO3
2. Реттік нөмірі 17-ші элементтің электрондық конфигурациясы
А) 3s23p2
В) 3s23p1
С) *3s23p5
D) 3s23p3
Е) 3s23p4
3. Концентрациялы азот қышқылы
А) тотықсыздандырғыш
В) *өте күшті тотықтырғыш
С) алтын мен платинаны ерітеді
D) металдармен әрекеттеспейді
Е) барлық металдарды пассивтендіреді
4. Сулы ерітіндіде тек анион бойынша гидролизденетін натрий тұзы
А) бромид
В) хлорид
С) *силикат
D) нитрат
Е) сульфат
5. Оттек газы
А) *түссіз
В) суда жақсы ериді
С) дәмді
D) өткір иісті
Е) ауада жеңіл
6. Электролиттерге жатады
А) спирт
В) металдар
С) бейметалдар
D) *тұздардың судағы ерітінділері
Е) қант
7. Сілтілік металдарға жатады
А) Na, Zn, Cu
В) Ca, Mg, Se
С) *К, Na, Li
D) Fe, Ca, Ni
Е) K, Ca, Mg
8. Органикалық қосылыстардағы көміртек атомдарының арасындағы химиялық байланысының түрі ....
А) иондық
В) * ковалентті полюссіз
С) сутектік
D) металдық
Е) ковалентті полюсті
9. Макромолекулаларда –CH2-HC=CH-CH2- қарапайым буыны бар зат:
А) *Бутадиен каучугі
В) Полипропилен
С) Полистирол
D) Хлоропренді каучук
Е) Полиэтилен
10. Кальцийдің сумен әрекеттесуінен түзілген күрделі заттың мольдік массасы:
А) 70 г/моль.
В) 80 г/моль.
С) 76 г/моль.
D) *74 г/моль.
Е) 78 г/моль.
11. Гидролизденетін тұз
А) NaCl
В) Na2O
С) *NaF
D) NaJ
Е) NaBr
12. Күкіртсутек толық жанбағанда түзілетін өнімдер:
А) * S, H2O
В) SO2, H2O
С) H2, SO2
D) SO3, H2O
Е) SO3, H2
13. 16,8 л аммиак синтездеу үшін (қ.ж) қажет сутектің көлемі
А) 72, 0 л
В) 30, 6 л
С) 33,6 л
D) *25,2 л
Е) 36,2 л
14. 200 г ізбестас ыдырағанда түзілетін көмірқышқыл газдың көлемі
А) 22,4 л
В) *44,8 л
С) 33,6 л
D) 5,6 л
Е) 11,2 л
15. Тұздар ерітіндісінен хромның ығыстырып шығаратын металы
А) марганец
В) * мыс
С) кальций
D) алюминий
Е) мырыш
16. Калий дихроматындағы хромның массалық үлесі (%)
А) 25
В) 65
С) *35
D) 55
Е) 45
17. Бензолдан бромбензол алу реакциясы
А) қосылу реакциясына жатады
В) *орын басу реакциясына жатады
С) ыдырау реакциясына жатады
D) жану реакциясына жатады
Е) тотығу реакциясына жатады
18. Массасы 60 г суда 1 моль формальдегидті ерітті. Ерітіндідегі формальдегидтің массалық үлесі:
А) 30,3 %
В) 50,3 %
С) *33,3 %
D) 40,3 %
Е) 32,3 %
19. Бензолдан, толуолдан, пентаннан, ксилолдан крекинг-бензинді ажырату жолы
А) *Қанықпаған көмірсутектерінің реактивтерімен (KМnO4, бром суы) қолдану.
В) Күміс нитратымен қолдану.
С) Күкірт қышқылының ерітіндісімен қолдану.
D) Ізбес суымен қолдану.
Е) Жағып, жалын арқылы.
20. Ацетиленнің жануының термохимиялық теңдеуі
2C2H2+5O24CO2+2H2O+2600 кДж.
Егер көлемі бойынша 20 % қоспасы бар, 25л ацетиленді (қ.ж.) жақса бөлініп шығатын жылу
А) 116,0 кДж.
В) 58 кДж.
С) 290 кДж.
D) *1160,7 кДж.
Е) 13,0 кДж.
21.
![]() өзгерістер тізбегінде
іске аспайтын стадиялар
өзгерістер тізбегінде
іске аспайтын стадиялар
А) 1,2
В) 2,3
С) 3,4
D) *1,3
Е) 1,4
22. 41 г натрий ацетатын 30 г натрий гидроксидімен әрекеттестіргенде (қ.ж.) түзілген метанның көлемі
А) *11,2 л
В) 1,4 л
С) 5,6 л
D) 2,8 л
Е) 22,4 л
23. Өзара әрекеттескенде үшіншілік бутил спиртін түзетін заттар жұбы:
А) * (CH3)2C=CH2 және H2O
В) (CH3)2CH2 және CH3Br
С) (CH3)3CCl және CH3Br
D) (CH3)3CH және NaOH
Е) (CH3)3CH және H2O
24. Техникада глюкозаны крахмалды гидролиздеу арқылы алады. Егер реакция өнімінің шығымы теориямен салыстырғанда 75 % болатын болса, 81 кг крахмалдан алынатын глюкозаның массасын есепте.
А) 36,5 кг
В) 69,5 кг
С) 48,5 кг
D) *67,5
Е) 56,5 кг
25. 10,3 г этиламиноацетатты алуға жұмсалатын аминосірке қышқылы мен этанолдың массасы
А) 7,8 г; 2,5 г
В) 6,8 г; 3,8 г
С) *7,5 г; 4,6 г
D) 6,2 г; 3,7 г
Е) 5,7 г; 2,5 г
14-нұсқа
1. Алмасу реакциясы
А) 2H2+O22H2O
В) 2KClO32KCl+3O3
С) *CuO+2HClCuCl2+ H2O
D) N2+3H22NH3
Е) Fe+CuCl2 FeCl2 +Cu
2. Ядродағы протон саны ...
А) топ нөмірін көрсетеді
В) период нөмірін көрсетеді
С) *рет нөмірін көрсетеді
D) ұшқыш сутекті қосылыстардың жалпы фомуласын көрсетеді
Е) жоғарғы оксид формуласын көрсетеді.
3. Алмаздың кристалл тор түйіндерінде орналасқан бөлшектер
А) аниондар
В) *атомдар
С) атомдар және молекулалар
D) катиондар
Е) молекулалар
4. Катион болып есептелетін бөлшек
А) SO42-
В) Cr2O72-
С) *NH4+
D) NO3-
Е) Сl-
5. Өнеркәсіпте оттегін алу әдісі
А) Ауаны ығыстыру әдісі
В) Суды ығыстыру әдісі
С) *Ауаны қысып, сұйылтуып, айдау
D) Электр тогы әсерімен суды айыру
Е) Сынап оксидін қыздырғанда
6. Қышқыл тұз
А) Na3PO4
В) *NaH2PO4
С) CuOHCl
D) K2NaPO4
Е) Ca3(PO4)2
7. Натрий атомының электрондық конфигурациясы:
А) *1s22s22p63s1
В) 1s22s22p63s23p63d104s1
С) 1s22s22p63s23p63d54s1
D) 1s22s22p1
Е) 2s22s1
8. Жалпы формуласы CnH2n-6 болатын қатардың мүшесі
А) нафталин
В) тротил
С) *бензол
D) бензин
Е) фенол
9. Метанальдің судағы 40%-тік ерітіндісі:
А) Алколят
В) Фенолят
С) *Формалин
D) Ацетат
Е) Этиленгликолят
10. Натрий нитратының 500 г 7 %-ті ерітіндісіне 200 г су қосқанда алынған ерітіндідегі NaNO3-тің массалық үлесі:
А) 1%
В) 2%
С) *5%
D) 4%
Е) 3%
11.
![]() тізбегіндегі Х, Ү
заттары
тізбегіндегі Х, Ү
заттары
А) MgO, Mg(OH)2
В) * MgOHCl, Mg(OH)2
С) MgOHCl, MgO
D) MgO, MgOHCІ
Е) Mg(OH)2, MgO
12. Лабораторияда HCl-ды алу үшін қажет H2SO4 мен NaCl–дың жағдайлары:
А)* NaCl(кат.)+H2SO4(конц.)![]()
В) NaCl(балқыма)+H2SO4(сұйт.)
С) NaCl(ертін)+H2SO4(сұйт.)
D) NaCl(ертін)+H2SO4(конц.)
Е) NaCl(кат.)+H2SO4(сұйт.)
13. H2O- H2S- H2Sе- H2Те – қатарында қышқылдар күшінің өзгеруі:
А) Кемиді
В) Артады, соңынан кемиді
С) Өзгермей қалады
D) *Артады
Е) Кемиді, соңынан артады
14. Азоттың ауа бойынша тығыздығы:
А) 0,25
В) *0,96
С) 0,74
D) 0,53
Е) 0,82
15. Оттектің массалық үлесі көп зат
А) PbO2
В) *CO2
С) SnO2
D) GeO2
Е) SiO2
16. Электролиз кезінде анодта жүретін процесс:
А) Айырылу
В) Орын басу
С) Тотықсыздану
D) *Тотығу
Е) Алмасу
17. Таза никель алуға болатын тәсіл
А) *Электрометаллургия
В) Көміртектітермия
С) Алюмотермия
D) Сутектітермия
Е) Металлотермия
18. 4,4 демителгексен-2 құрамына сәйкес заттың жалпы формуласы.
А) CnH2n+2
В) *CnH2n
С) CnH2n-6
D) CnH2n-4
Е) CnH2n-2
19. Мына өзгерістер схемасындағы А заты:
(C6H10O5)n C6H12O6A С2 H5OC2H5
А) * C2H5OH
В) CO2
С) CH3OH
D)
CH3 - CH – COOH
|
OH
Е) CH3COOH
20. 2NO+O22NO2+Q теңдеудегі тепе-теңдікті оңға ығыстыратын факторлар нөмірлері.
1. Оттектің концентрациясын көбейту
2. Азот (ІІ) оксидінің концентрациясын кеміту
3. Температураны арттыру
4. Қысымды азайту
5. Температураны төмендету
6. Қысымды арттыру
7. Катализатор қолдану.
А) *1 5 6.
В) 2 4 6
С) 1 4 6
D) 2 5 6
Е) 1 3 5
21. Егер дегидрлегенде 56 л сутек бөленетін болса, жұмсалған циклогексанның, түзілген бензолдың массалары
А) 30 г, 25 г,
В) *70 г, 65 г
С) 50 г, 45 г
D) 40 г, 35 г
Е) 60 г, 55 г
22. 35 г метил спиртінен 12 г диметил эфирі алынған болса, диметил эфирдің шығымы:
А) 88 %
В) 58 %
С) 68 %
D) *48 %
Е) 78 %
23. Массасы 360 кг глюкоза ашығанда, 300кг этил спиртінің ерітіндісі алынған. Осы ерітіндідегі спирттің массалық үлесі
А) 61,2
В) 61,4
С) *61,3
D) 60,0
Е) 61,1
24. Егер бірінші және екінші сатысында түзілген заттың шығымы 50%, ал соңғы сатысында 100 % болса, 33 г 2,4,6-триброманилин алу үшін қажет бензолдың массасы
А) 30,0 г
В) *31,2 г
С) 32,0 г
D) 29,2 г
Е) 32,8 г
25. 50 г полипропиленді толық жағу үшін қажет (қ.ж.) ауаның көлемі (Ауадағы оттектің көлемдік үлесі – 0,2.)
А) 400 л
В) 500 л
С) * 600 л
D) 700 л
Е) 300 л
16 нұсқа
-
Күрделі зат
А) Графит
В) *Су
С) Күкірт
D) Сутек
Е) Алмаз
-
VІ – топтың негізгі топшасы элементтерінің атомдарының электрондық конфигурациясының жалпы формуласы
А) ns2 np6
В) *ns2 np4
С) ns2 np5
D) ns2 np2
Е) ns2 np3
-
Ковалентті полюссіз байланысы бар қосылыс
А) натрий хлориді
В) хлорлы сутек
С) су
D) *оттек
Е) сутек пероксиді
-
Ион алмасу реакциясы
А) NH3+ H2O = NH4OH
В) *CaCl2+Na 2CO3=CaCO3+2NaCl
С) Zn+SnCl2=ZnCl2+Sn
D) NH3+HCl=NH4Cl
Е) Zn+Cl2=ZnCl2
-
Оттек жай зат түрінде... құрамында кездеседі
А) *атмосфера
В) дистилденген су
С) құм
D) гранит
Е) әктас
-
Алюминий гидроксидімен тұз қышқылы әрекеттескенде түзілетін орта тұз
А) Al (OH)3
В) *Al Cl3
С) AlOHCl2
D) Al2O3
Е) Al(OH)2Cl
-
Ерітіндісі жалынды кірпіш қызыл түске бояйтын қосылыс
А) ерігіш шыны
В) *ғаныш
С) кір сабын
D) сильвинит
Е) ас содасы
-
Циклопентанға тән жалпы формула
А) CnH 2n+2
В) CnH2n-2
С) CnH2n-6
D)* CnH2n
Е) CnH2n-1
-
Табиғи жоғары молекулалық қосылыстарға жататын зат:
А) глюкоза
В) *целюлоза
С) мальтоза
D) сахароза
Е) полиэтилен
-
Al2O3 +6HCl = 2AlCl3+3H2O +Q үрдісінің сипаты
А) *қайтымсыз және гетерогенді
В) қайтымсыз және гомогенді
С) қайтымды және экзотермиялық
D) қайтымсыз және эндотермиялық
Е) қайтымды және гетерогенді
-
250г 2% -ті ерітінді дайындау үшін қажет натрий хлоридінің массасы
А) *5г
В) 2г
С) 4г
D) 1г
Е) 3г
-
Егер күкірттің молярлық массасы 256г/моль болса, ондағы күкірттің атомдарының саны
А)* 8
В) 4
С) 7
D) 2
Е) 6
-
49г фосфор қышқылын алу үшін қажет фосфор (Ү) оксидінің массасы (г) және зат мөлшері (моль)
А) 14,8 және 0,15
В) 54,3 және 0,55
С)* 35,5 және 0,25
D) 48,2 және 0,45
Е) 32,8 және 0,35
-
Қозған күйіндегі конфигурациясы ... 3s13p33d0 болатын элемент
А) Sn
В) *Si
С) C
D) Al
Е) N
-
49г фосфор қышқылын алу үшін қажет фосфор (Ү) оксидінің массасы (г) және зат мөлшері (моль)
А) 14,8 және 0,15
В) 54,3 және 0,55
С)* 35,5 және 0,25
D) 48,2 және 0,45
Е) 32,8 және 0,35
-
Өзгерістер сызба-нұсқасында
+Cl2 +NaOH +HNO3 t0
Fe X1 X2 X3 X4
X1 және X4 заттары
А) Fe Cl2 және Fe2О3
В) Fe Cl2 және Fe
С) Fe Cl2 және FeО
D)* Fe Cl3 және Fe2О3
Е) Fe Cl3 және Fe(NО2)2
-
Этил спиртінен бутадиенді алғаш алған ғалым
А) В.В. Марковников
В) Н.Н. Семенов
С) М.В. Ломоносов
D)* С.В.Лебедев
Е) Н.Д.Зелинский
-
Этанол мен реакцияға түсетін зат:
А)* HBr
В) KBr
С) Ba (OH)2
D) NaOH
Е) H2O
-
22г этанальды гидрлегенде түзілген спиртті 177 мг суда ерітілді, ерітіндідегі спирттің массалық үлесі:
А) 11%
В) 10%
С) 14%
D)* 11,5%
Е) 13%
-
16г темір (ІІІ) оксидін толық тотықсыздандыру үшін қажет сутегінің мөлшері тең
А) 0,1 моль
В) 5 моль
С)* 0,3 моль
D) 3 моль
Е) 2 моль
-
20л 36,5% -ті тұз қышқылы ерітіндісін (р= 1,18г/мл) даярлау үшін (қ.ж.) қажет хлордың көлемі
А) 7,92м3
В)* 2,64 м3
С) 1,32м3
D) 5,28м3
Е) 4,44м3
-
13г пропенмен қосылу реакциясына түсетін бромның массасы:
А) 52,4г
В) 48г
С)* 49,5г
D) 32г
Е) 45,6г
-
575мл спирт (р= 0,8г/мл) алу үшін жұмсалатын глюкозаның массасы
А) 950г
В) 850г
С)* 900г
D) 970г
Е) 800г
-
Көлемі 8л метиламинді жағуға қажет ауаның (оттекті ң ауадағы көлемдік үлесі 0,2) (қ.ж.) көлемі:
А) 18л
В) 56л
С)* 90л
D) 8л
Е) 45л
-
Сызбанұсқадағы С заты:
+Н2О + NaOH NaOH, t0
Глицилглицин А В С
А)* CH3NH2
В) CH3COONa
С) C6H6
D) C2H6
Е) CH3COOH
17 нұсқа
-
Алмасу реакцияларында газдың түзілуі.
А) Қайтылымдықтың белгісі
В)* Қайтымсыздықтың белгісі
С) Экзотермиялықтың белгісі
D) Эндотермиялықтың белгісі
Е) Айырылудың белгісі
-
Химиялық қасиеттері ұқсас элементтер
А) Li және Be
В) Be және Ba
С) Na және Ag
D)* Li және Na
Е) Be және B
-
Беймолекулалық құрылысты зат
А)*NaH
В) CH4
С) H2O
D) NH3
Е) HNO3
-
Диссоциацияланғанда NO3- түзетін зат
А) KNO2
В) K2SO3
С) *NaNO3
D) H3PO4
Е) Fe (OH)3
-
Агрегаттық күйі сутекпен бірдей зат
А) Na
В) Ca
С) Al
D) *He
Е) S
-
Амфотерлі оксидтің қасиеті
А) сумен және қышқылмен әрекеттесуі
В) қышқылмен және қышқылдық оксидтермен әрекеттесуі
С) тұзбен және қышқылмен әрекеттесуі
D)* қышқылмен және негізбен де әрекеттесуі
Е) тұзбен және негізбен әрекеттесуі
-
Оттекті қышқыл -
А) *HNO3
В) HCl
С) CaO
D) CO2
Е) Zn (OH)2
-
Молекула құрамы бірдей болғанымен, құрылымы өзгеше болғандықтан, қасиеттері де өзгеше болатын органикалық заттар атауы
А) гомологтар
В) дальтонидтер
С) изотоптар
D) *изомерлер
Е) бертоллидтер
-
Химиялық синтез арқылы және өсімдіктерден алынатын жоғарғы молекулалы полимер
А) целюлоза
В) гликоген
С) резеңке
D) *каучук
Е) крахмал
-
Термохимиялық теңдеу бойынша: 4Р + 5О2 = 2Р2О5 + 3010кДж 62г фосфор жанғанда бөлінетін жылу мөлшері
А) 1485кДж
В) 1450кДж
С) 1350кДж
D)* 1505кДж
Е) 1400кДж
-
290г 20%-ті ерітінді дайындау үшін қажет натрий бромидінің массасы:
А) 48г
В) *58г
С) 29г
D) 14г
Е) 43г
-
Бөлшектердің саны көп зат:
А)* 224л Cl2
В) 254г J2
С) 38г F2
D) 160г Br2
Е) 160г O2
-
Аниондардың тотықсыздандырғыш қасиеттерінің арту қатары
А) *O 2-S 2-Se2-
В) Te2- Se2- S2-
С) Se2- Te2- S2-
D) S2-O2- Te2-
Е) Se2- Te2- Se2-
-
Қосылыстардағы азотттың ең көп массалық үлесі бар зат:
А) HNO3
В) Ca(NO3)2
С) N2O5
D)*NO
Е) KNO3
-
100л көміртек (ІІ) оксиді жанғанда қажет болатын оттектің көлемі (қ.ж.):
А) 100 л
В)* 50 л
С) 75 л
D) 150 л
Е) 125 л
-
32 г мыс ұнтағы 11,2 л оттек (қ.ж) бар ыдыста қатты қыздырылды. Түзілген оксидтің массасы:
А) *40 г
В) 20 г
С) 60 г
D) 2 г
Е) 0,4 г
-
102 г пентадиен – 1,3 зат мөлшері (моль)
А) 5,4
В) 2,3
С) 3,1
D)* 1,5
Е) 4,2
-
1,2,3-трихлорпропаннан глицерин алу үшін қажет зат:
А) С3Н6
В) СН3СООН
С) НВr
D) *H2O
Е) Na
-
22% 150г құмырсқа қышқылын бейтараптауға жұмсалатын натрий гидроксидінің массасы
А) 25,6г
В)* 28,7г
С) 22,3г
D) 26,3г
Е) 21,6г
-
40г мыс (ІІ) сульфаты бар ерітіндіге 16г темір ұнтағын қосқанда бөлінген мыстың массасы:
А) 40г
В) 24г
С) 28г
D)* 16г
Е) 32г
1 2 3 4
-
ККОНКCl KNO3 KNO2 өзгерістер тізбегіндегі әрекеттесетін реагенттердің дұрыс реті
А) O2,HCl, HNO3, O2
В) H2O, HCl, HNO3, O2
С)* H2O, CuCl2, AgNO3, t0
D) O2, CuCl2, AgNO3, O2
Е) H2O, HCl, AgNO3, H2O
-
Циклопарафиндердегі көміртектің массалық үлесі (%)
А) 95,7
В) 55,7
С)* 85,7
D) 65,7
Е) 75,7
-
Массасы 64,8г крахмалдан алынған глюкозаның шығымы 80% болса , осы глюкозаны күміс оксидінің аммиактағы ерітіндісімен тотықтырғанда тұнбаға түскен күмістің массасы
А) 69,18г
В) 69,16г
С)* 69,12г
D) 68,13г
Е) 69,95г
-
10,53г метиламинбутилат алу үшін шығымдылығы 90% болса, жұмсалатын амин қышқылы мен спирттің маасалары
А) 10,8г; 5,2г
В 1,5г ; 3,7г
С)* 10,3г; 3,2г
D) 8,7г ; 4,5г
Е) 9,5г ; 4,2г
-
11,2л (қ.ж.) сутек бөліну үшін натрий мен әрекеттесетін фенол және метанолдың массалары
А) 188г, 64г
В) 128г, 56г
С) 142г, 60г
D) *94г, 32г
Е) 150г, 30г
18 нұсқа
1.Химиялық реакцияның белгісі
А) балқуы
В) ұнтақталуы
С)* түс өзгеруі
Д) жылтырауы
Е) еруі
2.Электрондық конфигурациясы 1s2 2s2 2p6 болатын элемент
А) O
В) F
С)* Ne
Д) Ca
Е) C
3.Бромсутек молекуласында химиялық байланысты түзуге қатысатын электрон саны
А) 4
В) *2
С) 6
Д) 18
Е) 3
4.Сl- анионына реактив болатын зат
А) *Күміс нитраты
В) Натрий оксиді
С) Алюминий гидроксиді
Д) Калий нитраты
Е) индикатор
5.Қыздырғанда оттегімен әрекеттеспейді
А) темір
В) күкірт
С) фосфор
Д)* алтын
Е) мыс
6.Іс жүзінде жүрмейтін реакцияның схемасы
А![]() ) BaO
+H2O
) BaO
+H2O
В![]() ) SO2 +
H2O
) SO2 +
H2O
С![]() )* CuO+ H2O
)* CuO+ H2O
Д![]() ) P2O5 + H2O
) P2O5 + H2O
Е![]() )CaO +
H2O
)CaO +
H2O
7.Алкендер класының сипаттамасына жатпайды
А) кеңістікте молекуланаң құрылысы жазықтық
В) *гибридтену түрі sp3
С) валенттілік бұрышы 1200
Д) 1п байланыс
Е) С=С байланысының ұзындығы 0,134нм
8.Күрделі эфирлердің жалпы формуласы
А) R- NH2
В) ROR1
С) R-OH
Д)* RCOOR1
Е) NH2-R-COOH
9.Полиэтилен- ... полимер болады
А) әрі табиғи, әрі химиялық
В)* химиялық, синтетикалық
С) табиғи, өсімдік текті
Д) табиғи, жануар текті
Е) химиялық жасанды
1![]() 0.2HgO (қ) 2Hg (қ) + O2(г) –Q
0.2HgO (қ) 2Hg (қ) + O2(г) –Q
т![]() еңдеуінде
тепе-теңдікті оңға ығыстыратын жағдай
еңдеуінде
тепе-теңдікті оңға ығыстыратын жағдай
А) қысымды көтеру
В) температураны төмендету
С)* қысымды төмендету
Д) катализатор енгізу
Е) О2 концентрациясын арттыру
11.Гидроксоний ионындағы оттектің валенттілігі
А) *3
В) 1
4С)
Д0)
Е) 2
12.168г калий гидроксиді 63г азот қышқылымен әрекеттескенде түзілетін тұздың мөлшері (моль)
А) 4
В) 3
С) 0,5
Д) *1
Е) 2
13.Хлордың жалпы қасиетіне сай емес тұжырымдама:
А) Сары жасыл түсті,өткір иісті газ
В)* Тек тотықтырғыштық қасиеттері болады
С) Суда еріп,хлор суын түзеді
Д) Исі бар
Е) Ауадан 2,5 есе ауыр
14.6,12 мл суда 44,8 (қ.ж) күкіртсутек ерітілген. Ертіндідегі H2S- тің (%)
Массалық үлесі:
А)2,6%
В)*10%
С) 5,2%
Д) 12%
Е) 10,6% Fe
15.Аммиактың зертханада алыну реакциясы
А![]() ) NH4OH
+HNO3 NH4NO3+H2O
) NH4OH
+HNO3 NH4NO3+H2O
В![]() ) N2 +3H2
2NH3
) N2 +3H2
2NH3
С![]()
![]() ) *2NH4Cl+Ca(OH)2
CaCl2+2NH3
+2H2O
) *2NH4Cl+Ca(OH)2
CaCl2+2NH3
+2H2O
Д![]()
![]() ) 3NH3+H3PO4 (NH4)3PO4
) 3NH3+H3PO4 (NH4)3PO4
Е![]() ) NH4NO3 N2O
+2H2O
) NH4NO3 N2O
+2H2O
16.Көміртекпен қосылысы этинді алуға қолданатын металл:
А)Ba
В) Mg
С) K
Д) *Ca
Е) Na
17.Магниймен барлығы әрекеттесетін заттар тобы
А)*HCl , CO2 , FeSO4
В) HBr , H2O ,MgCl2
С) HNO3 ,KOH ,O2
Д) H2SO4 , H2O ,KCl
Е) H2SO4 , NaOH , H2O
18.Тек екіатомды спирттерге жататын зат:
А) *CH3 – CHOH- CHOH- C2H5
В)CH3-CH-CH3
![]()
CH2OH
С) CH3CH2OH
Д) CH2OH-CHOH-CH2-OH
Е) CH2OH-CHOH-CH-CH3
![]()
OH
19.Заттардың барлығы сутекті қосып ала алмайтын топ:
А) C2H4 , C6H6
В) C2H2 , CH3OH
С)*C3H8 , CH3NH2
![]()
![]() O
O
Д) CH3-C , C6H6
![]() H
H
Е)C2H2 , C3H4
20.Массасы 12г алюминий мен мыс(II) оксидтерінің қоспасы натрий гидроксидімен әрекеттескенде 11,25г натрий металюминаты түзілді.
Қоспадағы мыс оксидінің массасы:
А)9г
В) *5г
С) 7г
Д)6г
Е) 18г
21.Тотығу үрдісінің сызба-нұсқасы
А![]() )CrO4-2 Cr +3
)CrO4-2 Cr +3
В![]() )* Fe+3
FeO4-2
)* Fe+3
FeO4-2
С![]() ) Cr2O7-2
Cr0
) Cr2O7-2
Cr0
Д![]() ) MnO4-2
Mn+2
) MnO4-2
Mn+2
Е![]() ) MnO4-
MnO4-2
) MnO4-
MnO4-2
22.Құрамы 90% метан, 5%этан, 3%көміртек диоксиді және 2% азот газдарынан тұратын қоспанвң 50м3 көлемін жағу үшін қажет ауаның
көлемі (м3)
А)465
В) 486
С)* 497
Д)470
Е) 473
23.4г кальций карбидінен алынған ацетиленді толық гидрлегенде шығымы
75 % болса, алынатын этанның көлемі (қ.ж)
А)*1.05
В) 2.05
С) 3.05
Д)4.05
Е) 5.05
24.Егер шығымы 90%, ал картоптағы крахмалдың массалық үлесі 20% болса, 100кг картоптан алынатын глюкозаның массасы
А)21
В) 22
С) 24
Д)*20
Е) 23
25.Дипептид глицилглициндегі көміртектің массалық үлесі
А)8,36%
В) 21,36%
С) 40,36%
Д)*36,36%
Е) 35,36%
19- нұсқа
1. Fe3O4+Al арасындағы реакцияның типі.
А) Қосылу
В) Айырылу
С) * Орын басу
D) Алмасу
E) Бейтараптану
2.Сыртқы энергетикалық деңгейіндегі электрондық формуласы 4s24p4 болатын элемент атом.
А) Cr
В) Ti
С) * Se
D) Ge
E) S
3. Терісэлектрлігі өте алшақ атомдардың арасында болатын байланыс.
А) ковалентті полюсті
В) донор акцепторлы
С)* иондық
D) сутектік
E) ковалентті полюссіз
4.Ең күшті қышқыл.
А)* H2SO4
В) H2SiO3
С) H2SO3
D) H3PO4
E) H2CO3
5. Периодтық жүйедегі күкірттің орны.
А) 5-ші период VI B тобы
В) 2-ші период VI A тобы
С)* 3-ші период VI A тобы
D) 6-шы период II B тобы
E) 4-ші период VI A тобы
6. Қышқыл оксидтің формуласы.
А) ZnO
В) CaO
С)* Cl2O7
D) Na2O
E) Fe2O3
7. Пропеннің гомологы болмайтын зат.
А)* C4H6
В) C7H14
С) C5H10
D) C6H12
E) C2H4
8. 2,3,3- триметилпентан қышқылының формуласы.
А![]() ) CH3
) CH3
H3C –C – CH2 – CH2 – COOH
![]()
CH3
В) C2H5
![]() H3C – C – CH2
– CH2 - COOH
H3C – C – CH2
– CH2 - COOH
![]()
CH3
CH3
![]()
С) * H3C – CH2 – C – CH – COOH
![]()
![]()
CH3 CH3
D) H3C – CH2 – CH2 – CH – COOH
![]()
C2H5
E![]() ) H3C – CH – CH – CH2 – COOH
) H3C – CH – CH – CH2 – COOH
![]()
CH3 CH3
9. Ашық тізбекті глюкоза молекуласындағы гидроксил тобының саны.
А) 1
B)* 5
C) 3
D) 4
E) 2
10. 2 моль метан жанғанда 1604 кДж жылу бөлінетін болса, химиялық реакцияның жылу эффектісі CH4( r ) +2O2( r )= CO2 ( r )+2H2O + Q
А) 803 кДж
B)* 802 кДж
C) 804 кДж
D) 816 кДж
E) 798 кДж
11. Калий хлоридінің 400г 10%-ті және 100г 5%-ті ерітінділерін қосқанда алынған ерітіндідегі KCl – дың массалық үлесі.
А)* 9%
B) 7%
C) 8%
D) 10%
E) 6%
12. Өзгерістер тізбегінің осы стадиясында қышқыл қатысады.
N


 2 1
NH3 2 NH4Cl 3
NH3 4 N2
2 1
NH3 2 NH4Cl 3
NH3 4 N2
A) 1
B)* 2
C) 3
D) 4
E) 1,4
13. KClO3 – тегі барлық ковалентті байланыстардың саны.
A) 6
B) 2
C) 3
D)* 5
E) 4
14. 8 моль азот қышқылы айырылғанда бөлінетін оттектің мөлшері.
A) 1 моль
B) 8 моль
C)* 2 моль
D) 4 моль
E) 3 моль
15. Ерітінділері сілтілік орта көрсететін заттар.
A) Na2SO3 , K2SO4
B) Na2CO3 , K2SO4
C)* Na2CO3 , K2SiO3
D) Na2SiO3 , KNO3
E) NaNO3 , K2CO3
16. Катодта жүретін процесс.
A) Айырылу
B)* Тотықсыздану
C) Диссоциация
D) Тотығу
E) Бейтараптану
17. Өзгерістер тізбегіндегі тұнба түзілетін реакциялар.
C


![]() uO 1 CuCl2
2 Cu(OH)2 3
CuSO4 4 Cu3(PO4)2
uO 1 CuCl2
2 Cu(OH)2 3
CuSO4 4 Cu3(PO4)2
A)* 2.4
B) 1.3
C) 3.4
D) 2.3
E) 1.2
18. Орташа молекулалық массасы 100000 – ға тең полипропиленнің полимерлену дәрежесі және бір макромолекуласын синтездеуге жұмсалатын пропиленнің ( қ.ж ) көлемі.
A)* 2381;53,4 м3
B) 2431;49,4 м3
C) 2452;48,5 м3
D) 2331;52,5 м3
E) 2385;46,7 м3
19. Ацептиленнен тікелей алынатын заттар.
A) глицерин, фенол
B) глюкоза, метаналь
C)* этаналь, бензол
D) толуол, бутаналь
E) крахмал, этаналь
20. Құрамында 45% күкірті бар 1т пириттен шығымы 98% болса, түзілетін күкіртті газдың массасы (г)
A) 0,68
B) 0,78
C)* 0,47
D) 0,98
E) 0,88
21. Өзгерістер тізбегіндегі.
N


 a +O2 A t0 B
HNO3 C t0
D
a +O2 A t0 B
HNO3 C t0
D
A және D заттары:
A) Na2O және NaOH
B)* Na2O2 және NaNO2
C) Na2O2 және NaNO3
D) Na2O және Na2N
E) Na2O және NaNO3
22. Құрылысы төмендегідей заттың дұрыс аты:
CH3 C2H5 Br CH3
![]()
![]()
![]()
![]()
![]() Br – CH2
– CH – C – C – CH – CH3
Br – CH2
– CH – C – C – CH – CH3
![]()
Br Br
A) Тетрабром – диметил – этилгексан.
B) 2- метил -3,3- дибром -4-бром -4-этил – 5-метил – 6-бром.
C)* 1,3,4,4- тетрабром -2,5- диметил – 3-этил гексан.
D) Триметил – этил – бромметил – трибромбутан.
E) 5- метил – 3 – этил -4,4- дибром –пентан.
23. 39 г бензолды хлорлағанда 0,25 моль хлорбензол алынса, түзілген заттың шығымы (%-пен )
A) 30%
B) 40%
C) 70%
D)* 50%
E) 60%
24. Егер шығымы 55% болса, онда 30кг көміртек (II) оксиді бар синтез газдан түзілетін метанолдың массасы.
A)* 18,9кг
B) 23,9кг
C) 19,9кг
D) 21,9кг
E) 15,9кг
25. 15г сірке қышқылынан (әр сатысының шығымы 75% болса) алынатын 15% - тік аминсірке қышқылының массасы.
A) 75,3г
B) 67,8г
C)* 70,3г
D) 65,8г
E) 71,5г
20-нұсқа
1. 3 моль магний жанатын болса,түзілетін магний оксидінің зат мөлшері
а) 2,5 моль
в)* 3 моль
с) 2 моль
d) 1.5 моль
е) 4 моль
2. периодтық жүйенің үшіншісі периодын аяқтайтын элементтің сыртқы электрон қабатындағы электрондар саны
а)* 8
в) 6
с) 18
d) 14
e) 2
3. oң және теріс зарядталған бөлшектер
а) протон
в)* иондар
с) ядро заряды
d) атомдық масса
e) нейтрон
4. бейэлектролиттер деп... заттарды айтамыз
а) электр тоғын өткізетін
в) металдар
с) өзгеріссіз
d)* элект тоғын өткізбейтін
e) өзгеретін
5.тек қышқылдық қасиет көрсететін оксидтер
а)* so2
b) al2o2
c) mgo
d) cao
e) na2o
6. тек амфотерлі оксидтердің қатары
а)*al2o3 zno
b) beo2
c) zno, mgo
d)feo, no
e) zno, cao
7. кальций гидроксидімен әрекеттесетін зат
а)*co2
b)na 2
c)nacl
d)naoh
e)na2so4
8. молекуладағы атомдардың орналасу реті ... қарай анықталады .
а) атомдардың санына
b) тотығу дәрежесіне
c)* валенттілігіне
d)атомдардың түріне
e)салыстырмалы атомдық массасына
9. «көмірсулар»деп аталу себебі
а)алғашқы өкілдері хош иісті болған
b)*алғашқы зерттелген өкілдері көміртегі мен судан тұрған
c)құрамында гидроксил тобының болуына байланысты
d)құрамында карбонил тобының болуына байланысты
e)құрамында карбоксил тобының болуына байланысты.
10. этиленнің жану реакциясының термохимиялық теңдеуі: с2н4+3о 2=2со2+2н2о +1400 кдж, егер реакцияға 336л оттегі кірісетін болса, бөлінген жылудың мөлшері.
а) 5000 кдж
b) 8000кдж
c) 4000кдж
d)* 7000кдж
e) 6000кдж
11. судың молекуласының құрылысы
а) сызықтық
b)*бұрыштық
c) тетраэдрлік
d) жазықтық
e)зигзаг тәрізді
12. натрий гидроксидінің ерітіндісімен әрекеттесетін оксидтер қатары.
а) cro мен p2o 5
b)* ai2 o3 пен р2 о5
c) со мен р2 о5
d) al2 о3 мен со
e) сro мен со
13. натрий хлоридінің балқымасын электролиздегенде түзілетін заттар.
а) оттек пен хлор
b) оттек пен натрий гидроксиді
c)* хлор мен натрий
d) хлор мен натрий гидроксиді
e) натрий мен оттек
14. азот қосылыстарының формулалары берілген:
1.nh3; 2.n 2o5; 3. нno2 ; 4. n2o; 5. no. олардың азот атомының тотығу дәрежесінің кему ретімен орналасуы.
а) 5 4 3 2 1
b) 1 2 3 4 5
c)* 2 3 5 4 1
d) 2 4 3 5 1
e) 3 2 5 4 1
15. кальций оксидіне көмір қосып қатты қыздырғанда түзілетін газ
а)*со
b)со2
c)о2
d)н2
e)n2
16. мыс (ii) сульфаты ерітіндісін электролиздегенде түзілетін заттар:
(электродтар инертті)
а)*сu,o2
b)cu,so3
c)h2,o2
d)cu,so2
e)cu,h2
17. егер реакция нәтижесінде тек темір (iii) гидроксиді түзілген болса, онда реакцияға қатысатын заттар:
а)fe2o3 және h2o
b)fe және h2o2
c)*fe(oh)2 және h2o2
d)fe3o4 және h2o
e)feo және h2o
18.390г бензолды гидрлегенде 336г циклогексан алынған.реакция өнімінің шығымы
а)100%
b)95%
c)*80%
d)85%
e)90%
19. реакция өнімінің шығымы 70% болса, 330г ацетальдегидтен алынатын сірке қышқылының массасы(г)
а)*315
b)405
c)360
d)270
e)450
20. 79,2г темір (ii) сульфидіне артық мөлшерде тұз қышқылын қосып, түзілген газды натрий гидроксидінің 15-%-тік 240г ерітіндісі арқылы өткізгенде түзілген тұздың формуласы және массасы:
а)nahso4 , 40,4г
b)na2s, 50,4г
c)*nahs, 50,4г
d)na2so4 , 50,4г
e)na2so3, 44,4г
21.егер реакцияның шығымы 80% болса, 40 грамм метанды толық хлорлағанда түзілетін тетрахлорметанның массасы:
а)279г
b)285г
c)*308г
d)315г
e)320г
22. егер пропанол-1 дегидрациялап, алынған қосылысқа хлорсутекпен әсер етсек түзілетін өнім
а)1,2-дихлорпропан
b)*2-хлорпропан
c)хлорлы этил
d)винилхлорид
e)пропилхлорид
23. 190г 2% аминсірке қышқылының ерітіндісімен әрекеттесетін пропанолдың массасы
а)*3г
b)9г
c)18г
d)15г
e)6г
24. құрамында 45% этилен бар 500л этиленнің (қ.ж.)
этанмен қоспасынан алынатын полиэтилен массасы
а)320,38г
b)250,65г
c)380,25г
d)*281,25г
e)311,25г
25. өзгерістердің нәтижесінде түзілетін "d" заттың аталуы
+hono2 +[h]
c
 h4→c2h2→c6h6 a d
h4→c2h2→c6h6 a d
a)нитробензол
b)нитрозобензол
c)нитрофенол
d)*анилин
e)фенол
21-нұсқа
1.Орынбасу реакциясы:
А) Fe +S→
В) Cu (OH)2 →
С) ZnO +H2 SO4 →
D)* Zn + 2 HCl →
Е)Ca (OH)2 + 2 HCl →
2.Алтыншы периодтағы барлық элементтер саны
А) 2
В)* 32
С) 1
D) 23
Е) 8
3.Тотығу процесі
А) Заттың агрегаттық күйінің өзгеруі
В) элементтің валенттілігінің өзгеруі
С) электронды қосып алу
D)* электронды беру
Е) иондарды қосып алу
4)Иондық алмасу реакциясының нәтижесінде көміртек(IV)оксидің түзетің заттар:
А) Fe(NO3) 2 және NaCl
В)* Na2CO3 және H2SO4
С) K2SO4 және BaCl2
D) CuCl2 және KOH
Е) HCl және Al(OH)3
5. Сутек изотопы-протийдің таңбалануы
А)* 1H
В) 2H
С) 2H
D) 3H
Е) 1H
6.Сөндірілген ізбестің формуласы
А) CaO
В)* Ca(OH)2
С) Ca(HCO3)2
D) CaCO3
Е) CaHCO3
7.Қаныққан көмірсутектерді халықаралық номенклатура бойынша атағанда алдымен молекуладағы көміртек қанқасының…табады:
А) ацилді тізбегін
В) ең қысқа тізбегін
С)* ең ұзын тізбегін
D) цикілді тізбегін
Е) тармақты тізбегін анықтап алады
8.Альдегидтердің молекулалық массалары өсуіменбірге
А) суда ерігіштігі артады
В)* суда ерігіштігі кемиді
С) қайнау температуралары кемиді
D) қайнау температуралары өзгермейді
Е) тығыздығы кемиді
9.Жоғары молекулалық қосылыс-
А)* малекуласы қайталанып отыратын атомдар тобынан тұратын молекулалық массасы өте үлкен заттар.
В) 2 атомнан тұратын зат.
С) қайнау температурасы төмен заттар.
D) тек тірі организмдерде кездесетін зат.
Е) массасы өте үлкен зат.
10.Азот(II) оксиді тотыққанда азот(IV) оксидіне айналып,жылу бөлінеді.
Осы реакция типі және қысымды арттырғанда тепе-теңдіктің ығысуы
А) Эндотермиялық,тура жүретін реакция жағына.
В)* Экзотермиялық,тура реакция жағына.
С) Экзотермиялық, тепе-теңдік ауыспайды.
D) Эндотермиялық, тепе-теңдік ауыспайды.
Е) Экзотермиялық,кері реакция жағына.
11.Калий хлоридінің 250 г 6%-рітіндісіне 50 г су қосқанда алынған ерітіндідегі KCl-дың массалық үлесі…
А)* 5%
В) 2%
С) 3%
D) 4%
Е) 1%
12.Тұз қышқылмен әрекеттесетін зат.
А)* Темір(III) оксиді
В) Кремний(IV) оксиді
С) Фосфор (V) оксиді
D) Хром (VI) оксиді
Е) Темір (III) хлориді
13. 130 г ұнталған мырыш 100 г күкіртпен әрекеттескенде алынған мырыш сульфидінің моль саны.
А) 5
В) 3
С) 4
D)* 2
Е) 1
14.Өзгерістер сызбанұсқасы берілген:
1 2 3 4
N2→ NH3→(NH4)2SO4→NH4Cl→NH3 1 және 3 станцияларға қолданылатын реактивтер.
А) H2; HCl
В)* H2; BaCl2
С) H2; KCl
D) H2; NH4Cl
Е) H2; BaCl2
15.Метандағы көміртектің массалық үлесі.
А) 70%
В) 90%
С)* 75%
D) 85%
Е) 80%
16.Fe3O4-ті тұз қышқылында еріткенде түзілетін заттар
А)* FeCl2,FeCl3 және H2O
В) FeCl3; және H2O
С) FeCl2; және H2
D) FeCl3; және H2
Е) FeCl2; және H2O
17.Бутадиенді каучуктің монометрінің құрамы
А) 4 атом көміртек және 8 атом сутек
В) 6 атом көміртек және 4 атом сутек
С)* 4 атом көміртек және 6 атом сутек
D) 6 атом көміртек және 8 атом сутек
Е) 4 атом көміртек және 10 атом сутек
18.4,7 г фенол бром суының артық мөлшерімен әрекеттескенде шығымы 90% болса,түзілген өнім массасы.
А) 10,2 г
В) 22,7 г
С) 27,5 г
D)* 14,9 г
Е) 31,7 г
19.Төмендегі өзгерістерге А,В,С заттарының реттік нөмірлері
HCl NaOH CH3COOH
C2H4 → A → B → C
1) Винилхлорид. 2) Этаналь.
3) Этихлорид. 4) Этан қышқылы.
5) Этанол. 6) Екіэтил эфирі.
7) Этилацетат.
А) 2,4,7
В) 1,5,6
С) 2,4,6
D)* 3,5,7
Е) 2,4,5
20.Өзгерістер схемасы берілген
1 2 3 4
H2O→O2→Fe3O4→Fe→FeCl3
Фторды қолдануға болатын стадия:
А)* 1
В) 2
С) 3
D) 4
Е) 3,4
21. 230 г натрий 780 мл сумен әрекеттесетін болса,ерітіндіде түзілген сілтіні(%) массалық үлесі
А) 42,0
В)* 40,0
С) 41,0
D) 38,5
Е) 39,0
22. BaCl2-нің 260 г 4%-тік ерітіндісіне әзірлеу үшін қажет BaCl2·2 H2O кристаллогидратының массасы(г)
А) 10,4
В) 14,2
С) 21
D)* 12,2
E) 65
23. 14 г циклопентанның 12 л хлормен (қ.ж.) әрекеттескенде,шығымы 70% болса,түзілген хлорциклопентанның массасы
А) 15,6 г
В) 11,9 г
С) 17,2 г
D)* 14,6 г
E) 20,9 г
24.Шығымы 60% болып,54 г сүт қышқылын алуға жұмсалатын глюкозаның массасы
A) 89 г
B) 94 г
C)* 90 г
D) 85 г
E) 96 г
25.15,6 г бензолды нитрлегенде шығымы 90% нитробензол алынды.Оны әрі қарай тотықсыздандырғанда шығымы 75% аналин алынды.Алынған аналиннің массасы.
A) 12,8 г
B) 11,5 г
C) 10,5 г
D)* 12,6 г
E) 11,0 г
22-нұсқа
1.Гидрлену реакциясы:
А) Fe2O3 + 3H2 →2Fe +3H2O
В) ZnO +2HCl→ZnCl2 +H2O
С)* C3H6 +H2→ C3H8
D) H2 +Cl2→2HCl
Е) C2H4 +H2O→ C2H5OH
2.S-электрон бұлтының пішіні
А) гантель тәрізді
В) пирамида
С) тетраэдр
D)* шар
Е) сызықтық
3.Элементтердің терісэлектрлігі өсетін қатары:
А) Si-Al-Mg-Na
В) P-As-Sb-Bi
С) O-N-C-B
D)* Si-P-S-Cl
Е) Cr-Se-Mo-Te
4.Күшті электролит:
А) көмір ышқылының қаныққан ерітіндісі
В)* күкірт қышқылының ерітіндісі
С) су
D) әктіленген су
Е) күкіртсутектің қаныққан ерітіндісі
5.Қыздырған кезде сутекпен әрекеттеспейтін зат:
А) қалайы(ІІ)
В) қорғасын(ІІ) оксиді
С) мыс(ІІ) оксиді
D)* күкірт қышқылы
Е) калий оксиді
6. P2O5 +BaO→Ba3 (PO4 )2
А)* 5
В) 4
С) 7
D) 6
Е) 3
7.Құрамында 20 сутек атомы бар қаныққан көмірсутектің молярлық массасы:
А) 72 г/моль
В) 86 г/моль
С)* 128 г/моль
D) 114 г/моль
Е) 100 г/моль
8. Ақуыз денатурациясы
А)* Белоктардың екінші, үшінші, төртінші реттік құрылымының бүзылуы
В) Белок молекулалардың аминқышқылдарға ыдырауы
С) Белоктар құрамына кіретін аминқышқылдарының тотығуы.
D) Аминқышқылдарының полимерленуі.
Е) Аминоқышқылдарының дигиддрогенденуі.
9. Жоғары молекулалық қосылыстарды алатын реакция
А) Тотықтыру
В) Изомерлеу.
С)* Полимерлеу.
D) Гидролиздеу.
Е) Бейтараптау.
10. Температураны жоғарылатқанда тепе-теңдіқ күйдегі жүйенің тепе-теңдігі
...
А) газ молекулалары санының көбею реакциясы жағына ығысады
В) өрекеттесуші заттар реакциясы жағына ығысады
С)* жылу сіңіре жүретін реакция жағына ығысады
D) жылу боле жүретін реакция жағына ығысады
Е) газ молекулалары санының азаю реакциясы жағына ығысады
11. Екеуі де сумен өрекеттесетін заттар қатары
А)* СО2, Р2О3
В) NО2, С2Н6
С) Si O2,, C2H4
D)`NO2,, SiH4
E) SO2 , CH4
12.Мыс өрекеттессссспейтін қышқылдар жүбы
А) H3 PO4 ; HNO3 сұй
В) H2 SO4 конц; HNO конц.
С)* HCI ; H 2CO3
D) HNO3; өте сұй HNO3
E ) HNО3; өте сұй. HNO3
13.Реакция нәтижесінде күкірт тотықсыздандырғыш болатын реакция үрдісі:
А) C +S→
В)* S +O2 →
С) Cu +S→
D) Ca +S→
Е) P +S→
14.Найзағайдан кейінгі жаңбырдың «қышқыл» болуының себебі:
А)* N2 → NO →NO2→ HNO3
В) N2 →NH3→ N2 →Ca3N2
С) N2→ Mg3N3→NH3 →NH4OH
D) N2→Na3N →NaOH→NaNO3
Е) N2→ NO →NO2 →Mg (NO3 )2
15.Калий силикаты мен фосфор қышқылы арасындағы реакцияның толық иондық теңдеуіндегі барлық коэффициенттердің қосындысы:
А)* 28
В) 27
С) 25
D) 26
Е) 24
16.Al +O2 →Al 2O3 реакциясы теңдеуінде алюминийдің алдына қойылатын коэффициент:
А) 5
В)* 4
С) 3
D) 2
Е) 1
17.Егер іс жүзіндегі шығым 80 екені белгілі болса, 44,8 л (қ.ж) этиленді тікелей гидратациялау арқылы алынған этанолдың массасы:
А) 74,6 г
В)* 74 г
С) 73,8 г
D) 73,6 г
Е) 74,2 г
18.Қосылыстардың ішіндегі күрделі эфир:
А)
Н3С-С-О-С-СН3
║ ║
О О
В) Н3С-СН2-О-СН2-СН3
С)*
Н3С-С-О-СН3
║
О
D) СН3ОН
Е) Н3С-С-СН3
║
О
19.Изомерлерге жататын заттар жұбы:
А) Формальдегид және құмырсқа қышқылы
В)* Пентан және диметрилпропан
С) Бензол және фенол
D) Гексан және циклогексан
Е) Этанол және сірке қышқылы
20. 58,5 г натрий хлоридінің судағы ерітіндісін электролизденгенде анодта калий бромидінен бромды ығыстыратын газ түзілді.Түзілген бромның мөлшері:
А) 5 моль
В)* 0,5 моль
С) 3 моль
D) 4 моль
Е) 2 моль
21.Литий өте сұйылтылған азот қышқылымен әрекеттескенде азоттың тотықсыздану өнімі NH4NO3 болса, теңдеудегі коэффициенттердің жалпы саны:
А) 28
В) 26
С) 29
D)* 30
Е) 31
22.Темірдің массалық үлесі 0, 95 болатын металдан жасалған 3,54 г бұйым бөлшегін ерітуге қажет 14,6 % -тті тұз қышқылы еріндісінің массасы:
А)* 30 г
В) 49 г
С) 50 г
D) 25 г
Е) 45 г
23.Ауа бойынша тығыздығы 2,414-ке тең, құрамындағы көміртектің массалық үлесі 0,857 болатын циклоалканның формуласы:
А)* С 5Н10
В) С 4Н8
С) С 7Н14
D) С 6Н12
Е) С 3Н6
24.Толуолдың жақын гомологтарының саны:
А)* 5
В) 4
С) 3
D) 0
Е) 1
25.Картопта 20 % крахмал бар.Егер шығымы 75 % болса, онда 1620 кг картоптан алынатын глюкозаның массасы:
А)* 270 кг
В) 360 кг
С) 180 кг
D) 220 кг
Е) 300 кг
23-нұсқа
1. Аммоний ионы
A)* NH+4
B) AI3+
C) Hg2+
D) Sn2+
E) Ca2+
2. 2-ші энергетикалық деңгейдегі электрон саны
A) 1e
B) 32e
C) 18e
D)* 8e
E) 2e
3. Гептан молекуласындағы гибридтену типі
A) sp2
B)* sp3
C) sp2, sp3
D) sp
E) sp2, sp
4. Электролиттік диссоциациялану процесі
A) электр тогын өткізу
B)* электролиттердердің иондарға ыдырауы
C) иондарға мүлдем ыдырамауы
D) гидроксид ионының түзілуі
E) электр тогын өткізбеуі
5. Сілтілік жер металдар гидридтерінің жалпы формуласы
A)* MeH2
B) MeH3
C) MeH4
D) Me2H3
E) MeH
6. Аз еритін негіз:
A) мыс гидроксиді (ІІ)
B) мырыш гидроксиді
C)* кальций гидроксиді
D) калий гидроксиді
E) натрий гидроксиді
7. Тұздардың жіктелу қатары
A) қышқылдық, орта, еритін
B) *орта, қышқылдық, негіздік, қостұз
C) орта, сілтілер, қышқылдық
D) суда ерімейтін, амфотерлі, орта
E) амфотерлі, қышқылдық, орта
8. Бос радикалдың ең негізгі белгісі
A) Бос электрон жұбының болуында
B) Бос атомның болуында
C) Иондық байланыстың болуында
D)* Жұптаспаған электронның болуында
E) Атомдар арасында екі жұп электрондардың болуында
9. Пластмассалар құрамына кірмейтін зат
A) толықтырғыштар
B)* еріткіштер
C) тұрақтандырғыштар
D) бояғыш заттар
E) жұмсартқыштар
10. Термохимиялық теңдеуі С6Н12О6 + 6О2 = 6СО2 + 6Н2О + 2820кДж болса, 18г глюкоза тотыққанда бөлінетін жылу мөлшері:
A) 258кДж
B)* 282 кДж
C) 228 кДж
D) 248 кДж
E) 148 кДж
11. Иондардың тотықсыздану қасиеттері өсу ретімен орналасқан қатар
A) CI-, J-, Br-
B)* CI-, Br-, J-
C) Br-, J-, CI-
D) Br-, J-, Br-
E) J-, Br-, CI-
12. Күкірт (VІ) оксиді мен натрий гидроксиді әрекеттескендегі (орта тұз түзілсе) толық иондық теңдеудегі барлық коэффициенттер қосындысы
A) 6
B)* 9
C) 8
D) 7
E) 5
13. Бейтарап орта көрсететін тұз ерітіндісі
A)* натрий нитраты
B) мыс (ІІ) нитраты
C) алюминий нитраты
D) күміс нитраты
E) аммоний нитраты
14. 96г күйені жандырғанда түзілген көміртегі (ІV) оксидінің (қ.ж.) көлемі (л)
A) 177,2
B) 178,2
C)* 179,2
D) 175,2
E) 176,2
15. NаОН балқымасын электролиздегенде түзілетін заттар
A) Na2O, H2
B) Na, H2
C) H2, O2
D)* Na, O2
E) Na2O, O2
16. Алюминий қосылысы қышқылдық қасиет көрсететін реакцияның схемасы
A)* AI(OH)3 + OH- →
B) AI2(SO4)3 + H+ →
C) AI(OH)3 + H+ →
D) AI2O3 + H+ →
E) AIPO4 + H+ →
17. Мына өзгерістегі «Х» заты
СН4 → С2Н2 → Х→ С6Н5NО2
A)* бензол
B) циклогексан
C) хлорбензол
D) толуол
E) этилен
18. А және Б заттары
А + Н2О → пропанол-2 ← Б + NаОН
A) пропан-1, хлорпропан
B) пропаналь, 2-хлорпропан
C) 2-аминопропан, 1,2-дихлорпропан
D)* пропен, 2-хлорпропан
E) ацетилен, пропан қышқылы
19. Құрамында 54,54% көміртек, 9,1% сутек, 36,36% оттек бар альдегид
A) құмырсқа
B) валериан
C)* сірке
D) май
E) пропаналь
20. Көлемі 200мл, молярлық концентрациясы С(Nа2СО3) = 0,25моль/л ерітіндідегі натрий карбонатының массасы
A) 53г
B) 7,3г
C)* 5,3г
D) 10,6г
E) 106г
21. Темір (ІІ) хлоридінің гидролизінің 2 сатысының толық иондық теңдеуіндегі коэффициенттер қосындысы
A) 2
B) 4
C)* 6
D) 7
E) 5
22. Жартысы метаннан, жартысы этаннан тұратын көлемі 1м3 газ қоспасын жағу үшін қажет оттектің көлемі
A) 2,5м3
B)* 2,75м3
C) 3м3
D) 2,1м3
E) 2м3
23. 45кг глюкоза сүт қышқылды ашығын кезінде 40кг сүт қышқылы түзілді. Теориямен салыстырғанда реакция өнімінің шығымын есепте
A) 74%
B) 69%
C) 59%
D)* 88,9%
E) 42,6%
24. 32г кальций карбидінен алынған глицинмен әрекеттесуге жұмсалатын 10 натрий гидроксиді ерітіндісінің (тығыздығы 1,1г/мл) көлемі
A) 110мл
B)* 182мл
C) 136мл
D) 162мл
E) 190мл
25.Өзгерістерді жүззеге асыру үшін реагенттерді қосудың дұрыс реті
C
4, катал.
3
t
2
1

5
4H10 → C4H9CI → C8H18 → CO2 C6H12O6 → C6H12O7
A) HCI, Na, O2, O2, O2
B)* CI2, Na, O2, H2O, Ag2O
C) CI2, Na, O2, O2, KMnO4
D) HCI, Na, H2O, O2, KMnO4
E) CI2, Na, O2, O2, Ag2O
24-нұсқа
1. Химиялық реакцияға кіріскен заттардың массасы түзілген заттардың массасына тең
A)* Зат массасының сақталу заңы
B) Газдар заңы
C) Периодтық заңы
D) Авогадро заңы
E) Құрам тұрақтылық заңы
2. 19 протоны, 20 нейтроны және 19 электроны бар элементтің атом ядросының заряды
A)* 19
B) 26
C) 39
D) 40
E) 20
3. Электролит бола алмайтын қосылыс
A) Na3PO4
B)* Cu3(PO4)2
C) AI(NO3)3
D) Ba(CH3COO)2
E) KCI
4. Лабораторияда сутек алатын құралғы
A) ректификациялық қондырғы
B)* Кипп аппараты
C) Вюрц құтысы
D) Антицеклон
E) Циклон
5. Конфигурациясы ...6s2 болатын элемент
A) Po
B)* Ba
C) Mo
D) Ag
E) At
6. Қосымша топтың металдары –
A) s және p- элементтер
B) p және d- элементтер
C)* d және f- элементтер
D) p және f- элементтер
E) s және d- элементтер
7. Фенол натрий гидроксидімен әрекеттескенде түзілетін қосылыс
A)* натрий феноляты
B) бензол
C) ароматты спирт
D) фенол
E) гексан
8. Нәтижесінде глюкоза түзілетін реакция
A)* крахмал гидролизі
B) майдың гидролизі
C) жай эфир гидролизі
D) мононуклеотидтердің гидролизі
E) белок гидролизі
9. Белок денатурациясы –
A) оның суда еруі
B)* оның ІІ, ІІІ реттік құрылымдарының сыртқы әсерлерден бұзылуы
C) оның ерітіндіден бөлінуі
D) оның коллоид ерітінді түзуі
E) оның ауада тотығуы
10. 1 моль сұйық судың түзілу жылуы 286кДж тең болса, 7,2г су түзілгенде жұмсалатын жылу мөлшері
A) 110,4 кДж
B)* 114,4 кДж
C) 103,4 кДж
D) 104,4 кДж
E) 102,2 кДж
11. Cr2O3 + HNO3 → орта тұз + ...
теңдеуіндегі барлық коэффициенттердің қосындысы
A) 10
B) 13
C)* 12
D) 9
E) 11
12. Калий гидроксиді ерітіндісінде еритін қосылыс
A) NaOH
B) CsOH
C)* Be(OH)2
D) Ni(OH)2
E) Fe(OH)2
13. Натрий хлоратындағы химиялық байланыс
A) ковалентті полюссіз және полюсті
B) ковалентті полюсті және металдық
C)* ковалентті полюсті және иондық
D) иондық және металдық
E) иондық және сутектік
14. Eгер реакция нәтижесінде Mg(NO3)2 + N2 + H2O түзілген болса, онда әрекеттесуші заттар:
A) MgO және HNO3 (конц)
B) Mg(OH)2 және NO2
C)* Mg және HNO3 (сұйық)
D) MgO және HNO3 (сұйық)
E) Mg және N2O5
15. Қысқартылған иондық теңдей бойынша әрекеттесетін заттардың жұбы:
2H+ + CO32- → H2O + CO2↑
A) көмірқышқыл газы мен натрий гидроксиді
B)* натрий карбонаты мен тұз қышқылы
C) магний карбонаты мен натрий гидроксиді
D) көмірқышқыл газы мен су
E) калий карбонаты мен су
16. Бір-біріне изомер заттар:
а. CH2 = C – CH3
│
CH3
б. CH2 – CH – CH3
│ │
CH2 – CH2
в. CH3 – CH = CH – CH2 – C2H5
г. CH2 = CH – CH = CH2
д. CH2 – CH2
│ │
CH2 – CH2
е. CH3 – CH = CH – CH3
A) а, г
B) б, д
C)* а, д, е
D) а, г, е
E) в,б
17. Бутен -1 бромсутектен әрекеттескенде түзілетін зат:
A) 1- бормбутен-1
B) 1- бормбутен-2
C) 1- бромбутан
D)* 2- бромбутан
E) 2- бромбутен-2
18. Сірке альдегиді әрекеттесетін заттар жұбы:
A) сутекпен және сумен.
B) мыс(ІІ) гидроксидімен және кальций оксидімен
C) тұз қышқылымен және күміспен
D)* Ag2O-нің аммиактағы ерітіндісімен және оттекпен
E) натрий гидроксидімен және сутекпен
19. Поликонденсация реакциясы нәтижесінде алынатын зат:
A)*Фенолформальдегид смоласы
B) Полистирол
C) Бутадиенстирол
D) Полиэтилен
E) Полипропилен
20. Егер реакция өнімдері ретінде KCI + KCO3 + H2O түзілген болса, онда әрекеттесуші заттар:
A) HCI және KOH
B)* CI2 және KOH жоғары температурада
C) CI2 және H2O
D) HCIO4 және K
E) CI2 және KOH (қ.ж.)
21.Егер күкірт қышқылының молярлық концентрациясы 5 моль/л болса (ρ = 1,9г/мл), онда ерітіндегі қышқылдың массалық үлесі
A)* 26%
B) 25%
C) 27%
D) 28%
E) 29%
22. Озонатордан 100л (қ.ж.) оттек өткізіп, оның 20%-і озонға айналады. Реакциядан кейінгі газ қоспасының көлемі
A) 80,0л
B)* 93,3л
C) 13,3л
D) 90,3л
E) 18,3л
23. Калийдің 6,02·1022 бөлшектері концентрлі азот қышқылының 12,04·1023 молекуласымен әрекеттеседі. Реакцияға қатыспаған бөлшектердің саны (газ түрінде бөлінеді):
A) 6,02 · 1021
B) 4,1 · 1023
C)* 1,1 · 1024
D) 5,1 · 1022
E) 4,5 ·1023
24.6,72 л(қ.ж) пропанды толық жаққанда алынған өнімді ізбес суының артық мөлшерімен өндеді.Сол кезде 80 г тұңба түзілді. Тұздың шығымы
A) 87%
B)* 88,9%
C) 82%
D) 84%
E) 80,9%
25.Өзгерістер тізбегіндегі соңғы өнім Х5 –
C




H2SO4 (k)
t › 140ºC
Br2
KOH, спирт, tº
H2O, Hg2+
H2, Ni
2H5OH X1 X2 X3 X4 X5A) пропанол
B) сірке қышқылы
C)*этанол
D) этилен
E) этан
25–нұсқа
-
2 период элементтерінің сыртқы денгейде болатын
А) s – және d – электрондар
В) s – және f – электрондар
С)* s – және p – электрондар
D) p – және d – электрондар
E) p – және f – электрондар
2. Тұрақты тотығу дәрежесі + 2 болатын элемент…
А) Марганец
В)* Бериллий
С) Титан
D) Темiр
Е) Хром
3. Әлсіз электролиттерге жататын қосылыс...
А) * H2S
B) HCI
C) H2SO4
D) HI
E) HNO3
4. Kәдімгі жағдайда жай зат - сутектің агрегаттық күйі
А) сұйық
В) плазма
С)* газ
D) кристалл зат
Е) аморфты зат
5. Диссоциация кезінде хлорит-ион түзетін зат
A) HCIO4
B)* KCIO2
C) KCIO
D) KCI
E) HCIO
6. Бокситтің негізгі құрам бөлігі –
А) *AI2O3
B) CrO
C) P2O3
D) CaO
E) WO3
7. Сірке қышқылы қолданылады
А) пластмасса
В) бояулар алуда
С)* тамақ өнеркәсібінде
D) хош иісті заттар алуда
Е) отын ретінде
8. (С6 Н10О5)n формуласымен өрнектеледі:
A)* крахмал
В) рибоза
С) глицерин
D) фруктоза
Е) сахароза
9. Жоғары молекулалық қосылыстар қасиеті және қолданылуы бойынша мынадай болып бөлінеді:
А) полимерлер және мономерлер
В)* пластмассалар, эластомерлер және талшықтар
С) жасанды және табиғи
D) Өсімдік және жануар текті
Е) синтетикалық және табиғи
10. Құрамында 18,06 ∙1023 молекуласы бар судың (4 οС және 1 атм қысымдағы) көлемі
А) 67,2 л
В)* 54 мл
С) 22,4 л
D) 540 мл
Е) 44,8 л
11. Егер температура мен қысымды бір мезгілде арттырса, онда қай реакцияның тепе-тендігі оң жаққа қарай ығысытын реакция теңдеуі
А) Fe + C ↔ Fe + CO - Q
B) 2CO + O2 ↔ 2CO2 + Q
C)* 2N2 + O2 ↔ 2N2O - Q
D) 2NO + O2 ↔ 2NO2
E) 2H2O ↔ 2H2 + O2 - Q
12. Берілген сызба- нұсқадағы А, В элементтері
![]()
![]()
![]() А
А2О АОН
А
А2О АОН
![]() А2ВО3
А2ВО3
![]()
![]()
![]() В
ВО2 Н2ВО3
В
ВО2 Н2ВО3
А) * A – K, B - S
B) A – Fe, B – B
С) A – Cu, B -N
D) A – Na, В – Cr
E) A – AI, B – P
13. Құрамында 98 г ортофосфор қышқылы бар ерітіндіден 44,8 л аммиак жібергенде пайда болған тұз:
А) аммоний дигидрофосфаты
В) аммоний метафосфаты
С) аммоний ортофосфаты
D)* аммоний гидрофосфаты
Е) аммоний пирофосфаты
14. Темірдің (II) гидрокарбонатындағы π- байланыстардың жалпы саны
А) 3
В) 4
С) *2
D) 8
Е) 6
15. Іс жүзінде жүруі мүмкін реакция:
![]()
![]() А) *Na + H2O
А) *Na + H2O
![]() B) Cu + FeSO4
B) Cu + FeSO4
![]() C) ZnCI2 + Cu
C) ZnCI2 + Cu
![]() D) Hg + H2O
D) Hg + H2O
![]() E) Ag + HCI
E) Ag + HCI
16. Сыртқы электрондық денгейінің формуласы ... 3 d10 4s2 болатын элемент
А) Cr
B)* Zn
C) V
D) W
E) Cu
17. Құрамында 18 атом сутек бар алкеннің салыстырмалы молекулалық массасы
А) 132
В) *126
C) 142
D) 164
E) 108
18. 552 г этил спирті дегидратацияланғанда 333 г диэтил эфирі алынған. Реакция өнімінің массалық шығымы:
А) 100%
B) * 75%
C) 85%
D) 95%
E) 80%
19. 1,2 – диметилбензолдың толық жану теңдеуіндегі өнімдерінің формуласының алдындағы коэффициенттердің қосындысы
А) *26
В) 13
С) 15
D) 18
E) 10
20. 135 мл суда 25 г мыс купоросы СuSO4 ∙ 5H2O ерітілген. Алынған ерітіндідегі мыс ( ІІ) сульфатының массалық үлесі ( %)
А) *10
В) 16,7
С) 9
D) 7.5
E) 12
21. 2 мольден мыс (ІІ) нитратын айырғанда түзілетін оттектің көлемі
А) 44,8 л
B) 89,6 л
C)* 22,4 л
D) 112 л
E) 133,6 л
22. Концентрлі күкірт қышқылы мырышпен ережеге сай күкірт (ІҮ) оксидіне дейін тотықсызданады. 245 грамнан тұратын күкірт қышқылы мырышпен толық әрекеттескенде түзілетін күкірт (ІҮ) оксидінің массасы:
А) 64,0 г
В) 240 г
С) 128 г
D)* 80,0 г
Е) 160 г
23. 8,4 г циклогександы дегидрлегенде және 5,2 г ацетиленді тримерлегенде алынатын бензол массаларының қатынасы
А) 5:3
B) 3:1
C) 4:3
D)* 3:2
E) 4:1
24. Тығыздығы ρ = 0,88 г/мл , 65 мл бензол жарық қатысында хлормен әрекеттескенде түзілген гексахлоранның массасы
А) 253,4 г
В) 223,4 г
С)* 213,4 г
D) 243,4 г
Е) 233,4 г
25. 15 г сірке қышқылынынан алынатын құрамы С4Н8О3N2 дипептидтің массасы
А) 10,5 г
В) 12,5 г
С)* 16,5 г
D) 18,5 г
Е) 14,5 г
Тестовый материал взят из книжки-вопросника пробного тестирования Национального Центра тестирования МОН РК
Вариант 0106
ХИМИЯ
1. Берілген теңдеудің (... Fe + … Cl2 → … FeCl3) коэффициенттері
A) 1, 2, 3
B)* 2, 3, 2
C) 2, 2, 2
D) 2, 3 ,1
E) 1, 1, 1
2. Натрий атомының құрамындағы протон саны
A) 23
B)* 11
C) 12
D) 13
E) 15
3. Формуласы S8 болатын зат молекуласындағы химиялық байланыстың түрі
A) донорлы-акцепторлық
B) сутектік
C) коваленттік полюсті
D)* коваленттік полюссіз
E) иондық
4. Электрөткізгіштікті анықтайтын құралдың лампасы электродты осы затқа батырғанда жарқырап жанады
A) қант (қатты)
B) қант (ерітіндісі)
C) натрий хлориді (қатты)
D)* натрий хлориді (ерітіндісі)
E) спирт (ерітіндісі)
5. Оттектің адам ағзасындағы мөлшері (%)
A) 21,0
B) 32
C)* 65
D) 1,43
E) 49,13
6. Жалпы формуласы CnH2n-6 болатын заттың атауы
A) гексан
B)* бензол
C) циклогексан
D) ацетилен
E) октен
7. Иодсутектің бутен-1-мен әрекеттесуі ... жатады.
A) галогендену реакциясына
B)* қосып алу реакциясына
C) тотықсыздану реакциясына
D) гидрлену реакциясына
E) орын басу реакциясына
8. Нуклеин қышқылдарының белоктар ұқсастығы –
A) екеуі де полинуклеотидтер.
B) екеуінің мономерлері бірдей.
C) екеуі де полипептидтер.
D) екеуі де тек клетка ядросында болады.
E)* екеуі де биополимерлер.
9. Полиэтилен –
A) әрі табиғи, әрі химиялық полимер болады.
B)* химиялық, синтетикалық.
C) табиғи, өсімдік текті.
D) табиғи жануар текті.
E) химиялық, жасанды.
10. 5,6 литр (қ.ж.) метан жанғанда 401 кДж жылу бөлінетін жағдайда реакцияның жылу эффектісі CH4(r) + 2O2(r) = CO2(r) + 2H2O + Q
A) 1602 кДж
B) 1590 кДж
C) 1601 кДж
D) 1600 кДж
E)* 1604 кДж
11. Массалық үлесі 56% ерітінді түзе алатын зат:
A) әк тас.
B) гипс.
C) бор.
D) мәрмәр.
E)* калий перманганаты.
12. Натрий тетрагидроксоцинкатының формуласы
A) Zn(OH)Cl
B) ZN(OH)2SO4
C) Na2ZnO2
D)* Na2[Zn(OH)4]
E) Zn(OH)2
13. Аммоний гидрофосфаты түзілгенде, аммиак пен ортофосфор қышқылы арасындағы реакция теңдеуіндегі коэффициенттер қосындысы:
A)
2.![]()
B) 3.
C) 6.
D)* 4.
E) 5.
14. СО2, СО, СН4 қосылыстарындағы көміртектің валенттіліктерін көрсететін қатар
A) 2, 1, 4
B)* 4, 2, 4
C) 1, 1, 1
D) 4, 2 ,2
E) 2, 2, 4
15. Ізбесті сөндіру реакциясының нөмірі:
Ca ![]() CaCl2
CaCl2
![]() CaCO3
CaCO3 ![]() CaO
CaO![]() Ca(OH)2
Ca(OH)2
![]() CaCO3
CaCO3
A)* 4.
B) 2.
C) 3.
D) 5.
E) 1.
16. 1,5 моль октанның массасы:
A) 175 г.
B)* 171 г.
C) 180 г.
D) 232 г.
E) 86,5 г.
17. Тек екіатомды спирттерге жататын зат:
A)* CH3 – CHOH – CHOH – C2H5
CH3 – CH – CH3
B![]() )
)
CH2OH![]()
C) CH3CH2OH
D) CH2OH – CHOH - CH2 - OH
CH2OH – CHOH- CH – CH3
E![]() )
)
OH
18. Құрамында төрт сутек атомы бар күрделі эфирдің салыстырмалы молекулалық массасы
A)* 60
B) 102
C) 88
D) 74
E) 116
19. Мына заттардың ішінен 2-хлорпропанның формуласын анықта
A) CH3 - CH2 - CH2Cl
B) CH3Cl
C) CH3 - CH2 - CH2Br
D) H3C - CH - CH2Cl
![]()
CH3
E)* CH3 - CH – CH3
![]()
Cl
20.
NH3 ![]() X1
X1 ![]() X2
X2 ![]() X3
X3 ![]()
![]() X4
X4
тізбегі бойынша 224 л аммиактан алынатын Х4 затының массасы (қ.ж.)
A) 17 г
B)* 800 г
C) 80 г
D) 160 г
E) 85 г
21. Өзгерістер схемасы берілген:
H2O ![]() O2
O2 ![]() Fe3O4
Fe3O4 ![]() Fe
Fe![]() FeCl3.
FeCl3.
Фторды қолдануға болатын стадия:
A) 3, 4.
B) 2.
C) 3.
D) 4.
E)* 1.
22. Көлемі 2,8 л күкірт сутекті (қ.ж.) мыс (ІІ) сульфатының артық мөлшеріне жібергенде массасы 11,4 г тұнба алынды. Реакция өнімінің практикалық шығымы:
A) 55%.
B) 85%.
C) 75%.
D)* 95%.
E) 65%.
23. Темір (ІІ) оксиді мен темір (ІІІ) оксидінің қоспасының 37 грамын сутегімен тотықсыздандырғанда темірдің 28 грамы алынды. Қоспадағы оксидтердің массалық үлестерін анықтаңыз.
A) 68% FeО және 32% Fe2О3
B) 83% FeО және 17% Fe2О3
C) 90% FeО және 10% Fe2О3
D)* 73% FeО және 27% Fe2О3
E) 65% FeО және 35% Fe2О3
24. 0,1 моль темір 75г 20%-ті мыс (ІІ) сульфаты ерітіндісімен әрекеттескенде түзілетін мыстың массасы (г)
A) 8
B) 5
C) 7
D)* 6
E) 9
25. Картопта 20% крахмал бар. Егер шығымы 75% болса, онда 1620 кг картоптан алынатын глюкозаның массасы:
A) 300 кг
B)* 270 кг
C) 180 кг
D) 220 кг
E) 360 кг

шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
