
УДК 544.4
ХИМИЯЛЫҚ КИНЕТИКАНЫҢ ІРГЕЛІ ЗАҢДЫЛЫҚТАРЫ МЕН ТЕОРИЯЛЫҚ НЕГІЗДЕРІН ТАЛДАУ
FUNDAMENTAL LAWS AND THEORETICAL BASIS OF CHEMICAL KINETICS ANALYSIS
Орынбаева А.Д1, Тулеуова А.A1, Ахтаева М.Б2
6B01512 – Химия-биология мамандығының 3 курс студенттері
Абай атындағы Қазақ Ұлттық Педагогикалық Университеті, Алматы қ., Қазақстан
aidana729232@gmail.com , tuleuovaaitilek@gmail.com
АҢДАТПА
Бұл жұмыста химиялық кинетиканың негізгі заңдылықтары мен реакциялардың жүру механизмдері әдебиеттерге шолу жасау арқылы қарастырылған. Зерттеу барысында реакция жылдамдығына әсер ететін концентрация, температура және катализатор сияқты факторлардың рөліне талдау жасалды. Массалар әрекеттесу заңы мен Аррениус теңдеуінің физикалық мағынасы ашылып, олардың химиялық үдерістерді сипаттаудағы маңызы көрсетілген. Тұтастай алғанда, жұмыс химиялық кинетика саласындағы іргелі ұғымдарды теориялық тұрғыдан жинақтауға бағытталған.
ABSTRACT
This paper provides a theoretical review of the fundamental laws of chemical kinetics and the mechanisms of chemical reactions based on a comprehensive literature analysis. The study examines the role of key factors such as concentration, temperature, and catalysts in determining reaction rates. The physical significance of the Law of Mass Action and the Arrhenius equation is clarified, demonstrating their importance in describing chemical processes. Overall, the work aims to consolidate fundamental concepts in the field of chemical kinetics through a theoretical lens.
Кілт сөздер: химиялық кинетика, реакция жылдамдығы, белсендіру энергиясы, массалар әрекеттесу заңы, Аррениус теңдеуі.
Keywords: chemical kinetics, reaction rate, activation energy, Law of Mass Action, Arrhenius equation.
Химиялық кинетика — реакциялардың жүру жылдамдығы мен механизмін зерттейтін химияның іргелі саласы. Кез келген химиялық процестің тиімділігі тек өнімнің шығуымен ғана емес, оның уақыттық сипаттамаларымен анықталады [1]. Кинетикалық параметрлерді білу реакцияны басқаруға және оңтайлы жағдайларды таңдауға мүмкіндік береді [2].
Химиялық кинетиканың концептуалды негіздері
Кинетиканың дамуына Л. Вильгельми, Я. Вант-Гофф, С. Аррениус және Н. Семенов секілді ғалымдар елеулі үлес қосты. Бұл ғылымның басты нысаны — элементар акт мен реакция механизмі [2]. Реакциялар фазалық күйіне қарай гомогенді (бір фаза ішінде) және гетерогенді (фазалар бөліну шекарасында) болып бөлінеді [3].
Біздің пайымдауымызша, реакция механизмін түсіну — күрделі химиялық процестерді бақыланатын деңгейге шығарудың жалғыз жолы. М. А. Хұсайын атап өткендей, кинетикалық сызбаны құру арқылы біз реагенттердің өнімге айналу жолындағы барлық аралық сатыларды қадағалай аламыз [2].
Концентрация факторы және Массалар әрекеттесу заңы
Химиялық кинетиканың негізгі постулаты (Массалар әрекеттесу заңы) бойынша, гомогенді реакцияның жылдамдығы әрекеттесуші заттардың концентрацияларының көбейтіндісіне тура пропорционал [4]:
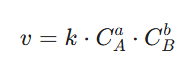
Мұндағы k (жылдамдық константасы) — заттардың табиғаты мен температураға тәуелді, бірақ концентрацияға бағынбайтын тұрақты шама [1].
Концентрацияны өзгерту — реакцияны басқарудың ең қолжетімді әдісі. Алайда, практикада тек концентрацияны арттыру әрдайым тиімді бола бермейді, себебі бұл жүйедегі қысымның артуына немесе жанама реакциялардың тездетілуіне әкеп соғуы мүмкін. Сондықтан k константасының физикалық мағынасын терең түсіну маңызды.
Температураның әсері және Аррениус теңдеуі
Вант-Гофф ережесі бойынша температура 10 К-ге артқанда жылдамдық 2-4 есе өседі [1].
![]()
Бірақ бұл ереже төмен температураларда ғана тиімді. Дәлірек сипаттаманы Аррениус теңдеуі береді [2]:
Аррениустың теңдеуіне сәйкес белсендіру энергиясы төмен болған сайын (яғни, потенциал кедергі төмен болған сайын), жылдамдық константасы ұлғаяды, соған сәйкес реакцияның жылдамдығы температураға тәуелді болады [2].
![]()
мұндағы A – экспонента алдындағы көбейткіш, Еа – активтену энергиясы, R – универсал газ тұрақтысы.
Біздің қарастыруымызша, катализаторларды қолдану — бұл Аррениус заңдылығын "айналып өтудің" бірегей жолы. Мысалы, сутек пероксидінің (H2O2) ыдырауында катализатор Ea мәнін төмендету арқылы процесті миллиондаған есе жеделдетеді [2]. Бұл — табиғаттағы энергия шығынын азайтудың ең ұтымды механизмі.
Сутек пероксиді өздігінен су мен оттегіге ыдырайды, бірақ бұл процесс қалыпты жағдайда өте баяу жүреді. Реакция теңдеуі: 2H2O2 →2H2O + O2
Бұл реакция экзотермиялық (жылу бөледі) және оның жылдамдығын катализаторлардың (мысалы, MnO2 немесе қандағы каталаза ферменті) көмегімен миллиондаған есе арттыруға болады.
А) Концентрацияның әсері:
Түрлі концентрациядағы (3%, 10%, 30%) H2O2 ерітінділерін салыстырғанда, концентрлі ерітіндіде молекулалардың соқтығысу жиілігі жоғары болады. Сәйкесінше, уақыт бірлігінде бөлінетін оттегі көлемі артады.
Ә) Температураның әсері және Аррениус заңы:
Ерітіндіні қыздырғанда молекулалардың кинетикалық энергиясы артады. Бұл активтену энергиясының кедергісінен өте алатын "активті" молекулалар санын көбейтеді. Экспериментте 20°C және 40°C-тағы жылдамдықты салыстыру арқылы Вант-Гофф коэффициентін анықтауға болады.
Активтену энергиясының физикалық мәні
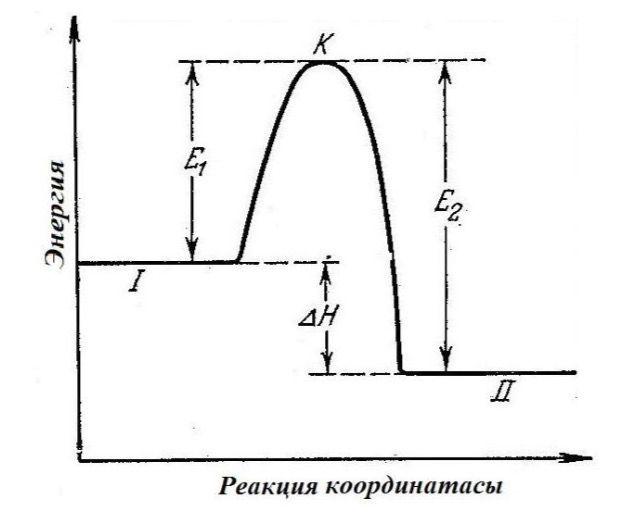
Активтену энергиясы (Ea) — бұл жүйенің бастапқы күйден соңғы күйге өтуі үшін қажетті минималды энергетикалық тосқауыл (барьер). Ол молекулалардың орташа энергиясы мен олардың химиялық әрекеттесуге түсуі үшін ие болуы тиіс энергия деңгейінің айырмасымен анықталады [2].
 [2].
[2].
-
Тура реакция (E1): Бастапқы реагенттердің (І күй) активтелген кешенге (К деңгейі) өтуіне қажет энергия.
-
Кері реакция (E2): Реакция өнімдерінің (ІІ күй) қайтадан активтену нүктесіне жетуі үшін жұмсалатын энергия.
-
Жылу эффектісі (H): Бастапқы заттар мен өнімдердің энергетикалық деңгейлерінің айырымы. Экзотермиялық реакцияларда жүйе төменірек энергетикалық деңгейге көшіп, энергия бөледі [2].
Активтену энергиясы — бұл химиялық реакцияның "рұқсат қағазы" іспеттес. Егер молекулалардың соқтығысу энергиясы осы тосқауылдан (Ea) төмен болса, реакция жүрмейді. Сондықтан температураны көтеру немесе катализатор қосу арқылы біз осы "энергетикалық кедергіні" жеңуге көмектесеміз. Бұл — кез келген химиялық процесті басқарудың іргелі механизмі.
САЛЫСТЫРМАЛЫ ТАЛДАУ
Осы ақпараттарды талдай келе: К. Н. Белик пен К. И. Киенскаяның оқулығы (2015) заманауи физикалық химияның математикалық аппаратына негізделген. Авторлар кинетикалық заңдылықтарды қорытып шығаруда қатаң логикалық және формулалық жүйені ұстанады. Оқулықтың 259–302 беттері аралығындағы материалдарда реакция жылдамдығының уақытқа тәуелділігі дифференциалдық және интегралдық түрде өте егжей-тегжейлі сипатталған. М. А. Хұсайынның еңбегінде (2014) материалды баяндау классикалық оқыту әдістемесіне жақын. Автор ұғымдарды қарапайымнан күрделіге қарай сатылап түсіндіреді. 259-295 беттерді қамтитын бұл тарауда теориялық қағидалар химиялық эксперименттер мен нақты химиялық реакциялардың мысалдарымен көбірек толықтырылған, бұл оқырманның процесті көз алдына елестетуіне көмектеседі.
Л. Вильгельми алғашқы сандық есептеулер арқылы химиялық кинетиканың негізін қаласа, Я. Вант-Гофф реакциялардың жылдамдығы мен ретін анықтайтын динамикалық заңдылықтарды ғылыми жүйеге келтірді. Вильгельми мен Вант-Гофф реакцияның жүру барысына назар аударса, С. Аррениус молекулалардың белсенділігіне тоқталып, жылдамдықтың температураға тәуелділігін көрсететін маңызды теңдеуді ұсынды. Аррениус қарапайым реакциялардың энергетикалық кедергілерін зерттегенімен, Н. Семенов пен С. Хиншелвуд күрделірек тізбекті процестердің механизмін ашып, теорияны жаңа деңгейге көтерді. Егер алғашқы ғалымдар (Вильгельми, Вант-Гофф) химиялық өзгерістің математикалық сипаттамасына басымдық берсе, кейінгі нобель сыйлығының лауреаттары (Семенов пен Хиншелвуд) реакцияның ішкі тармақталу табиғатын негіздеді. Осылайша, бұл ғалымдардың зерттеулері қарапайым есептеулерден бастап (Вильгельми), температуралық әсерге (Аррениус), соңында күрделі тізбекті реакциялар теориясына (Семенов, Хиншелвуд) дейінгі біртұтас ілімді құрады.
Әдебиеттерге жасалған талдау нәтижесінде химиялық кинетиканың іргелі заңдылықтары бойынша келесідей тұжырымдар жасалды. Біріншіден, реакция жылдамдығы әрекеттесуші заттардың табиғаты мен олардың концентрациясына тікелей тәуелді екені нақтыланды. Екіншіден, температураның жоғарылауы молекулалардың активтену энергиясын жеңуге көмектесіп, үдерісті айтарлықтай жылдамдататыны Аррениус заңымен дәлелденді. Жалпы алғанда, жинақталған теориялық мәліметтер химиялық кинетиканың заманауи технологиялардағы шешуші рөлін айқындайды.
ПАЙДАЛАНЫЛҒАН ӘДЕБИЕТТЕР
1.Белик К. Н., Киенская К. И. Физикалық және коллоидтық химия: Оқулық. — М.: Юрайт, 2015. — 259–302 бб.
2.Хұсайын М. А. Физикалық және коллоидтық химия: Оқулық. — Алматы: Эверо, 2014. — 259-295 бб.
3.Еремин В. В. және т.б. Теориялық және қолданбалы химияның негіздері. — М.: Экзамен, 2018. — 145-160 бб.
4.Стромберг А. Г., Семченко Д. П. Физикалық химия: Оқулық. — М.: Высшая школа, 2009. — 312-340 бб.
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Тезис ХИМИЯЛЫҚ КИНЕТИКАНЫҢ ІРГЕЛІ ЗАҢДЫЛЫҚТАРЫ МЕН ТЕОРИЯЛЫҚ НЕГІЗДЕРІН ТАЛДАУ
УДК 544.4
ХИМИЯЛЫҚ КИНЕТИКАНЫҢ ІРГЕЛІ ЗАҢДЫЛЫҚТАРЫ МЕН ТЕОРИЯЛЫҚ НЕГІЗДЕРІН ТАЛДАУ
FUNDAMENTAL LAWS AND THEORETICAL BASIS OF CHEMICAL KINETICS ANALYSIS
Орынбаева А.Д1, Тулеуова А.A1, Ахтаева М.Б2
6B01512 – Химия-биология мамандығының 3 курс студенттері
Абай атындағы Қазақ Ұлттық Педагогикалық Университеті, Алматы қ., Қазақстан
aidana729232@gmail.com , tuleuovaaitilek@gmail.com
АҢДАТПА
Бұл жұмыста химиялық кинетиканың негізгі заңдылықтары мен реакциялардың жүру механизмдері әдебиеттерге шолу жасау арқылы қарастырылған. Зерттеу барысында реакция жылдамдығына әсер ететін концентрация, температура және катализатор сияқты факторлардың рөліне талдау жасалды. Массалар әрекеттесу заңы мен Аррениус теңдеуінің физикалық мағынасы ашылып, олардың химиялық үдерістерді сипаттаудағы маңызы көрсетілген. Тұтастай алғанда, жұмыс химиялық кинетика саласындағы іргелі ұғымдарды теориялық тұрғыдан жинақтауға бағытталған.
ABSTRACT
This paper provides a theoretical review of the fundamental laws of chemical kinetics and the mechanisms of chemical reactions based on a comprehensive literature analysis. The study examines the role of key factors such as concentration, temperature, and catalysts in determining reaction rates. The physical significance of the Law of Mass Action and the Arrhenius equation is clarified, demonstrating their importance in describing chemical processes. Overall, the work aims to consolidate fundamental concepts in the field of chemical kinetics through a theoretical lens.
Кілт сөздер: химиялық кинетика, реакция жылдамдығы, белсендіру энергиясы, массалар әрекеттесу заңы, Аррениус теңдеуі.
Keywords: chemical kinetics, reaction rate, activation energy, Law of Mass Action, Arrhenius equation.
Химиялық кинетика — реакциялардың жүру жылдамдығы мен механизмін зерттейтін химияның іргелі саласы. Кез келген химиялық процестің тиімділігі тек өнімнің шығуымен ғана емес, оның уақыттық сипаттамаларымен анықталады [1]. Кинетикалық параметрлерді білу реакцияны басқаруға және оңтайлы жағдайларды таңдауға мүмкіндік береді [2].
Химиялық кинетиканың концептуалды негіздері
Кинетиканың дамуына Л. Вильгельми, Я. Вант-Гофф, С. Аррениус және Н. Семенов секілді ғалымдар елеулі үлес қосты. Бұл ғылымның басты нысаны — элементар акт мен реакция механизмі [2]. Реакциялар фазалық күйіне қарай гомогенді (бір фаза ішінде) және гетерогенді (фазалар бөліну шекарасында) болып бөлінеді [3].
Біздің пайымдауымызша, реакция механизмін түсіну — күрделі химиялық процестерді бақыланатын деңгейге шығарудың жалғыз жолы. М. А. Хұсайын атап өткендей, кинетикалық сызбаны құру арқылы біз реагенттердің өнімге айналу жолындағы барлық аралық сатыларды қадағалай аламыз [2].
Концентрация факторы және Массалар әрекеттесу заңы
Химиялық кинетиканың негізгі постулаты (Массалар әрекеттесу заңы) бойынша, гомогенді реакцияның жылдамдығы әрекеттесуші заттардың концентрацияларының көбейтіндісіне тура пропорционал [4]:
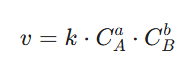
Мұндағы k (жылдамдық константасы) — заттардың табиғаты мен температураға тәуелді, бірақ концентрацияға бағынбайтын тұрақты шама [1].
Концентрацияны өзгерту — реакцияны басқарудың ең қолжетімді әдісі. Алайда, практикада тек концентрацияны арттыру әрдайым тиімді бола бермейді, себебі бұл жүйедегі қысымның артуына немесе жанама реакциялардың тездетілуіне әкеп соғуы мүмкін. Сондықтан k константасының физикалық мағынасын терең түсіну маңызды.
Температураның әсері және Аррениус теңдеуі
Вант-Гофф ережесі бойынша температура 10 К-ге артқанда жылдамдық 2-4 есе өседі [1].
![]()
Бірақ бұл ереже төмен температураларда ғана тиімді. Дәлірек сипаттаманы Аррениус теңдеуі береді [2]:
Аррениустың теңдеуіне сәйкес белсендіру энергиясы төмен болған сайын (яғни, потенциал кедергі төмен болған сайын), жылдамдық константасы ұлғаяды, соған сәйкес реакцияның жылдамдығы температураға тәуелді болады [2].
![]()
мұндағы A – экспонента алдындағы көбейткіш, Еа – активтену энергиясы, R – универсал газ тұрақтысы.
Біздің қарастыруымызша, катализаторларды қолдану — бұл Аррениус заңдылығын "айналып өтудің" бірегей жолы. Мысалы, сутек пероксидінің (H2O2) ыдырауында катализатор Ea мәнін төмендету арқылы процесті миллиондаған есе жеделдетеді [2]. Бұл — табиғаттағы энергия шығынын азайтудың ең ұтымды механизмі.
Сутек пероксиді өздігінен су мен оттегіге ыдырайды, бірақ бұл процесс қалыпты жағдайда өте баяу жүреді. Реакция теңдеуі: 2H2O2 →2H2O + O2
Бұл реакция экзотермиялық (жылу бөледі) және оның жылдамдығын катализаторлардың (мысалы, MnO2 немесе қандағы каталаза ферменті) көмегімен миллиондаған есе арттыруға болады.
А) Концентрацияның әсері:
Түрлі концентрациядағы (3%, 10%, 30%) H2O2 ерітінділерін салыстырғанда, концентрлі ерітіндіде молекулалардың соқтығысу жиілігі жоғары болады. Сәйкесінше, уақыт бірлігінде бөлінетін оттегі көлемі артады.
Ә) Температураның әсері және Аррениус заңы:
Ерітіндіні қыздырғанда молекулалардың кинетикалық энергиясы артады. Бұл активтену энергиясының кедергісінен өте алатын "активті" молекулалар санын көбейтеді. Экспериментте 20°C және 40°C-тағы жылдамдықты салыстыру арқылы Вант-Гофф коэффициентін анықтауға болады.
Активтену энергиясының физикалық мәні
Активтену энергиясы (Ea) — бұл жүйенің бастапқы күйден соңғы күйге өтуі үшін қажетті минималды энергетикалық тосқауыл (барьер). Ол молекулалардың орташа энергиясы мен олардың химиялық әрекеттесуге түсуі үшін ие болуы тиіс энергия деңгейінің айырмасымен анықталады [2].
 [2].
[2].
-
Тура реакция (E1): Бастапқы реагенттердің (І күй) активтелген кешенге (К деңгейі) өтуіне қажет энергия.
-
Кері реакция (E2): Реакция өнімдерінің (ІІ күй) қайтадан активтену нүктесіне жетуі үшін жұмсалатын энергия.
-
Жылу эффектісі (H): Бастапқы заттар мен өнімдердің энергетикалық деңгейлерінің айырымы. Экзотермиялық реакцияларда жүйе төменірек энергетикалық деңгейге көшіп, энергия бөледі [2].
Активтену энергиясы — бұл химиялық реакцияның "рұқсат қағазы" іспеттес. Егер молекулалардың соқтығысу энергиясы осы тосқауылдан (Ea) төмен болса, реакция жүрмейді. Сондықтан температураны көтеру немесе катализатор қосу арқылы біз осы "энергетикалық кедергіні" жеңуге көмектесеміз. Бұл — кез келген химиялық процесті басқарудың іргелі механизмі.
САЛЫСТЫРМАЛЫ ТАЛДАУ
Осы ақпараттарды талдай келе: К. Н. Белик пен К. И. Киенскаяның оқулығы (2015) заманауи физикалық химияның математикалық аппаратына негізделген. Авторлар кинетикалық заңдылықтарды қорытып шығаруда қатаң логикалық және формулалық жүйені ұстанады. Оқулықтың 259–302 беттері аралығындағы материалдарда реакция жылдамдығының уақытқа тәуелділігі дифференциалдық және интегралдық түрде өте егжей-тегжейлі сипатталған. М. А. Хұсайынның еңбегінде (2014) материалды баяндау классикалық оқыту әдістемесіне жақын. Автор ұғымдарды қарапайымнан күрделіге қарай сатылап түсіндіреді. 259-295 беттерді қамтитын бұл тарауда теориялық қағидалар химиялық эксперименттер мен нақты химиялық реакциялардың мысалдарымен көбірек толықтырылған, бұл оқырманның процесті көз алдына елестетуіне көмектеседі.
Л. Вильгельми алғашқы сандық есептеулер арқылы химиялық кинетиканың негізін қаласа, Я. Вант-Гофф реакциялардың жылдамдығы мен ретін анықтайтын динамикалық заңдылықтарды ғылыми жүйеге келтірді. Вильгельми мен Вант-Гофф реакцияның жүру барысына назар аударса, С. Аррениус молекулалардың белсенділігіне тоқталып, жылдамдықтың температураға тәуелділігін көрсететін маңызды теңдеуді ұсынды. Аррениус қарапайым реакциялардың энергетикалық кедергілерін зерттегенімен, Н. Семенов пен С. Хиншелвуд күрделірек тізбекті процестердің механизмін ашып, теорияны жаңа деңгейге көтерді. Егер алғашқы ғалымдар (Вильгельми, Вант-Гофф) химиялық өзгерістің математикалық сипаттамасына басымдық берсе, кейінгі нобель сыйлығының лауреаттары (Семенов пен Хиншелвуд) реакцияның ішкі тармақталу табиғатын негіздеді. Осылайша, бұл ғалымдардың зерттеулері қарапайым есептеулерден бастап (Вильгельми), температуралық әсерге (Аррениус), соңында күрделі тізбекті реакциялар теориясына (Семенов, Хиншелвуд) дейінгі біртұтас ілімді құрады.
Әдебиеттерге жасалған талдау нәтижесінде химиялық кинетиканың іргелі заңдылықтары бойынша келесідей тұжырымдар жасалды. Біріншіден, реакция жылдамдығы әрекеттесуші заттардың табиғаты мен олардың концентрациясына тікелей тәуелді екені нақтыланды. Екіншіден, температураның жоғарылауы молекулалардың активтену энергиясын жеңуге көмектесіп, үдерісті айтарлықтай жылдамдататыны Аррениус заңымен дәлелденді. Жалпы алғанда, жинақталған теориялық мәліметтер химиялық кинетиканың заманауи технологиялардағы шешуші рөлін айқындайды.
ПАЙДАЛАНЫЛҒАН ӘДЕБИЕТТЕР
1.Белик К. Н., Киенская К. И. Физикалық және коллоидтық химия: Оқулық. — М.: Юрайт, 2015. — 259–302 бб.
2.Хұсайын М. А. Физикалық және коллоидтық химия: Оқулық. — Алматы: Эверо, 2014. — 259-295 бб.
3.Еремин В. В. және т.б. Теориялық және қолданбалы химияның негіздері. — М.: Экзамен, 2018. — 145-160 бб.
4.Стромберг А. Г., Семченко Д. П. Физикалық химия: Оқулық. — М.: Высшая школа, 2009. — 312-340 бб.

шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
