Атом құрылысы
Атом құрылысы

#1 слайд
Резерфорд тәжірибесі
Атомның құрылысы
1 слайд
Резерфорд тәжірибесі Атомның құрылысы

#2 слайд
Оқу мақсаты
- 9.6.1.7 α - бөлшегінің шашырауы бойынша
Резерфорд тәжірибесін сипаттау
2 слайд
Оқу мақсаты - 9.6.1.7 α - бөлшегінің шашырауы бойынша Резерфорд тәжірибесін сипаттау

#3 слайд
Атом ны ң тарихы 19 ғ-дың соңында ашылған электрон
мен радиоактивтіліктің қасиеттерін анықтаудан
басталады.
Атом туралы ұғым ертедегі гректерден бастау алды.
Бірақ ол материяның бөлінбейтін тұтас бөлшегі деген
теріс ұғым болып қалыптасты.
Атом құрылысының күрделі екендігі Дж. Томсон
ашқан электронның қасиеттерінен байқала бастады.
3 слайд
Атом ны ң тарихы 19 ғ-дың соңында ашылған электрон мен радиоактивтіліктің қасиеттерін анықтаудан басталады. Атом туралы ұғым ертедегі гректерден бастау алды. Бірақ ол материяның бөлінбейтін тұтас бөлшегі деген теріс ұғым болып қалыптасты. Атом құрылысының күрделі екендігі Дж. Томсон ашқан электронның қасиеттерінен байқала бастады.

#4 слайд
Атом
модельдерінің
дамуы
Ертедегі атом туралы идеялар:
*2500ж бұрын – Демокрит-
атом бөлінбейді
4 слайд
Атом модельдерінің дамуы Ертедегі атом туралы идеялар: *2500ж бұрын – Демокрит- атом бөлінбейді

#5 слайд
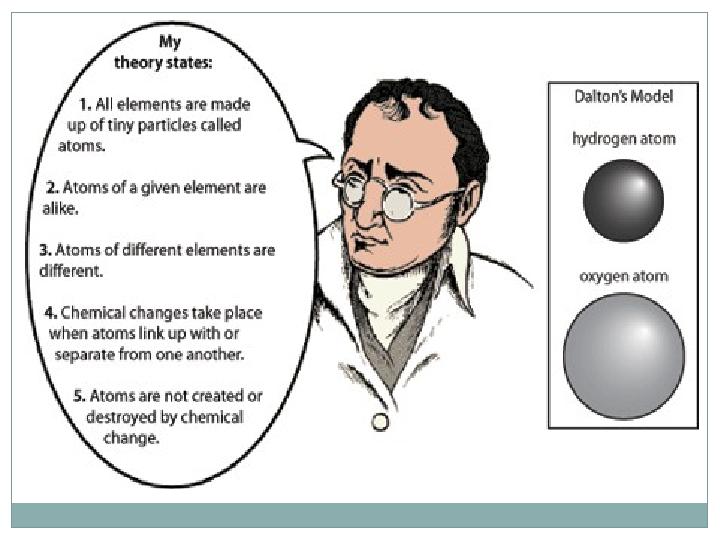
Дальтонның моделі (1808)
•
Заттар
бөлінбейтін
атомдардан
тұрады;
5 слайд
Дальтонның моделі (1808) • Заттар бөлінбейтін атомдардан тұрады;
#6 слайд
6 слайд

#7 слайд
Джон Дальтон моделі
Барлық
элементтер
атомдардан
тұрады;
Ұқсас
элементтердің
атомдары ұқсас;
Атомдар
химиялық
реакция кезінде
жоғалмайды;
7 слайд
Джон Дальтон моделі Барлық элементтер атомдардан тұрады; Ұқсас элементтердің атомдары ұқсас; Атомдар химиялық реакция кезінде жоғалмайды;

#8 слайд
ТОМСОН Джозеф
Джон
18.12 1856 ж. –
30.08. 1940 ж.
1906 ж-Нобель
сыйлығы.
Томсон моделі
бойынша атом өзі оң
зарядталған, және ол
теріс зарядталған
электрондардан тұрады
8 слайд
ТОМСОН Джозеф Джон 18.12 1856 ж. – 30.08. 1940 ж. 1906 ж-Нобель сыйлығы. Томсон моделі бойынша атом өзі оң зарядталған, және ол теріс зарядталған электрондардан тұрады

#9 слайд
Томсон электронды ашқан ғалым
ретінде белгілі;
Томсон жүргізген эксперимент
нәтижесінде катод сәулелері
зарядталған параллель пластиналар
арасында бұрылатындығын анықтады;
Сәулелердің бұрылуына қарап, олар
теріс зарядты бөлшектерден тұрады
делінді.
Кейінірек бұл бөлшектер электрондар
деп аталды. Thompson’s Model
9 слайд
Томсон электронды ашқан ғалым ретінде белгілі; Томсон жүргізген эксперимент нәтижесінде катод сәулелері зарядталған параллель пластиналар арасында бұрылатындығын анықтады; Сәулелердің бұрылуына қарап, олар теріс зарядты бөлшектерден тұрады делінді. Кейінірек бұл бөлшектер электрондар деп аталды. Thompson’s Model

#10 слайд
10 слайд

#11 слайд
Hans Geiger Ernest Marsden эксперименті
Gold foil эксперименті
Rutherford эксперименті 1909 ж ,
Ernest Rutherford басшылығымен орындалды
Атомның « Plum pudding » моделінің құлдырауына әкелдіАлтын фольгамен
жасалған эксперимент
Ernest
Rutherford
11 слайд
Hans Geiger Ernest Marsden эксперименті Gold foil эксперименті Rutherford эксперименті 1909 ж , Ernest Rutherford басшылығымен орындалды Атомның « Plum pudding » моделінің құлдырауына әкелдіАлтын фольгамен жасалған эксперимент Ernest Rutherford

#12 слайд
Ядро оң зарядталған, оның радиусы 10 – 13см. Атомның массасы түгел
дерлік ядроға шоғырланған. Оны айнала әртүрлі орбитамен теріс
зарядталған электрондар қозғалып жүреді. Ең шеткі электрон орбитасының
радиусы атомның радиусына тең. Бұл үлгі Күн жүйесінің құрылымына
ұқсайтындықтан оны атомның планетарлық моделі деп атады. Модель
бойынша атом көлемінің басым көпшілігі «бос» болып шығады, ядроның
радиусы атомның радиусынан 100 000 есе. Атом күрделі жүйе, оның
центрінде оң зарядталған ядро бар, оның заряды + Ze ( мұндағы Z –
элементтің реттік нөмірі). Ядроны айнала электрондар қозғалып жүреді,
қалыпты күйде олардың саны Z - ке тең. Резерфорд моделі атом құрылысын
дұрыс түсіндіре білді.
Ядро атом көлемінің өте кішкене орталық бөлігін алып тұрады. Ядроның
диаметрі 10 - 12 – 10 - 13 см, ал атомның диаметрі 10 - 8 см шамасында.
12 слайд
Ядро оң зарядталған, оның радиусы 10 – 13см. Атомның массасы түгел дерлік ядроға шоғырланған. Оны айнала әртүрлі орбитамен теріс зарядталған электрондар қозғалып жүреді. Ең шеткі электрон орбитасының радиусы атомның радиусына тең. Бұл үлгі Күн жүйесінің құрылымына ұқсайтындықтан оны атомның планетарлық моделі деп атады. Модель бойынша атом көлемінің басым көпшілігі «бос» болып шығады, ядроның радиусы атомның радиусынан 100 000 есе. Атом күрделі жүйе, оның центрінде оң зарядталған ядро бар, оның заряды + Ze ( мұндағы Z – элементтің реттік нөмірі). Ядроны айнала электрондар қозғалып жүреді, қалыпты күйде олардың саны Z - ке тең. Резерфорд моделі атом құрылысын дұрыс түсіндіре білді. Ядро атом көлемінің өте кішкене орталық бөлігін алып тұрады. Ядроның диаметрі 10 - 12 – 10 - 13 см, ал атомның диаметрі 10 - 8 см шамасында.

#13 слайд
Классикалық физика негіздеріне сүйеніп атомның
құрылысы мен негізгі қасиеттерін теориялық
тұрғыдан түсіндіруге тырысқан. Эрнест Резерфорд
атом құрылысының моделін ұсынды.
13 слайд
Классикалық физика негіздеріне сүйеніп атомның құрылысы мен негізгі қасиеттерін теориялық тұрғыдан түсіндіруге тырысқан. Эрнест Резерфорд атом құрылысының моделін ұсынды.

#14 слайд
Атомның ішінде электр зарядтарының
орналасу тәртібін анықтау үшін 1911 жылы
Резерфорд өзінің шекірттері Г. Гейгер және
Э.Марсденмен бірге альфа -бөлшектер шоғын өте
жұқа алтын фольгадан өткізіп, бірнеше
тәжірибелер жасады. Осы тәжірибелерді зерделеу
нәтижесінде атомның ядролық, басқаша айтсақ,
планетарлық моделі өмірге келді.
14 слайд
Атомның ішінде электр зарядтарының орналасу тәртібін анықтау үшін 1911 жылы Резерфорд өзінің шекірттері Г. Гейгер және Э.Марсденмен бірге альфа -бөлшектер шоғын өте жұқа алтын фольгадан өткізіп, бірнеше тәжірибелер жасады. Осы тәжірибелерді зерделеу нәтижесінде атомның ядролық, басқаша айтсақ, планетарлық моделі өмірге келді.
#15 слайд
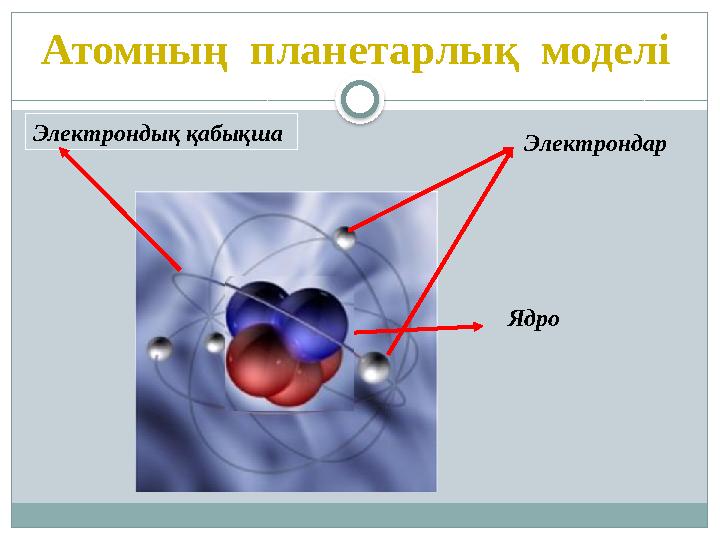
Атомның планетарлық моделі
ЯдроЭлектрондық қабықша
Электрондар
15 слайд
Атомның планетарлық моделі ЯдроЭлектрондық қабықша Электрондар

#16 слайд
Прибордың ішінде фольга болмағанда дөңгелек пайда болады
16 слайд
Прибордың ішінде фольга болмағанда дөңгелек пайда болады
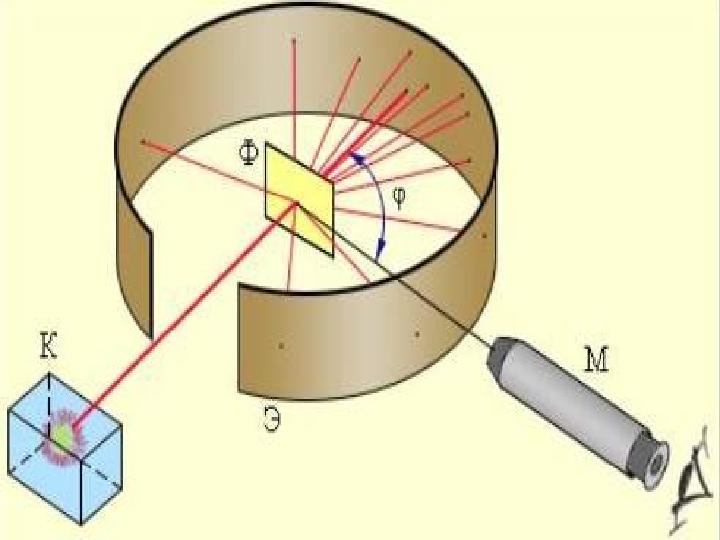
#17 слайд
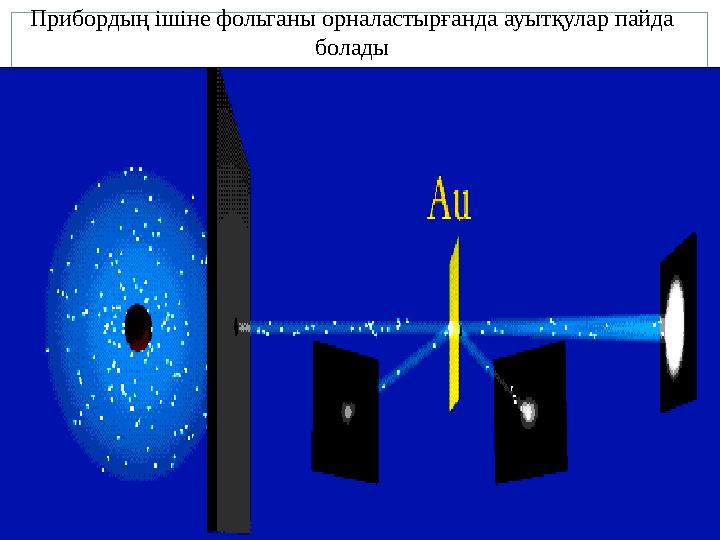
Прибордың ішіне фольганы орналастырғанда ауытқулар пайда
болады
17 слайд
Прибордың ішіне фольганы орналастырғанда ауытқулар пайда болады
#18 слайд
18 слайд

#19 слайд
Бақыланды Қорытынды
Альфа бөлшектердің
көпшілігі фольга арқылы
тура өтіп кеткен
Бөлшектердің біразы
фольгадан кері үлкен
бұрышқа ауытқыған
Өте аз бөлшектер барған
жолымен тура кері
ауытқыған Атом ядросы оның
өлшемімен
салыстырғанда өте
кішкентай, және онда
массаның көп бөлігі
шоғырланған, сондай
ақ оң зарядтыАтомдардың көп бөлігі
бос кеңістік
19 слайд
Бақыланды Қорытынды Альфа бөлшектердің көпшілігі фольга арқылы тура өтіп кеткен Бөлшектердің біразы фольгадан кері үлкен бұрышқа ауытқыған Өте аз бөлшектер барған жолымен тура кері ауытқыған Атом ядросы оның өлшемімен салыстырғанда өте кішкентай, және онда массаның көп бөлігі шоғырланған, сондай ақ оң зарядтыАтомдардың көп бөлігі бос кеңістік

#20 слайд
Осы бақылаулардан кейін
Резерфорд мынадай қорытынды
жасады:
Атом шамасымен салыстырғанда өте
кішкентай, альфа бөлшектерді тебе алатын
оң зарядтан тұрады;
20 слайд
Осы бақылаулардан кейін Резерфорд мынадай қорытынды жасады: Атом шамасымен салыстырғанда өте кішкентай, альфа бөлшектерді тебе алатын оң зарядтан тұрады;
#21 слайд
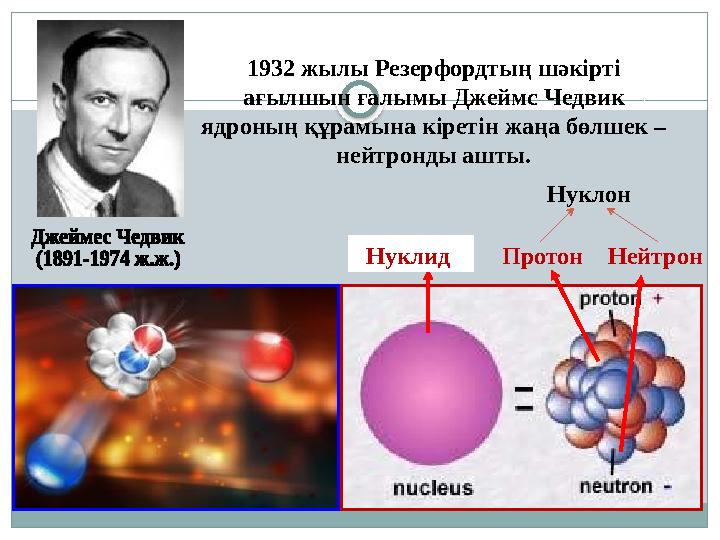
Протон Нейтрон Нуклид 1932 жылы Резерфордтың шәкірті
ағылшын ғалымы Джеймс Чедвик
ядроның құрамына кіретін жаңа бөлшек –
нейтронды ашты.
Нуклон
21 слайд
Протон Нейтрон Нуклид 1932 жылы Резерфордтың шәкірті ағылшын ғалымы Джеймс Чедвик ядроның құрамына кіретін жаңа бөлшек – нейтронды ашты. Нуклон
#22 слайд
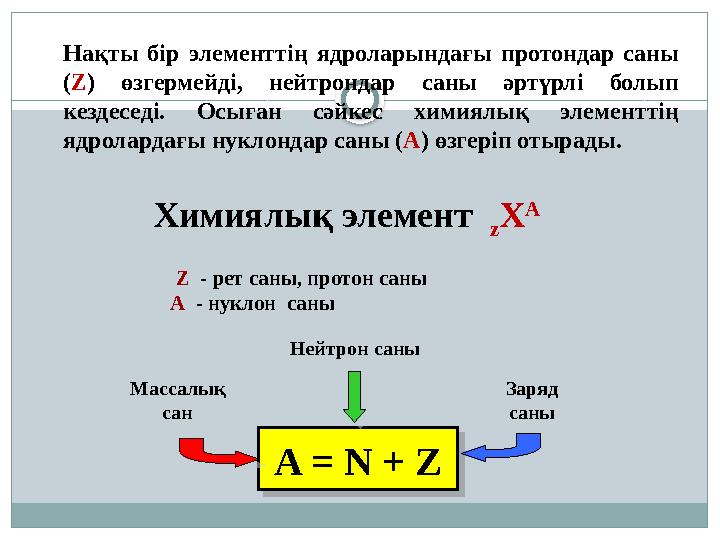
Нақты бір элементтің ядроларындағы протондар саны
( Z ) өзгермейді, нейтрондар саны әртүрлі болып
кездеседі. Осыған сәйкес химиялық элементтің
ядролардағы нуклондар саны ( А ) өзгеріп отырады.
Химиялы қ элемент
z Х А
A = N + ZМассалық
сан Заряд
саныНейтрон саныZ - рет саны, протон саны
А - нуклон саны A = N + Z
22 слайд
Нақты бір элементтің ядроларындағы протондар саны ( Z ) өзгермейді, нейтрондар саны әртүрлі болып кездеседі. Осыған сәйкес химиялық элементтің ядролардағы нуклондар саны ( А ) өзгеріп отырады. Химиялы қ элемент z Х А A = N + ZМассалық сан Заряд саныНейтрон саныZ - рет саны, протон саны А - нуклон саны A = N + Z

#23 слайд
Резерфорд моделі
бойынша
Оң заряд атомның центрінде
шоғырланған. Атом массасының түгелдей
дерлігі оның центріндегі ядрода
шоғырланған.
Атом ядросы көлемі өте аз, сондықтан
атомның көп бөлігі бос кеңістік;
Теріс зарядты электрон ядроны айнала
қозғалатындықтан, ол ядроға құлап
кетпейді;
Алтын атомы ядросының өлшемі м14
10 3
23 слайд
Резерфорд моделі бойынша Оң заряд атомның центрінде шоғырланған. Атом массасының түгелдей дерлігі оның центріндегі ядрода шоғырланған. Атом ядросы көлемі өте аз, сондықтан атомның көп бөлігі бос кеңістік; Теріс зарядты электрон ядроны айнала қозғалатындықтан, ол ядроға құлап кетпейді; Алтын атомы ядросының өлшемі м14 10 3
#24 слайд
1
1/1840th +1
none
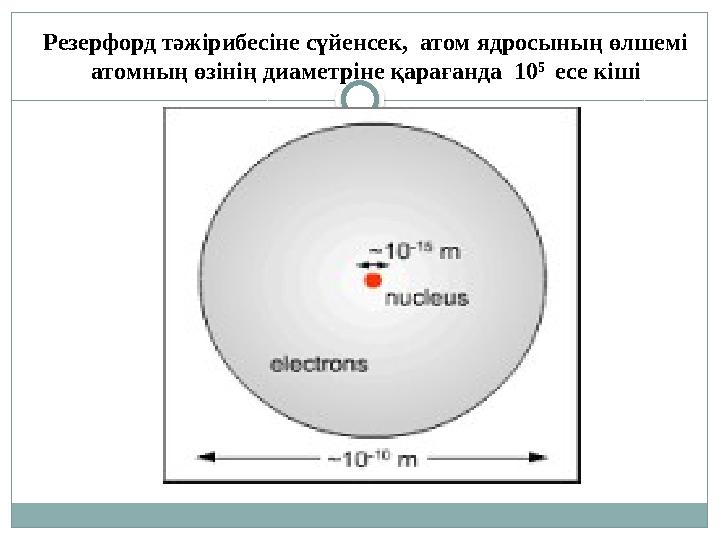
-1Резерфорд тәжірибесіне сүйенсек, атом ядросының өлшемі
атомның өзінің диаметріне қарағанда 10 5
есе кіші
24 слайд
1 1/1840th +1 none -1Резерфорд тәжірибесіне сүйенсек, атом ядросының өлшемі атомның өзінің диаметріне қарағанда 10 5 есе кіші

#25 слайд
Атом ядросы
протондар мен
нейтрондардан
тұрады;
Электрондар
ядроны
айнала
қозғалады
25 слайд
Атом ядросы протондар мен нейтрондардан тұрады; Электрондар ядроны айнала қозғалады
#26 слайд
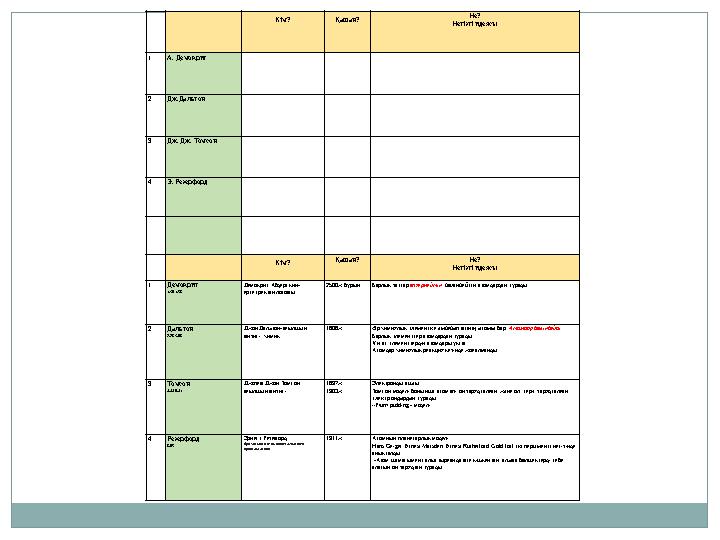
Кім? Қашан? Не?
Негізгі идеясы
1 А. Демокрит
2 Дж.Дальтон
3 Дж. Дж. Томсон
4 Э. Резерфорд
Кім? Қашан? Не?
Негізгі идеясы
1 Демокрит
1,30-1,58 Демокрит Абдерский-
ерте грек философы 2500ж бұрын Барлық заттар өзгермейтін , бөлінбейтін атомдардан тұрады;
2 Дальтон
2,28-3,08 Джон Дальтон-ағылшын
физигі, химик 1808ж Әр химиялық э лементке әмбебап өзінің атомы бар. Атомдар бөлінбейді
Барлық элементтер атомдардан тұрады;
Ұқсас элементтердің атомдары ұқсас;
Атомдар химиялық реакция кезінде жоғалмайды;
3 Томсон
4,44-6,41 Джозеф Джон Томсон,
ағылшын физигі 1897ж
1903ж Электронды ашты
Томсон моделі бойынша атом өзі оң зарядталған, және ол теріс зарядталған
электрондардан тұрады
« Plum pudding » моделі
4 Резерфорд
8,05- Эрнест Резефорд
британский физик новозеландского
происхождения 1911ж Атомның планетарлық моделі;
Hans Geiger, Ernest Marsden, Ernest Rutherford Gold foil эксперименті негізінде
анықталды:
- Атом шамасымен салыстырғанда өте кішкентай, альфа бөлшектерді тебе
алатын оң зарядтан тұрады;
26 слайд
Кім? Қашан? Не? Негізгі идеясы 1 А. Демокрит 2 Дж.Дальтон 3 Дж. Дж. Томсон 4 Э. Резерфорд Кім? Қашан? Не? Негізгі идеясы 1 Демокрит 1,30-1,58 Демокрит Абдерский- ерте грек философы 2500ж бұрын Барлық заттар өзгермейтін , бөлінбейтін атомдардан тұрады; 2 Дальтон 2,28-3,08 Джон Дальтон-ағылшын физигі, химик 1808ж Әр химиялық э лементке әмбебап өзінің атомы бар. Атомдар бөлінбейді Барлық элементтер атомдардан тұрады; Ұқсас элементтердің атомдары ұқсас; Атомдар химиялық реакция кезінде жоғалмайды; 3 Томсон 4,44-6,41 Джозеф Джон Томсон, ағылшын физигі 1897ж 1903ж Электронды ашты Томсон моделі бойынша атом өзі оң зарядталған, және ол теріс зарядталған электрондардан тұрады « Plum pudding » моделі 4 Резерфорд 8,05- Эрнест Резефорд британский физик новозеландского происхождения 1911ж Атомның планетарлық моделі; Hans Geiger, Ernest Marsden, Ernest Rutherford Gold foil эксперименті негізінде анықталды: - Атом шамасымен салыстырғанда өте кішкентай, альфа бөлшектерді тебе алатын оң зарядтан тұрады;

#27 слайд
Резерфорд тәжірибесінен туындайтын
негізгі салдарлар:
Альфа-бөлшектерінің көпшілігі фольгадан ауытқымай түзу өтеді.
2 Кейбір альфа-бөлшектер фольгадан өткенде сәл ауытқиды.
3 Альфа-бөлшектердің өте аз бөлігі фольга кері шағылады!
Резерфорд тәжірибесінен туындайтын қорытынды:
1.Атомның көп бөлігі бос кеңістік (1-салдар)
2.Атомның оң зарядталған шағын аймағы (ядросы) бар (2-салдар)
3.Атомның өте кішкене және қатты аймағы (ядросы) бар (3-салдар)
27 слайд
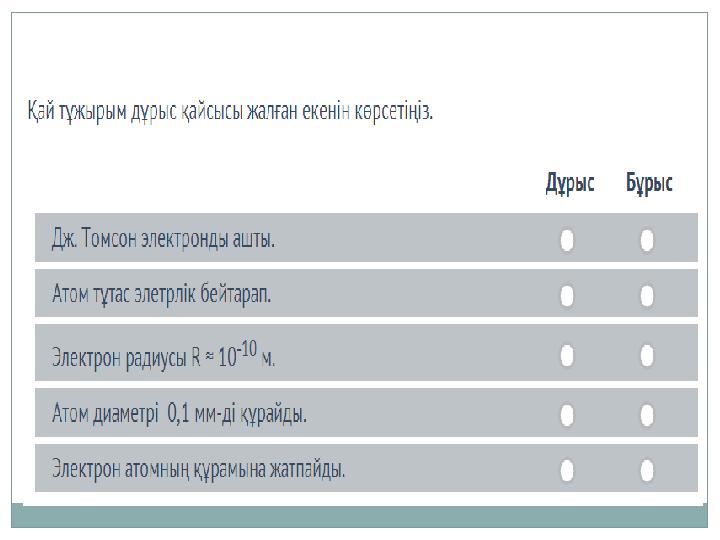
Резерфорд тәжірибесінен туындайтын негізгі салдарлар: Альфа-бөлшектерінің көпшілігі фольгадан ауытқымай түзу өтеді. 2 Кейбір альфа-бөлшектер фольгадан өткенде сәл ауытқиды. 3 Альфа-бөлшектердің өте аз бөлігі фольга кері шағылады! Резерфорд тәжірибесінен туындайтын қорытынды: 1.Атомның көп бөлігі бос кеңістік (1-салдар) 2.Атомның оң зарядталған шағын аймағы (ядросы) бар (2-салдар) 3.Атомның өте кішкене және қатты аймағы (ядросы) бар (3-салдар)
#28 слайд
28 слайд

#29 слайд
29 слайд

шағым қалдыра аласыз
















