Энтропияның күй ықтималдығымен байланысы


#1 слайд
Энтропияның күй
ықтималдығымен
байланысы
1 слайд
Энтропияның күй ықтималдығымен байланысы
#2 слайд
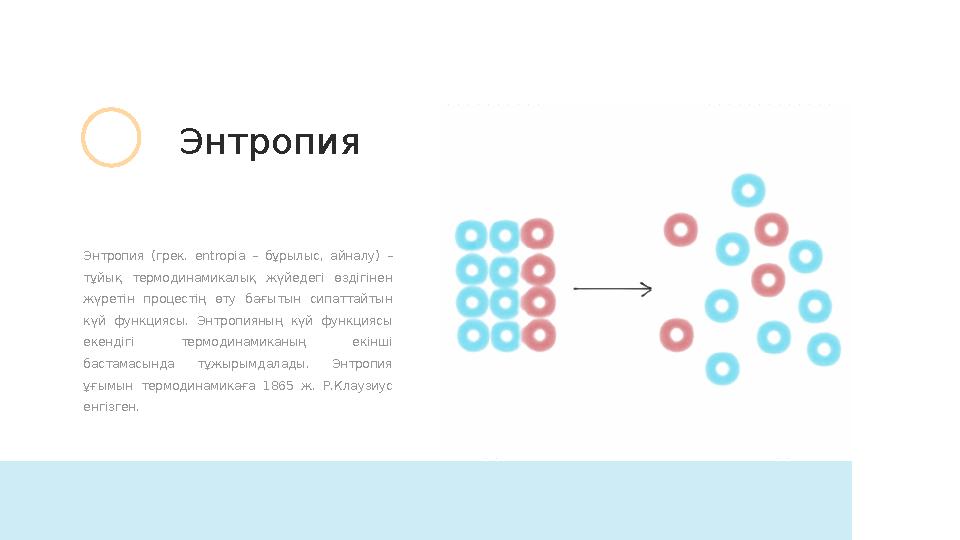
Энтропия (грек. е ntrop і a – бұрылыс, айналу) –
тұйық термодинамикалық жүйедегі өздігінен
жүретін процестің өту бағытын сипаттайтын
күй функциясы. Энтропияның күй функциясы
екендігі термодинамиканың екінші
бастамасында тұжырымдалады. Энтропия
ұғымын термодинамикаға 1865 ж. Р.Клаузиус
енгізген. Энтропия
2 слайд
Энтропия (грек. е ntrop і a – бұрылыс, айналу) – тұйық термодинамикалық жүйедегі өздігінен жүретін процестің өту бағытын сипаттайтын күй функциясы. Энтропияның күй функциясы екендігі термодинамиканың екінші бастамасында тұжырымдалады. Энтропия ұғымын термодинамикаға 1865 ж. Р.Клаузиус енгізген. Энтропия
#3 слайд
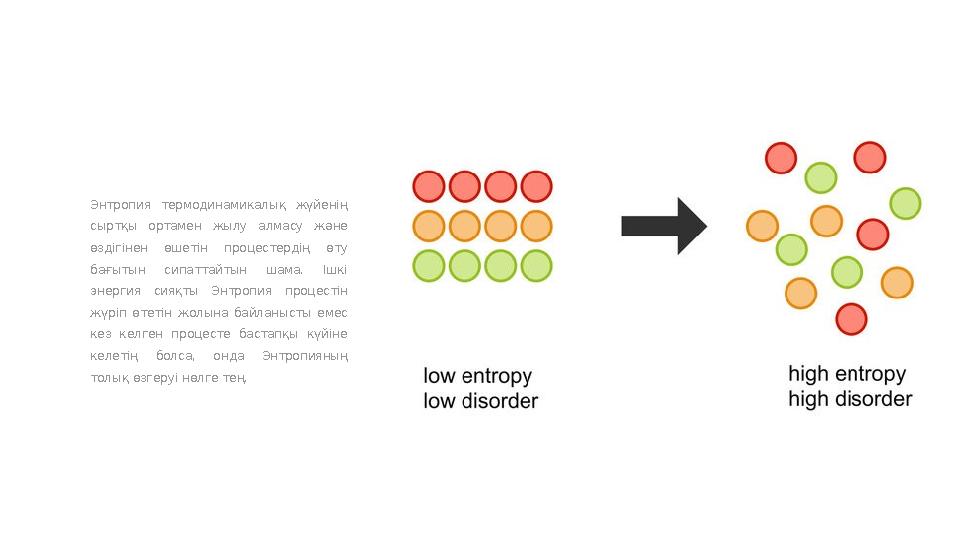
Энтропия термодинамикалық жүйенің
сыртқы ортамен жылу алмасу және
өздігінен өшетін процестердің өту
бағытын сипаттайтын шама. Ішкі
энергия сияқты Энтропия процестін
жүріп өтетін жолына байланысты емес
кез келген процесте бастапқы күйіне
келетің болса, онда Энтропияның
толық өзгеруі нөлге тең.
3 слайд
Энтропия термодинамикалық жүйенің сыртқы ортамен жылу алмасу және өздігінен өшетін процестердің өту бағытын сипаттайтын шама. Ішкі энергия сияқты Энтропия процестін жүріп өтетін жолына байланысты емес кез келген процесте бастапқы күйіне келетің болса, онда Энтропияның толық өзгеруі нөлге тең.
#4 слайд
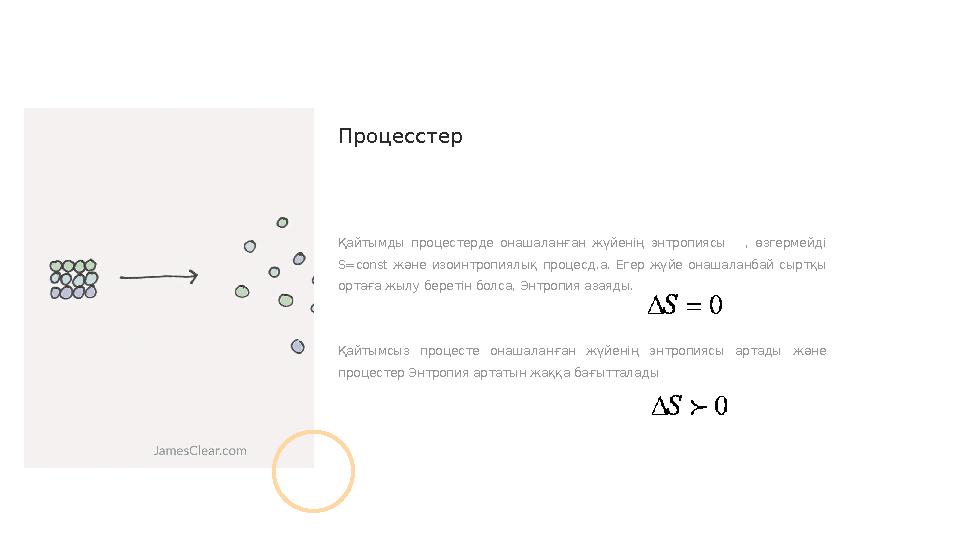
Қайтымды процестерде онашаланған жүйенің энтропиясы , өзгермейді
S=const және изоинтропиялық процесд.а. Егер жүйе онашаланбай сыртқы
ортаға жылу беретін болса, Энтропия азаяды.
Қайтымсыз процесте онашаланған жүйенің энтропиясы артады және
процестер Энтропия артатын жаққа бағытталады Процесстер
4 слайд
Қайтымды процестерде онашаланған жүйенің энтропиясы , өзгермейді S=const және изоинтропиялық процесд.а. Егер жүйе онашаланбай сыртқы ортаға жылу беретін болса, Энтропия азаяды. Қайтымсыз процесте онашаланған жүйенің энтропиясы артады және процестер Энтропия артатын жаққа бағытталады Процесстер

#5 слайд
Энтропияжүйені құрайтын бөлшектердін бей
берекетсіздігінің өлшемі.
Изотермиялық
Изобаралық
Изохоралық
Адиабаталық S=const
5 слайд
Энтропияжүйені құрайтын бөлшектердін бей берекетсіздігінің өлшемі. Изотермиялық Изобаралық Изохоралық Адиабаталық S=const

#6 слайд
Қайтымды адиабатты процесс, энтропияның өзгеруін
болдырмайды. Сондықтан, оны, изоэнтропийлі процесс деп
атайды. Екі рет кездесетін көрсеткіштердің бар болуына
сәйкес, сыртқы ортамен, энергетикалық пішіндегі әрекетте
болуы. Әрекеттік шарты үшін, байланыстырушы
температура Т жылу алмасуы және меншікті энтропия S
жолымен, осындай қос көрсеткіштерді құрады. Энтропия
экстенсивті (аудитивті) шама болады, себебі энтропия зат,
осыған қарағанда оның анықтамасы, осы заттардың ( S =
mS) санды мөлшеріне пропорционалды, Т мұнда S
функциясында болады.
6 слайд
Қайтымды адиабатты процесс, энтропияның өзгеруін болдырмайды. Сондықтан, оны, изоэнтропийлі процесс деп атайды. Екі рет кездесетін көрсеткіштердің бар болуына сәйкес, сыртқы ортамен, энергетикалық пішіндегі әрекетте болуы. Әрекеттік шарты үшін, байланыстырушы температура Т жылу алмасуы және меншікті энтропия S жолымен, осындай қос көрсеткіштерді құрады. Энтропия экстенсивті (аудитивті) шама болады, себебі энтропия зат, осыған қарағанда оның анықтамасы, осы заттардың ( S = mS) санды мөлшеріне пропорционалды, Т мұнда S функциясында болады.

#7 слайд
Энтропияның абсолютты
шамасын, кейбір тұрақты
дәлдікпен есептеуге болады.
Себебі, оның абсолютты шамасына емес, энтропиялық
өзгеруіне жиі көңіл аударады, оның бастапқы есептелуін
шартты түрде таңдайды (әрекеттегі қалыпты физикалық күй,
ал су үшін, үш қатты нүкте күйі). Энтропия бірлігі - Дж/(кгК).
Химиялық реакцияны зерттеу кезінде тұрақтыны білу үшін,
энтропияның абсолютты шамасының бастапқысын есептеуі
үшін өте үлкен практикалық мәні бар. Нернстің ашқан
принципінің атауындағы, Нернстің жылулық теоремасымен
көрсетілген тұрақтылығын таңдауды іске асыруға болады.
Теореманың тұжырымдауына байланысты, қандай да
болмасын жүйенің энтропиясы кезіндегі абсолютты нольде,
әр уақытта нөлге тең жағдайында қабылдануы мүмкін.
7 слайд
Энтропияның абсолютты шамасын, кейбір тұрақты дәлдікпен есептеуге болады. Себебі, оның абсолютты шамасына емес, энтропиялық өзгеруіне жиі көңіл аударады, оның бастапқы есептелуін шартты түрде таңдайды (әрекеттегі қалыпты физикалық күй, ал су үшін, үш қатты нүкте күйі). Энтропия бірлігі - Дж/(кгК). Химиялық реакцияны зерттеу кезінде тұрақтыны білу үшін, энтропияның абсолютты шамасының бастапқысын есептеуі үшін өте үлкен практикалық мәні бар. Нернстің ашқан принципінің атауындағы, Нернстің жылулық теоремасымен көрсетілген тұрақтылығын таңдауды іске асыруға болады. Теореманың тұжырымдауына байланысты, қандай да болмасын жүйенің энтропиясы кезіндегі абсолютты нольде, әр уақытта нөлге тең жағдайында қабылдануы мүмкін.

#8 слайд
Нернст принципі, тәжірибе жолымен анықталған. Ол,
статистикалық механиканың теориялық дәледенуімен
табылады. Бұл жерде, мыналарды атап өту керек. Өйткені
Нернстің теоремасына байланысты, энтропия - абсолютты
нөл айналасында, қандай да өзгеру күйі кезінде, өзгеріске
ұшырамайды, сондықтан заттар, жылу алмасуға қабілетсіз
болады, онда, бұдан шығуы, салдар ретінде есептелген,
осы Нернстің тұжырымдауынша, жылу динамикасының
үшінші заңы бойынша, жылуды алып кету жолымен,
абсолютты нөлге қол жетпестігі туралы айтылады.
8 слайд
Нернст принципі, тәжірибе жолымен анықталған. Ол, статистикалық механиканың теориялық дәледенуімен табылады. Бұл жерде, мыналарды атап өту керек. Өйткені Нернстің теоремасына байланысты, энтропия - абсолютты нөл айналасында, қандай да өзгеру күйі кезінде, өзгеріске ұшырамайды, сондықтан заттар, жылу алмасуға қабілетсіз болады, онда, бұдан шығуы, салдар ретінде есептелген, осы Нернстің тұжырымдауынша, жылу динамикасының үшінші заңы бойынша, жылуды алып кету жолымен, абсолютты нөлге қол жетпестігі туралы айтылады.

#9 слайд
https://kk.wikipedia.org/wiki/
Энтропия
01 https://stud.kz/referat/show/48893
0 3Пайдаланылған
әдебиеттер
тізімі:
https://mykonspekts.ru/1-
18178.html
0 2 http://engime.org/poek-042-14-2-06-
20-4401-20092-baspa-2010-j.html?
page=530 4
9 слайд
https://kk.wikipedia.org/wiki/ Энтропия 01 https://stud.kz/referat/show/48893 0 3Пайдаланылған әдебиеттер тізімі: https://mykonspekts.ru/1- 18178.html 0 2 http://engime.org/poek-042-14-2-06- 20-4401-20092-baspa-2010-j.html? page=530 4

#10 слайд
Назар
аударғандарыңызға
рахмет!!!
10 слайд
Назар аударғандарыңызға рахмет!!!

шағым қалдыра аласыз






 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
