ІІ топтың негізгі топша металдарының жалпы сипаттамасы. Кальций және магний.
ІІ топтың негізгі топша металдарының жалпы сипаттамасы. Кальций және магний.


#1 слайд
Сабақтың тақырыбы
1 слайд
Сабақтың тақырыбы
#2 слайд
С а б а қ т ы ң м а қ с а т ы :Білімділік:
ІІ-топтың негізгі топша металдарына
жалпы сипаттама беру,
Д.И.Менделеевтің периодтық
жүйесінің негізгі топшасындағы
кальций мен магний металдар
жайында алған білімдерін кеңейту
және тереңдету.
Тәрбиелік:
Оқушыларды қоршаған ортаны
қорғауға,ұжымдық жұмыс
істеу қабілетіне,ізденімпаздыққа,
жауапкершілікке тәрбиелеу .Тәрбиелік:
Оқушыларды қоршаған ортаны
қорғауға,ұжымдық жұмыс
істеу қабілетіне,ізденімпаздыққа,
жауапкершілікке тәрбиелеу . Дамытушылық:
Металдардың қасиеттерін,
маңызын талдау, реакция
теңдеулері арқылы жаза
білуді әрі қарай дамыту ,
қорытындысын шығаруға
үйрету.Химия пәнінен алған
білімдерін жетілдіру, өз бетінше
іздену қабілетін дамыту.С а б а қ т ы ң м а қ с а т ы : Білімділік:
ІІ-топтың негізгі топша металдарына
жалпы сипаттама беру,
Д.И.Менделеевтің периодтық
жүйесінің негізгі топшасындағы
кальций мен магний металдар
жайында алған білімдерін кеңейту
және тереңдету. Дамытушылық:
Металдардың қасиеттерін,
маңызын талдау, реакция
теңдеулері арқылы жаза
білуді әрі қарай дамыту ,
қорытындысын шығаруға
үйрету.Химия пәнінен алған
білімдерін жетілдіру, өз бетінше
іздену қабілетін дамыту.
2 слайд
С а б а қ т ы ң м а қ с а т ы :Білімділік: ІІ-топтың негізгі топша металдарына жалпы сипаттама беру, Д.И.Менделеевтің периодтық жүйесінің негізгі топшасындағы кальций мен магний металдар жайында алған білімдерін кеңейту және тереңдету. Тәрбиелік: Оқушыларды қоршаған ортаны қорғауға,ұжымдық жұмыс істеу қабілетіне,ізденімпаздыққа, жауапкершілікке тәрбиелеу .Тәрбиелік: Оқушыларды қоршаған ортаны қорғауға,ұжымдық жұмыс істеу қабілетіне,ізденімпаздыққа, жауапкершілікке тәрбиелеу . Дамытушылық: Металдардың қасиеттерін, маңызын талдау, реакция теңдеулері арқылы жаза білуді әрі қарай дамыту , қорытындысын шығаруға үйрету.Химия пәнінен алған білімдерін жетілдіру, өз бетінше іздену қабілетін дамыту.С а б а қ т ы ң м а қ с а т ы : Білімділік: ІІ-топтың негізгі топша металдарына жалпы сипаттама беру, Д.И.Менделеевтің периодтық жүйесінің негізгі топшасындағы кальций мен магний металдар жайында алған білімдерін кеңейту және тереңдету. Дамытушылық: Металдардың қасиеттерін, маңызын талдау, реакция теңдеулері арқылы жаза білуді әрі қарай дамыту , қорытындысын шығаруға үйрету.Химия пәнінен алған білімдерін жетілдіру, өз бетінше іздену қабілетін дамыту.
#3 слайд
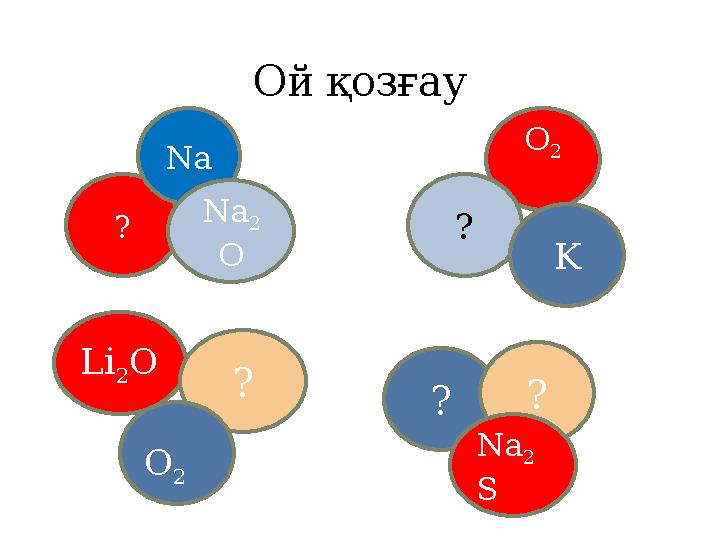
Ой қозғау
? Na
Na
2
O
Li
2 O
?
O
2 O
2
?
K
? ?
Na
2
S
3 слайд
Ой қозғау ? Na Na 2 O Li 2 O ? O 2 O 2 ? K ? ? Na 2 S

#4 слайд
1. NaOH а) бертолле тұзы
2. KMnO
4 ә) натрий сульфаты
3. KClO 3
б) ас тұзы
4. Na
2 SO
4 в) натрий гидрокарбонаты
5. NaHCO
3 г) калий перманганаты
6. N а CI д) күйдіргіш натрСәйкестендіру тесті.
4 слайд
1. NaOH а) бертолле тұзы 2. KMnO 4 ә) натрий сульфаты 3. KClO 3 б) ас тұзы 4. Na 2 SO 4 в) натрий гидрокарбонаты 5. NaHCO 3 г) калий перманганаты 6. N а CI д) күйдіргіш натрСәйкестендіру тесті.

#5 слайд
Тіл- өнері
1. РОЫНҚАҒС
2. АСПЫН
3. АЫҚЙАЛ
4. ҮМКСІ
5 слайд
Тіл- өнері 1. РОЫНҚАҒС 2. АСПЫН 3. АЫҚЙАЛ 4. ҮМКСІ

#6 слайд
«Мен кіммін»
1.Ең қатты металл
2.Ең қиын балқитын металл
3.Сұйық металл
4.Ең иілімді металл
5.Ең жеңіл металл
6.Ең ауыр металл
6 слайд
«Мен кіммін» 1.Ең қатты металл 2.Ең қиын балқитын металл 3.Сұйық металл 4.Ең иілімді металл 5.Ең жеңіл металл 6.Ең ауыр металл

#7 слайд
“ Ой қозғау”
7 слайд
“ Ой қозғау”

#8 слайд
+4 Be …2s 2
+2 Mg…3s 2
+20 Ca…4s 2
+38 Sr…5s 2
+56 Ba…6s 2
+88 Ra…7s 2Атомдардың электрондық
формулалары
8 слайд
+4 Be …2s 2 +2 Mg…3s 2 +20 Ca…4s 2 +38 Sr…5s 2 +56 Ba…6s 2 +88 Ra…7s 2Атомдардың электрондық формулалары
#9 слайд
Периодтық жүйе
Группы элементов
I IIIII VIIIIV V VI VII
II I
III
VII VI VIV 21
3
4
5
6
7Периоды
Ряды
98
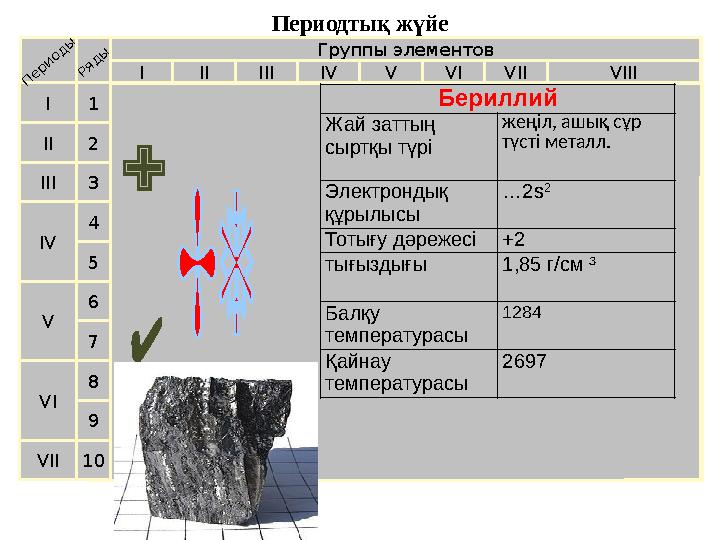
10 Бериллий
Жай заттың
сыртқы түрі жеңіл, ашық сұр
түсті металл.
Электрондық
құрылысы … 2s 2
Тотығу дәрежесі +2
тығыздығы 1,85 г/см ³
Балқу
температурасы 1284
Қайнау
температурасы 2697
9 слайд
Периодтық жүйе Группы элементов I IIIII VIIIIV V VI VII II I III VII VI VIV 21 3 4 5 6 7Периоды Ряды 98 10 Бериллий Жай заттың сыртқы түрі жеңіл, ашық сұр түсті металл. Электрондық құрылысы … 2s 2 Тотығу дәрежесі +2 тығыздығы 1,85 г/см ³ Балқу температурасы 1284 Қайнау температурасы 2697
#10 слайд
Периодтық жүйе
Элементтердің топтары
I IIIII VIIIIV V VI VII
II I
III
VII VI VIV 21
3
4
5
6
7Периоды
қатары
98
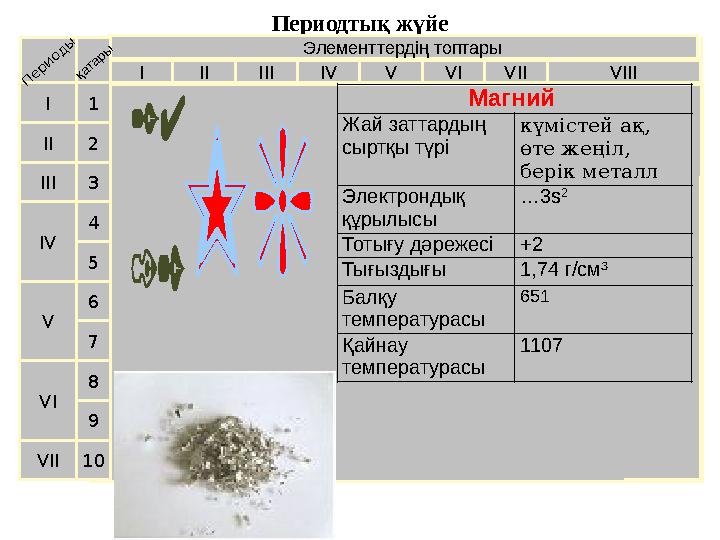
10 Магний
Жай заттардың
сыртқы түрі күмістей ақ,
өте жеңіл,
берік металл
Электрондық
құрылысы … 3s 2
Тотығу дәрежесі +2
Тығыздығы 1,74 г/см³
Балқу
температурасы 651
Қайнау
температурасы 1107
10 слайд
Периодтық жүйе Элементтердің топтары I IIIII VIIIIV V VI VII II I III VII VI VIV 21 3 4 5 6 7Периоды қатары 98 10 Магний Жай заттардың сыртқы түрі күмістей ақ, өте жеңіл, берік металл Электрондық құрылысы … 3s 2 Тотығу дәрежесі +2 Тығыздығы 1,74 г/см³ Балқу температурасы 651 Қайнау температурасы 1107

#11 слайд
Периодтық жүйе
Элементтің топтары
I IIIII VIIIIV V VI VII
II I
III
VII VI VIV 21
3
4
5
6
7Периоды
Ряды
98
10 Кальций
Жай заттың
сыртқы түрі Кальций ақ
түсті, жеңіл
Электрондық
құрылысы … 4s 2
Тотығу дәрежесі +2
Тығыздығы 1,55 г/см ³
Балқу
температурасы 840
Қайнау
температурасы 1440
11 слайд
Периодтық жүйе Элементтің топтары I IIIII VIIIIV V VI VII II I III VII VI VIV 21 3 4 5 6 7Периоды Ряды 98 10 Кальций Жай заттың сыртқы түрі Кальций ақ түсті, жеңіл Электрондық құрылысы … 4s 2 Тотығу дәрежесі +2 Тығыздығы 1,55 г/см ³ Балқу температурасы 840 Қайнау температурасы 1440
#12 слайд
Периодтық жүйе
Элементтердің топтары
I IIIII VIIIIV V VI VII
II I
III
VII VI VIV 21
3
4
5
6
7Периоды
қатары
98
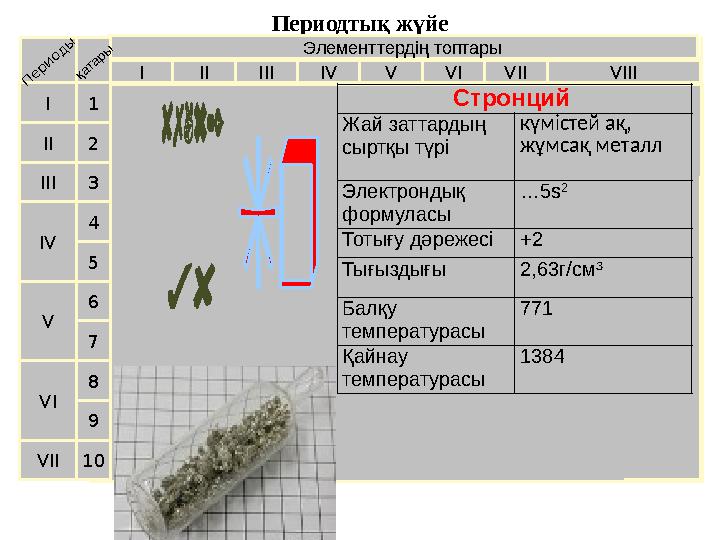
10 Стронций
Жай заттардың
сыртқы түрі күмістей ақ,
жұмса қ металл
Электрондық
формуласы … 5s 2
Тотығу дәрежесі +2
Тығыздығы 2,63г/см³
Балқу
температурасы 771
Қайнау
температурасы 1384
12 слайд
Периодтық жүйе Элементтердің топтары I IIIII VIIIIV V VI VII II I III VII VI VIV 21 3 4 5 6 7Периоды қатары 98 10 Стронций Жай заттардың сыртқы түрі күмістей ақ, жұмса қ металл Электрондық формуласы … 5s 2 Тотығу дәрежесі +2 Тығыздығы 2,63г/см³ Балқу температурасы 771 Қайнау температурасы 1384
#13 слайд
Периодтық жүйе
Элементтердің топтары
I IIIII VIIIIV V VI VII
II I
III
VII VI VIV 21
3
4
5
6
7Периоды
қатары
98
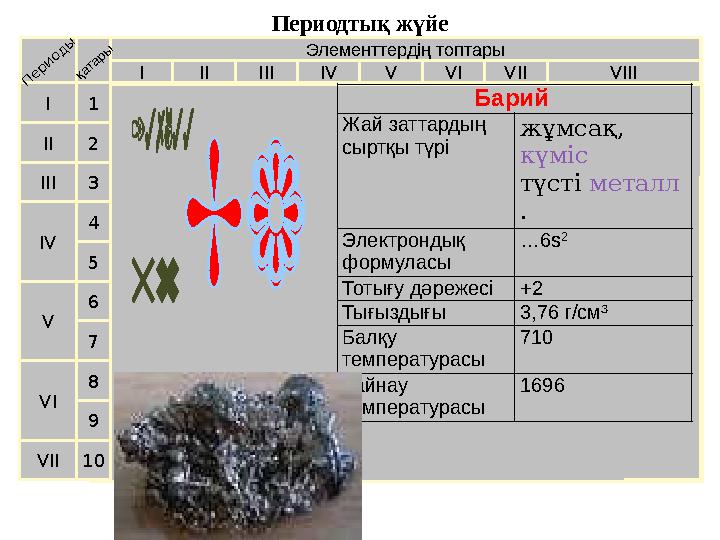
10 Барий
Жай заттардың
сыртқы түрі жұмсақ,
күміс
түсті металл
.
Электрондық
формуласы … 6s 2
Тотығу дәрежесі +2
Тығыздығы 3,76 г/см³
Балқу
температурасы 710
Қайнау
температурасы 1696
13 слайд
Периодтық жүйе Элементтердің топтары I IIIII VIIIIV V VI VII II I III VII VI VIV 21 3 4 5 6 7Периоды қатары 98 10 Барий Жай заттардың сыртқы түрі жұмсақ, күміс түсті металл . Электрондық формуласы … 6s 2 Тотығу дәрежесі +2 Тығыздығы 3,76 г/см³ Балқу температурасы 710 Қайнау температурасы 1696
#14 слайд
Элементтердің топтары
I IIIII VIIIIV V VI VII
II I
III
VII VI VIV 21
3
4
5
6
7Периоды
қатары
98
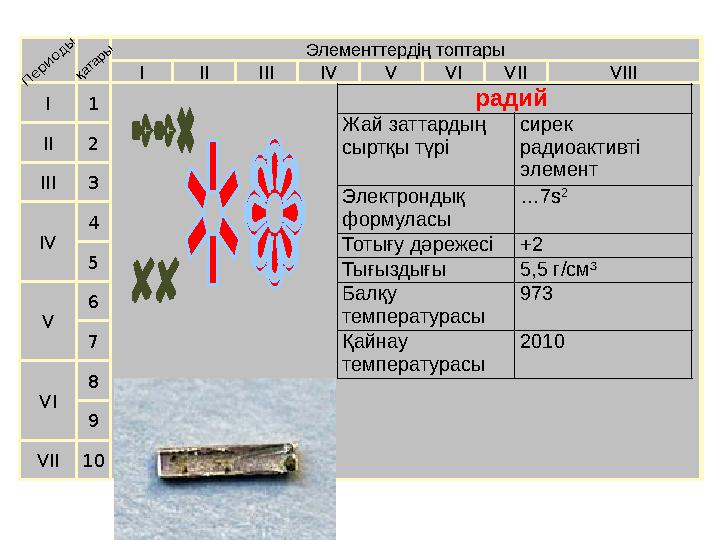
10 радий
Жай заттардың
сыртқы түрі сирек
радиоактивті
элемент
Электрондық
формуласы … 7s 2
Тотығу дәрежесі +2
Тығыздығы 5,5 г/см³
Балқу
температурасы 973
Қайнау
температурасы 2010
14 слайд
Элементтердің топтары I IIIII VIIIIV V VI VII II I III VII VI VIV 21 3 4 5 6 7Периоды қатары 98 10 радий Жай заттардың сыртқы түрі сирек радиоактивті элемент Электрондық формуласы … 7s 2 Тотығу дәрежесі +2 Тығыздығы 5,5 г/см³ Балқу температурасы 973 Қайнау температурасы 2010
#15 слайд
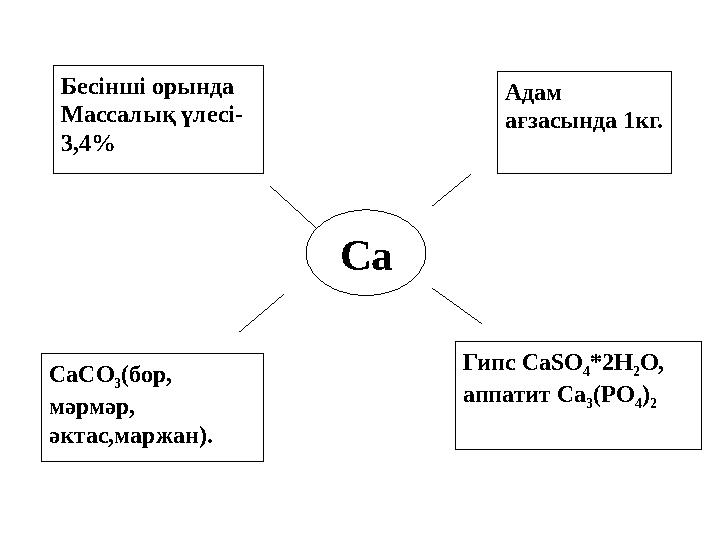
Бесінші орында
Массалық үлесі-
3,4 %
СаСО
3 ( бор,
мәрмәр,
әктас,маржан ) . Адам
ағзасында 1кг.
Гипс CaSO
4 *2H
2 O ,
аппатит Ca
3 (PO
4 )
2 Са
15 слайд
Бесінші орында Массалық үлесі- 3,4 % СаСО 3 ( бор, мәрмәр, әктас,маржан ) . Адам ағзасында 1кг. Гипс CaSO 4 *2H 2 O , аппатит Ca 3 (PO 4 ) 2 Са
#16 слайд
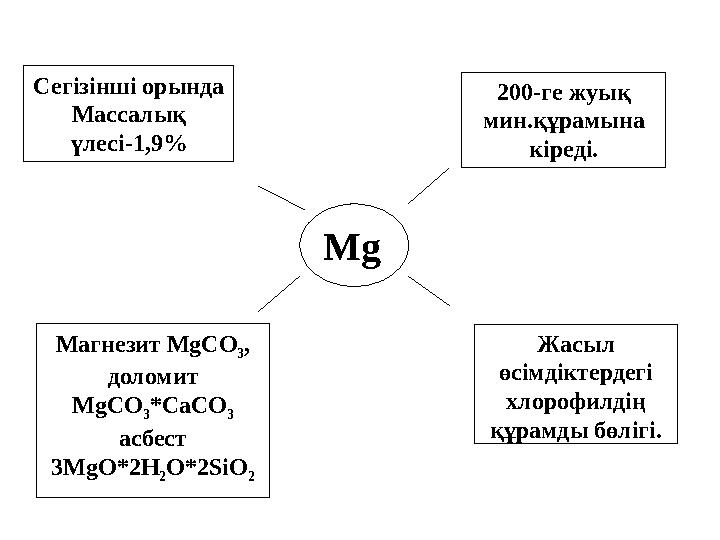
Сегізінші орында
Массалық
үлесі-1,9 %
Магнезит MgCO
3 ,
доломит
MgCO
3 *CaCO
3
асбест
3 MgO*2H
2 O*2SiO
2 Жасыл
өсімдіктердегі
хлорофилдің
құрамды бөлігі. 200-ге жуық
мин.құрамына
кіреді.
Mg
16 слайд
Сегізінші орында Массалық үлесі-1,9 % Магнезит MgCO 3 , доломит MgCO 3 *CaCO 3 асбест 3 MgO*2H 2 O*2SiO 2 Жасыл өсімдіктердегі хлорофилдің құрамды бөлігі. 200-ге жуық мин.құрамына кіреді. Mg

#17 слайд
Химиялық қасиеттері
( тоты қсыздандырғыштар, т.д.+2 )
17 слайд
Химиялық қасиеттері ( тоты қсыздандырғыштар, т.д.+2 )
#18 слайд
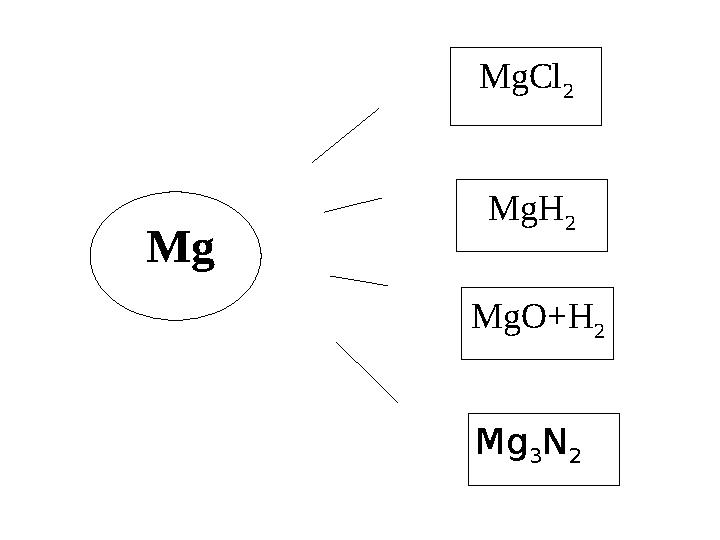
Mg MgCl
2
MgH
2
MgO+H
2
Mg
3 N
2
18 слайд
Mg MgCl 2 MgH 2 MgO+H 2 Mg 3 N 2
#19 слайд
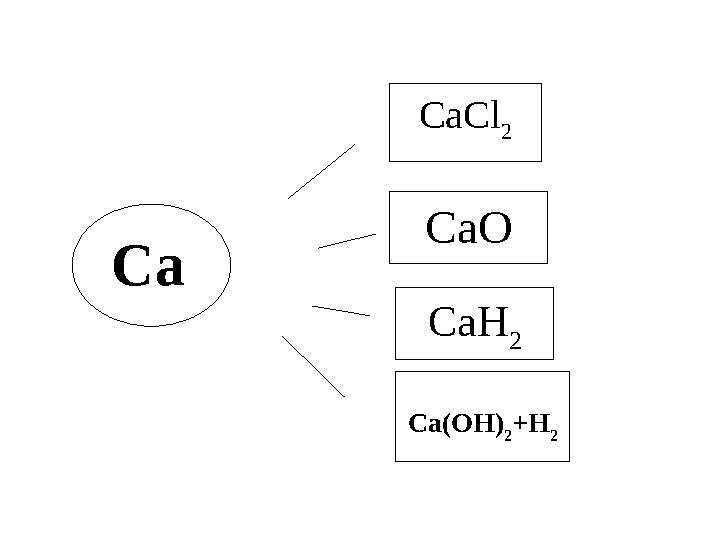
Ca CaCl
2
CaO
CaH
2
Ca(OH)
2 +H
2
19 слайд
Ca CaCl 2 CaO CaH 2 Ca(OH) 2 +H 2

#20 слайд
1828 жылы неміс химигі Ф. Велер
(1800-1882) берилийді алды.Берилий элементінің ашылуы
Қолданылуы
Баяу балқитын металдардың бериллидтері — авиация
және ракета жасауда аса қажетті зат. Рентген
сәулелері бериллийден жақсы өтетін болғандықтан,
одан рентген трубкаларының терезелерін дайындайды.
Бериллий әр түрлі құймалар және коррозияға
берік болат алуда,
электротехникада,атом реакторларын жасауда
кең түрде қолданылады.
Қазақстанда бериллий Өскемендегі титан - магний
комбинатында өндіріледі. Фридрих Вёлер
20 слайд
1828 жылы неміс химигі Ф. Велер (1800-1882) берилийді алды.Берилий элементінің ашылуы Қолданылуы Баяу балқитын металдардың бериллидтері — авиация және ракета жасауда аса қажетті зат. Рентген сәулелері бериллийден жақсы өтетін болғандықтан, одан рентген трубкаларының терезелерін дайындайды. Бериллий әр түрлі құймалар және коррозияға берік болат алуда, электротехникада,атом реакторларын жасауда кең түрде қолданылады. Қазақстанда бериллий Өскемендегі титан - магний комбинатында өндіріледі. Фридрих Вёлер

#21 слайд
1808 ж. ағылшын ғалымы
Г.Дэви (1778 — 1829) ашқан.Магний элементінің ашылуы
Гемфри
Дэви Қолданылуы
Магний құймаларының
өнеркәсібінде, құймаларды
легирлеуде, қиын тотықсызданатын
және сирек металдарды металлотерм.
жолмен алу үшін (мыс., T і, Zr, Hf, U,
т.б.), магний органик. қосылыстар
синтезінде қолданылады.
21 слайд
1808 ж. ағылшын ғалымы Г.Дэви (1778 — 1829) ашқан.Магний элементінің ашылуы Гемфри Дэви Қолданылуы Магний құймаларының өнеркәсібінде, құймаларды легирлеуде, қиын тотықсызданатын және сирек металдарды металлотерм. жолмен алу үшін (мыс., T і, Zr, Hf, U, т.б.), магний органик. қосылыстар синтезінде қолданылады.

#22 слайд
1808 ж. ағылшын ғалымы
Г.Дэви (1778 — 1829) алған.Кальций элементінің ашылуы
Кальций инертті газды тазартып болат , никель , мыс ,
т.б. металдарды балқыту үшін қоспа ретінде
пайдаланылады.
Кальцийдің қосылыстары құрылыста кеңінен
қолданылады. Қолданылуы
Гемфри
Дэви
22 слайд
1808 ж. ағылшын ғалымы Г.Дэви (1778 — 1829) алған.Кальций элементінің ашылуы Кальций инертті газды тазартып болат , никель , мыс , т.б. металдарды балқыту үшін қоспа ретінде пайдаланылады. Кальцийдің қосылыстары құрылыста кеңінен қолданылады. Қолданылуы Гемфри Дэви

#23 слайд
1808 ж. ағылшын ғалымы
Г.Дэви (1778 — 1829) алған.Стронций элементінің
ашылуы
Гемфри Дэви Қолданылуы
Медицинада дәрілер даярлайды, фото,
кино ісінде, лабораториялық реактив ретінде де қолданылады.
23 слайд
1808 ж. ағылшын ғалымы Г.Дэви (1778 — 1829) алған.Стронций элементінің ашылуы Гемфри Дэви Қолданылуы Медицинада дәрілер даярлайды, фото, кино ісінде, лабораториялық реактив ретінде де қолданылады.

#24 слайд
1808 ж. ағылшын
ғалымы
Гемфри Дэви (1778 — 1829)
алған.Барий элементінің ашылуы
Гемфри Дэви Қолданылуы
Оның қорытпалары газ жұтқыштар ретінде, электронды лампыларда ,
ал оның оксиді катодтарға қаптау жасау үшін қолданылады.
Барий карбонаты BaCO
3 барийдың басқа қосылыстарын алуға, шыны
өнеркәсібінде қолданылады
Барий сульфаты BaSO
4 рентген сәулелерін жақсы жұтатын қасиетке ие
болғандықтан, ақ пигмент ретінде медицинада қолданылады
24 слайд
1808 ж. ағылшын ғалымы Гемфри Дэви (1778 — 1829) алған.Барий элементінің ашылуы Гемфри Дэви Қолданылуы Оның қорытпалары газ жұтқыштар ретінде, электронды лампыларда , ал оның оксиді катодтарға қаптау жасау үшін қолданылады. Барий карбонаты BaCO 3 барийдың басқа қосылыстарын алуға, шыны өнеркәсібінде қолданылады Барий сульфаты BaSO 4 рентген сәулелерін жақсы жұтатын қасиетке ие болғандықтан, ақ пигмент ретінде медицинада қолданылады

#25 слайд
1910 жылы М.Кюри-
П.Кюри француз
химиктері радий
элементін ашты.Радий элементінің
ашылуы
М.Кюри және П.Кюри Қолданылуы
a) әртүрлі салада қолданылатын атом
реакторлары(өндірістердегі сәулеленулер
медицинада және эксперименталды мақсатарда қолданылады).
б) өндірісте, медицинада немес ғылымси зерттеу мақсаттарында
қолданылатын ашық түрдегі радиоактивті заттар.
в) радиациялық химияда
Тұрмыстық және медициналық приборлар қолданады.
25 слайд
1910 жылы М.Кюри- П.Кюри француз химиктері радий элементін ашты.Радий элементінің ашылуы М.Кюри және П.Кюри Қолданылуы a) әртүрлі салада қолданылатын атом реакторлары(өндірістердегі сәулеленулер медицинада және эксперименталды мақсатарда қолданылады). б) өндірісте, медицинада немес ғылымси зерттеу мақсаттарында қолданылатын ашық түрдегі радиоактивті заттар. в) радиациялық химияда Тұрмыстық және медициналық приборлар қолданады.
#26 слайд
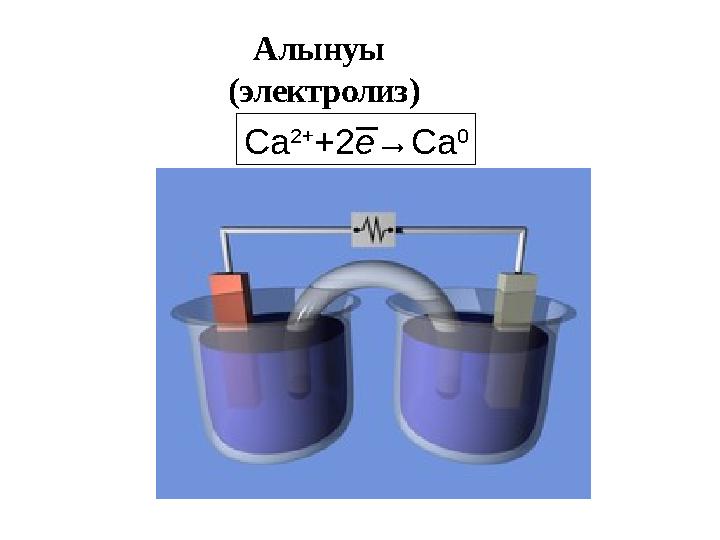
Ca 2+
+2 e →Ca 0Алынуы
( электролиз )
26 слайд
Ca 2+ +2 e →Ca 0Алынуы ( электролиз )

#27 слайд
1. Сыртқы деңгейінде екі электрон бар:
2. Табиғатта Са және Mg ғана көп, ал қалғандары
аз таралған:
3. ІІА-топ металдары барлығы ауыр металдар:
4. Тотығу дәрежесі +2 :
5. Кальцийдың атомдық массасы 40,08 :
6. ІІА-топ металдары барлығы–күшті
тотықтырғыштар:
7. Радий –сирек радиоактивті элемент:
8. Оларға ROH – типті гидроксидтер сәйкес келеді:Графикалық диктант
( иә - “ ” , жоқ - “ –”)⌃
27 слайд
1. Сыртқы деңгейінде екі электрон бар: 2. Табиғатта Са және Mg ғана көп, ал қалғандары аз таралған: 3. ІІА-топ металдары барлығы ауыр металдар: 4. Тотығу дәрежесі +2 : 5. Кальцийдың атомдық массасы 40,08 : 6. ІІА-топ металдары барлығы–күшті тотықтырғыштар: 7. Радий –сирек радиоактивті элемент: 8. Оларға ROH – типті гидроксидтер сәйкес келеді:Графикалық диктант ( иә - “ ” , жоқ - “ –”)⌃
#28 слайд
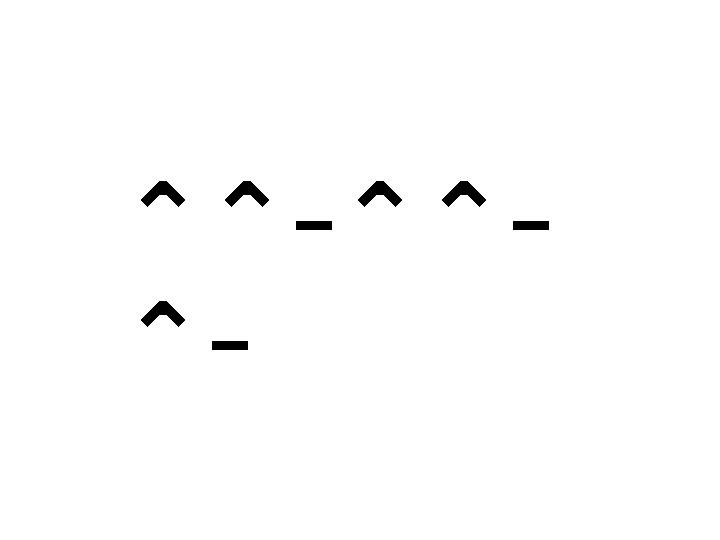
– –⌃⌃ ⌃⌃
–
⌃
28 слайд
– –⌃⌃ ⌃⌃ – ⌃

#29 слайд
Үйге тапсырма
§5.5-5.8,100 бет, конспект «Алюминий .Темір »
29 слайд
Үйге тапсырма §5.5-5.8,100 бет, конспект «Алюминий .Темір »

#30 слайд
Бағалау
30 слайд
Бағалау

шағым қалдыра аласыз
















