Презентация:Табиғаттағы су. 8 сынып. Химия
Презентация:Табиғаттағы су. 8 сынып. Химия


#1 слайд
Табиғаттағы су.
8 сынып. Химия Оқу мақсаты:
8.4.2.6 -судың табиғатта кең таралғандығын, бірегей қасиеттерін
және оның өмір үшін маңызын түсіндіру;
8.4.2.7 -судың табиғаттағы айналымын түсіндіру
Тараз қаласы Тұрар Рысқұлов атындағы №48 орта мектептің
химия пәні мұғалімі: Туймеева Г.Х.
1 слайд
Табиғаттағы су. 8 сынып. Химия Оқу мақсаты: 8.4.2.6 -судың табиғатта кең таралғандығын, бірегей қасиеттерін және оның өмір үшін маңызын түсіндіру; 8.4.2.7 -судың табиғаттағы айналымын түсіндіру Тараз қаласы Тұрар Рысқұлов атындағы №48 орта мектептің химия пәні мұғалімі: Туймеева Г.Х.

#2 слайд
Судың табиғатта таралуы
Жалпы су қорының 2%-ы тұщы су.
Ауа құрамының 1%-4%ыЖер бетінің 71% -ы
Тірі ағзалардың 60-70%-ы Өсімдіктердің 90 % -ы
Нәрестеде - 80%
Жас балада - 70%
Ересек адамда – 60-64%
Қарт адамдарда - 55%
2 слайд
Судың табиғатта таралуы Жалпы су қорының 2%-ы тұщы су. Ауа құрамының 1%-4%ыЖер бетінің 71% -ы Тірі ағзалардың 60-70%-ы Өсімдіктердің 90 % -ы Нәрестеде - 80% Жас балада - 70% Ересек адамда – 60-64% Қарт адамдарда - 55%

#3 слайд
Судың физикалық қасиеттері
Су Н
2 О - сутегі оксиді, оттегінің сутекті қосылысы
ковалент полюсті байланысқа, бұрышты құрылысқа ие,
молекулалық кристал торлы зат. Су молекуласы - өзара
сутектік байланыс арқылы байланысады және сол себепті су
сұйықтық.
Таза су — түссіз, иіссіз, дәмсіз сұйықтық .
Судың қабаты 5 м асқанда көгілдір түсті болып көрінеді.
Табиғи суға дәмді натрий хлориді береді.
Қалыпты қысымда 100°С-та қайнайды да, 0°С-да мұзға (р=0,92 г/см 3
) айналады,
сонда оның көлемі 9 %-ға артады. Температурасы 4°С болғанда, тығыздығы
1г/см 3
(судың ерекшелігі).
Судың жылу сыйымдылығы өте жоғары .
Мысалы: жаздың аптап ыстық күндерінде су жылуды сіңіріп, өзеннің маңайын
салқындатып тұрады, ал қыста жиналған жылуды су біртіндеп ауаға береді,
сондықтан қатты аязды күндерде өзеннің беті тұманданып тұрады.
Су электр тогын нашар өткізеді , себебі суда бейтарап орта болады.
Су – еріткіш. Суда көптеген қатты, сұйық және газ тәріздес заттар ериді .
Су - беттік керілу күшіне ие.
Су – терморегулятор. 104,45 0
3 слайд
Судың физикалық қасиеттері Су Н 2 О - сутегі оксиді, оттегінің сутекті қосылысы ковалент полюсті байланысқа, бұрышты құрылысқа ие, молекулалық кристал торлы зат. Су молекуласы - өзара сутектік байланыс арқылы байланысады және сол себепті су сұйықтық. Таза су — түссіз, иіссіз, дәмсіз сұйықтық . Судың қабаты 5 м асқанда көгілдір түсті болып көрінеді. Табиғи суға дәмді натрий хлориді береді. Қалыпты қысымда 100°С-та қайнайды да, 0°С-да мұзға (р=0,92 г/см 3 ) айналады, сонда оның көлемі 9 %-ға артады. Температурасы 4°С болғанда, тығыздығы 1г/см 3 (судың ерекшелігі). Судың жылу сыйымдылығы өте жоғары . Мысалы: жаздың аптап ыстық күндерінде су жылуды сіңіріп, өзеннің маңайын салқындатып тұрады, ал қыста жиналған жылуды су біртіндеп ауаға береді, сондықтан қатты аязды күндерде өзеннің беті тұманданып тұрады. Су электр тогын нашар өткізеді , себебі суда бейтарап орта болады. Су – еріткіш. Суда көптеген қатты, сұйық және газ тәріздес заттар ериді . Су - беттік керілу күшіне ие. Су – терморегулятор. 104,45 0

#4 слайд
Судың химиялық қасиеттері
1. Жай заттармен әрекеттесуі
•
Белсенді металл + су = сілті + сутек газы
2Na + 2H
2 O = 2NaOH + H
2 ↑
•
Орташа белсенді металл + су буы = металл оксиді + сутек
Zn + H
2 O = t = ZnO + H
2
•
Бейметалмен әрекеттесуі: C + 2 H
2 O = CO
2 + 2 H
2
2.Күрделі заттармен әрекеттесуі:
•
Металл оксидтері + су = негіз CaO+ H
2 O = Ca(OH)
2 + Q
•
Бейметалл оксидтері + су = қышқыл P
2 O
5 + 3H
2 O = 2H
3 PO
4
•
Белсенділігі жоғары металл гидриді + су = негіз + сутегі
NaH + НОН = NaOH + Н
2 ↑
•
Кейбір тұздар + су = кристаллогидрат
CuS О
4 + 5 H
2 О = CuS О
4 * 5 H
2 О мыс купоросы;
FeS О
4 * 7H
2 О темір купоросы;
Na
2 S О
4 * 10H
2 О глаубер тұзы.
4 слайд
Судың химиялық қасиеттері 1. Жай заттармен әрекеттесуі • Белсенді металл + су = сілті + сутек газы 2Na + 2H 2 O = 2NaOH + H 2 ↑ • Орташа белсенді металл + су буы = металл оксиді + сутек Zn + H 2 O = t = ZnO + H 2 • Бейметалмен әрекеттесуі: C + 2 H 2 O = CO 2 + 2 H 2 2.Күрделі заттармен әрекеттесуі: • Металл оксидтері + су = негіз CaO+ H 2 O = Ca(OH) 2 + Q • Бейметалл оксидтері + су = қышқыл P 2 O 5 + 3H 2 O = 2H 3 PO 4 • Белсенділігі жоғары металл гидриді + су = негіз + сутегі NaH + НОН = NaOH + Н 2 ↑ • Кейбір тұздар + су = кристаллогидрат CuS О 4 + 5 H 2 О = CuS О 4 * 5 H 2 О мыс купоросы; FeS О 4 * 7H 2 О темір купоросы; Na 2 S О 4 * 10H 2 О глаубер тұзы.

#5 слайд
Суды анықтау әдістері
Ауа құрамындағы су буын анықтау.
Мұздатқыштан алынған ыдыстың
сыртында су тамшылары түзіледі.
Органикалық заттар құрамындағы суды
анықтау.
Органикалық заттар жанғанда көмірқышыл
газы және су түзіледі.
М. Крахмал + О 2 = СО 2 + Н 2 О
CuS О
4 + 5 H
2 О = CuS О
4 * 5 H
2 О мыс купоросы
5 слайд
Суды анықтау әдістері Ауа құрамындағы су буын анықтау. Мұздатқыштан алынған ыдыстың сыртында су тамшылары түзіледі. Органикалық заттар құрамындағы суды анықтау. Органикалық заттар жанғанда көмірқышыл газы және су түзіледі. М. Крахмал + О 2 = СО 2 + Н 2 О CuS О 4 + 5 H 2 О = CuS О 4 * 5 H 2 О мыс купоросы

#6 слайд
Суды анықтау әдістері
Су қатысында түсін өзгертетін тұздар жәрдемінде
анықтау
Көптеген тұздар су қатысында түсін өзгертеді. Суды анықтау
үшін сусыз мыс (II) сульфаты ерітіндісі мен кобальт (II)
хлориді қолданылады.
-таза кобальт хлориді (II) көк түсті. Ол су молекулаларына оңай
қосылып , қою қызыл түске ауысады.
C о Cl
2 + 4 H
2 О = CoCl
2 * 4 H
2 О
кобальт хлоридінің тетрагидраты ;
-ақ түсті ұнтақ түріндегі сусыз мыс (II) сульфаты су
молекуласымен әрекеттескен соң көк түске өзгереді.
CuS О
4 + 5 H
2 О = CuS О
4 * 5 H
2 О мыс купоросы;
CoCl
2 * 2 H
2 О
күлгін
6 слайд
Суды анықтау әдістері Су қатысында түсін өзгертетін тұздар жәрдемінде анықтау Көптеген тұздар су қатысында түсін өзгертеді. Суды анықтау үшін сусыз мыс (II) сульфаты ерітіндісі мен кобальт (II) хлориді қолданылады. -таза кобальт хлориді (II) көк түсті. Ол су молекулаларына оңай қосылып , қою қызыл түске ауысады. C о Cl 2 + 4 H 2 О = CoCl 2 * 4 H 2 О кобальт хлоридінің тетрагидраты ; -ақ түсті ұнтақ түріндегі сусыз мыс (II) сульфаты су молекуласымен әрекеттескен соң көк түске өзгереді. CuS О 4 + 5 H 2 О = CuS О 4 * 5 H 2 О мыс купоросы; CoCl 2 * 2 H 2 О күлгін
#7 слайд
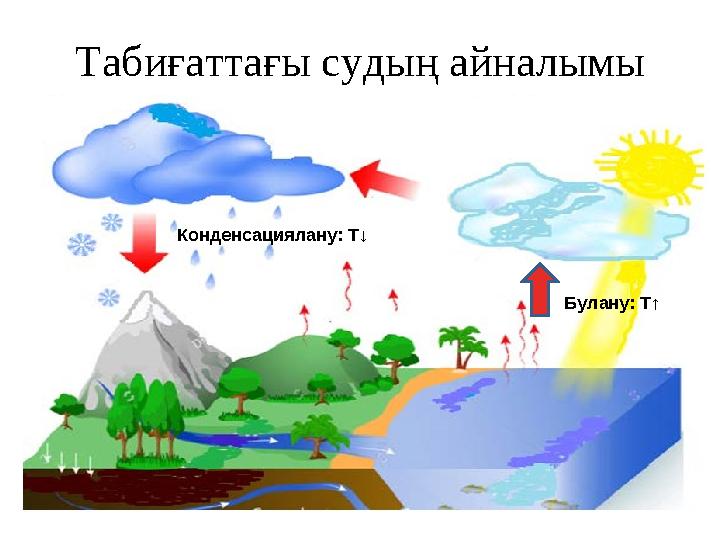
Табиғаттағы судың айналымы
Булану: Т↑ Конденсациялану: Т ↓
7 слайд
Табиғаттағы судың айналымы Булану: Т↑ Конденсациялану: Т ↓

#8 слайд
Табиғаттағы судың айналымы
•
1. Күн қызуының әсерінен
су буланып, атмосфераға
көтеріледі.
•
2. Осы тазартылған бу
конденсацияланып, яғни
қоюланып, бұлттар
түзеді.
•
3. Сосын, жауын-шашын
түрінде қайтадан жерге
түседі.
https://chemege.ru/video-po-obshhej-ximii/
8 слайд
Табиғаттағы судың айналымы • 1. Күн қызуының әсерінен су буланып, атмосфераға көтеріледі. • 2. Осы тазартылған бу конденсацияланып, яғни қоюланып, бұлттар түзеді. • 3. Сосын, жауын-шашын түрінде қайтадан жерге түседі. https://chemege.ru/video-po-obshhej-ximii/

#9 слайд
Су – тіршілік көзі
9 слайд
Су – тіршілік көзі

#10 слайд
Бекіту:деңгейлік тапсырма.
1-деңгей
1.Су дәмсіз, бірақ біз қолданатын судың дәмі бар. Неліктен?
2.Су сұйық, мұз қатты зат, ал неліктен су мұздағанда мұз су бетінде
орналасады?
3. 1 кг су және 1 кг спиртті қайнатқанда қай бірі бірінші қайнайды? Себебін
түсіндіріңдер.
4.Су сутегінің оксиді, оттегінің сутекті қосылысы болып келеді.
Бейметалдардаң сутекті қосылысы ұшқыш болып келеді, бірақ су неліктен
сұйық болуының себебін түсіндіріңдер.
5.Неліктен мұздатқыштан алынған ыдыстың сыртында су тамшылары
түзіледі?
6.Суға фенолфталеин және лакмус ертінділерін тамызғанда су қандай түске
енеді? Себебі не?
2-деңгей
1 .Li + H
2 O = Ba + H
2 O = K
2 O + H
2 O = P
2 O
5 + H
2 O =
2 . Мыс купоросы CuS О
4 * 5H
2 О молекуласы құрамындағы судың массалық
үлесін есептеңдер.
3. –деңгей
1.108 грамм су айырылғанда түзілген сутегінің (қ.ж.) көлемін табыңдар.
2.3 моль көміртегі (IV) оксиді сумен әсерлескенде түзілген
көмірқышқылының массасын табыңдар.
10 слайд
Бекіту:деңгейлік тапсырма. 1-деңгей 1.Су дәмсіз, бірақ біз қолданатын судың дәмі бар. Неліктен? 2.Су сұйық, мұз қатты зат, ал неліктен су мұздағанда мұз су бетінде орналасады? 3. 1 кг су және 1 кг спиртті қайнатқанда қай бірі бірінші қайнайды? Себебін түсіндіріңдер. 4.Су сутегінің оксиді, оттегінің сутекті қосылысы болып келеді. Бейметалдардаң сутекті қосылысы ұшқыш болып келеді, бірақ су неліктен сұйық болуының себебін түсіндіріңдер. 5.Неліктен мұздатқыштан алынған ыдыстың сыртында су тамшылары түзіледі? 6.Суға фенолфталеин және лакмус ертінділерін тамызғанда су қандай түске енеді? Себебі не? 2-деңгей 1 .Li + H 2 O = Ba + H 2 O = K 2 O + H 2 O = P 2 O 5 + H 2 O = 2 . Мыс купоросы CuS О 4 * 5H 2 О молекуласы құрамындағы судың массалық үлесін есептеңдер. 3. –деңгей 1.108 грамм су айырылғанда түзілген сутегінің (қ.ж.) көлемін табыңдар. 2.3 моль көміртегі (IV) оксиді сумен әсерлескенде түзілген көмірқышқылының массасын табыңдар.

#11 слайд
Назарларыңызға рақмет!Үйге тапсырма:
-54 –”Табиғаттағы су” тақырыбын оқу;
-201 беттегі 3 тапсырма.
11 слайд
Назарларыңызға рақмет!Үйге тапсырма: -54 –”Табиғаттағы су” тақырыбын оқу; -201 беттегі 3 тапсырма.

шағым қалдыра аласыз
















