Зат мөлшері


#1 слайд
Сабақтың тақырыбы.
Зат мөлшері
Зат мөлшері - атомдар саны
ретінде. Авогадро саны.
1 слайд
Сабақтың тақырыбы. Зат мөлшері Зат мөлшері - атомдар саны ретінде. Авогадро саны.

#2 слайд
2
1
3
4
Сабақтағы көңіл-күйің қандай?
2 слайд
2 1 3 4 Сабақтағы көңіл-күйің қандай?

#3 слайд
Есепте!
Тапсырма
Осы заттардың молекулалық
массаларын есептеңдер
І топ P ; PH3 ; P2O5; H3PO4 ; Na3PO4
І топ Fe ; FeCl2 ; FeO ; FeS ; FeSO4
3 слайд
Есепте! Тапсырма Осы заттардың молекулалық массаларын есептеңдер І топ P ; PH3 ; P2O5; H3PO4 ; Na3PO4 І топ Fe ; FeCl2 ; FeO ; FeS ; FeSO4
#4 слайд
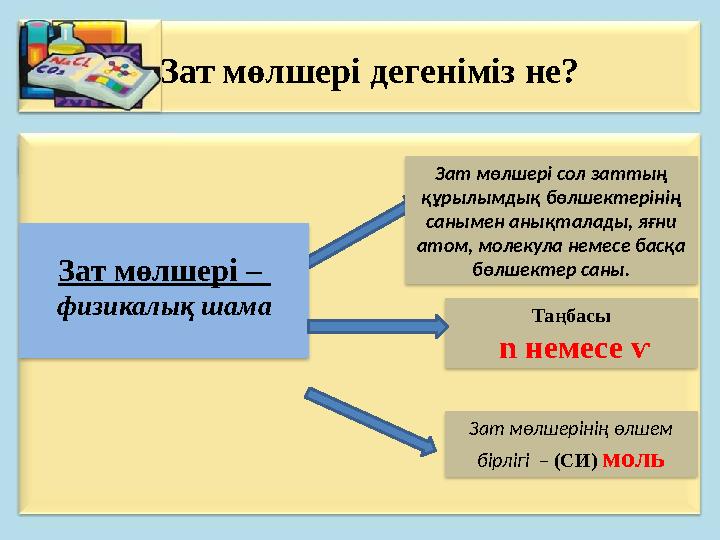
Зат мөлшері –
физикалық шама
Зат мөлшері сол заттың
құрылымдық бөлшектерінің
санымен анықталады, яғни
атом, молекула немесе басқа
бөлшектер саны.
Таңбасы
n немесе ѵ
Зат мөлшерінің өлшем
бірлігі
–
(СИ) моль
Зат мөлшері дегеніміз не?
4 слайд
Зат мөлшері – физикалық шама Зат мөлшері сол заттың құрылымдық бөлшектерінің санымен анықталады, яғни атом, молекула немесе басқа бөлшектер саны. Таңбасы n немесе ѵ Зат мөлшерінің өлшем бірлігі – (СИ) моль Зат мөлшері дегеніміз не?

#5 слайд
Моль дегеніміз не?
•Моль – берілген заттың
құрылымдық бөлшектері 12г
көміртегіндегі атом санына
сәйкес келетін зат мөлшері. ν
(ню) әрпімен белгіленеді,
құрылымдық бөлшектер саны
N
a
әрпімен белгіленеді.
5 слайд
Моль дегеніміз не? •Моль – берілген заттың құрылымдық бөлшектері 12г көміртегіндегі атом санына сәйкес келетін зат мөлшері. ν (ню) әрпімен белгіленеді, құрылымдық бөлшектер саны N a әрпімен белгіленеді.

#6 слайд
Заттың керекті мөлшерін қалай
өлшеп алуға болады?
•Зат мөлшерін моль арқылы өрнектеген
сияқты молярлық масса зат массасын
грамм арқылы көрсетеді. Демек, «Заттың
молярлық массасы М зат массасының зат
мөлшеріне қатынасына тең шама»
М=m / ν
•Мысалы: 1) M(H
2
)= 2 г/моль;
•2) M(O
2
) =32 г/моль; 3) M(H
2
O) =18
г/моль
6 слайд
Заттың керекті мөлшерін қалай өлшеп алуға болады? •Зат мөлшерін моль арқылы өрнектеген сияқты молярлық масса зат массасын грамм арқылы көрсетеді. Демек, «Заттың молярлық массасы М зат массасының зат мөлшеріне қатынасына тең шама» М=m / ν •Мысалы: 1) M(H 2 )= 2 г/моль; •2) M(O 2 ) =32 г/моль; 3) M(H 2 O) =18 г/моль
#7 слайд
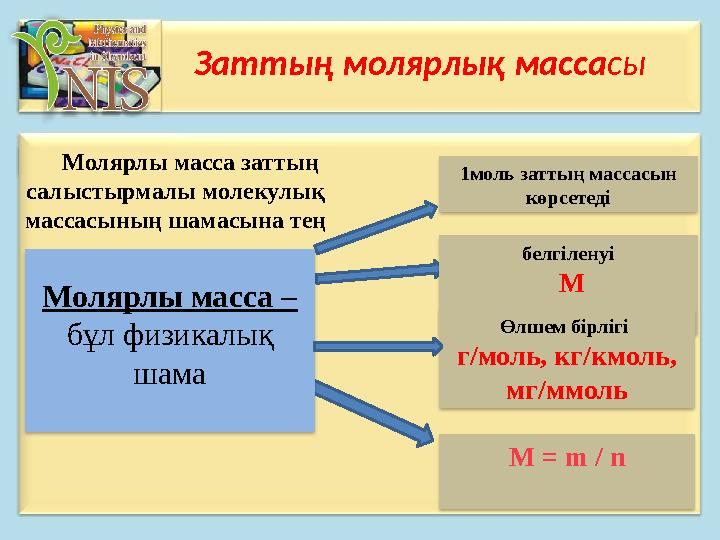
Молярлы масса заттың
салыстырмалы молекулық
массасының шамасына тең
Молярлы масса –
бұл физикалық
шама
1моль заттың массасын
көрсетеді
белгіленуі
М
Өлшем бірлігі
г/моль, кг/кмоль,
мг/ммоль
М = m / n
Заттың молярлық массасы
7 слайд
Молярлы масса заттың салыстырмалы молекулық массасының шамасына тең Молярлы масса – бұл физикалық шама 1моль заттың массасын көрсетеді белгіленуі М Өлшем бірлігі г/моль, кг/кмоль, мг/ммоль М = m / n Заттың молярлық массасы

#8 слайд
Авагадро саны
•Зат мөлшері мен бөлшек (атом, молекула
т.б) сандары арасында байланыс,
ѵ = N / NA
Формуласы арқылы өрнекеледі. Мұндағы N –
бөлшек саны, NA – Авагадро тұрақтысы,
N
А = 6,02∙10
23
моль-1
8 слайд
Авагадро саны •Зат мөлшері мен бөлшек (атом, молекула т.б) сандары арасында байланыс, ѵ = N / NA Формуласы арқылы өрнекеледі. Мұндағы N – бөлшек саны, NA – Авагадро тұрақтысы, N А = 6,02∙10 23 моль-1
#9 слайд
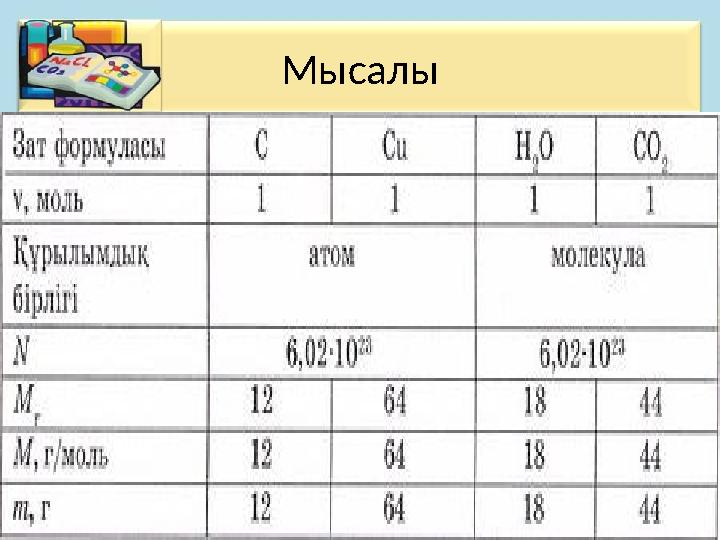
Мысалы
9 слайд
Мысалы
#10 слайд
ошибка
ошибка
ошибка молодец
молодец ошибка
ошибка
молодец
молодец
ошибка
ошибка
ошибка
молодец
ошибка
ошибка
ошибка
ошибка
ошибка
18
32
2
H
2
O
2
SO
3
H
2
O
S Ar O
2
H
2
SO
2
SO
3
S
O
2
Al
H
2
H
2
S Cr
Al S SO
2
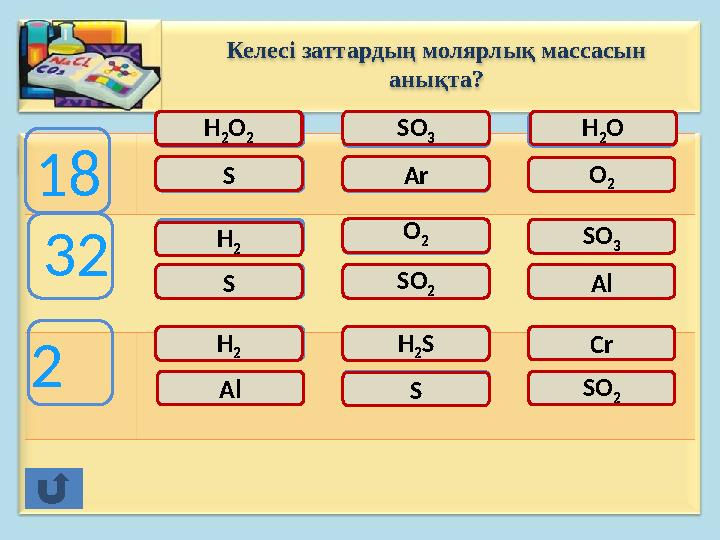
Келесі заттардың молярлық массасын
анықта?
10 слайд
ошибка ошибка ошибка молодец молодец ошибка ошибка молодец молодец ошибка ошибка ошибка молодец ошибка ошибка ошибка ошибка ошибка 18 32 2 H 2 O 2 SO 3 H 2 O S Ar O 2 H 2 SO 2 SO 3 S O 2 Al H 2 H 2 S Cr Al S SO 2 Келесі заттардың молярлық массасын анықта?

#11 слайд
Зат мөлшері ұғымын қолданып
есептер шығару
Зат мөлшері
M
m
n
Mnm
11 слайд
Зат мөлшері ұғымын қолданып есептер шығару Зат мөлшері M m n Mnm
#12 слайд
07.03.2025
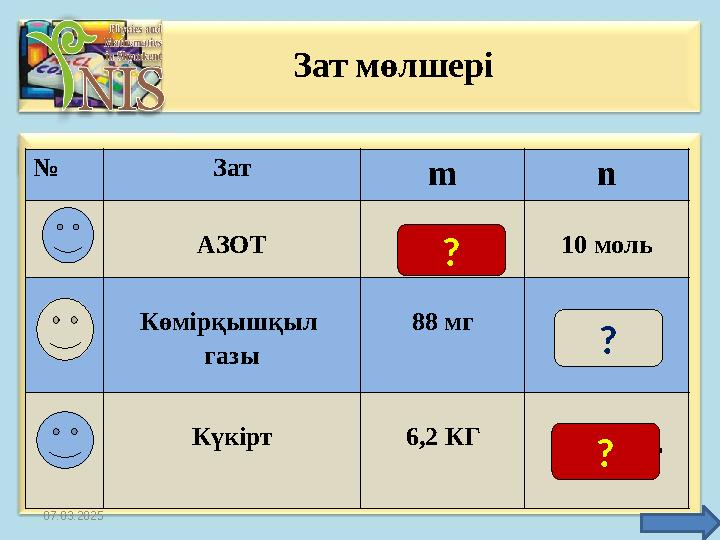
№ Зат m n
1
АЗОТ 28 г 10 моль
2
Көмірқышқыл
газы
88 мг 2 ммоль
3
Күкірт 6,2 КГ
0,2 кмоль
?
?
?
Зат мөлшері
12 слайд
07.03.2025 № Зат m n 1 АЗОТ 28 г 10 моль 2 Көмірқышқыл газы 88 мг 2 ммоль 3 Күкірт 6,2 КГ 0,2 кмоль ? ? ? Зат мөлшері

#13 слайд
Бер:
n(N
2
) = 10 моль
Табу керек:
m (N
2) - ?
Шешуі:
M (N
2)= 28 г/моль
m (N
2)=10 моль*28 г/моль
= 280 г
Жауабы: m (N
2
)= 280г
Зат мөлшері
Mnm
13 слайд
Бер: n(N 2 ) = 10 моль Табу керек: m (N 2) - ? Шешуі: M (N 2)= 28 г/моль m (N 2)=10 моль*28 г/моль = 280 г Жауабы: m (N 2 )= 280г Зат мөлшері Mnm
#14 слайд
Бер:
m(CO
2) = 88 мг
Табу керек:
n(CO
2) - ?
Шешуі:
M(CO
2
) = 44 мг/ммоль
Жауабы: n(CO
2
) = 2
ммоль
Зат мөлшері
M
m
n
ммоль
ммольмг
мг
COn 2
/44
88
)(
2
14 слайд
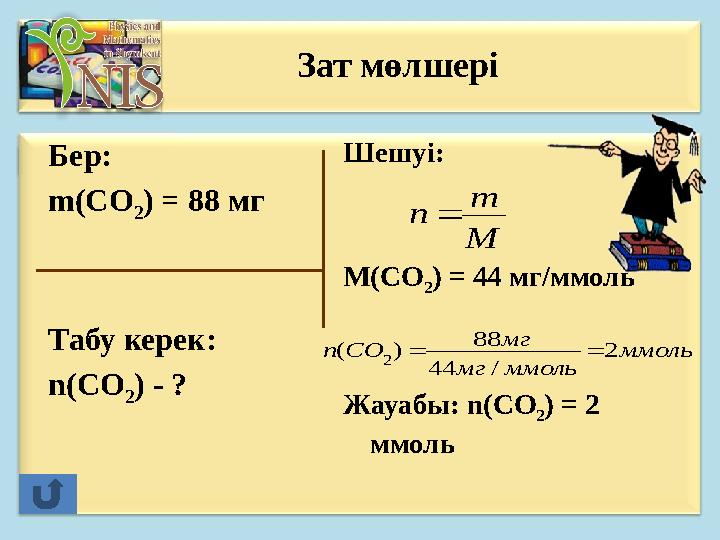
Бер: m(CO 2) = 88 мг Табу керек: n(CO 2) - ? Шешуі: M(CO 2 ) = 44 мг/ммоль Жауабы: n(CO 2 ) = 2 ммоль Зат мөлшері M m n ммоль ммольмг мг COn 2 /44 88 )( 2

#15 слайд
Бер:
m (S) = 6.2 кг
Табу керек:
n (S) - ?
Шешуі:
M(S) = 32 кг/кмоль
Жауабы: n (S) =0,2 кмоль
Зат мөлшері
M
m
n
кмоль
кмолькг
кг
Sn 2,0
/32
2.6
)(
15 слайд
Бер: m (S) = 6.2 кг Табу керек: n (S) - ? Шешуі: M(S) = 32 кг/кмоль Жауабы: n (S) =0,2 кмоль Зат мөлшері M m n кмоль кмолькг кг Sn 2,0 /32 2.6 )(

#16 слайд
Есептер шығару!
Тапсырма Берілген зат мөлшері бойынша массасын табыңдар
І топ
а)0,3 моль O2; ә) 0,5 мольН2О
б)10 моль NH3; в) 4 моль СаСO3
ІІ топ
а)0,3 моль N2; ә) 0,2 мольСuO
б)10 моль SO2; в) 0,5 моль H2SO4
ІІІ топ
а)0,5 моль О2; ә) 4 мольН2О
б)5 моль NH3; в) 3 моль СаСO3
16 слайд
Есептер шығару! Тапсырма Берілген зат мөлшері бойынша массасын табыңдар І топ а)0,3 моль O2; ә) 0,5 мольН2О б)10 моль NH3; в) 4 моль СаСO3 ІІ топ а)0,3 моль N2; ә) 0,2 мольСuO б)10 моль SO2; в) 0,5 моль H2SO4 ІІІ топ а)0,5 моль О2; ә) 4 мольН2О б)5 моль NH3; в) 3 моль СаСO3

#17 слайд
Тапсырма Салыстыру тапсырмасы
І топ
Массалары бірдей 200 г әктасы СаСO3 және күйдіргіш
натр NaOH берілген.Осылардың қайсысының зат мөлшері
көп екенін есептеңдер.
І топ
Массалары бірдей 800 г мыс тұзы СuSO4 және күйдіргіш
натр NaOH берілген.Осылардың қайсысының зат мөлшері
көп екенін есептеңдер.
ІІІ топ
Массалары бірдей 400 г әктасы СаСO3 және магний
оксиді MgO берілген.Осылардың қайсысының зат
мөлшері көп екенін есептеңдер.
17 слайд
Тапсырма Салыстыру тапсырмасы І топ Массалары бірдей 200 г әктасы СаСO3 және күйдіргіш натр NaOH берілген.Осылардың қайсысының зат мөлшері көп екенін есептеңдер. І топ Массалары бірдей 800 г мыс тұзы СuSO4 және күйдіргіш натр NaOH берілген.Осылардың қайсысының зат мөлшері көп екенін есептеңдер. ІІІ топ Массалары бірдей 400 г әктасы СаСO3 және магний оксиді MgO берілген.Осылардың қайсысының зат мөлшері көп екенін есептеңдер.

#18 слайд
Газдың молярлық көлемі :
Газдың мольдік көлемі –
берілген газ көлемінің оның
химиялық зат мөлшеріне
қатынасына тең шама
n
V
Vm
18 слайд
Газдың молярлық көлемі : Газдың мольдік көлемі – берілген газ көлемінің оның химиялық зат мөлшеріне қатынасына тең шама n V Vm

#19 слайд
Авогадро заңының
салдары:
Әртүрлі газдардың бірдей
молекулалар саны бірдей
қысымда және
температурада бірдей
көлемді алады. Қалыпты
жағдайда кез
келген газдың
мольдік көлемі:
./4,22
1
4,22
3
3
мольдм
моль
дм
n
V
Vm
19 слайд
Авогадро заңының салдары: Әртүрлі газдардың бірдей молекулалар саны бірдей қысымда және температурада бірдей көлемді алады. Қалыпты жағдайда кез келген газдың мольдік көлемі: ./4,22 1 4,22 3 3 мольдм моль дм n V Vm

#20 слайд
Деңгейлік тапсырма.
І-деңгей.
1) Молярлық масса деген не?
2). 3 моль, 6моль судың массасын тап.
ІІ-деңгей.
1. Егер заттың 2 молі 80 г, ал 4 молі 160г болса, белгісіз заттың
молярлық массасы қанша болатынын есепте.
2. Егер 1 моль затта молекула саны 6,02∙10
23
бар екенін біле отырып 1,5
моль Са; 3 моль АІ-де қанша молекула болатынын есепте.
ІІІ- деңгей
1.Атомсаны 12,04∙10
23
және 36,12∙10
23
болатын азот затының мөлшерін тап.
2. Массасы 476 г болатын натрий оксидінің зат мөлшерін тап.
20 слайд
Деңгейлік тапсырма. І-деңгей. 1) Молярлық масса деген не? 2). 3 моль, 6моль судың массасын тап. ІІ-деңгей. 1. Егер заттың 2 молі 80 г, ал 4 молі 160г болса, белгісіз заттың молярлық массасы қанша болатынын есепте. 2. Егер 1 моль затта молекула саны 6,02∙10 23 бар екенін біле отырып 1,5 моль Са; 3 моль АІ-де қанша молекула болатынын есепте. ІІІ- деңгей 1.Атомсаны 12,04∙10 23 және 36,12∙10 23 болатын азот затының мөлшерін тап. 2. Массасы 476 г болатын натрий оксидінің зат мөлшерін тап.

#21 слайд
Проблемалық жайт!
•Таразының бір табақшасына оқушы 5 моль
мыс оксиді СuO ұнтағынан және екінші
табақшасына кремний оксидінің SіO2
4 молін салды. Бұл кезде таразы тепе-
теңдікте бола ма?
• Егер тепе- теңдікте болмаса тепе- теңдікке
келтіру үшін оқушы не істеуі керек болады?
Жауаптарыңызды нақты фактілермен
дәлелдеңдер.
21 слайд
Проблемалық жайт! •Таразының бір табақшасына оқушы 5 моль мыс оксиді СuO ұнтағынан және екінші табақшасына кремний оксидінің SіO2 4 молін салды. Бұл кезде таразы тепе- теңдікте бола ма? • Егер тепе- теңдікте болмаса тепе- теңдікке келтіру үшін оқушы не істеуі керек болады? Жауаптарыңызды нақты фактілермен дәлелдеңдер.
#22 слайд
Өзіңді тексер
Тест
22 слайд
Өзіңді тексер Тест
#23 слайд
Ошибка
Ошибка
Ошибка
m=n×M
n=
МолодецОшибка
Молодец Ошибка
Ошибка
Ошибка
Ошибка
Молодец Ошибка
Зат
мөлшері
Масса
Молярлы
масса
Молекула
саны
Зат мөлшері
Молярлы
масса
Молекул
а саны
Масса
Молярлы
масса
Масса
Молекул
а саны
Зат мөлшері
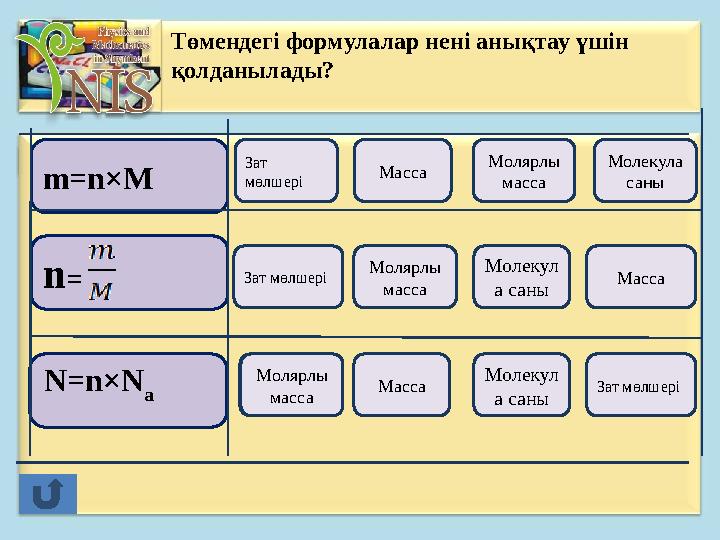
Төмендегі формулалар нені анықтау үшін
қолданылады?
N=n×N
а
23 слайд
Ошибка Ошибка Ошибка m=n×M n= МолодецОшибка Молодец Ошибка Ошибка Ошибка Ошибка Молодец Ошибка Зат мөлшері Масса Молярлы масса Молекула саны Зат мөлшері Молярлы масса Молекул а саны Масса Молярлы масса Масса Молекул а саны Зат мөлшері Төмендегі формулалар нені анықтау үшін қолданылады? N=n×N а

#24 слайд
Зат мөлшеріне
ұй жұмысы
1. Сұраққа жауап беріңіз:
Егер қант кесегінің біреуінің массасы 1,3г болса, қанттың
қанша молекуласы қант-рафинатының құрамында болады.
2. Шығармашылық тапсырма:
Зат мөлшері тақырыбына есептер құрастырып келу
Кроссворд құрастыру «Моль – зат мөлшері»
24 слайд
Зат мөлшеріне ұй жұмысы 1. Сұраққа жауап беріңіз: Егер қант кесегінің біреуінің массасы 1,3г болса, қанттың қанша молекуласы қант-рафинатының құрамында болады. 2. Шығармашылық тапсырма: Зат мөлшері тақырыбына есептер құрастырып келу Кроссворд құрастыру «Моль – зат мөлшері»
#25 слайд
Рефлексия
Түсінген жоқпын
Түсіндім бірақ
але толықтыру
керек
Бәрін түсіндім
25 слайд
Рефлексия Түсінген жоқпын Түсіндім бірақ але толықтыру керек Бәрін түсіндім

шағым қалдыра аласыз
















