
МКҚК Орал «Сервис» технологиялық колледжі
Б е к і т е м і
н___________
Басшының оқу ісі жөніндегі
орынбасары Н.А.Мамбетова

Ашық сабақ
17 (17А) топ элементтері
Дайындаған: Муратова Ж.Р.
2021-2022
1.Жалпы мәліметтер
Курс, оқу жылы, топ __І курс, 2021-2022оқу жылы 15топ
Сабақ типі : Аралас сабақ
2. Мақсаты, міндеттер:
1.
Топтағы
галогендердің қасиеттерінің өзгеру заңдылықтарын
білу.
3. Оқу-жаттығу процесінде
білім алушылар меңгеретін күтілетін нәтижелер және (немесе) кәсіби
дағдылар тізбесі
1) Галогендерге периодтық жүйеде орналасуы бойынша сипаттайды;
2) Галогендердің тотығу-тотықсыздану реакция теңдеулерін, электрөткізгіштігін анықтайды; 3)Галогендерді физикалық қасиеттері мен химиялық қасиеттері бойынша сипаттайды;;
4) Топтағы галогендердің қасиеттерінің өзгеру заңдылықтарын түсіндіреді;
5)Хлорид-, бромид-, йодид-, иондарға сапалы реакциялар жүргізеді;
6) Йодтың адам ағзасындағы биологиялық рөлін, йод тапшылығына байланысты аурулардың пайда болуын түсіндіреді.
4. Қажетті ресурстар: постер, стикер, түрлі-түсті фломастерлер, интербелсенді тақта,түрлі-түсті қағаз
5. Сабақтың барысы
1.Сәлемдесу, студенттерді түгендеу, топқа бөлу 5 мин
2. Үй тапсырмасын тексеру 10 мин
(өткен тақырып бойынша сұрақтар)
3. Жаңа сабақ . Видеокөрсетілім. Видеокөрсетілім бойынша сұрақтар 15 мин
Галогендер VIIA топшада орналасқан, олар: фтор F, хлор Сl, бром Вr, йод I, астат At. Астат - радиобелсенді элемент.[
Табиғатта таралуы
Хлор табиғатта активті элемент болғандықтан тек қосылыстар күйінде кездеседі. Негізінен сілтілік және сілтілік-жер (II) металдарының хлоридтері күйінде; олар карналлит KC1*MgCl2*6Н2О, сильвинит NaCl*KCl, бишофит MgCl2*6Н2О, галит тас тұзы NaCl, т.б.
Атом құрылысы
Хлор III периодтың, VII топтың негізгі топшасының элементі, 35,417С1 ядросындағы протон сандары 17, яғни ядро заряды +17, электрондар саны 17, нейтрондар саны 18. Хлор атомының электрондық формуласы: ls22s22p63s23p5, валенттілік электрондары 3s23p53d0.
Алынуы
Өндірісте хлорды ас тұзының балқымасын электролиздеу арқылы алатындығын айтқанбыз. Осы әдіспен жұмыс істейтін зауыт Павлодарда орналасқан.
Зертханада концентірлі тұз қышкылына марганец диоксидін (МnО2) қосып, тотықтыру арқылы алады.
Молекула құрылысы
Хлор молекуласы да басқа галогендердікі сияқты екі атомды. С12 молекуласы хлордың 3р-деңгейшесінде орналасқан дара электрон бұлттарының қабысуынан болады, арасына бір байланыс түзіледі.
Физикалық қасиеттері
Хлор - сарғыш-жасыл түсті тұншықтырғыш улы газ. Онымен тек тартпа шкафтың ішінде жұмыс жасау керек. Хлор ауадан 2,5 еседей ауыр. (Daya = М(С12)/М(ауа) = 71/29 = 2,45), сондықтан оны ауаны ығыстыру арқылы жинайды, ыдыстың аузын жоғары қаратып ұстауға да болады. Суды ығыстыру арқылы жинауға болмайды, себебі хлор сумен химиялық әрекеттесіп, хлор «суын» түзеді.
4.17(7А) топ элементтерінің құрамы мен құрылысын анықтау 10 мин
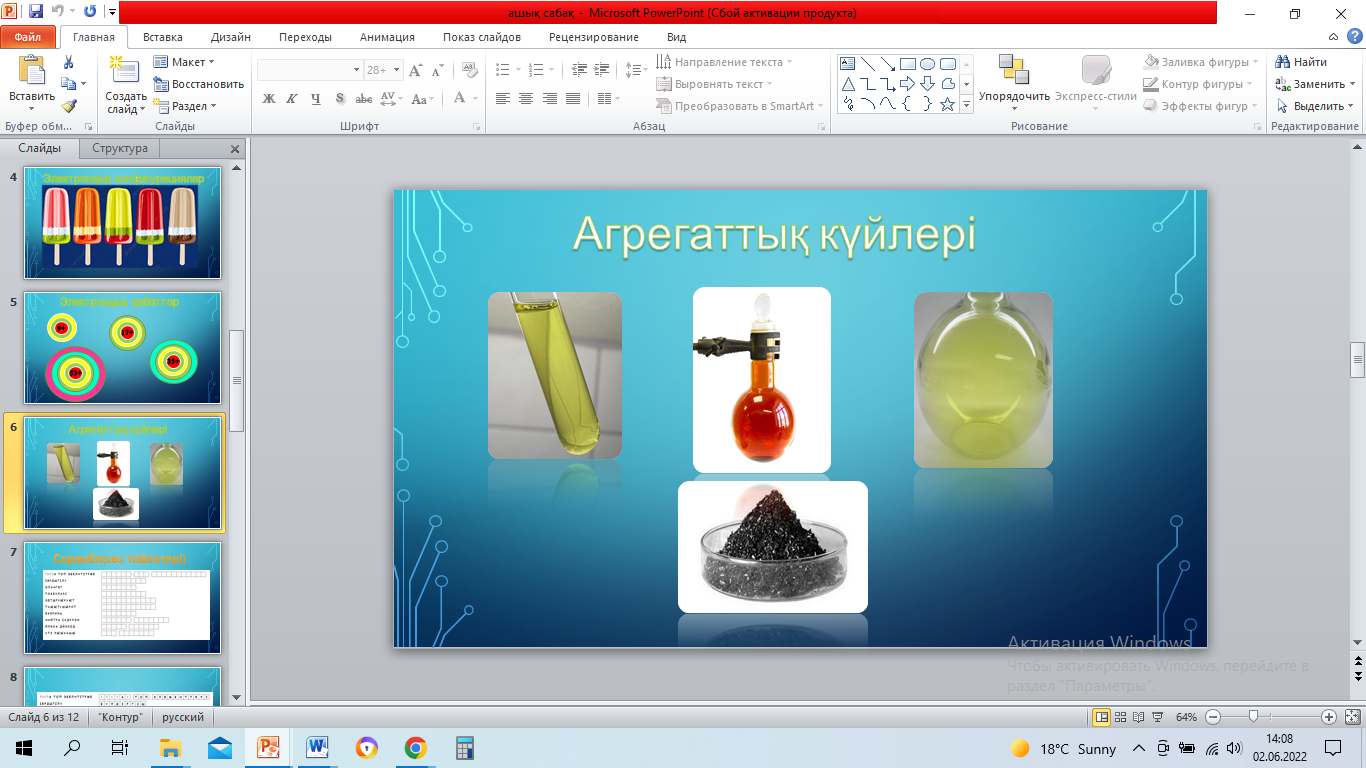
Дискриптор:
-
Атомның құрылысын(протон,нейтрон,электрон) жазады
-
Электрондық конфигурациясы жазады
-
Электрондық қабаттарға электрондарды орналастырады
-
Түсі мен агрегаттық күйі бойынша
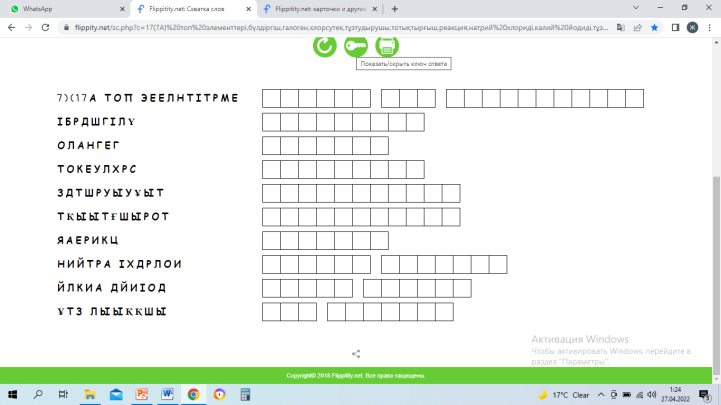
5.Скрамбл (сөз тізбегін құру) 5 мин
6.Сен білесің бе? Қызықты мәліметтер. Постер қорғау 20 мин
7.Йодпен тәжірибе жасау 10 мин
Бірнеше тамшы йод тұндырмасына аздап су қосыңдар және осы ерітінді көмегімен тағамдардың құрамында крахмалдың бар-жоғын анықтаңдар. Ол үшін картоп, сәбіз кесінділеріне, ұнға, ақ және қара нанға, бұршаққа, күндіз үзіліп алынған жасыл жапыраққа йод ерітіндісін тамызып көріңдер. Бақылау қорытындыларын жазыңдар.
8. Flippity сайтында тест жұмысы 5 мин
9.Кері байланыс 5 мин
10Қорытындылау. Бағалау. Үйге тапсырма беру 5 мин
6. Сабақ бойынша рефлексия
Сабақ мақсаттары/ оқу мақсаттары дұрыс қойылғанба? Студенттердің барлығы ОМ қолжеткізді ме?
Жеткізбесе, неліктен?
Сабақта саралау дұрыс жүргізілдіме?
Сабақтың уақыттық кезеңдері сақталдыма?
Сабақ жоспарынан қандай ауытқулар болды, неліктен?
7. Үй тапсырмасы: §54. 16 бет (1-10)
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Ашық сабақ "17 (7А) топ элементтері"
МКҚК Орал «Сервис» технологиялық колледжі
Б е к і т е м і
н___________
Басшының оқу ісі жөніндегі
орынбасары Н.А.Мамбетова

Ашық сабақ
17 (17А) топ элементтері
Дайындаған: Муратова Ж.Р.
2021-2022
1.Жалпы мәліметтер
Курс, оқу жылы, топ __І курс, 2021-2022оқу жылы 15топ
Сабақ типі : Аралас сабақ
2. Мақсаты, міндеттер:
1.
Топтағы
галогендердің қасиеттерінің өзгеру заңдылықтарын
білу.
3. Оқу-жаттығу процесінде
білім алушылар меңгеретін күтілетін нәтижелер және (немесе) кәсіби
дағдылар тізбесі
1) Галогендерге периодтық жүйеде орналасуы бойынша сипаттайды;
2) Галогендердің тотығу-тотықсыздану реакция теңдеулерін, электрөткізгіштігін анықтайды; 3)Галогендерді физикалық қасиеттері мен химиялық қасиеттері бойынша сипаттайды;;
4) Топтағы галогендердің қасиеттерінің өзгеру заңдылықтарын түсіндіреді;
5)Хлорид-, бромид-, йодид-, иондарға сапалы реакциялар жүргізеді;
6) Йодтың адам ағзасындағы биологиялық рөлін, йод тапшылығына байланысты аурулардың пайда болуын түсіндіреді.
4. Қажетті ресурстар: постер, стикер, түрлі-түсті фломастерлер, интербелсенді тақта,түрлі-түсті қағаз
5. Сабақтың барысы
1.Сәлемдесу, студенттерді түгендеу, топқа бөлу 5 мин
2. Үй тапсырмасын тексеру 10 мин
(өткен тақырып бойынша сұрақтар)
3. Жаңа сабақ . Видеокөрсетілім. Видеокөрсетілім бойынша сұрақтар 15 мин
Галогендер VIIA топшада орналасқан, олар: фтор F, хлор Сl, бром Вr, йод I, астат At. Астат - радиобелсенді элемент.[
Табиғатта таралуы
Хлор табиғатта активті элемент болғандықтан тек қосылыстар күйінде кездеседі. Негізінен сілтілік және сілтілік-жер (II) металдарының хлоридтері күйінде; олар карналлит KC1*MgCl2*6Н2О, сильвинит NaCl*KCl, бишофит MgCl2*6Н2О, галит тас тұзы NaCl, т.б.
Атом құрылысы
Хлор III периодтың, VII топтың негізгі топшасының элементі, 35,417С1 ядросындағы протон сандары 17, яғни ядро заряды +17, электрондар саны 17, нейтрондар саны 18. Хлор атомының электрондық формуласы: ls22s22p63s23p5, валенттілік электрондары 3s23p53d0.
Алынуы
Өндірісте хлорды ас тұзының балқымасын электролиздеу арқылы алатындығын айтқанбыз. Осы әдіспен жұмыс істейтін зауыт Павлодарда орналасқан.
Зертханада концентірлі тұз қышкылына марганец диоксидін (МnО2) қосып, тотықтыру арқылы алады.
Молекула құрылысы
Хлор молекуласы да басқа галогендердікі сияқты екі атомды. С12 молекуласы хлордың 3р-деңгейшесінде орналасқан дара электрон бұлттарының қабысуынан болады, арасына бір байланыс түзіледі.
Физикалық қасиеттері
Хлор - сарғыш-жасыл түсті тұншықтырғыш улы газ. Онымен тек тартпа шкафтың ішінде жұмыс жасау керек. Хлор ауадан 2,5 еседей ауыр. (Daya = М(С12)/М(ауа) = 71/29 = 2,45), сондықтан оны ауаны ығыстыру арқылы жинайды, ыдыстың аузын жоғары қаратып ұстауға да болады. Суды ығыстыру арқылы жинауға болмайды, себебі хлор сумен химиялық әрекеттесіп, хлор «суын» түзеді.
4.17(7А) топ элементтерінің құрамы мен құрылысын анықтау 10 мин

Дискриптор:
-
Атомның құрылысын(протон,нейтрон,электрон) жазады
-
Электрондық конфигурациясы жазады
-
Электрондық қабаттарға электрондарды орналастырады
-
Түсі мен агрегаттық күйі бойынша
5.Скрамбл (сөз тізбегін құру) 5 мин

6.Сен білесің бе? Қызықты мәліметтер. Постер қорғау 20 мин

7.Йодпен тәжірибе жасау 10 мин
Бірнеше тамшы йод тұндырмасына аздап су қосыңдар және осы ерітінді көмегімен тағамдардың құрамында крахмалдың бар-жоғын анықтаңдар. Ол үшін картоп, сәбіз кесінділеріне, ұнға, ақ және қара нанға, бұршаққа, күндіз үзіліп алынған жасыл жапыраққа йод ерітіндісін тамызып көріңдер. Бақылау қорытындыларын жазыңдар.
8. Flippity сайтында тест жұмысы 5 мин
9.Кері байланыс 5 мин
10Қорытындылау. Бағалау. Үйге тапсырма беру 5 мин
6. Сабақ бойынша рефлексия
Сабақ мақсаттары/ оқу мақсаттары дұрыс қойылғанба? Студенттердің барлығы ОМ қолжеткізді ме?
Жеткізбесе, неліктен?
Сабақта саралау дұрыс жүргізілдіме?
Сабақтың уақыттық кезеңдері сақталдыма?
Сабақ жоспарынан қандай ауытқулар болды, неліктен?
7. Үй тапсырмасы: §54. 16 бет (1-10)

шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
