
АЛЬДЕГИДТЕР ЖӘНЕ КЕТОНДАР
Оксоқосылыстар деп – молекуласында карбонил тобы бар көмірсутектердің туындысын айтамыз:
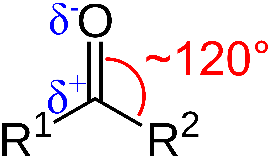
Карбонил тобындағы
қос байланыстың электрондық құрылысы бір
 бір
бір  байланыстарымен
сипатталады және әрдайым осы соңғы байланыстың электрондық бұлты
жазықтықта орналасқан перпендикуляр байланыста берілген көміртегі
атомының
байланыстарымен
сипатталады және әрдайым осы соңғы байланыстың электрондық бұлты
жазықтықта орналасқан перпендикуляр байланыста берілген көміртегі
атомының  байланысы
орналасқан.
байланысы
орналасқан.
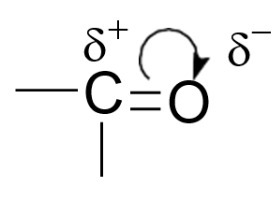
Карбонил тобындағ қос байланыс қарастырылған этиленді көмірсутектің қос байланысынан ерекшеленеді. Байланыстың ерекшелігі карбонил тобының қос байланысы күшті тартқыш электронды оттегі атомының электр терістігінен көміртегі атомын қосып алады, сондықтан бұл байланыс полярланған.
-
Номенклатурасы
Альдегидтер – су атомымен және көміртек радикалымен байланысқан солекуласында карбонил тобы бар органикалық қосылыстарды айтады (RCHO жалпы формуласының қосылыстары), кетондар – екі көмірсутектің радикалымен байланысқан карбонил тобы бар органикалық қосылыстарды айтамыз (RR’CO жалпы формуласының қосылыстары. R және R' топтары алифатты немесе хош иісті болуы мүмкін):

Альдегидтерде де, кетондарда да C=O карбонил тобы бар және олар көбінесе карбонил қосылыстары ретінде қарастырылады. Карбонил тобының болуы альдегидтер мен кетондардың химиялық қасиеттерін анықтайды. Альдегидтер мен кетондардың көптеген қасиеттері ұқсас. Алайда, альдегидтердегі карбонил тобының жанында сутегі атомы, ал кетондардың карбонил тобының жанында екі органикалық радикал бар. Құрылымдағы бұл айырмашылық қасиеттердегі айырмашылықты анықтайды: А) альдегидтер оңай тотығады, ал кетондар қиын тотығады; б) альдегидтер нуклеофильді қосылу реакцияларындағы кетондарға қарағанда белсендірек – карбонил қосылыстарына тән реакция.
Көптеген альдегидтерде қышқыл сөзін альдегид сөзімен алмастыру арқылы тиісті карбон қышқылдарының атауларынан түзілетін тривиальды атаулар бар.
IUPAC номенклатурасы бойынша альдегид атаулары келесідей қалыптасады:
1. Негіз ретінде SNO тобын қамтитын ең ұзын тізбек алынады, оны тиісті алканның атауына –аль аяқталуын қосу арқылы атайды.
2. Алмастырғыштың орны сандармен белгіленеді, карбонил көміртегі бірінші болып саналады. Екінші көміртегі атомындағы көміртек атомы көміртегі диоксиді атомына сәйкес келеді:

Ең қарапайым алифатты кетонның тривиальды атауы бар ацетон. Көптеген басқа алифатты кетондар үшін бұл атау әдетте карбонил тобының көміртегімен байланысты екі радикалдың атауларынан тұрады, оларға соңы қосылады кетон. Карбонил тобы бензол сақинасымен байланысқан кетон атауларының соңы фенон болады.
IUPAC номенклатурасына сәйкес:
1. Негіз ретінде карбонил тобы бар ең ұзын тізбек алынады, оны -он соңын қосу арқылы атайды тиісті алканның атауына.
2. Әр түрлі топтардың позициясы карбонил тобы ең кіші Нөмірді алатындай етіп сандармен белгіленеді:


-
Физикалық қасиеттері
Карбонил тобы – полярлық топ, сондықтан альдегидтер мен кетондардың қайнау температурасы бірдей молекулалық салмағы бар сәйкес көмірсутектерге қарағанда жоғары. Алайда, альдегидтер мен кетондар күшті молекулааралық түзе алмайтындығына байланысты сутегі байланыстары, олардың қайнау температурасы тиісті спирттерге қарағанда едәуір төмен.
Альдегидтер мен кетондардың карбонил тобы су молекулаларымен күшті сутегі байланыстарын құра алатындықтан, төменгі альдегидтер мен кетондар сумен кез келген пропорцияда араласады.
-
Алу жолдары
Альдегидтер мен кетондарды алу тәсілдері айтарлықтай өзгереді, сондықтан біз оларды бөлек қарастырамыз. Альдегидтерді алудың негізгі әдістері:
-
Бастапқы спирттердің тотығуы (дегидрлеу):

-
Алкендердің гидроформилденуі:

-
Метилбензолдардың тотығуы:

-
Карбон қышқылының хлорангидридтерін тотықсыздандыру:

Кетондар әдетте келесі әдістердің бірімен алынады:
-
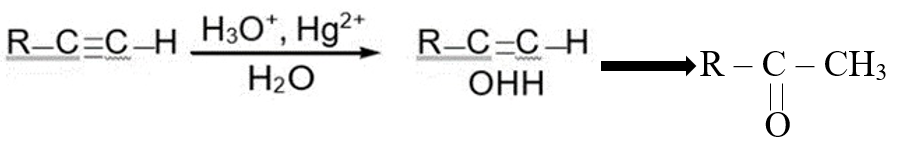
Алкиндердің гидратациясы:
-
Екіншілік спирттердің тотығуы:

-
Фридель-Крафтс бойынша ацилирлеу:

-
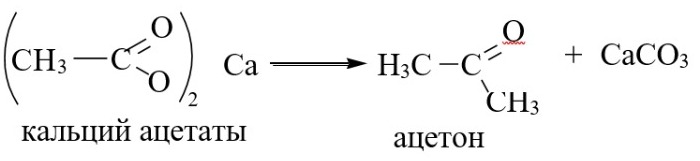
Карбон қышқылы тұздарының пиролизі:
-
Дигалогеналкандердің гидролизі:

-
Ацетиленді н/е гомологтарын Кучеров реакциясының жағдайларында сыландырса да өздеріне сай сірке альдегиді н/е кетондар түзіледі:
HC  CH
+
H2O
CH
+
H2O
 CH3
-CHO
CH3
-CHO
R![]()
![]() –
C
–
C  CH +
H2O
CH +
H2O
 R – C –
CH3
R – C –
CH3
O
1.3.1. Алкендердің гидроформилденуі. Оксосинтез
Өнеркәсіпте альдегидтер СО және Н2 (синтез-газ) қоспасын тікелей қосу арқылы алынадыолефиндерге 100-200оС кезінде 100-200 атм. қысыммен – Кобальт HCo(CO)4 немесе никель катализаторларының қатысуымен. Бұл бастапқы олефинге қарағанда бір көміртегі атомы көп болатын қалыпты және тармақталған құрылымның альдегидтерін шығарады:

Егер реакция жоғары температурада (185оС) жүргізілсе, онда реакцияның негізгі өнімдері тиісті спирттер болады:

1.3.2. Карбон қышқылы тұздарының пиролизі
Карбон қышқылдарының кальций немесе барий тұздарын "құрғақ айдау" кетондарды өндірудің ескі және жалпы әдісі болып табылады. Бір негізді тұздар ашық тізбекті кетондарды, ал екі негізді тұздар циклдік кетондарды шығарады. Түзілген кетон молекуласында бастапқы тұз молекуласынан бір көміртек атомы аз:

Реакцияны 400–500оС металл оксидтерінің қатысында жүреді. (ThO2, MnO2, CaO, ZnO).
1.3.3. Дигалоалкандардың гидролизі
Сумен әрекеттескенде (гидролиз реакциясы) құрамында бір көміртек атомында екі галоген атомы бар R2CHHal2 дигалалкандары (геминальды дигалалкандар деп аталады) қышқылдар немесе негіздер болған кезде альдегидтер немесе кетондар оңай алынады. Реакциялар R2СН(OH)2 тұрақсыз геминальды спирттердің аралық түзілуі мен ыдырауы арқылы өтеді. Егер екі галоген де соңғы көміртек атомдарының бірінде болса, онда альдегидтер алынады, ал егер екі галоген де орташа көміртек атомдарының бірінде болса, онда кетондар алынады. Мысалы:
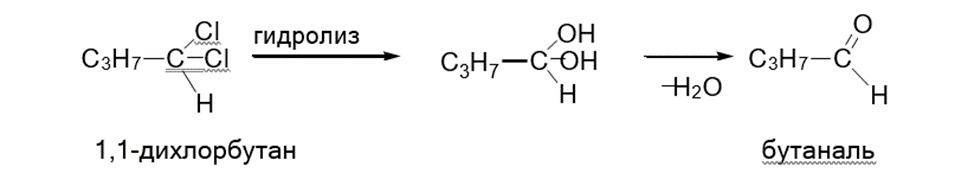

![]()
О
-
Химиялық қасиеттері
Альдегидтер мен кетондардың химиялық қасиеттері карбонил тобының болуымен анықталады. Бұл топ, біріншіден, нуклеофильді шабуылдың орны, екіншіден, байланысқан сутегі атомдарының қышқылдығын арттырады
көміртек атомымен.
Карбонил тобында көміртек-оттегі қос байланысы бар; жылжымалы диоксид электрондары оттегіге қатты тартылғандықтан, карбонил тобының көміртегі Электрон тапшылығы орталығы, ал карбонил тобының оттегі Электроны артық:
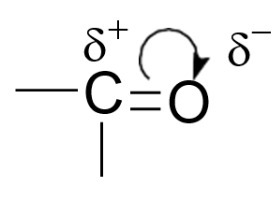
Мұндай топқа қандай реактивтер шабуыл жасайды? Бұл реакциялардағы ең маңызды кезең Электрон тапшылығы карбонил көміртегімен байланыс түзетіндіктен, карбонил тобы Электрон артық нуклеофильді реагенттермен әрекеттесуге бейім. Альдегидтер мен кетондардың типтік реакциялары АN нуклеофильді қосылу реакциялары болады.
Альдегидтер кетондарға қарағанда нуклеофильді қосылу (AN) реакциясына оңай түседі. Реактивтіліктің бұл айырмашылығы реакцияның аралық күйінің сипатына сәйкес келеді және электронды және кеңістіктік факторлардың бірлескен әсерімен түсіндіріледі. Кетонда екінші алкил немесе арил тобы, ал альдегидтерде сутегі атомы бар. Екінші алкил немесе арил тобы альдегидтегі сутегі атомынан үлкен, сондықтан ол өтпелі күйдегі кеңістіктік қиындықтардың көбеюіне кедергі келтіреді. Алкил тобы электрондарды береді және осылайша оттегідегі теріс зарядты күшейту арқылы өтпелі күйді тұрақтандырады. Электронды тартатын индуктивті әсері бар арил тобы өтпелі күйді тұрақтандырады және осылайша реакцияны тездетеді деп күтуге болады, алайда, бұл әсер резонанс салдарынан бастапқы кетонды одан әрі тұрақтандырады және нәтижесінде қарастырылып отырған реакцияда кетонды дезактивациялайды:

-
Тотығу:
Барлық органикалық қосылыстардың ішінде альдегидтер оңай тотығады. Олар карбон қышқылдарына перманганат немесе калий бихроматы сияқты реагенттердің әсерінен ғана емес, күміс ионы сияқты әлсіз тотықтырғыштардың әсерінен де айналады. Күміс ионының тотығуы сілтілі ортаны қажет етеді, ал ерімейтін күміс оксидінің тұнбасын болдырмау үшін күрделі түзуші реагент – аммиак қосылады.
Толленс реактивінде күрделі байланысқан күміс ионы Ag(NH3)2+. Альдегид тотыққан кезде күміс ионы бос күміске дейін азаяды (қолайлы жағдайда ол айна түрінде шығарылады).

Кетондар күміс иондарымен тотықпайды!
Бұл реакция негізінен альдегидтерді анықтау үшін және әсіресе оларды кетондардан ажырату үшін қолданылады.
Кетондардың тотығуы көміртек – көміртек байланысының үзілуін қажет етеді, сондықтан тек қатаң жағдайларда болады (ерекшелік-галоформ реакциясы). Реакция синтезге сирек қызығушылық тудырады: көптеген кетондар карбонил тобының кез келген жағынан ыдырап, қышқыл қоспасының пайда болуына әкелуі мүмкін.
-
альдегидтер:

-
метилкетондар:

-
Тотықсыздану:
Альдегидтер бастапқы спирттерге, ал кетондар каталитикалық гидрлеу арқылы немесе LiAlH4 литий алюминий гидриді немесе NaBH4 натрий борогидриді сияқты тотықсыздандырғыш реагенттерді қолдану арқылы қайталама спирттерге азаяды:

-
спирт арқылы тотықсыздану:

-
көміртек арқылы тотықсыздану:

-
Гриньяр реактивінің қосылуы:

-
HCN қосылуы:
Гидроциан қышқылының альдегидтерге және кетондардың көпшілігіне қосылуы циангидриндердің пайда болуына әкеледі. Кеңістіктегі қиын кетондар бұл реакцияға түспейді.
Гидроциан қышқылының өзі өте баяу қосылады, өйткені HCN әлсіз нуклеофил болып табылады. HCN-ден цианид анионын (күшті нуклеофил) тудыруы мүмкін калий цианидін немесе басқа негізді қосу қосылу реакциясының жылдамдығын айтарлықтай арттырады:

-
Натрий бисульфитіне қосылуы:
Натрий бисульфиті альдегидтерге және көптеген кетондарға (әсіресе метилкетондарға) қосылыс өнімін қалыптастыру үшін қосылады:

Құрамында көлемді алмастырғыштар бар кетондар кеңістіктегі қиындықтарға байланысты бұл реакцияға түспейді.
Бисульфиті бар қоспалар әдетте карбонилді қосылыстарды карбонил емес қосылыстардан бөлу үшін алынады. Карбонилді қосылысты оны бисульфит туындысына айналдыру арқылы тазартуға болады, содан кейін кристалды қоспаны карбонил емес қоспалардан бөліп, карбонилді қосылысты қалпына келтіруге болады.
-
Аммиак туындыларымен қосылуы:
Аммиакпен байланысты кейбір қосылыстар карбонил тобына қосылып, туындылар түзеді, оларды альдегидтер мен кетондарды анықтау үшін қолдануға болады, өйткені оксимдер, гидразондар, фенилгидразондар, семикарбазондар – тән балқу температурасы бар қатты кристалды заттар. Бұл туындыларда бастапқы қосындыдан су молекуласын жою нәтижесінде пайда болатын көміртек–азот қос байланысы бар.


-
Фосфор илидтерінің қосылуы. Виттиг Реакциясы:
Альдегидтер мен кетондар фосфор илидтерімен әрекеттесіп, алкендер мен трифенилфосфин оксидін береді. Бұл реакция Виттиг реакциясы деп аталады және алкендерді алу үшін кеңінен қолданылады:

-
Спирттермен қосылуы:
Жүктеу
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Бейорганикалық, коллоидты және физикалық химия
Бейорганикалық, коллоидты және физикалық химия
АЛЬДЕГИДТЕР ЖӘНЕ КЕТОНДАР
Оксоқосылыстар деп – молекуласында карбонил тобы бар көмірсутектердің туындысын айтамыз:
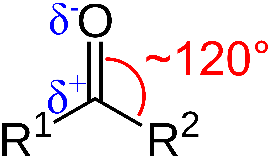
Карбонил тобындағы
қос байланыстың электрондық құрылысы бір
 бір
бір  байланыстарымен
сипатталады және әрдайым осы соңғы байланыстың электрондық бұлты
жазықтықта орналасқан перпендикуляр байланыста берілген көміртегі
атомының
байланыстарымен
сипатталады және әрдайым осы соңғы байланыстың электрондық бұлты
жазықтықта орналасқан перпендикуляр байланыста берілген көміртегі
атомының  байланысы
орналасқан.
байланысы
орналасқан.
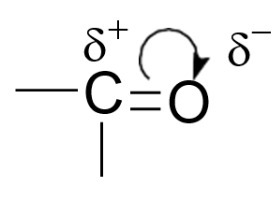
Карбонил тобындағ қос байланыс қарастырылған этиленді көмірсутектің қос байланысынан ерекшеленеді. Байланыстың ерекшелігі карбонил тобының қос байланысы күшті тартқыш электронды оттегі атомының электр терістігінен көміртегі атомын қосып алады, сондықтан бұл байланыс полярланған.
-
Номенклатурасы
Альдегидтер – су атомымен және көміртек радикалымен байланысқан солекуласында карбонил тобы бар органикалық қосылыстарды айтады (RCHO жалпы формуласының қосылыстары), кетондар – екі көмірсутектің радикалымен байланысқан карбонил тобы бар органикалық қосылыстарды айтамыз (RR’CO жалпы формуласының қосылыстары. R және R' топтары алифатты немесе хош иісті болуы мүмкін):

Альдегидтерде де, кетондарда да C=O карбонил тобы бар және олар көбінесе карбонил қосылыстары ретінде қарастырылады. Карбонил тобының болуы альдегидтер мен кетондардың химиялық қасиеттерін анықтайды. Альдегидтер мен кетондардың көптеген қасиеттері ұқсас. Алайда, альдегидтердегі карбонил тобының жанында сутегі атомы, ал кетондардың карбонил тобының жанында екі органикалық радикал бар. Құрылымдағы бұл айырмашылық қасиеттердегі айырмашылықты анықтайды: А) альдегидтер оңай тотығады, ал кетондар қиын тотығады; б) альдегидтер нуклеофильді қосылу реакцияларындағы кетондарға қарағанда белсендірек – карбонил қосылыстарына тән реакция.
Көптеген альдегидтерде қышқыл сөзін альдегид сөзімен алмастыру арқылы тиісті карбон қышқылдарының атауларынан түзілетін тривиальды атаулар бар.
IUPAC номенклатурасы бойынша альдегид атаулары келесідей қалыптасады:
1. Негіз ретінде SNO тобын қамтитын ең ұзын тізбек алынады, оны тиісті алканның атауына –аль аяқталуын қосу арқылы атайды.
2. Алмастырғыштың орны сандармен белгіленеді, карбонил көміртегі бірінші болып саналады. Екінші көміртегі атомындағы көміртек атомы көміртегі диоксиді атомына сәйкес келеді:

Ең қарапайым алифатты кетонның тривиальды атауы бар ацетон. Көптеген басқа алифатты кетондар үшін бұл атау әдетте карбонил тобының көміртегімен байланысты екі радикалдың атауларынан тұрады, оларға соңы қосылады кетон. Карбонил тобы бензол сақинасымен байланысқан кетон атауларының соңы фенон болады.
IUPAC номенклатурасына сәйкес:
1. Негіз ретінде карбонил тобы бар ең ұзын тізбек алынады, оны -он соңын қосу арқылы атайды тиісті алканның атауына.
2. Әр түрлі топтардың позициясы карбонил тобы ең кіші Нөмірді алатындай етіп сандармен белгіленеді:


-
Физикалық қасиеттері
Карбонил тобы – полярлық топ, сондықтан альдегидтер мен кетондардың қайнау температурасы бірдей молекулалық салмағы бар сәйкес көмірсутектерге қарағанда жоғары. Алайда, альдегидтер мен кетондар күшті молекулааралық түзе алмайтындығына байланысты сутегі байланыстары, олардың қайнау температурасы тиісті спирттерге қарағанда едәуір төмен.
Альдегидтер мен кетондардың карбонил тобы су молекулаларымен күшті сутегі байланыстарын құра алатындықтан, төменгі альдегидтер мен кетондар сумен кез келген пропорцияда араласады.
-
Алу жолдары
Альдегидтер мен кетондарды алу тәсілдері айтарлықтай өзгереді, сондықтан біз оларды бөлек қарастырамыз. Альдегидтерді алудың негізгі әдістері:
-
Бастапқы спирттердің тотығуы (дегидрлеу):

-
Алкендердің гидроформилденуі:

-
Метилбензолдардың тотығуы:

-
Карбон қышқылының хлорангидридтерін тотықсыздандыру:

Кетондар әдетте келесі әдістердің бірімен алынады:
-
Алкиндердің гидратациясы:

-
Екіншілік спирттердің тотығуы:

-
Фридель-Крафтс бойынша ацилирлеу:

-
Карбон қышқылы тұздарының пиролизі:

-
Дигалогеналкандердің гидролизі:

-
Ацетиленді н/е гомологтарын Кучеров реакциясының жағдайларында сыландырса да өздеріне сай сірке альдегиді н/е кетондар түзіледі:
HC  CH
+
H2O
CH
+
H2O
 CH3
-CHO
CH3
-CHO
R![]()
![]() –
C
–
C  CH +
H2O
CH +
H2O
 R – C –
CH3
R – C –
CH3
O
1.3.1. Алкендердің гидроформилденуі. Оксосинтез
Өнеркәсіпте альдегидтер СО және Н2 (синтез-газ) қоспасын тікелей қосу арқылы алынадыолефиндерге 100-200оС кезінде 100-200 атм. қысыммен – Кобальт HCo(CO)4 немесе никель катализаторларының қатысуымен. Бұл бастапқы олефинге қарағанда бір көміртегі атомы көп болатын қалыпты және тармақталған құрылымның альдегидтерін шығарады:

Егер реакция жоғары температурада (185оС) жүргізілсе, онда реакцияның негізгі өнімдері тиісті спирттер болады:

1.3.2. Карбон қышқылы тұздарының пиролизі
Карбон қышқылдарының кальций немесе барий тұздарын "құрғақ айдау" кетондарды өндірудің ескі және жалпы әдісі болып табылады. Бір негізді тұздар ашық тізбекті кетондарды, ал екі негізді тұздар циклдік кетондарды шығарады. Түзілген кетон молекуласында бастапқы тұз молекуласынан бір көміртек атомы аз:

Реакцияны 400–500оС металл оксидтерінің қатысында жүреді. (ThO2, MnO2, CaO, ZnO).
1.3.3. Дигалоалкандардың гидролизі
Сумен әрекеттескенде (гидролиз реакциясы) құрамында бір көміртек атомында екі галоген атомы бар R2CHHal2 дигалалкандары (геминальды дигалалкандар деп аталады) қышқылдар немесе негіздер болған кезде альдегидтер немесе кетондар оңай алынады. Реакциялар R2СН(OH)2 тұрақсыз геминальды спирттердің аралық түзілуі мен ыдырауы арқылы өтеді. Егер екі галоген де соңғы көміртек атомдарының бірінде болса, онда альдегидтер алынады, ал егер екі галоген де орташа көміртек атомдарының бірінде болса, онда кетондар алынады. Мысалы:


![]()
О
-
Химиялық қасиеттері
Альдегидтер мен кетондардың химиялық қасиеттері карбонил тобының болуымен анықталады. Бұл топ, біріншіден, нуклеофильді шабуылдың орны, екіншіден, байланысқан сутегі атомдарының қышқылдығын арттырады
көміртек атомымен.
Карбонил тобында көміртек-оттегі қос байланысы бар; жылжымалы диоксид электрондары оттегіге қатты тартылғандықтан, карбонил тобының көміртегі Электрон тапшылығы орталығы, ал карбонил тобының оттегі Электроны артық:
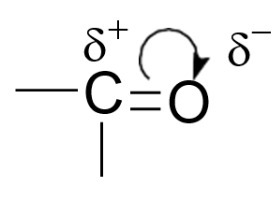
Мұндай топқа қандай реактивтер шабуыл жасайды? Бұл реакциялардағы ең маңызды кезең Электрон тапшылығы карбонил көміртегімен байланыс түзетіндіктен, карбонил тобы Электрон артық нуклеофильді реагенттермен әрекеттесуге бейім. Альдегидтер мен кетондардың типтік реакциялары АN нуклеофильді қосылу реакциялары болады.
Альдегидтер кетондарға қарағанда нуклеофильді қосылу (AN) реакциясына оңай түседі. Реактивтіліктің бұл айырмашылығы реакцияның аралық күйінің сипатына сәйкес келеді және электронды және кеңістіктік факторлардың бірлескен әсерімен түсіндіріледі. Кетонда екінші алкил немесе арил тобы, ал альдегидтерде сутегі атомы бар. Екінші алкил немесе арил тобы альдегидтегі сутегі атомынан үлкен, сондықтан ол өтпелі күйдегі кеңістіктік қиындықтардың көбеюіне кедергі келтіреді. Алкил тобы электрондарды береді және осылайша оттегідегі теріс зарядты күшейту арқылы өтпелі күйді тұрақтандырады. Электронды тартатын индуктивті әсері бар арил тобы өтпелі күйді тұрақтандырады және осылайша реакцияны тездетеді деп күтуге болады, алайда, бұл әсер резонанс салдарынан бастапқы кетонды одан әрі тұрақтандырады және нәтижесінде қарастырылып отырған реакцияда кетонды дезактивациялайды:

-
Тотығу:
Барлық органикалық қосылыстардың ішінде альдегидтер оңай тотығады. Олар карбон қышқылдарына перманганат немесе калий бихроматы сияқты реагенттердің әсерінен ғана емес, күміс ионы сияқты әлсіз тотықтырғыштардың әсерінен де айналады. Күміс ионының тотығуы сілтілі ортаны қажет етеді, ал ерімейтін күміс оксидінің тұнбасын болдырмау үшін күрделі түзуші реагент – аммиак қосылады.
Толленс реактивінде күрделі байланысқан күміс ионы Ag(NH3)2+. Альдегид тотыққан кезде күміс ионы бос күміске дейін азаяды (қолайлы жағдайда ол айна түрінде шығарылады).

Кетондар күміс иондарымен тотықпайды!
Бұл реакция негізінен альдегидтерді анықтау үшін және әсіресе оларды кетондардан ажырату үшін қолданылады.
Кетондардың тотығуы көміртек – көміртек байланысының үзілуін қажет етеді, сондықтан тек қатаң жағдайларда болады (ерекшелік-галоформ реакциясы). Реакция синтезге сирек қызығушылық тудырады: көптеген кетондар карбонил тобының кез келген жағынан ыдырап, қышқыл қоспасының пайда болуына әкелуі мүмкін.
-
альдегидтер:

-
метилкетондар:

-
Тотықсыздану:
Альдегидтер бастапқы спирттерге, ал кетондар каталитикалық гидрлеу арқылы немесе LiAlH4 литий алюминий гидриді немесе NaBH4 натрий борогидриді сияқты тотықсыздандырғыш реагенттерді қолдану арқылы қайталама спирттерге азаяды:

-
спирт арқылы тотықсыздану:

-
көміртек арқылы тотықсыздану:

-
Гриньяр реактивінің қосылуы:

-
HCN қосылуы:
Гидроциан қышқылының альдегидтерге және кетондардың көпшілігіне қосылуы циангидриндердің пайда болуына әкеледі. Кеңістіктегі қиын кетондар бұл реакцияға түспейді.
Гидроциан қышқылының өзі өте баяу қосылады, өйткені HCN әлсіз нуклеофил болып табылады. HCN-ден цианид анионын (күшті нуклеофил) тудыруы мүмкін калий цианидін немесе басқа негізді қосу қосылу реакциясының жылдамдығын айтарлықтай арттырады:

-
Натрий бисульфитіне қосылуы:
Натрий бисульфиті альдегидтерге және көптеген кетондарға (әсіресе метилкетондарға) қосылыс өнімін қалыптастыру үшін қосылады:

Құрамында көлемді алмастырғыштар бар кетондар кеңістіктегі қиындықтарға байланысты бұл реакцияға түспейді.
Бисульфиті бар қоспалар әдетте карбонилді қосылыстарды карбонил емес қосылыстардан бөлу үшін алынады. Карбонилді қосылысты оны бисульфит туындысына айналдыру арқылы тазартуға болады, содан кейін кристалды қоспаны карбонил емес қоспалардан бөліп, карбонилді қосылысты қалпына келтіруге болады.
-
Аммиак туындыларымен қосылуы:
Аммиакпен байланысты кейбір қосылыстар карбонил тобына қосылып, туындылар түзеді, оларды альдегидтер мен кетондарды анықтау үшін қолдануға болады, өйткені оксимдер, гидразондар, фенилгидразондар, семикарбазондар – тән балқу температурасы бар қатты кристалды заттар. Бұл туындыларда бастапқы қосындыдан су молекуласын жою нәтижесінде пайда болатын көміртек–азот қос байланысы бар.


-
Фосфор илидтерінің қосылуы. Виттиг Реакциясы:
Альдегидтер мен кетондар фосфор илидтерімен әрекеттесіп, алкендер мен трифенилфосфин оксидін береді. Бұл реакция Виттиг реакциясы деп аталады және алкендерді алу үшін кеңінен қолданылады:

-
Спирттермен қосылуы:

шағым қалдыра аласыз















