
10.3AТотығу-тотықсыздану реакциялары
|
|
|
|
Оқу мақсаты |
10.2.3.1 электронды баланс әдісімен тотығу‑ тотықсыздану реакциясы теңдеулерін құрастыру; 10.2.3.2 жартылай иондық реакция әдісімен тотығу – тотықсыздану реакция теңдеулерін құрастыру; 10.2.3.4 сулы ерітіндідегі химиялық реакциялардың жүру мүмкіндігін болжау үшін стандартты электродтық потенциалдар кестесін қолдану;
|
|
Бағалау критерийі |
Білім алушы: |
|
|
- электронды баланс әдісімен тотығу‑ тотықсыздану реакциясы теңдеулерін құрастырады; - жартылай иондық реакция әдісімен тотығу – тотықсыздану реакция теңдеулерін құрастырады; - электродты потенциал қатарын (металдардың электрохимиялық кернеу қатары) қолдана отырып, сулы ерітіндідегі химиялық реакциялардың жүру мүмкіндігін болжайды;
|
|
Ойлау дағдыларының деңгейлері |
Білу және түсіну, қолдану |
|
Орындау уақыты |
20 минут |
Тапсырма
-
(а) Тотығу дәрежесі ауыспалы элемент атомдарының сипаттамасын формулалармен сәйкестендіріңіз: [3]
|
Тотығу дәрежесінің өзгеруі |
Тотығу дәрежесінің өзгеру формулалары |
|
A. Тотығу дәрежесі жоғары атомдар |
2N⁻³ – 6e → NO₂ |
|
B. Тотығу дәрежесі төмен атомдар |
2N⁵⁺ + 10e → NO₂ |
|
C. Тотығу дәрежесі аралық атомдар |
NO₂ – 6e → 2N⁺³ |
-
(b) Берілген реакцияларды электрондық баланс әдісімен теңестіріңіз: [2]
KMnO₄ + HCl → KCl + MnCl₂ + Cl₂ + H₂O
![]()
-
(а) Электрондық – иондық баланс әдісінің электрондық баланс әдісінен айырмашылығы: [1]
![]()
-
(b) Берілген реакцияларды электрондық – иондық баланс әдісімен теңестіріңіз: [2]
KMnO₄ + H₂SO₄ + Na₂SO₃ → MnSO₄ + K₂SO₄ + Na₂SO₄ + H₂O
![]()
![]()
-
(а) Суреттегі берілген процестерді пайдаланып, Fe + CuSO₄ → FeSO₄ + Cu тоқтүзуші реакцияның теңдеуі бойынша гальваникалық элементтің сызбанұсқасын құрастырыңыз: [1]
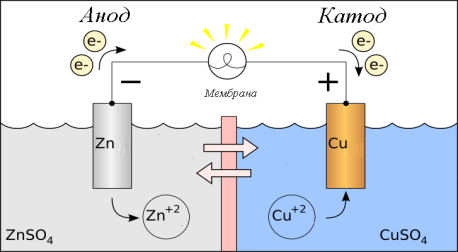
![]()
-
(b) Берілген реакцияның стандартты ЭҚК-сын есептеңіз: [2]
Fe ↔ Fe²⁺ + 2e⁻ (–0,44 V)
Cu²⁺ + 2e⁻ ↔ Cu (+0,34 V)
![]()
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
Ескерту |
|
Білім алушы |
||||
|
электронды баланс әдісімен тотығу‑ тотықсыздану реакциясы теңдеулерін құрастырады; сипаттамасын жазады; |
1 а) |
тотығу дәрежесі ауыспалы элемент атомдарының сипаттамасын формулалармен сәйкестендіреді |
3 |
|
|
1b) |
Берілген реакцияларды электрондық баланс әдісімен теңестіреді |
2 |
|
|
|
жартылай иондық реакция әдісімен тотығу – тотықсыздану реакция теңдеулерін құрастырады; |
2 а) |
Электрондық – иондық баланс әдісінің электрондық баланс әдісінен айырмашылығын сипаттайды |
1
|
|
|
2 b) |
Берілген реакцияларды электрондық – иондық баланс әдісімен теңестіреді |
2 |
|
|
|
электродты потенциал қатарын (металдардың электрохимиялық кернеу қатары) қолдана отырып, сулы ерітіндідегі химиялық реакциялардың жүру мүмкіндігін болжайды; |
3 а) |
гальваникалық элементтің сызбанұсқасын құрастырады |
1 |
|
|
3 b) |
берілген реакцияның стандартты ЭҚК сын есептейді |
2 |
|
|
|
Барлығы |
11 |
|
||
ЖАУАПТАРЫ
1. (а) Тотығу дәрежесінің өзгеруін сәйкестендіру:
|
Тотығу дәрежесінің өзгеруі |
Тотығу дәрежесінің өзгеру формулалары |
|
A. Тотығу дәрежесі жоғары атомдар |
1.
NO₂ – 6e → 2N⁺³ |
|
B. Тотығу дәрежесі төмен атомдар |
2.
2N⁵⁺ + 10e → NO₂ |
|
C. Тотығу дәрежесі аралық атомдар |
3.
2N⁻³ – 6e → NO₂ |
1. (b) Электрондық баланс әдісімен теңестіру:

![]()
2. (a) Электрондық-иондық баланс әдісінің электрондық баланс әдісінен айырмашылығы:
Электрондық баланс әдісі – реакциядағы электрондардың берілуін теңестіруге негізделген, ал электрондық-иондық баланс әдісі – барлық иондардың әсерін ескеріп, ортаның қышқылдық немесе сілтілік болуына қарай теңдеуді құруға мүмкіндік береді.
![]()
2.(b) Электрондық-иондық баланс әдісімен реакцияны теңестіру:

![]()
3. (a) Гальваникалық элементтің сызбанұсқасы:
Реакция:
Fe+CuSO4→FeSO4+Cu
Электродтар:
-
Ано́д: Fe→Fe2++2e−
-
Катод: Cu2++2e−→Cu
|
Ано́д (-) (тотығу) |
Электролит ерітіндісі |
Катод (+) (тотықсыздану) |
|
Fe → Fe²⁺ + 2e⁻ |
Cu²⁺ ерітіндісі |
Cu²⁺ + 2e⁻ → Cu |
3. (b) Гальваникалық элементтің стандартты ЭҚК-сын есептеу:

жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
бжб 10 сынып
10.3AТотығу-тотықсыздану реакциялары
|
|
|
|
Оқу мақсаты |
10.2.3.1 электронды баланс әдісімен тотығу‑ тотықсыздану реакциясы теңдеулерін құрастыру; 10.2.3.2 жартылай иондық реакция әдісімен тотығу – тотықсыздану реакция теңдеулерін құрастыру; 10.2.3.4 сулы ерітіндідегі химиялық реакциялардың жүру мүмкіндігін болжау үшін стандартты электродтық потенциалдар кестесін қолдану;
|
|
Бағалау критерийі |
Білім алушы: |
|
|
- электронды баланс әдісімен тотығу‑ тотықсыздану реакциясы теңдеулерін құрастырады; - жартылай иондық реакция әдісімен тотығу – тотықсыздану реакция теңдеулерін құрастырады; - электродты потенциал қатарын (металдардың электрохимиялық кернеу қатары) қолдана отырып, сулы ерітіндідегі химиялық реакциялардың жүру мүмкіндігін болжайды;
|
|
Ойлау дағдыларының деңгейлері |
Білу және түсіну, қолдану |
|
Орындау уақыты |
20 минут |
Тапсырма
-
(а) Тотығу дәрежесі ауыспалы элемент атомдарының сипаттамасын формулалармен сәйкестендіріңіз: [3]
|
Тотығу дәрежесінің өзгеруі |
Тотығу дәрежесінің өзгеру формулалары |
|
A. Тотығу дәрежесі жоғары атомдар |
2N⁻³ – 6e → NO₂ |
|
B. Тотығу дәрежесі төмен атомдар |
2N⁵⁺ + 10e → NO₂ |
|
C. Тотығу дәрежесі аралық атомдар |
NO₂ – 6e → 2N⁺³ |
-
(b) Берілген реакцияларды электрондық баланс әдісімен теңестіріңіз: [2]
KMnO₄ + HCl → KCl + MnCl₂ + Cl₂ + H₂O
![]()
-
(а) Электрондық – иондық баланс әдісінің электрондық баланс әдісінен айырмашылығы: [1]
![]()
-
(b) Берілген реакцияларды электрондық – иондық баланс әдісімен теңестіріңіз: [2]
KMnO₄ + H₂SO₄ + Na₂SO₃ → MnSO₄ + K₂SO₄ + Na₂SO₄ + H₂O
![]()
![]()
-
(а) Суреттегі берілген процестерді пайдаланып, Fe + CuSO₄ → FeSO₄ + Cu тоқтүзуші реакцияның теңдеуі бойынша гальваникалық элементтің сызбанұсқасын құрастырыңыз: [1]

![]()
-
(b) Берілген реакцияның стандартты ЭҚК-сын есептеңіз: [2]
Fe ↔ Fe²⁺ + 2e⁻ (–0,44 V)
Cu²⁺ + 2e⁻ ↔ Cu (+0,34 V)
![]()
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
Ескерту |
|
Білім алушы |
||||
|
электронды баланс әдісімен тотығу‑ тотықсыздану реакциясы теңдеулерін құрастырады; сипаттамасын жазады; |
1 а) |
тотығу дәрежесі ауыспалы элемент атомдарының сипаттамасын формулалармен сәйкестендіреді |
3 |
|
|
1b) |
Берілген реакцияларды электрондық баланс әдісімен теңестіреді |
2 |
|
|
|
жартылай иондық реакция әдісімен тотығу – тотықсыздану реакция теңдеулерін құрастырады; |
2 а) |
Электрондық – иондық баланс әдісінің электрондық баланс әдісінен айырмашылығын сипаттайды |
1
|
|
|
2 b) |
Берілген реакцияларды электрондық – иондық баланс әдісімен теңестіреді |
2 |
|
|
|
электродты потенциал қатарын (металдардың электрохимиялық кернеу қатары) қолдана отырып, сулы ерітіндідегі химиялық реакциялардың жүру мүмкіндігін болжайды; |
3 а) |
гальваникалық элементтің сызбанұсқасын құрастырады |
1 |
|
|
3 b) |
берілген реакцияның стандартты ЭҚК сын есептейді |
2 |
|
|
|
Барлығы |
11 |
|
||
ЖАУАПТАРЫ
1. (а) Тотығу дәрежесінің өзгеруін сәйкестендіру:
|
Тотығу дәрежесінің өзгеруі |
Тотығу дәрежесінің өзгеру формулалары |
|
A. Тотығу дәрежесі жоғары атомдар |
1.
NO₂ – 6e → 2N⁺³ |
|
B. Тотығу дәрежесі төмен атомдар |
2.
2N⁵⁺ + 10e → NO₂ |
|
C. Тотығу дәрежесі аралық атомдар |
3.
2N⁻³ – 6e → NO₂ |
1. (b) Электрондық баланс әдісімен теңестіру:

![]()
2. (a) Электрондық-иондық баланс әдісінің электрондық баланс әдісінен айырмашылығы:
Электрондық баланс әдісі – реакциядағы электрондардың берілуін теңестіруге негізделген, ал электрондық-иондық баланс әдісі – барлық иондардың әсерін ескеріп, ортаның қышқылдық немесе сілтілік болуына қарай теңдеуді құруға мүмкіндік береді.
![]()
2.(b) Электрондық-иондық баланс әдісімен реакцияны теңестіру:

![]()
3. (a) Гальваникалық элементтің сызбанұсқасы:
Реакция:
Fe+CuSO4→FeSO4+Cu
Электродтар:
-
Ано́д: Fe→Fe2++2e−
-
Катод: Cu2++2e−→Cu
|
Ано́д (-) (тотығу) |
Электролит ерітіндісі |
Катод (+) (тотықсыздану) |
|
Fe → Fe²⁺ + 2e⁻ |
Cu²⁺ ерітіндісі |
Cu²⁺ + 2e⁻ → Cu |
3. (b) Гальваникалық элементтің стандартты ЭҚК-сын есептеу:


шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
