
Жиынтық бағалауға арналған
әдістемелік ұсыныстар
Химия
8-сынып
«Жиынтық бағалау тапсырмаларының жинағы» әдістемелік құралы мұғалімге 8-сынып білім алушыларына «Химия» пәні бойынша жиынтық бағалауды жоспарлау, ұйымдастыру және өткізуге көмек құралы ретінде құрастырылған. Әдістемелік құрал 8-сынып «Химия» пәні бойынша ұзақ мерзімді оқу бағдарламасы негізінде дайындалған.
Бөлім бойынша жиынтық бағалаудың тапсырмалары мұғалімге білім алушылардың тоқсан бойынша жоспарланған оқу мақсаттарына жету деңгейін анықтауға мүмкіндік береді.
Әдістемелік құралда бөлім бойынша жиынтық бағалауды өткізуге арналған бағалау критерийлері мен дескрипторлары бар тапсырмалар ұсынылған. Дескрипторлары мен балдары бар тапсырмалар ұсыныс түрінде берілген.
Әдістемелік құрал жалпы орта білім беретін мектеп мұғалімдеріне, мектеп әкімшілігіне, білім беру бөлімінің әдіскерлеріне, критериалды бағалау бойынша мектеп, өңірлік үйлестірушілеріне және басқа да мүдделі тұлғаларға арналған.
Әдістемелік ұсыныстарды дайындау барысында ресми интернет-сайттағы қолжетімді ресурстар (суреттер, фотосуреттер, мәтіндер, аудио және бейнематериалдар) қолданылды.
1-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 4
8.1А «Атомдағы электрондардың қозғалысы» 4
8.1B «Заттардың формулалары және химиялық реакция теңдеулері» 8
8.1С «Металдар белсенділігін салыстыру» 12
2-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 15
8.2А, 8.2В «Зат мөлшері» және «Стехиометриялық есептеулер» 5
8.2C «Химиялық реакциядағы энергиямен танысу» 19
8.2D «Сутек. Оттек және озон» 23
3-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 27
8.3A «Химиялық элементтердің периодтық жүйесі» 27
8.3B «Химиялық байланыс түрлері» 31
8.3C «Ерітінділер және ерігіштік» 35
4-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 38
8.4A «Бейорганикалық қосылыстардың негізгі кластары. Генетикалық байланыс» .. 38
8.4B «Көміртек және оның қосылыстары» 42
1-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 48
2-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 57
3-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 64
4-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 69
«Атомдағы электрондардың қозғалысы» бөлімі бойынша
жиынтық бағалау
Оқу мақсаттары 8.1.3.1 Атомда электрондар ядродан
арақашықтығы артқан сайын біртіндеп
энергетикалық деңгейлер бойынша
таралатынын түсіну
8.1.3.4 Алғашқы 20 химиялық элементтердің
электрондық конфигурациясын және
электронды – графикалық формулаларын жаза
білу
8.1.3.5 Атомдар электрондарды қабылдай немесе
жоғалта алатынын және осының нәтижесінде
иондар түзілетінін түсіну
8.1.3.6 «Нөлдік қосынды» әдісімен
қосылыстардың формуласын құрастыру
Бағалау критерийлері Білім алушы:
• Атомдағы электрондардың энергетикалық
деңгейлерде орналасу ретін түсіндіреді.
• Алғашқы 20 химиялық элементтің электрондық және электронды - графикалық формулаларын
жазады.
• Қосып алатын немесе беретін электрондар саны
мен атом арасындағы байланысты анықтайды.
• «Нөлдік қосынды» әдісімен қосылыстардың
формуласын құрастырады.
Ойлау
дағдыларының
деңгейі Білу және түсіну,
қолдану
Орындалу уақыты 20 минут
Тапсырмалар
1. Келесі химиялық элементтер берілген: көміртек, натрий, фосфор, аргон.
Атом құрылысы және электрондардың энергетикалық деңгейлерде таралуы туралы тұжырымдар қай элементке қатысты айтылғанын анықтаңыз.
А) Сыртқы қабатында 1 электроны бар
В) Екі энергетикалық деңгейі бар
С) Сыртқы қабаты толық, аяқталған
D) 15 протоны, 15 электроны бар
|
С |
Na |
P |
Ar |
|
|
|
|
|
[2]
2. Химиялық элемент атомы мен электрондардың энергетикалық деңгейлерге таралуын сәйкестендіріңіз.
-
S А. 2е) 8е) 2е)
-
Al В. 2е) 8е) 8е) 1е)
-
K С. 2е) 8е ) 3е)
-
O D. 2е) 6е )
-
Mg Е. 2е) 8е )
-
Ne F. 2е) 8е) 6е)
[2]
Химия қысқы мерзімді жоспарлар жинағы. 8 сынып.
Д.Х Аширова, Н.Б. Бактыбаева.
3. Берілген химиялық элементтердің электрондық және графикалық формула-
ларын құрыңыз.
|
Химиялық элемент |
Электрондық формуласы |
Графикалық формуласы |
|
В |
|
|
|
Ne |
|
|
|
Si |
|
|
|
K |
|
|
[2]
4. (а) Натрий және күкірт атомдарындағы электрондардың таралуын сызбаға нүктемен көрсетіңіз.






![]()
![]()
Натрий атомы Күкірт атомы [1]
(b) Натрий және күкірт атомдарының иондарға айналуының сызбасын көрсетіңіз.






![]()
![]()
Натрий ионы Күкірт ионы
[1]
(с) Cыртқы энергетикалық деңгейдегі электрондар саны мен ион түзу (катион немесе анионға айналу) қасиеттерінің арасындағы байланысты түсіндіріңіз.
____________________________________________________________________________________________________________________________________________
[1]
Химия қысқы мерзімді жоспарлар жинағы. 8 сынып. Д.Х Аширова, Н.Б. Бактыбаева.
5. Химиялық қосылыстың молекула құрамы бойынша «нөлдік қосынды» әдісімен формуласын құрастырыңыз.
Азот (ІІІ) пен сутек
_____________________________________________________________________
[1]
Қалыптастырушы бағалауға арналған тапсырмалар жинағы. Химия 8-сынып
Балл қою кестесі
|
Бағалау критерийлері |
Тапсырма |
Дескрипторлар |
Балл |
|
Атомдағы электрондардың энергетикалық деңгейлерде орналасу ретін түсіндіреді
|
1 |
Берілген 4 тұжырымдарды химиялық элементке қатысты дұрыс анықтайды |
2 |
|
Атомдағы электрондардың энергетикалық деңгейлерде орналасу ретін түсіндіреді |
2 |
Берілген химиялық элементтердің электрондарының энергетикалық деңгейлерге таралуын анықтайды. |
1 |
|
Екінші бағанада берілген электрондардың энергетикалық деңгейлерге таралуымен сәйкестендіреді |
1 |
||
|
Химиялық элементтің электрондық конфигурациясын және электронды – графикалық формуларын жазады |
3 |
Берілген химиялық элементтердің электрондық формулаларын анықтайды |
1 |
|
Берілген химиялық элементтердің электронды-графикалық формулаларын анықтайды |
1 |
||
|
Қосып алатын немесе беретін электрондар саны мен атом арасындағы байланысты анықтайды
|
4 |
Натрий және күкірт атомдарының электрондарының энергетикалық деңгейлерге таралуын сызбада нүктемен көрсетеді |
1 |
|
Натрий және күкірт атомдарының иондарға айналуын сызбада нүктемен көрсетеді |
1 |
||
|
Сыртқы энергетикалық деңгейдегі электрондар саны мен ион түзу қасиеттерінің арасындағы байланысты анықтайды |
1 |
||
|
«Нөлдік қосынды» әдісімен қосылыстың формуласын құрастырады |
5 |
«Нөлдік қосынды» әдісімен берілген қосылыстардың формулаларын құрастырады |
1 |
|
Барлығы |
10 |
||
«Заттардың формулалары және химиялық реакция теңдеулері» бөлімі бойынша жиынтық бағалау
|
|
|
|
Оқу мақсаты |
8.2.3.1 Заттар құрамындағы элементтердің массалық үлесін табу, элементтердің массалық үлесі бойынша заттардың формуласын құрастыру; 8.2.3.3 Реакцияға қатысатын және түзілетін заттардың формулаларын жаза отырып, химиялық реакция теңдеуін құрастыру; 8.2.3.4 Заттар массасының сақталу заңын білу; 8.2.2.1 Бастапқы және түзілген заттардың саны мен құрамы бойынша химиялық реакцияларды жіктеу; 8.2.2.2 Табиғаттағы және тірі ағзалар мен адам тіршілігіндегі химиялық реакцияларды сипаттау. |
|
Бағалау критерийі |
Білім алушы: |
|
|
● Заттар құрамындағы элементтердің массалық үлесін табады, элементтердің массалық үлесі бойынша заттардың формуласын анықтайды ● Реагенттер мен өнімдерді жазу арқылы химиялық реакция теңдеуін жазады ● Зат массасының сақталу заңын тұжырымдайды ● Реакцияға қатысатын және реакция нәтижесінде түзілген заттардың саны мен құрамы бойынша химиялық реакцияларды жіктейді ● Табиғаттағы және тірі ағзалар мен адам тіршілігіндегі химиялық реакцияларды түсіндіреді |
|
|
|
|
Ойлау дағдыларының деңгейлері |
Қолдану, жоғары деңгей дағдылары |
|
|
|
|
Орындау уақыты |
20 минут |
Тапсырма
1. а) Химиялық элементтер жалпы молекуланың белгілі бір бөлігін құрайды. Фосфор (V) оксиді құрамындағы оттегінің массалық үлесін (%) анықтаңыз:
A) 11
B) 20
C) 34
D) 43
E) 56
Жауабы: _______________ [1]
b) Қосылыстардағы элементтердің мөлшерін білу оларды тиімді қолдану үшін қажет. Заттың құрамындағы натрийдің массалық үлесі - 54,5%, оттектің массалық үлесі - 40%, сутектің массалық үлесі – 5,5% көрсетеді. Қосылыстың формуласын анықтаңыз.
[1]
2. Химиялық реакция теңдеуі реагенттердің өнімдерге айналуын сипаттайды. Нүктелердің орнына тиісті формулаларды жазып, реакция теңдеуін құрастырыңыз.
Na + … → Na2S
H2CO3 → … + CO2
Са + O2 → …
Ag2O → Ag + … [4]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / Н.Нұрахметов, К.А.Сарманова, К.М.Жексембина - Алматы: «Мектеп», 2016
3. Төменде берілген суретте реакцияның жүру барысы көрсетілген. Реакция барысында зат массасының сақталу заңы сақталған ба, жауабыңызды түсіндіріңіз.

http://cubino.pl/2016/10/euro6-motorem-postepu/
[1]
4. Бастапқы заттар мен өнімдердің құрамы бойынша химиялық реакция теңдеуін жіктеңіз және әр типке мысал келтіріңіз.
![]()
Химиялық реакция типтері
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Алмасу
![]()
![]()
![]()
![]()
![]()
Айырылу
![]()
![]()
2NO + O2 → 2NO2
![]()
![]()
Mg + 2HCl → MgCl2 + Н2
[4]
5. Адам өміріндегі көптеген күнделікті қолданатын заттары және іс-әрекеттері химиялық процестерге негізделген. Мысалы жану және баяу тотығу процестері, әр процеске бір мысал келтіріңіз және жану мен баяу тотығу процесінің екі ұқсастығы мен айырмашылығын жазыңыз.
Мысалы:
Ұқсастығы:
Айырмашылығы:
[5]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
Ескерту |
|
Білім алушы |
||||
|
Заттар құрамындағы элементтердің массалық үлесін табады, элементтердің массалық үлесі бойынша заттардың формуласын анықтайды |
1(a) |
Қосылыс құрамындағы оттегінің массалық үлесінің мәнін анықтайды |
1 |
|
|
1(b) |
Массалық үлестің мәні бойынша қосылыстың формуласын анықтайды |
1 |
|
|
|
Реагенттер мен өнімдерді жазу арқылы химиялық реакция теңдеуін жазады |
2 |
Натрий сульфидінің түзілу реакция теңдеуін құрастырады |
1 |
|
|
Көмірқышқылының ыдырау реакция теңдеуін құрастырады |
1 |
|
||
|
Кальций мен оттегінің әрекеттесу реакция теңдеуін құрастырады |
1 |
|
||
|
Күміс оксидінің ыдырау реакция теңдеуін құрастырады |
1 |
|
||
|
Зат массасының сақталу заңын тұжырымдайды |
3 |
Зат массаның сақталу заңын тұжырымдайды |
1 |
|
|
Реакцияға қатысатын және реакция нәтижесінде түзілген заттардың саны мен құрамы бойынша химиялық реакцияларды жіктейді |
4 |
Қосылу реакциясын ажыратады |
1 |
|
|
Айырылу реакциясын ажыратады |
1 |
|
||
|
Орынбасу реакциясын ажыратады |
1 |
|
||
|
Алмасу реакциясын ажыратады |
1 |
|
||
|
Табиғаттағы және тірі ағзалар мен адам тіршілігіндегі химиялық реакцияларды түсіндіреді |
5 |
Жану реакциясына бір мысал жазады
|
1 |
|
|
Баяу тотығу процесіне бір мысал жазады |
1 |
|
||
|
Жану және баяу тотығу процестерінің өзара екі ұқсастығын жазады |
1 |
|
||
|
Жану процесінің баяу тотығу процесінен екі айырмашылығын жазады |
1 |
|
||
|
Баяу тотығу процесінің жану процесінен екі айырмашылығын жазады |
1 |
|
||
|
Барлығы |
16 |
|
||
«Металдар белсенділігін салыстыру» бөлімі бойынша жиынтық бағалау
|
|
|
|
Оқу мақсаты |
8.2.4.2 Белсенді металдардың салқын сумен, ыстық су немесе бумен әрекеттесуін сипаттау; 8.2.4.3 Металдар коррозиясын туындатуға әсер ететін жағдайларды зерттеу; 8.2.4.5 Металдардың қышқылдармен әрекеттесуінің реакция теңдеулерін құрастыру; 8.2.4.8 Металдардың белсенділік қатарын қолданып металдардың таныс емес орынбасу реакцияларының жүру мүмкіндігін болжау. |
|
Бағалау критерийі |
Білім алушы: |
|
|
● Белсенді металдардың салқын сумен, ыстық су немесе бумен әрекеттесуін сипаттайды; ● Металдар коррозиясын туындатуға әсер ететін жағдайларды зерттейді; ● Металдардың қышқылдармен әрекеттесуінің реакция теңдеулерін жазады; ● Металдардың белсенділік қатарын қолданып металдардың таныс емес орынбасу реакцияларының жүру мүмкіндігін болжайды. |
|
Ойлау дағдыларының деңгейлері |
Қолдану, жоғары деңгей дағдылары |
|
Орындау уақыты |
20 минут |
Тапсырма
1. Металдардың сумен әрекеттесуі берілген кестені қажетті сөздермен толықтырыңыз.
|
Металл |
Сумен әрекеттескендегі металдың белсенділігі |
Түзілген өнімдер |
|
Калий |
|
|
|
Мырыш |
|
|
|
Алтын |
|
|
[3]
2. а) Неліктен табиғатта алтынның бос күйінде кездесетінін, ал мырыштың бос күйінде кездеспейтінің түсіндіріңіз.
________________________________________________________________
__________________________________________________________________
[2]
b) Неліктен ертеректе темір ақша жасауда күмісті пайдаланды?
__________________________________________________________________
[1]
с) Металдар коррозиясының алдын алу үшін бір ұсыныс жазыңыз.
__________________________________________________________________
[1]
3. Металдардың қышқылдармен әрекеттесу белсенділігі әр түрлі. Төменде берілген реакция теңдеулерін жазыңыз.
1) Мырыштың сұйылтылған тұз қышқылымен әрекеттесуі
______________________________________________________________________
2) Магнийдің сұйылтылған күкірт қышқылымен әрекеттесуі
______________________________________________________________________
3) Күмістің сұйылтылған тұз қышқылымен әрекеттесуі
______________________________________________________________________
[3]
4. a) Оқушы химия зертханасында металдар мен тұздарды пайдалана отырып тәжірибе жасады. Металдар мен тұз ерітінділері арасында мүмкін болатын реакция теңдеулерін анықтаңыз (х-реакция жүрмейді, ˅ - реакция жүреді).
|
Тұз ерітінділері |
Мыс |
Қалайы |
Магний |
|
Мырыш сульфаты |
|
|
|
|
Темір хлориді |
|
|
|
|
Қорғасын (ІІ) нитраты |
|
|
|
Мүмкін болған реакция теңдеулерін жазыңыз:
___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
[4]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
Ескерту |
|
Білім алушы |
||||
|
Белсенді металдардың салқын сумен, ыстық су немесе бумен әрекеттесуін сипаттайды;
|
1 |
Калийдің сумен әрекеттесу белсенділін және реакция өнімін жазады Мырыштың сумен әрекеттесу белсенділін және реакция өнімін жазады Алтынның сумен әрекеттесу белсенділін және реакция өнімін жазады |
1 1 1 |
|
|
Металдар коррозиясын туындатуға әсер ететін жағдайларды зерттейді |
2 а) |
Табиғатта алтынның бос күйінде кездесу себебін жазады |
1 |
|
|
Табиғатта мырыштың қосылыс түрінде кездесу себебін жазады |
1 |
|
||
|
2 b) |
Күмістің темір ақша жасауда қолданылу себебін жазады |
1 |
|
|
|
2 с) |
Металдар коррозиясының алдын алудың бір ұсынысын жазады |
1 |
|
|
|
Металдардың қышқылдармен әрекеттесуінің реакция теңдеулерін жазады; |
3 |
Мырыштың сұйылтылған тұз қышқылымен әрекеттесу теңдеуін жазады |
1 |
|
|
Магийдің сұйылтылған тұз қышқылымен әрекеттесу теңдеуін жазады |
1 |
|
||
|
Күмістің сұйылтылған тұз қышқылымен әрекеттесу теңдеуін жазады |
1 |
|
||
|
Металдардың белсенділік қатарын қолданып металдардың таныс емес орынбасу реакцияларының жүру мүмкіндігін болжайды |
4 а) |
Мыстың тұз ертініділерімен мүмкін болатын реакция теңдеулерін жазады |
1 |
|
|
Қалайының тұз ертініділерімен мүмкін болатын реакция теңдеулерін жазады |
1 |
|
||
|
Магнийдің тұз ертініділерімен мүмкін болатын реакция теңдеулерін жазады |
1 |
|
||
|
b) |
Металдардың белсенділік қатарына байланысты орынбасу реакцияларның жүру мүмкіндігін жазады |
1 |
|
|
|
c) |
Берілген металдардың белсенділік қатарын жазады |
1 |
|
|
|
Барлығы |
15 |
|
||
«Зат мөлшері» және «Стехиометриялық есептеулер» бөлімдері
бойынша жиынтық бағалау
|
Оқу мақсаты |
8.1.1.3 Масса, зат мөлшері және құрылымдық санын есептеу; 8.2.3.5 Химиялық реакция теңдеулері бойынша заттың массасын, зат мөлшерін есептеу; 8.2.3.6 Авогадро заңын білу және стандартты жағдайлардағы газдар көлемін есептеуде молярлық көлемді қолдану; 8.2.3.7 Газдардың салыстырмалы тығыздығын және заттың молярлық массасын салыстырмалы тығыздық бойынша есептеу 8.2.3.8 Газдардың қатысуымен жүретін реакциялар бойынша есептер шығаруда газдардың көлемдік қатынас заңын қолдану |
|
Бағалау критерийі |
Білім алушы ● Зат массасы, мөлшері және құрылымдық бөлшектер санын есептеуде формуланы қолданып есептейді; ● Химиялық реакция теңдеуі бойынша зат массасын, зат мөлшерін анықтайды; ● Молярлық көлемді қолданып есептеулер жүргізеді; ● Салыстырмалы тығыздық бойынша газдың тығыздығын және заттың молярлық массасын есептейді; ● Есептер шығаруда газдардың көлемдік қатынас заңын қолданып есептеулер жүргізеді. |
|
Ойлау дағдыларының деңгейі |
Қолдану, жоғары деңгей дағдылары |
|
Орындалу уақыты |
20 минут |
Тапсырма
1. Молекулалар саны 12,04•1023 тең оттек газының зат мөлшері және массасын есептеңіз.
А) 3 моль және 96 г
В) 2 моль және 64 г
С) 1 моль және 32 г
D) 0,5 моль және 16 г
[2]
2. Массасы 26 г мырыш сұйылтылған тұз қышқылымен әрекеттесті. Түзілген мырыш хлоридінің массасын, зат мөлшерін табыңыз.
а) Мырыштың сұйылтылған тұз қышқылымен әрекеттесуінің реакция теңдеуін жазыңыз.
___________________________________________________________________
[1]
b) Мырыш хлоридінің массасын есептеңіз.
_________________________________________________________________________________________________________________________________________
[1]
c) Мырыш хлоридінің зат мөлшерін есептеңіз.
_________________________________________________________________________________________________________________________________________
[1]
3.Газдардың күйін сипаттайтын шамалар: қысым, көлем, температура. Газдарды сипаттағанда көбінесе қысым мен температураны тұрақты етіп алып, көлемнің өзгерістерін қарастырамыз, көлемнің өзгерісі газдар үшін деңгейлес болады, себебі олардың молекулааралық қашықтықтары шамамен бірдей.

Келесі тұжырымдардың шындық не жалған екендігін анықтап, кестеге шындық болса «+», жалған болса « -» белгісін қойыңыз.
|
Тұжырымдар |
Шындық |
Жалған |
|
5 моль азот молекуласының (қ.ж.) көлемі 112 л/моль болады |
|
|
|
1 моль сутек молекуласының (қ.ж.) көлемі 11,2 л/моль болады |
|
|
|
0,5 моль неон атомының көлемі 11,2 л/моль болады |
|
|
|
2 моль хлор молекуласының (қ.ж.) көлемі 22,4 л/моль болады |
|
|
[2]
4. Белгісіз газдың ауа бойынша салыстырмалы тығыздығы 1,103-ке тең. Осы газдың молярлық массасын табыңыз.
![]()
![]()
![]()
[1]
5. Табиғатта найзағай ойнағанда аудағы азот оттекпен қосылып, азот(II) оксидін түзеді.
-
Осы құбылыс кезінде жүретін реакцияның теңдеуін жазыңыз.
_______________________________________________________________________________________________________________________________________
[1]
-
Реакцияға түсетін газдардың көлемдік қатынасын анықтаңыз.
__________________________________________________________________________________________________________________________________________________________________________________________________________________
[1]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
|
Білім алушы |
|||
|
Зат массасы, мөлшері және құрылымдық бөлшектер санын есептеуде формуланы қолданып есептейді |
1 |
оттек газының зат мөлшерін есептейді; |
1 |
|
оттек газының массасын есептейді; |
1 |
||
|
Химиялық реакция теңдеуі бойыншазат массасын, зат мөлшерін анықтайды |
2 |
мырыштың сұйылтылған тұз қышқылымен әрекеттесуінің реакция теңдеуін жазады; |
1 |
|
мырыш хлоридінің массасын табады; |
1 |
||
|
мырыш хлоридінің зат мөлшерін табады; |
1 |
||
|
Молярлық көлемді қолданып есептеулер жүргізеді |
3 |
кестеге шындық болса «+» қояды; |
1 |
|
жалған болса « -» белгісін қояды; |
1 |
||
|
Салыстырмалы тығыздық бойынша газдың тығыздығын және заттың молярлық массасын есептейді |
4 |
ауамен салыстырғандағы тығыздығы бойынша белгісіз газдың молярлық массасын есептейді; |
1 |
|
Есептер шығаруда газдардың көлемдік қатынас заңын қолданып есептеулер жүргізеді |
5 |
азот(II) оксидін түзілунің реакция теңдеуін жазады; |
1 |
|
газдардың көлемдік қатынасын анықтайды. |
1 |
||
|
Барлығы |
10 |
||
«Химиялық реакциядағы энергиямен танысу» бөлімі бойынша
жиынтық бағалау
Оқу мақсаты 8.3.1.1 Заттың жану реакциясының өнімі көбінесе
оксид екенін және құрамында көміртегі бар
отын оттекте жанғанда, көмірқышқыл газы,
иіс газы немесе көміртек түзілетінін түсіну
-
8.3.1.2 Парниктік эффекттің себептерін түсіндіру және
-
шешу жолдарын ұсыну
-
8.3.1.3 Экзотермиялық реакциялар жылу бөле
-
жүретінін, ал эндотермиялық реакциялар
-
жылу сіңіре жүретінін білу
8.3.1.5 Энергия өзгерісін бөлшектердің кинетикалық
теориясы тұрғысынан түсіндіру
Бағалау критерийі Білім алушы
• Көміртекті отындар жанғанда түзілетін
оксидтерді және олардың қасиеттерін
анықтайды
• Парниктік эффектінің себептерін түсіндіреді
және шешу жолдарын ұсынады
• Экзотермиялық және эндотермиялық
реакцияларды ажыратады
• Энергия өзгерісін бөлшектердің кинетикалық
теориясы тұрғысынан сипаттайды
Ойлау дағдыларының деңгейі Білу және түсіну
Қолдану
Жоғары деңгей дағдылары
Орындалу уақыты 20 минут
Тапсырма
1(a) «Иіс газы» деп аталатын көміртек оксидінің формуласын белгілеңіз.
-
CO2
-
CH4
-
С3H8
-
SO2
-
СО
[1]
(b) Көміртек оксидтері жөніндегі тұжырымның шындық/жалғандығын «˅» белгісін қою арқылы анықтаңыз.
|
Тұжырымдар |
Шындық |
Жалған |
|
Көміртек(IV) оксиді жануды қолдамайды |
|
|
|
Көміртек(II) оксиді отын толық жанғанда түзіледі |
|
|
|
Көміртек(II) оксиді түссіз, иіссіз, өте улы газ |
|
|
|
Көміртек(II) оксидінің тотықтырғыш қасиеті бар |
|
|
|
Көміртек(IV) оксиді тұрмыстық пропан газы жанғанда түзіледі |
|
|
[5]
2. Атмосфераның құрамы мен жағдайы ғарышпен жер арасындағы сәуле, жылу алмасу процесіне әсер етеді. Күннен жерге немесе жерден ғарышқа қуат берілу процесі биосферадағы температураны белгілі бір деңгейде сақтайды. Мұнда биосферадағы температура жағдайын сақтап тұруда жерге жылу қуатын алып келетін күн радиациясының рөлі жоғары. Осы процесс бірі-бірімен тығыз байланыста болады. Сондықтан жердегі жылу балансының өзгеруі биосфераның орта температурасының ұлғаюына әкелуі мүмкін.
https://kk.wikipedia.org/wiki/ Парниктік эффект
(а) Парниктік эффектінің пайда болу себептеріне үш мысал келтіріп, түсіндіріңіз.
___________________________________________________________________________________________________________________________________________________________________________________________________________
[1]
(b) Парниктік эффектінің салдарларын азайтудың екі жолын ұсыныңыз.
1._____________________________________________________________________
2._____________________________________________________________________
[1]
3. Экзотермиялық, эндотермиялық, жылу эффектісі, термохимиялық теңдеу терминдерін сипаттайтын тұжырымдармен сәйкестендіріңіз.
|
Терминдер |
Тұжырымдар |
|
1. Экзотермиялық |
А) Химиялық реакцияның жылу эффектісі көрсетілген теңдеу |
|
2. Эндотермиялық |
В) Химиялық реакция кезінде бөлінетін немесе сіңірілетін жылу мөлшері |
|
3. Жылу эффектісі |
С) Жылу сіңіре жүретін реакция |
|
4. Термохимиялық теңдеу |
D) Жылу бөле жүретін реакция
|
1.______ 2._____ 3._____ 4._____
[4]
4. Фосфор оттекпен жарық шығара отырып, қарқынды жанады. Фосфор жанғанда, ақ түтін будақтап, оның оксиді түзіледі. Фосфордың жану реакциясының жылу эффектісі 3010 кДж тең.
https://surak.baribar.kz/648573/
(а) Осы реакцияның термохимиялық теңдеуін жазып көрсетіңіз.
__________________________________________________________________________________________________________________________________________________________________ [1]
(b) Азот пен оттектің аз мөлшерлері найзағай ойнаған кезде өзара әрекеттесіп, оксид түзеді. Осы құбылыс кезінде химиялық реакция энергиясы өзгереді. Энергия тұрғысынан реакция типін ажыратып жазыңыз.
_______________________________________________________________________________________________________________________________________________________________________________________________________________
[1]
Балл қою кестесі
|
Бағалау критерийі |
Тапсыр ма № |
Дескриптор |
Балл |
|
Білім алушы |
|||
|
Көміртекті отындар жанғанда түзілетін оксидтерді және олардың қасиеттерін анықтайды |
1 |
«Иіс газы» деп аталатын көміртек оксидінің формуласын анықтайды |
1 |
|
Көміртек (IV) оксиді жануды қолдамайды деген тұжырымның шындық екенін анықтайды |
1 |
||
|
Көміртек (II) оксиді отын толық жанғанда түзіледі деген тұжырымның жалған екенін анықтайды |
1 |
||
|
Көміртек (II) оксиді түссіз, иіссіз, өте улы газ деген тұжырымның шындық екенін анықтайды |
1 |
||
|
Көміртек (II) оксидінің тотықтырғыш қасиеті бар деген тұжырымның жалған екенін анықтайды |
1 |
||
|
Көміртек(IV) оксиді тұрмыстық пропан газы жанғанда түзіледі деген тұжырымның шындық екенін анықтайды |
1 |
||
|
Парниктік эффектінің себептерін түсіндіреді және шешу жолдарын ұсынады |
2 |
Парниктік эффектінің пайда болу себептеріне үш мысал келтіріп, түсіндіреді |
1 |
|
Парниктік эффектінің салдарларын азайтудың екі жолын ұсынады |
1 |
||
|
Экзотермиялық және эндотермиялық реакцияларды ажыратады |
3 |
Химиялық реакцияның жылу эффектісі көрсетілген теңдеудің термохимиялық теңдеу екенін сәйкестендіреді |
1 |
|
Жылу бөле жүретін реакциялар экзотермиялық екенін сәйкестендіреді |
1 |
||
|
Жылу сіңіре жүретін реакциялар эндотермиялық екенін сәйкестендіреді |
1 |
||
|
Химиялық реакция кезінде бөлінетін немесе сіңірілетін жылу мөлшерінің жылу эффектісі екенін сәйкестендіреді |
1 |
||
|
Энергия өзгерісін бөлшектердің кинетикалық теориясы тұрғысынан сипаттайды |
4 |
Фосфордың жану реакциясының термохимиялық теңдеуін жазады |
1 |
|
Энергия тұрғысынан реакция типін анықтайды. |
1 |
||
|
Барлығы |
14 |
||
«Сутек. Оттек және озон» бөлімі бойынша жиынтық бағалау
|
Оқу мақсаты |
8.4.2.1 Сутекті алу және оның қасиеттері мен қолданылуын зерттеу;
|
|
Бағалау критерийі |
Білім алушы ● Сутектің алыну жолын және оның қасиеттері мен қолданылуын сипаттайды; ● Оттекті алудың реакция теңдеуін және оттектің қасиеттері мен қолданылуын сипаттайды; ● Оттектің аллотропиялық түрөзгерістерінің құрамы мен қасиеттерін сәйкестендіреді; ● Озон қабатының маңызын түсіндіреді. |
|
Ойлау дағдыларының деңгейі |
Қолдану, жоғары деңгей дағдылары |
|
Орындалу уақыты |
20 минут |
Тапсырма
1. Зертханада сутекті алуға болатын заттардың қатарын көрсетіңіз
A) HNO3, Н2О,NaOH
B) СН4, С, Н2О
C) Н2О,Zn, НСl, Са
D) КMnO4, H2O, НCIO3
[]
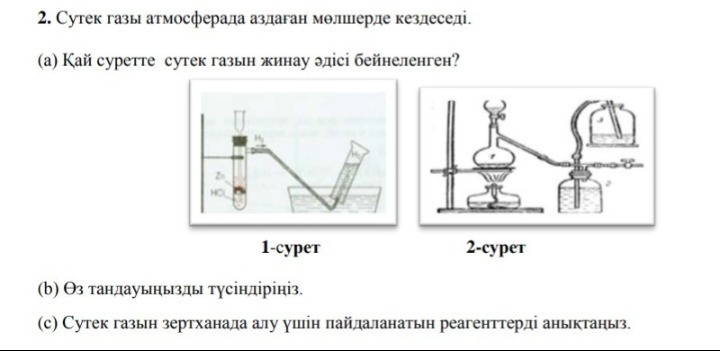
(d) Жиналған газ сутегі газы екендігін дәлелдеңіз.
__________________________________________________________________________________________________________________________________________________________________________________________________________________
(e) Сутектің қолданылуына мысал келтіріңіз.
___________________________________________________________________________________________________________________________________________
[5]
3. Оттегі – химияның ең маңызды элементі және Жер бетіндегі көптеген тірі ағзалардың тыныс алуын қамтамасыз етеді.
а) Оттек туралы келесі тұжырымдардың шындық не жалған екендігін анықтап, кестеге шындық болса «+», жалған болса « -» белгісін қойыңыз.
|
Тұжырымдар |
Шындық |
Жалған |
|
1 Иіссіз, дәмсіз, түссіз газ |
|
|
|
2 Аудан жеңіл |
|
|
|
3 Суды ығыстыру арқылы жинауға болады |
|
|
|
4 -1830С сұйылады |
|
|
|
5 Суда жақсы ериді |
|
|
[2]
b) Өзгерістер тізбегі берілген: КМnO4 → А → Р2O5
c) А затын анықтаңыз __________________________________________________
[1]
d) КMnO4 -тен А затын алудың реакция теңдеуін жазыңыз
______________________________________________________________________
[1]
e) А затының алдына қойылатын коэффициентті анықтаңыз
4Р + А → 2Р2O5
______________________________________________________________________
[1]
4. Зат мөлшері 2 моль оттек(қ.ж.) қандай көлем алады?
![]()
[1]
5. Озон – химиялық формуласы О3 болып келетін оттегінің аллотропиялық түр өзгерісі. Түсі қою көк, өткір иісті газ,ал сұйық озон күлгін көк; балқу t – 192,7°С, қайнау t – 112°С. Суда ерігіштігі 0,394 г/л (0°С-та).
Төменде берілген сурет бойынша озонның қолданылу салаларын анықтаңыз.
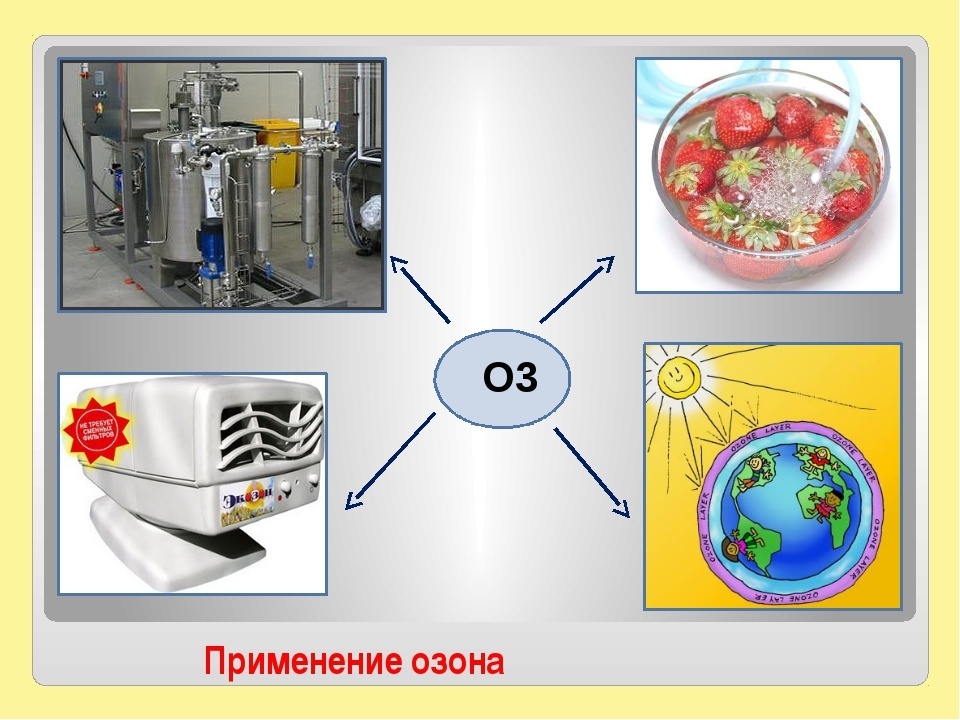
[1]
6. Озон қабаты (озоносфера) бүкіл Жер шарын 10-50 км аралығында қоршап тұр, ал ең көп жинақталуы 20-25 км биіктікте болады. «Озон тесігі» деген атау алып, Антарктида үстіндегі кеңістікте озон мөлшерінің (50%) төмендеуіне байланысты ең бірінші озон қабатының жұқаруы 1985 жылы жүрт назарына ілікті. Содан бергі өлшеулер нәтижесі озон қабатының азаюын дәлелдеуде. Жердің озон қабатының бұзылуы адам, жануарлар, өсімдіктер мен микроағзалар тіршілігі үшін қатер болып табылады.
Озон қабатының бұзылуына себеп болатын жағдайларға екі мысал келтіріп жазыңыз.
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
[2]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
|
Білім алушы |
|||
|
Сутекті алу және оның қасиеттері мен қолданылуын сипаттайды |
1, 2 |
зертханада сутекті қандай заттардан алуға болатынын анықтайды; |
1 |
|
қай суретте сутек газын жинау әдісі көрсетілгенін дұрыс анықтайды; |
1 |
||
|
Өз таңдауын түсіндіреді; |
1 |
||
|
сутек газын зертханада алу үшін қолданылатын реактивтерді анықтайды; |
1 |
||
|
жиналған газдың сутек екенін дәлелдейді; |
1 |
||
|
сутектің қолданылуына мысал келтіреді; |
1 |
||
|
Оттекті алудың реакция теңдеуін және оттектің қасиеттері мен қолданылуын сипаттайды |
3,4 |
кестеге шындық болса «+» қояды; |
1 |
|
жалған болса « -» белгісін қояды; |
1 |
||
|
тізбектегі А затын анықтайды; |
1 |
||
|
калий перманганатын айырып А затын алудың реакция теңдеуін жазады; |
1 |
||
|
А затының алдына қойылатын коэффициентті анықта |
1 |
||
|
зат мөлшері белгілі газдың көлемін дұрыс есептейді; |
1 |
||
|
Оттектің аллотропиялық түрөзгерістерінің құрамы мен қасиеттерін сәйкестендіреді |
5 |
берілген сурет бойынша озонның қолданылу салаларын анықтайды; |
1 |
|
Озон қабатының маңызын түсіндіреді |
6 |
озон қабатының бұзылуына себеп болатын жағдайларға екі мысал келтіріп жазады; |
2 |
|
Барлығы |
15 |
||
«Химиялық элементтердің периодтық жүйесі» бөлімі бойынша жиынтық бағалау
|
|
|
|
Оқу мақсаты |
8.2.1.1 Топ, период, атом нөмірінің физикалық мәнін түсіндіру; 8.2.1.3 Топтар мен периодтарда элементтер қасиеттерінің заңдылықпен өзгеретінін түсіндіру; 8.2.1.4 Периодтық жүйедегі орны бойынша химиялық элементті сипаттау; 8.2.1.6 Химиялық элементтердің табиғи ұяластарын білу және сілтілік металдар, галогендер, инертті элементтердің ұяластарына мысалдар келтіру; 8.2.1.7 Химиялық элементтің периодтық кестеде орналасуына сай қасиеттерін болжау. |
|
Бағалау критерийі |
Білім алушы: |
|
|
● Топ, период, атом нөмірінің физикалық мәнін сипаттайды; ● Элементтер қасиеттерінің топтар мен периодтарда заңдылықпен өзгеретінін түсіндіреді; ● Химиялық элементтерді периодтық жүйедегі орны бойынша сипаттайды; ● Химиялық элементтердің табиғи ұяластарын атайды және олардың таңбасын жазады; ● Периодтық кестеде орналасуына байланысты химиялық элементтің қасиетін болжайды. |
|
Ойлау дағдыларының деңгейлері |
Қолдану, жоғары деңгей дағдылары |
|
Орындау уақыты |
20 минут |
Тапсырма
1. Элементтердің келесі қатары берілген. Берілген тұжырымдар мен химиялық элементтер арасындағы сәйкестікті анықтаңыз.
|
Тұжырымдар |
Химиялық элементтер |
|
1) элементтің 6 электроны бар |
A) Ag |
|
2) элементтің 7 нейтроны бар |
B) Al |
|
3) элементтің 5 энергетикалық деңгейі бар |
C) N |
|
4) элементтің протон санының мәні 3-ке тең |
D) Li |
|
5) элементтің соңғы энергетикалық деңгейінде 3 электрон бар |
E) C |
1) ___ 2)___ 3)___ 4)____ 5)___
[2]
2. a) Берілген кесте бойынша дұрыс жауаптарды анықтаңыз.
|
|
Период бойынша (солдан оңға қарай) |
Топ бойынша (жоғарыдан төмен қарай) |
|
1) Энергетикалық деңгей саны |
А) өзгермейді B) 1 энергетикалық деңгейге артады |
C) өзгермейді D) 1 энергетикалық деңгейге артады |
|
2) Сыртқы энергетикалық деңгейдегі электрон саны |
А) 1-ге артады B) тұрақты |
C) 1-ге артады D) тұрақты |
1) _______________
2) _______________
[2]
b) Берілген химиялық элементтердің қасиеттерінің периодты өзгеруіне байланысты тұжырымдардың бос орындарын қажетті сөздермен толықтырыңыз.

Период бойынша (солдан оңға қарай)
![]()
![]()


2. Атом радиусы ______________
1. Салыстырмалы атомдық масса _______________

Топ бойынша (жоғарыдан төмен қарай)
![]()
![]()


4. Оттекпен қосылысындағы валенттілігі ____________
3. Металдық қасиет ___________
[2]
3. Химиялық элементтің нейтрон санының мәні 12-ге тең. Бұл элемент ядролық реакторларда жылу тасымалдаушы ретінде, органикалық реакцияларда өршіткі, медицинада радиоактивті изотоп күйінде қолданылады. Периодтық жүйедегі орны және атом құрылысы тұрғысынан химиялық элементке сипаттама беріңіз.
1. Элементтің атомдық нөмірі __________________________________________
2. Периодтық жүйедегі орны ___________________________________________
3. Атом құрамы _____________________________________________________
4. Элементтен түзілген жай заттың қасиеті _______________________________
[4]
4. Берілген химиялық элементтерді табиғи ұялас топтарына топтастырыңыз және әр топты екі мысалмен толықтырыңыз.
Na, Cl, He, Li, Br, Ne, Rb, I, Kr
|
Табиғи топтар |
Ұялас элементтер |
Мысалдар |
|
Сілтілік металдар |
|
|
|
Галогендер |
|
|
|
Инертті газдар |
|
|
[3]
5. Кестеде бірінші топтың негізгі топша элементінің физикалық және химиялық қасиеттері берілген. Литий элементі үшін бос орындарды өз болжамыңызбен толықтырыңыз.
|
Химиялық элемент |
Валенттілігі |
Физикалық қасиеті |
Сумен әрекеттесуі |
|
Натрий |
І |
Ашық металдық жылтыры бар |
Шабытты |
|
|
|
|
|
[3]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
Ескерту |
|
Білім алушы |
||||
|
Топ, период, атом нөмірінің физикалық мәнін сипаттайды
|
1 |
Атом нөмірінің физикалық мәнін сипаттайды Периодтың физикалық мәнін сипаттайды |
1 1 |
|
|
Элементтер қасиеттерінің топтар мен периодтарда заңдылықпен өзгеретінін түсіндіреді |
2 а) |
Энергетикалық деңгей санының периодты өзгеруін анықтайды |
1 |
|
|
Сыртқы энергетикалық деңгейдегі электрон санының периодты өзгеруін анықтайды |
1 |
|
||
|
2 b) |
Химиялық элементтердің период бойынша өзгеретін қасиеттерін сипаттайды |
1 |
|
|
|
Химиялық элементтердің топ бойынша өзгеретін қасиеттерін сипаттайды |
1 |
|
||
|
Химиялық элементтерді периодтық жүйедегі орны бойынша сипаттайды |
3 |
Химиялық элементтің атомдық нөмірін анықтайды |
1 |
|
|
Периодтық жүйедегі орнын сипаттайды |
1 |
|
||
|
Атом құрамын анықтайды |
1 |
|
||
|
Элемент түзетін жай зат қасиетін сипаттайды |
1 |
|
||
|
Химиялық элементтердің табиғи ұяластарын атайды және олардың таңбасын жазады |
4 |
Сілтілік металдарды анықтайды, мысалдар келтіреді |
1 |
|
|
Галогендерді анықтайды, мысалдар келтіреді |
1 |
|
||
|
Инертті газдарды анықтайды, мысалдар келтіреді |
1 |
|
||
|
Периодтық кестеде орналасуына байланысты химиялық элементтің қасиетін болжайды |
5 |
Химиялық элементтің валенттілігін анықтайды |
1 |
|
|
Химиялық элементтің физикалық қасиетін сипаттайды |
1 |
|
||
|
Химиялық элементтің сумен әрекеттесуін сипаттайды |
1 |
|
||
|
Барлығы |
16 |
|
||
«Химиялық байланыс түрлері» бөлімі бойынша жиынтық бағалау
Оқу мақсаты 8.1.4.1 Электртерістілік ұғымы негізінде атомдар
арасындағы ковалентті байланыстың түзілуін
түсіндіру;
8.1.4.2 Иондық байланыстың түзілу механизмін
сипаттау және иондық қосылыстардың
қасиеттерін болжау;
8.1.4.3 Заттар қасиеттерінің кристалдық тор типтеріне
тәуелділігін түсіндіру.
Бағалау критерийі Білім алушы
-
Берілген формулалардағы электртерістігі үлкен элементті анықтайды
-
Атомдар арасындағы ковалентті байланыстың
түзілуін сипаттайды
-
Иондық байланыстың түзілу механизмін сипаттайды, иондық қосылыстардың қасиеттерін болжайды
-
Заттар қасиеттерінің кристалдық тор типтеріне тәуелділігін түсіндіреді
Ойлау дағдыларының Білу және түсіну деңгейі Қолдану
Жоғары деңгей дағдылары
Орындалу уақыты 20 минут
Тапсырма
1.Берілген формулалардағы электртерістілігі жоғары элементті анықтаңыз.
А) KCl
В) CuS
С) HF
D) CaO
Е) HI [1]
2. а) Атомдар арасында ковалентті байланыстың түзілуін электрондардың ортақ жұбы арқылы түзілуін көрсетіңіз.




![]()
![]()
![]()
сутегі сутегі
Ковалентті байланыстың бұл түрі электртерістілігі қандай атомдар арасында түзіледі ?
Ковалентті байланыстың бұл түрін қалай атайды?
______________________________________________________________________[2]



 b)
b)
![]()
![]()
![]() сутегі
йод
сутегі
йод
Ковалентті байланыстың бұл түрі электртерістілігі қандай атомдар арасында түзіледі ?
Ковалентті байланыстың бұл түрін қалай атайды?
______________________________________________________________________[1]
3. а) Берілген атомдар арасында иондық байланыстың түзілу механизмін көрсетіңіз.






![]()
калий хлор
[1]
b) Құрамында иондық байланысы бар, натрий хлоридінің кейбір физикалық қасиеттері туралы тұжырымдардың шындық не жалған екенін (˅) белгісімен анықтаңыз.
|
Тұжырым |
Шындық |
Жалған |
|
Натрий хлориді қатты, кристалл зат |
|
|
|
Қаттылығы және балқу температурасы төмен |
|
|
|
Суда жақсы ериді, органикалық еріткіште нашар ериді |
|
|
|
Ерітінділері мен балқымалары электр тогын мүлдем өткізбейді |
|
|
|
Балқу температурасы 801ºC |
|
|
[1]
Есептер мен жаттығулар жинағы, 8-сыныпқа арналған оқулық /Ә.Е.Темірбулатова, -Алматы: "Мектеп," 2004 жыл. 100-102 беттер/
4. Берілген заттардың формулалары бойынша кристалдық торын, балқу және қайнау температурасын анықтап, тор көзді толтырыңыз.
|
№ |
Формулалары |
Кристалдық торлардың түрі |
tºқайнау |
tºбалқу |
|
1 |
С |
|
|
|
|
2 |
СО2 |
|
|
|
|
3 |
NaCl |
|
|
|
[2]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / М.Қ.Оспанова, Қ.С.Ахуадиева, Т.Г.Белоусова, - Алматы:Мектеп,2018. 126-136 беттер.
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
|
Білім алушы |
|||
|
Берілген формулалардағы электртерістігі үлкен элементті анықтайды |
1 |
Электртерістігі үлкен элементті анықтайды |
1 |
|
Атомдар арасындағы ковалентті байланыстың түзілуін сипаттайды |
2 а) |
Ковалентті байланыс түрлерін ажыратады |
1 |
|
H2 -молекуласындағы ковалентті байланыстың түзілуі механизмін анықтайды |
1 |
||
|
2 b) |
HI- молекуласындағы ковалентті байланыстың түзілу механизмін құрастырады |
1 |
|
|
Иондық байланыстың түзілу механизмін сипаттайды, иондық қосылыстардың қасиеттерін болжайды |
3 а) |
Калий хлоридіндегі байланыстың түзілу механизмін құрастырады |
1 |
|
3 b) |
Натрий хлоридінің физикалық қасиетін болжап, анықтайды |
1 |
|
|
Заттар қасиеттерінің кристалдық тор типтеріне тәуелділігін түсіндіреді |
4 |
Кристалдық торлар түрін анықтайды |
1 |
|
Балқу және қайнау температурасын анықтайды |
1 |
||
|
Барлығы |
8 |
||
«Ерітінділер және ерігіштік» бөлімі бойынша жиынтық бағалау
Оқу мақсаты 8.3.4.1 Заттардың судағы ерігіштігі бойынша жіктеу;
8.3.4.5 Еріген заттың массалық үлесі мен ерітіндінің
белгілі массасы бойынша еріген заттың
массасын есептеу;
8.3.4.6 Ерітіндідегі заттың молярлық концентрациясын
есептеу.
Бағалау критерийлері Білім алушы:
-
Суда ерігіштігіне байланысты заттарды жіктейді;
-
Массалық үлесі мен ерітіндінің белгілі массасы
бойынша еріген заттың массасын анықтайды;
-
Ерітіндідегі заттың пайыздық және молярлық концентрациясын анықтайды.
Ойлау дағдыларының деңгейлері Білу және түсіну
Қолдану
Орындалу уақыты 20 минут
Тапсырма
1![]()
![]()
![]()

![]()
![]()
![]()
![]()
![]()

Заттар ддддддддддддддллРРРррржжжжжжжжжжжжжжжжЗзЗзвввхххххрррррррррььььтиммЗаттаЗаттарЗзатта
![]()
![]()
![]()
[2]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / М.Қ.Оспанова, Қ.С.Ахуадиева, Т.Г.Белоусова, - Алматы:Мектеп,2018.138-141 беттер.
2. Натрий хлоридінің массалық үлесі 10% -тік массасы 300 г ерітіндісін даярлау үшін қажетті тұз бен судың массаларын есептеңіз.
|
|
[3]
3. а) Айран ұйыту үшін 4 кг сүтке 40 г ұйытқы салынды. Айран ұйытқының массалық үлесін есептеңіз.
|
|
[2]
b) Калий гидроксидінің көлемі 1500 мл ерітіндісінде 16 г еріген зат болса, осы ерітіндінің молярлық концентрациясы қанша болатынын есептеңіз.
|
|
[2]
Есептер мен жаттығулар жинағы, 8-сыныпқа арналған оқулық /Ә.Е.Темірбулатова, -Алматы: "Мектеп," 2004 жыл. 56-63 беттер/
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
|
Білім алушы |
|||
|
Суда ерігіштігіне байланысты заттарды жіктейді |
1 |
заттарды суда ерігіштігіне байланысты жіктейді |
1 |
|
әр түріне бір-екі мысалдан келтіреді |
1 |
||
|
Массалық үлесі мен ерітіндінің белгілі массасы бойынша еріген заттың массасын анықтайды |
2 |
еріген заттың және еріткіштің массасын табуға арналған формуланы қолданады |
1 |
|
еріген затты анықтайды |
1 |
||
|
еріткіштің массасын анықтайды |
1 |
||
|
Ерітіндідегі заттың пайыздық және молярлық концентрациясын анықтайды |
3 а) |
массалық үлесті табуға арналған формуланы қолданады |
1 |
|
массалық үлесті анықтайды |
1 |
||
|
3 b) |
ерітіндегі заттың молярлық концентрациясын табуға арналған формуланы қолданады |
1 |
|
|
ерітіндінің молярлық концентрациясын анықтайды |
1 |
||
|
Барлығы |
9 |
||
«Бейорганикалық қосылыстардың негізгі кластары. Генетикалық байланыс» бөлімі бойынша жиынтық бағалау.
Оқу мақсаты 8.3.4.7 Оксидтердің жіктелуін және қасиеттерін сипаттайтын
реакция теңдеулерін құрастыру;
8.3.4.8 Қышқылдардың жіктелуін, қасиеттерін білу және түсіну,
олардың химиялық қасиеттерін сипаттайтын реакция теңдеулерін
құрастыру;
8.3.4.9 Негіздердің жіктелуі мен қасиеттерін білу және түсіну,
олардың химиялық қасиеттерін сипаттайтын реакция
теңдеулерін құрастыру;
8.3.4.12 Бейорганикалық қосылыстардың негізгі кластары
арасындағы генетикалық байланысты зерттеу.
Бағалау критерийлері Білім алушы:
● Оксидтердің, қышқылдардың және негіздердің
жіктелуін, қасиеттерін анықтайды, реакция
теңдеулерін құрастырады
●Бейорганикалық қосылыстардың негізгі кластары
арасындағы генетикалық байланысты анықтайды
Ойлау дағдыларының деңгейлері Білу және түсіну
Қолдану
Орындалу уақыты 25 минут
Тапсырма
1. Калий оксидіне ( K2O) қатысты тұжырымды (-дарды) анықтаңыз.
А) қышқылдық
В) екі дайлы
С) негіздік
D) тұз түзетін
Е) түз түзбейтін
[1]
2. Сызбанұсқасы берілген, нүктелердің орнына тиісті формулаларды жазып, реакция теңдеуін құрастырыңыз.
CaO + H2O → …
Li2O +…→ LiCl +H2O
SO2 + NaOH →… + …
N2O5 + ...→ HNO3
BeO + KOH→ … + H2O
ZnO + HCl → … + H2O
[3]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / М.Қ.Оспанова, Қ.С.Ахуадиева, Т.Г.Белоусова, - Алматы:Мектеп,2018.153-154 беттер.
3. а) Берілген қышқылды жіктелуі бойынша сипаттаңыз.

құрамы бойынша
_............................___________________________


негізділігі бойынша
...............................


![]()
![]()
H2SiO3
ерігіштігі бойынша
.................................
[3]
b) Күкірт қышқылын мырыш оксидімен әрекеттесу реакция теңдеуін құрастырыңыз.
______________________________________________________________________
[1]
4. а) Суда еритін және суда ерімейтін негіздерді сәйкестендіріңіз.
|
№ |
Түрлері |
Негіздердің формулалары |
|
1
|
суда еритін негіздер (сілтілер) |
А. Cu(OH)2 |
|
В. LiOH |
||
|
С. Fe(OH)3 |
||
|
D. NaOH |
||
|
2
|
суда ерімейтін негіздер |
Е. Zn(OH)2 |
|
F. Al(OH)3 |
||
|
G. Ca(OH)2 |
||
|
H. KOH |
1._____________________________________
2._____________________________________
[2]
ә) Негіздердің қышқылдармен бейтараптану реакциясына бір мысал келтіріңіз.
____________________________________________________________________
[1]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / М.Қ.Оспанова, Қ.С.Ахуадиева, Т.Г.Белоусова, - Алматы:Мектеп,2018. 167-169-беттер.
5. Берілген заттардың формулаларын қолданып, генетикалық қатар құрыңыз.
K2O , H3PO4, K2CO3, P, Ca3(PO4)2 , P2O5, Na, NaOH, K
______________________________________________________________________
[2]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
|
Білім алушы |
|||
|
Оксидтердің, қышқылдардың және негіздердің жіктелуін, қасиеттерін анықтайды, реакция теңдеулерін құрастырады |
1 |
Калий оксидіне қатысты тұжырымдарды анықтайды. |
1 |
|
2 |
Негіздік оксидтердің сумен және қышқылдар мен реакция теңдеуін құрастырады. |
1 |
|
|
Қышқылдық оксидтердің сумен және сілтілермен реакция теңдеуін құрастырады. |
1 |
||
|
Екідайлы оксидтердің сілтілермен және қышқылдармен реакция теңдеуін құрастырады. |
1 |
||
|
3 а) |
Қышқылдарды құрамы бойынша жіктейді. |
1 |
|
|
Қышқылдарды негізділігі бойынша жіктейді. |
1 |
||
|
Қышқылдарды ерігіштігі бойынша жіктейді. |
1 |
||
|
3 b) |
Күкірт қышқылымен мырыш оксидінің арасындағы реакция теңдеуін құрастырады. |
1 |
|
|
4 |
Суда еритін негіздерді сәйкестендіреді. |
1 |
|
|
Суда ерімейтін негіздерді сәйкестендіреді. |
1 |
||
|
Негіздердің бейтараптану реакциясына мысал келтіріп жазады. |
1 |
||
|
Бейорганикалық қосылыстардың негізгі кластары арасындағы гентикалық байланысты анықтайды |
5
|
Берілген заттардың формулаларын қолданып, генетикалық қатар құрыңыз. |
2 |
|
Барлығы |
13 |
||
8.4 В «Көміртек және оның қосылыстары» тарауы бойынша жиынтық бағалау
|
Оқу мақсаты |
8.4.3.1 Көміртек неліктен көптеген қосылыстарында төрт байланыс түзетінін түсіндіру; |
|
|
8.4.3.3 Көміртектің аллотропиялық түр өзгерістерінің құрылысын және қасиеттерін салыстыру; |
|
|
8.4.3.5 Көміртектің физикалық және химиялық қасиеттерін зерттеу; |
|
|
8.4.3.7 Көмірқышқыл газын ала алу, оны анықтау және қасиеттерін зерттеу. |
|
Бағалау критерийі |
Білім
алушы |
|
|
• Көміртектің аллотропиялық түр өзгерістерінің құрылысын және қасиеттерін салыстырады; |
|
|
• Көміртек минералдарының: мрамор мен магнезиттің формуласын анықтайды және олардың құрамындағы көміртектің массалық үлесін есептейді; |
|
|
• Көміртектің физикалық және химиялық қасиеттерін сипаттайтын химиялық реакцияларды құрады; |
|
|
• Зертханада көмірқышқыл газын алып, оны анықтайды, қасиеттерін сипаттайды. |
|
Ойлау дағдыларының деңгейі |
Қолдану, жоғарғы деңгей |
|
Орындау уақыты |
20 минут |
Тапсырмалар
1. Бос орындарға қажетті сөздерді қойыңыз.
Көміртек __________ периодта ________топта орналасқан, _____________ байланыс түзеді,_______ электрон қосып алады және___________электрон беріп жібере алады. Қосылыстарында_________ тотығу дәрежесін көрсетеді және ___________ валентті.
[1]
2. Көміртек мрамор және магнезит минералдарының құрамына кіреді. Қай минералдың құрамында көміртектің массалық үлесі көп екенін анықтаңыз.
|
|
[5]
3. Көміртектің аллотропиялық түр өзгерістері мен қолдану саласы арасындағы сәйкестікті бағдарша арқылы көрсетіңіз.
|
Аллотропиялық түр өзгерістері |
Қолданылуы |
|
Графит |
Лазер қондырғыларында, қымбат тастар. |
|
Карбин |
Микроэлектроникадағы нанотүтікшелер |
|
Алмаз |
Қарындаш, қара бояу, электродтар. |
|
Фуллерен |
Жасанды қан тамырлары. |
[4]
4. Реакция теңдеуін аяқтаңыз:
-
С + Ва→ ________________________________________________
-
C + Al2O3→_______________________________________________
-
C + O2(жеткіліксіз)→__________________________________________
[3]
5. «+» белгісі арқылы көмірқышқыл газының физикалық қасиеті мен алынуына байланысты шындық, жалған тұжырымдарды анықтаңыз.
|
Тұжырымдар |
Шындық |
Жалған |
|
1. Түссіз, иіссіз, дәмсіз газ |
|
|
|
2. Мрамор мен тұз қышқылының әрекеттесуі арқылы алынады. |
|
|
|
3. Ауадан жеңіл. |
|
|
|
4. Көмір жанғанда пештерді оттек жеткіліксіз жағдайларда түзіледі. |
|
|
[1]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
|
Көміртектің қосылыстарында көбінесе 4 байланыс түзетінін түсіндіреді. |
1 |
Периодтық жүйедегі орны бойынша көміртек атомының валенттік мүмкіндігін анықтайды. |
1 |
|
Минералдардың формуласы анықтап, құрамындағы көміртектің массалық үлесі қайсысында көбірек екенін есептейді. |
2 |
Мрамордың формуласын жазады. |
1 |
|
Магнезиттің формуласын жазады. |
1 |
||
|
Мрамордың құрамындағы көміртектің массалық үлесін есептейді. |
1 |
||
|
Магнезиттің құрамындағы көміртектің массалық үлесін есептейді. |
1 |
||
|
Мрамор мен магнезиттің құрамындағы көміртектің массалық үлестерін салыстырады. |
1 |
||
|
Көміртектің аллотропиялық түр өзгерістерінің қолданылу салаларын зерттейді. |
3 |
Графиттің қолданылу саласын анықтайды. |
1 |
|
Алмаздың қолданылу саласын анықтайды. |
1 |
||
|
Карбиннің қолданылу саласын анықтайды. |
1 |
||
|
Фуллереннің қолданылу саласын анықтайды. |
1 |
||
|
Көміртектің химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрады. |
4 |
Көміртек пен барийдің арасындағы химиялық реакция теңдеуін жазады. |
1 |
|
Көміртек пен алюминий оксидінің арасындағы химиялық реакция теңдеуін жазады. |
1 |
||
|
Көміртектің оттек жеткіліксіз жағдайындағы химиялық реакция теңдеуін жазады. |
1 |
||
|
Көмірқышқыл газының қасиетін және алыну жолдарын сипаттайды. |
5 |
Көмірқышқыл газын сипаттайтын дұрыс жауаптарды таңдайды. |
1 |
|
Жалпы балл |
14 |
||
8.4С «Су» бөлімі бойынша жиынтық бағалау
|
Оқу мақсаты:
|
8.4.2.6. Судың кең таралуын, ерекше қасиеттерін және адам өміріндегі маңызын түсіндіру; |
|
|
8.4.2.7 Табиғаттағы судың айналымын түсндіру; |
|
|
8.4.2.9 Судың кермектігін және оны жою жолдарын түсіндіру. |
|
Бағалау критерийлері:
|
Білім алушылар:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ойлау дағдыларының деңгейі: |
Білу, түсіну және қолдану. |
|
Орындау уақыты: |
20 минут |
Тапсырмалар:
1. Келесі сөйлемдерге қажетті сөздерді қойып, сөйлемдерді аяқтаңыз:
Су әмбебап ........................................................................................................................
Судың агрегаттық күйлері: ...................................................................................................
Судың қайнау температурасы...............................................................................................
Судың қату температурасы ..................................................................................................
Судың тығыздығы .................................................................................................................
Табиғи судың құрамында ....................................................................................................
[3]
2. Шындық пен жалған тұжырымдарды « + », « - » таңбаларымен анықтаңыз:
|
Тұжырымдамалар |
Шындық |
Жалған |
|
Судың молекуласының құрылысы сызықтық |
|
|
|
Адам организмі 70 % судан тұрады |
|
|
|
CuSO4* 5 H2O мыс купоросы көгілдір түсті |
|
|
|
Су белсенді металдармен және олардың оксидтерімен әрекеттеспейді |
|
|
|
Сүйектегі судың мөлшері 31% |
|
|
[2]
3. «Судың кермектігінің түрлері» кестесін толтырыңыз:
|
Кермектік түрлері |
Кермектікті жою жолдары (реакция теңдеулері) |
|
Уақытша (карбонатты) кермектік судың құрамында
__________________________ болуына байланысты. |
_________________________________________ |
|
Тұрақты кермектік судың құрамында
__________________________ болуына байланысты. |
_________________________________________________ |
[4]
4![]() . а ) Суды тазалау этаптарын
көрсетіңіз:
. а ) Суды тазалау этаптарын
көрсетіңіз:
![]()
![]()
![]()
![]()
b) Суды дезинфекциялайтын зат формуласын анықтаңыз:
А) Cl2
Б) I2
В) F2
С) P
[2]
5. Судың табиғаттағы айналымы схемасындағы бос жерлерді толтырыңыз:
![]()
![]()
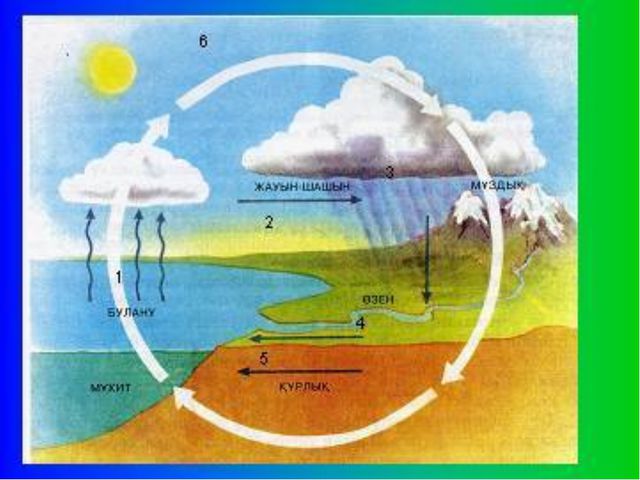
https://infourok.ru/prezentaciya-k-otkritomu-uroku-krugovorot-vodi-v-prirode-1721776.html
[2]
Балл қою кестесі
|
Бағалау критерийлері |
№ |
Дескрипторлар |
Балл |
|
Оқушылар |
|
|
|
|
Судың физикалық қасиеттерін сипаттайды; |
1 |
Судың агрегаттық күйлерін дұрыс анықтайды. |
1 |
|
Судың қайнау және балқу температурасын дұрыс жазады. |
1 |
||
|
Судың ерекшелігін сипаттайды. |
1 |
||
|
Су молекуласының құрылысын және қасиеттерін анықтайды; |
1 |
Судың қасиеттерін сипаттайтын шындық, жалған тұжырымдарды дұрыс анықтайды. |
2 |
|
Судың кермектігін және оны жою жолдарын сипаттайды; |
1 |
Суды қайнату арқылы гидрокарбонаттарды ыдырату теңдеуін жазады. |
1 |
|
Соданың гидрокарбонатқа әсерін сипаттайтын реакция теңдеуін жазады. |
1 |
||
|
Ізбес суының судың кермектігін жою теңдеуін жазады. |
1 |
||
|
Соданың сульфаттарды жою теңдеуін жазады. |
1 |
||
|
Суды тазалау процесін сипаттайды; |
2 |
Суды тазалау этаптарын дұрыс жазады. Суды дезинфекциялауға арналған заттың формуласын табады. |
1 1 |
|
Табиғаттағы судың айналымын сипаттайды. |
1 |
Судың булануын жазады. Бұлттың түзілуін жазады. |
1 1 |
|
Барлығы |
13 |
||
I ТОҚСАННЫҢ ЖИЫНТЫҚ БАҒАЛАУ СПЕЦИФИКАЦИЯСЫ
I тоқсанның жиынтық бағалауына шолу
Жиынтық бағалаудың өткізілу уақыты - 40 минут
Балл саны - 25
Тапсырмалар түрлері:
КТБ- Көп таңдауды бар тапсырмалар;
ҚЖ- Қысқа жауапты қажет ететін тапсырмалар;
ТЖ -Толық жауапты қажет ететін тапсырмалар.
Жиынтық бағалаудың құрылымы
Берілген нұсқа көп таңдауы бар тапсырмаларды, қысқа және толық жауапты қажет ететін сұрақтарды қамтитын 12 тапсырмадан тұрады. Көп таңдауы бар тапсырмаларға оқушылар ұсынылған жауап нұсқаларынан дұрыс жауабын таңдау арқылы жауап береді.
Қысқа жауапты қажет ететін сұрақтарға сөздер немесе қысқа сөйлемдер түрінде жауап береді. Толық жауапты қажет ететін сұрақтарда оқушыдан жоғары балл жинау үшін тапсырманың шешімін табудың әр қадамын анық көрсетуі талап етіледі. Оқушының тапсырмаларды орындауда тиімді тәсілдерді таңдай білуі және оны қолдана алу қабілеті бағаланады. Тапсырмалардың ішінде бірнеше құрылымдық бөліктерден/сұрақтардан тұратын түрлеріде кездеседі.
I тоқсан бойынша жиынтық бағалау тапсырмаларының сипаттамасы
|
Бөлім |
Тексерілетін мақсат |
Ойлау дағдыларының деңгейі |
Тапсы рма саны* |
№ тапсыр ма* |
Тапсыр ма түрі* |
Орын дау уақыты, мин* |
Балл* |
Бөлім бойынша балл |
|
Атомдағы электрондарды ң қозғалысы |
8.1.3.1 Атомда электрондар ядродан арақашықтығы артқан сайын біртіндеп энергетикалық деңгейлер бойынша таралатынын түсіну |
Білу және түсіну |
1 |
2 |
КТБ |
2 |
1 |
8 |
|
8.1.3.4 Алғашқы 20 химиялық элементтің электрондық конфигурациясын және электронды- графикалық формуларын жаза білу |
Қолдану |
1 |
6 |
ТЖ |
6 |
2 |
||
|
8.1.3.5 Атомдар электрондарды қабылдай немесе жоғалта алатынын және осының нәтижесінде иондар түзілетінін түсіну |
Білу және түсіну |
2 |
1,5 |
КТБ |
5 |
3 |
||
|
8.1.3.6 «Нольдік қосынды» әдісімен қосылыстардың формуласын құрастыру |
Қолдану |
1 |
3 |
ҚЖ |
3 |
2 |
||
|
Заттардың формулалары және химиялық реакция теңдеулері |
8.2.3.1 Заттар құрамындағы элементтердің массалық үлесін табу, элементтердің массалық үлесі бойынша заттардың формуласын шығару |
Қолдану |
2 |
9 |
ТЖ |
6 |
3 |
8 |
|
8.2.3.3 Реакцияға қатысатын және түзілетін заттардың формуласын жаза отырып, химиялық реакциялар теңдеулерін құру; |
Қолдану |
1 |
4 |
КЖ |
2 |
2 |
||
|
8.2.2.1 Бастапқы және түзілген заттардың саны мен құрамы бойынша химиялық реакцияларды жіктеу |
Білу және түсіну |
2 |
7,8 |
ҚЖ |
2 |
3 |
||
|
Металдар белсенділігін салыстыру |
8.2.4.3 Металдар коррозиясын туындатуға әсер ететін жағдайларды зерттеу |
Жоғарғы деңгей дағдылары |
1 |
10 |
ТЖ |
4 |
4 |
9 |
|
8.2.2.5 Металдардың қышқылдармен әрекеттесуінің реакция теңдеулерін құрастыру |
Қолдану |
1 |
11 |
ҚЖ |
5 |
2 |
||
|
8.2.4.8 Металдардың белсенділік қатарын қолданып металдардың таныс емес орынбасу реакцияларының жүру мүмкіндігін болжау |
Жоғарғы деңгей дағдылары |
1 |
12 |
ТЖ |
5 |
3 |
||
|
Барлығы |
|
|
|
|
|
|
25 |
|
«Химия» пəнінен I тоқсанға арналған жиынтық бағалаудың тапсырмалары
1. Натрий атомы үшін дұрыс тұжырымдарды анықтаңыз.
1) Натрийдің сыртқы электрондық қабатында 1 электрон бар
2) Натрий сыртқы қабатындағы 1 электронды беріп жібере алады
3) Натрий сыртқы қабатына 2 электрон қосып алады
4) Na+ ионын түзе алады
5) Na1 ионын түзе алады
A) 3,5
B) 2,4
C) 1,2,4
D) 3,4,5
[1]
2. 1, 2, 3 және 4 - энергетикалық деңгейлердегі электрондардың
максимал санының өсу ретімен орналасқанын белгілеңіз.
A) 2е; 4е; 8е; 18е B) 2е;8е; 32е; 18е C) 2е; 8е; 18е; 32е D) 8е; 18е; 32е; 2е
[1]
3. Төменде берілген қосылыстардың формуласын «нольдік қосынды»
әдісі бойынша құрастырыңыз:
-
Fe3+ және S2-
-
Cl7+ және O2-
[2]
4. Фосфор оттекпен жарық шығара отырып, қарқынды жанып, фосфор(V) оксидін түзеді. Фосфор(V) оксиді суда ерігенде фосфор қышқылы түзіледі. Осы өзгерістерді сипаттайтын реакция теңдеулерін жазып көрсетіңіз.
1) Фосфордың жануы
2) Фосфор(V) оксидінің сумен әрекеттесуі
[2]
5. Кестеде берілген атомдар мен иондарды электрондық формуласымен cәйкестендіріңіз.
-
Атомдар мен иондар
Электрондық формуласы
А. Al3+
1. 1s22s22p63s23p64s2
В. Са
2. 1s22s22p63s23p6
С. Сl1-
3. 1s22s22p63s2
D. Mg
4. 1s22s22p6
A.____ B._____ C._____ D._____
[2]
6. Алюминий – күміс түсті ақ металл, жылуды және электр тогын жақсы өткізеді. Жер қыртысында таралуы бойынша элементтер арасында 4-, металдар арасында 1- орында. Табиғатта оның жүздеген минералдары кездеседі.
https://kk.wikipedia.org/wiki
Алюминийдің периодтық жүйедегі орнын ескере отырып оның электрондық конфигурациясы мен электронды-графикалық формуласын жазып кестені толтырыңыз.
|
Электрондық конфигурациясы |
Электронды-графикалық формуласы |
|
|
|
[2]
7. Кестеде берілген химиялық реакциялардың типтерін анықтаңыз.
|
№ |
Химиялық реакция теңдеулері |
Реакция типі |
|
1 |
MgO + SO2 → MgSO3 |
|
|
2 |
Cu + HgCI2 → Hg + CuCI2 |
|
|
3 |
Cu(OH)2 → CuO + H2O |
|
|
4 |
3NaOH + FeCI3 → Fe(OH)3↓ + 3NaCI |
|
[2]
8. Сөйлемді мұқият оқып, бос орындарды толтырыңыз:
Бір күрделі зат айырылып, нәтижесінде бірнеше жай немесе күрделі заттар түзілетін реакция _________________________ реакциясы деп аталады.
[1]
9. Ас содасы ақ түсті, кристалды ұнтақ. Улы емес, өртенбейді, жарылмайды. Медицинада, химиялық өнеркәсібінде, тамақ өнеркәсібінде т.б. қолданылады.
Ас содасының құрамы 27,38% натрий, 1,19% сутек, 14,29% көміртек, 57,14% оттектен тұратындығы белгілі болса ас содасының формуласын жазыңыз.
[3]
https://kk.wikipedia.org/wiki/
_________________________________________________________________________________
10. Металдар мен құймалар әр түрлі заттармен жанасқанда, олармен әрекеттесіп, химиялық қосылыстар түзеді. Әсіресе жаңбыр, топырақ ылғалы, ауа әсерінен қоршаған ортадағы металдар бүлініп желінеді. Бұл кезде металдан жасалған бұйымның қасиеті мүлдем өзгеріп, ол біртіндеп бүліне бастайды. Бұл өте зиянды әрі қауіпті процесс жемірілу деп аталады (коррозия — лат. korrosio — желіну деген сөз).
(a) Алюминийден жасалған бұйымдармен салыстырғанда, темірден жасалған бұйымдардың жылдам жемірілуге ұшырауының себебін түсіндіріңіз.
______________________________________________________________________________________________________________________________________________
__________________________________________________________________
[2]
(b) Коррозиядан қорғаудың кез-келген екі жолын ұсыныңыз:
![]()
______________________________________________________________________
[2]
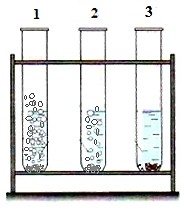 11(a) Суретте металдардың
қышқылдармен
11(a) Суретте металдардың
қышқылдармен
әрекеттесуі көрсетілген:
№1 сынауықта – реакция шабытты жүріп, көп
мөлшерде газ бөлінеді;
№2 сынауықта – реакция белсенді жүріп, газ бөлінеді;
№3 сынауықта – реакция белгілері байқалмайды.
https://www.google.kz/search
Тапсырма:
№1 және №2 сынауықтардағы металдарды
анықтаңыз:
№1 сынауық
№2 сынауық
[2]
(b) Анықталған №1 және №2 сынауықтардағы металдардың қышқылмен әрекеттесу реакция теңдеуін жазып теңестіріңіз.
_________________________________________________________________________________________________________________________________________
12. Арман кобальт металының белсенділігін тексеріп көру үшін оны ішінде әртүрлі ерітінділер бар стаканға салып, тәжірибе жасады.
а) Төменде берілген кестеге «+» немесе «-» белгісін қою арқылы кобальт металының қайсыларымен әрекеттескенін анықтаңыз.
-
-
-
-
AgNO3
HCl
ZnSO4
CaCl2
Со
-
-
-
b) Кобальт металының осындай қасиет көрсетуінің себебін түсіндіріңіз.
![]()
[3]
|
Балл қою кестесі |
||||||||||||||
|
№ |
Жауап |
Балл |
Қосымша ақпарат |
|||||||||||
|
1 |
C |
1 |
|
|||||||||||
|
2 |
C |
1 |
|
|||||||||||
|
3 |
Fe2S3 |
1 |
|
|||||||||||
|
Cl2O7 |
1 |
|||||||||||||
|
4 |
4P + 5O2→ 2P2O5 |
1 |
|
|||||||||||
|
P2O5+3H2O→2 H3 PO4 |
1 |
|||||||||||||
|
5 |
А.4 В.1 |
1 |
Кез келген екі дұрыс жауап үшін 1 балл |
|||||||||||
|
С.2 Д.3 |
1 |
|||||||||||||
|
6 |
1s 22s22p63s23p1 |
1 |
|
|||||||||||
|
|
1 |
|||||||||||||
|
7 |
1 |
Қосылу |
1 |
Кез келген екі дұрыс жауап үшін 1 балл |
||||||||||
|
2 |
Орынбасу |
|||||||||||||
|
3 |
Айырылу |
1 |
||||||||||||
|
4 |
Алмасу |
|||||||||||||
|
8 |
Алмасу |
1 |
Басқа жауап Қабылданбайды. |
|||||||||||
|
9 |
NaxHyCzOn= ω /Ar: ω/Ar: ω /Ar |
1 |
|
|||||||||||
|
ω(Na): ω (H): ω(C) : ω (O) =27,38/23: 1,19/1: 14,29/12: 57,14/16 =1:1:1:4 |
1 |
|
||||||||||||
|
NaHCO3 |
1 |
|
||||||||||||
|
10 |
Алюминий металының бетінде оксидтен тұратын өте жұқа қабықша пайда болып, металды қоршаған ортамен жанасудан сақтап тұрады. |
1 |
|
|||||||||||
|
Темір металында ондай оксидтен тұратын қабықша жоқ. Темірдің таттануы оттектің әсерінен болады. |
1 |
Басқаша тұжырымдалған дұрыс жауаптарда қабылданады. |
||||||||||||
|
Металл бетін жемірілуге қарсы тұрақты қабатпен қаптау. |
1 |
Мысалы: лакпен, бояумен т.с.с жауаптарда қабылданады |
||||||||||||
|
Жемірілуді баяулататын тежегіш(ингибитор) заттарды енгізу. |
1 |
|
||||||||||||
|
11 |
№1 сынауықтағы магний Mg +2HCl = MgCl2+H2 |
1 |
||||||||||||
|
№2 сынауықтағы мырыш Zn +2HCl = ZnCl2+H2 |
1 |
|||||||||||||
|
12 |
|
1
|
Zn, Ca металдары активтік қатарда Со алдында тұр. Сондықтан оларды ығыстыра алмайды деген жауап қабылданады. |
|||||||||||
|
Кобальт металы активтік қатарда өзінен кейінгілерін тұздар ерітіндісінен ығыстырып шығарады. |
1 |
|||||||||||||
|
Активтік қатарда сутекке дейін орналасқан металдар сутекті қышқылдардан ығыстыра алады. |
1 |
|||||||||||||
|
|
Барлығы |
25 |
|
|||||||||||
2-ТОҚСАННЫҢ ЖИЫНТЫҚ БАҒАЛАУ СПЕЦИФИКАЦИЯСЫ
2-тоқсанның жиынтық бағалауына шолу
Жиынтық бағалаудың өткізілу уақыты – 40 минут
Балл саны - 25
Тапсырмалар түрлері:
КТБ – Көп таңдауы бар тапсырмалар;
ҚЖ – Қысқа жауапты қажет ететін тапсырмалар;
ТЖ – Толық жауапты қажет ететін тапсырмалар.
Жиынтық бағалаудың құрылымы
Ұсынылған нұсқада көп жауапты таңдауы бар сұрақтар, қысқа және толық жауапты қажет ететін құрылымдастырылған сұрақтардан тұратын тапсырмалар қолданылады. Нұсқада 11 тапсырма бар.
Көп таңдауы бар тапсырмаларға оқушылар бір немесе бірнеше дұрыс жауабын таңдау және сәйкестендіру арқылы жауап береді.
Қысқа жауапты қажет ететін сұрақтарға оқушылар қажетті сөздерді бос орындарға толтыру және сұрақтарға қысқа жауап беру арқылы жауап береді.
Толық жауапты қажет ететін сұрақтар оқушылардың формулаларды қолданып, химиялық есептерді шығару дағдысын, заттардың химиялық қасиеттеріне сәйкес химиялық реакция теңдеулерін жазу дағдысын, химиялық реакциялардың жүру процестерін түсіндіру және салдарларын көрсететін логикалық ойлау дағдысын, стехиометриялық есептер шығару дағдысын, химиялық реакция теңдеуін құру дағдысын көрсетеді.
2-тоқсан бойынша тапсырмаларының сипаттамасы
|
Бөлім |
Тексерілетін мақсат |
Ойлау дағдылары-ның деңгейі |
Тапсырма саны * |
№ тапсырма * |
Тапсыр-ма түрі * |
Орындау уақыты * |
Балл * |
Бөлім бойынша балл |
|
Зат мөлшері |
8.1.1.3 Масса, зат мөлшері және құрылымдық бөлшектер санын анықтау |
Қолдану |
2 |
1, 2 |
КТБ |
4 |
3 |
3 |
|
Сехио-метрия-лық есептеу-лер |
8.2.3.5 Химиялық реакция теңдеулері бойынша заттың массасын, зат мөлшерін есептеу |
Қолдану |
1 |
6 |
ТЖ |
4 |
2 |
6 |
|
8.2.3.6 Авогадро заңын білу және қалыпты және стандартты жағдайдардағы газдар көлемін есептеуде молярлық көлемді қолдану |
Қолдану |
2 |
3, 4 |
КТБ |
6 |
4 |
||
|
Химия-лық реакциядағы энергиямен танысу |
8.3.1.1 Заттың жану реакциясының өнімі көбінесе оксид екенін және құрамында көміртегі бар отын оттекте жанғанда, көмірқышқыл газы, иіс газы немесе көміртек түсілетінін түсіну |
Білу және түсіну |
1 |
5 |
ҚЖ |
3 |
2 |
6 |
|
8.3.1.3 Экзотермиялық реакциялар жылу бөле жүретінін, ал эндотермиялық реакциялар жылу сіңіре жүретінін білу |
Білу және түсіну |
1 |
7 |
ҚЖ |
2 |
2 |
||
|
8.3.1.5 Энергия өзгерісін бөлшектердің кинетикалық теориясы тұрғысынан түсіндіру |
Жоғары деңгей дағдылары |
1 |
11 |
ТЖ |
6 |
2 |
||
|
Сутек. Оттек және озон |
8.4.2.1 Сутекті алу және оның қасиеттері мен қолданылуын зерттеу |
Қолдану |
1 |
8 |
ТЖ |
5 |
4 |
10 |
|
8.4.2.3 Оттекті алу және оның қасиеттері мен қолданылуын зерттеу |
Қолдану |
1 |
9 |
ҚЖ/ТЖ |
5 |
4 |
||
|
8.4.2.5 Жер бетіндегі озон қабатының маңызын түсіндіру |
Білу және түсіну |
1 |
10 |
ТЖ |
5 |
2 |
||
|
|
Барлығы |
|
11 |
|
|
40 |
25 |
25 |
«Химия» пәнінен 2-тоқсанға арналған
жиынтық бағалаудың тапсырмалары
1. Молекула саны 128 г көмірқышқыл газында қанша атом оттек бар екенін анықтаңыз.
A) 6,023*1023
B) 17,52*1023
C) 24,10*1023
D) 27,53*1023
E) 48,18*1023 [1]
2. 0,5 моль алюминий сульфидінің (Al2S3) массасы мен молекула санын анықтаңыз.
A) 29,5 г
B) 43 г
C) 61,5 г
D) 75 г
E) 3,01*1023
F) 6,02*1023
G) 12,04*1023 [2]
3. Төменде берілген газдарға арналған Авогадро заңы туралы тұжырымдардың шындық не жалған екенін (˅) белгісімен анықтаңыз.
|
Тұжырым |
Шындық |
Жалған |
|
Мольдік көлемнің мәні тұрақсыз шама. |
|
|
|
Мольдік көлем арқылы газдардың көлемін есептеуге болады. |
|
|
|
Қалыпты жағдайда кез келген заттың көлемдері бірдей болады. |
|
|
|
Кез келген жағдайда көлемдері бірдей газдардың массалары тең болады. |
|
|
|
Қалыпты жағдайда 1 моль оттектің көлемі 1 моль көмірқышқыл газының көлеміне тең. |
|
|
[1]
4. Төменде берілген заттардың мәндері мен көлемдері арасындағы сәйкестікті анықтаңыз.
|
Заттардың мәні |
Көлем |
|
1) 0,5 моль азот |
A) 11,2 л |
|
2) 32 г метан (СН4) |
B) 33,6 л |
|
3) 1,5 моль аммиак (NH3) |
C) 44,8 л |
1)________ 2) _____________ 3) __________ [3]
5. Күнделікті тұрмыста әртүрлі заттардың жануын байқайсыңдар. Төменде берілген жану реакциялары тұжырымдарының бос орындарын қажетті сөздермен толықтырыңыз.
Жану ________ реакция болып табылады, себебі реакция нәтижесінде жылу мен жарық бөлінеді. Жану реакциясының негізгі белгісі – реагент ретінде жануды қолдайтын ____________ болуы және реакция нәтижесінде _____________ _______, су және жылудың бөлінуі. Жану реакциясының өнімі ___________ деп аталады. Отын толық жанғанда ___________ _____ бөлінеді, шала жану кезінде ___ _____ және ______ бөлінеді, олар улы газдар.
Қажетті сөздер: көмірқышқыл газы, оттегі, иіс газы, оксид, күйе, химиялық, көмірқышқыл газы
[2]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / М.Қ.Оспанова, Қ.С.Аухадиева, Т.Г.Белоуосова. – Алматы: Мектеп, 2018
6. Сутегі – ХХІ ғасырдың отыны. Оны суды айыру арқылы зертханада алуға болады. 4 г сутегін алу үшін қажет судың массасы мен зат мөлшерін анықтаңыз.
[2]
7. Берілген эндотермиялық және экзотермиялық реакцияға байланысты тұжырымдардың бос орындарын қажетті сөздермен толықтырыңыз.
Найзағай кезінде озонның түзілуінде энергия __________. Табиғи газ жанғанда энергия ________. Жылу бөле жүретін реакцияларда кинетикалық энергия ________. _____________ рeaкцияда температура төмендейді. Экзотермиялық реакцияда зат бөлшектері ______ жылдамдықпен қозғалады.
Қажетті сөздер: эндотермиялық, жоғарылайды, жоғары, бөлінеді, сіңіріледі
[2]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / М.Қ.Оспанова, Қ.С.Аухадиева, Т.Г.Белоуосова. – Алматы: Мектеп, 2018
8. Сутегі – ең кең тараған элемент, тіпті Күн массасының 75%-н құрайды.
a) Сутектің қолданылу салаларына екі мысал келтіріңіз:
1)____________________________________________________________
2)____________________________________________________________
[1]
b) Төменде берілген айналымдарды іске асыруға мүмкін реакция теңдеулерін жазыңыз.
1 2
С → H2 → NH3
↓ 3
NaH
1)_________________________________________________________________2)_________________________________________________________________3)________________________________________________________________
[3]
9. Оттегі адамдардың есте сақтау, назар аудару және физикалық қасиеттерін арттырады. Организмге түскен оттектің 20%-ы мидың жұмысына жұмсалады. Оттегінің химиялық белсенділігі де жоғары.
а) Оттектің берілген заттармен әрекеттесуінің реакция теңдеулерін жазыңыз:
1) Al
2) Са
_________________________________________________________________________________________________________________________________
[2]
b) Оттектің қолданылатын салаларын анықтаңыз.
A) метил спиртін алуда
B) тұз қышқылын алуда
C) су астында тыныс алуға
D) мұнай өнімдерін өңдеуде
E) қатты майларды алуда
[1]
с) Оттекті күрделі заттарды қыздырып, айыру арқылы алады. Өршіткі марганец (ІV) оксидінің қатысында сутек пероксиді (Н2О2) шабытты реакцияға түсіп, оттек газын түзеді. Реакция теңдеуін жазыңыз.
[1]
10. Адам тіршілігінің нәтижесінде озон қабаты жұқарады. Озон қабатының жұқаруына суретте көрсетілген факторлар әсер етеді.
https://www.syl.ru/article/188050/new_chto-takoe-ozonovyiy-sloy-zemli-problemyi-ozonovogo-sloya
а) Осы факторлардың біреуінің озон қабатына қалай әсер ететінін жазыңыз.
_______________________________________________________________
[1]
b) Озон қабатының жұқаруының бір салдарын көрсетіңіз.
_____________________________________________________________
[1]
11. CaCO3 → CaO + CO2 реакциясында энергия өзгереді.
а) Жылудың бөлінуі немесе сіңірілуіне байланысты реакцияның типін анықтаңыз.
______________________________________________________________[1]
b) Энергия өзгерісін бөлшектердің кинетикалық теориясы тұрғысынан түсіндіріңіз.
_______________________________________________________________
_______________________________________________________________
________________________________________________________________
[1]
Балл қою кестесі
|
№ |
Жауап |
Балл |
Қосымша ақпарат |
|
1 |
B |
1 |
|
|
2 |
D |
1 |
|
|
E |
1 |
|
|
|
3 |
Мольдік көлем арқылы газдардың көлемін есептеуге болады. Қалыпты жағдайда 1 моль оттектің көлемі 1 моль көмірқышқыл газының көлеміне тең. |
1 |
2 дұрыс жауап үшін 1 балл |
|
4 |
1) A |
1 |
|
|
2) C |
1 |
|
|
|
3) B |
1 |
|
|
|
5 |
Химиялық, оттегі, көмірқышқыл газы |
1 |
Екі сөйлемдегі барлық дұрыс жауап үшін 1 балл беріледі. |
|
Оксид, көмірқышқыл газы, иіс газы, күйе |
1 |
Екі сөйлемдегі барлық дұрыс жауап үшін 1 балл беріледі. |
|
|
6 |
2 моль, 36 г |
2 |
Әр дұрыс жауап үшін 1 балл |
|
7 |
Сіңіріледі, бөлінеді, жоғарылайды |
1 |
Үш сөйлемдегі барлық дұрыс жауап үшін 1 балл беріледі. |
|
Эндотермиялық, жоғары |
1 |
Екі сөйлемдегі барлық дұрыс жауап үшін 1 балл беріледі. |
|
|
8 |
а) Отын ретінде, металдарды дәнекерлеу |
1 |
Кез келген екі дұрыс саланы атап жазса 1 балл беріледі. |
|
b) 1. C + H2O → CO + H2↑ |
1 |
|
|
|
2. N2 + 3H2 → 2NH3 |
1 |
|
|
|
3. 2Na + H2 → 2NaH |
1 |
|
|
|
9 |
a) 4Al + 3O2 → 2Al2O3 |
1 |
|
|
2Са + О2 → 2СаО |
1 |
|
|
|
b) C |
1 |
|
|
|
c) 2H2O2 → 2H2O + O2 |
1 |
|
|
|
10 |
a) Хлор қосылыстары күн радиациясы әсерінен хлор атомдарына ыдырап, озонның молекулаларымен реакцияға түседі. |
1 |
Хлор атомы озон молекулаларымен әрекеттесіп, озон молекуласын бұзады. |
|
b) Климаттың өзгеруі |
1 |
Кез келген дұрыс салдарды жазса 1 балл беріледі. |
|
|
11 |
а) Эндотермиялық реакция |
1 |
|
|
b) Молекулалар баяу/жай қозғалғандықтан, кинетикалық энергия кемиді. Бөлшектер арасында қашықтық/кеңістік кішірейеді/азаяды. |
1 |
Бөлшектер арасындағы байланыс күшейеді деген жауап қабылданады. |
|
|
|
Барлығы |
25 |
|
3-ТОҚСАННЫҢ ЖИЫНТЫҚ БАҒАЛАУ СПЕЦИФИКАЦИЯСЫ
3-тоқсанның жиынтық бағалауына шолу
Жиынтық бағалаудың өткізілу уақыты – 40 минут
Балл саны – 25
Тапсырма түрлері:
КТБ – Көп таңдауы бар тапсырмалар;
ҚЖ – Қысқа жауапты қажет ететін тапсырмалар;
ТЖ – Толық жауапты қажет ететін тапсырмалар.
Жиынтық бағалаудың құрылымы
Берілген нұсқада әртүрлі тапсырмалар: көп жауапты таңдауы бар сұрақтар, қысқа және толық жауапты қажет ететін сұрақтар қолданылады.
Көп таңдауы бар тапсырмаларда оқушылар бір және бірнеше дұрыс жауапты таңдайды. Қысқа жауапты қажет ететін сұрақтарға сөздер немесе қысқа сөйлемдер түрінде жауап береді. Толық жауапты қажет ететін сұрақтарда білім алушылар логикалық ойлау және шығармашылық дағдыларын көрсетеді. Толық жауапты қажет ететін тапсырмаларды орындау барысында оқушылар өздерінің түсініктерін, ойлау деңгейін көрсетеді.
Нұсқада 15 тапсырма берілген.
3-тоқсан бойынша жиынтық бағалау тапсырмаларының сипаттамасы
|
Бөлім |
Тексерілетін мақсат |
Ойлау |
Тап-сыр-ма |
№ сырма |
Тап-сыр |
Орындау |
Балл* |
Бөлім ша балл |
|
Химиялық |
8.2.1.1 Топ, период, атом нөмірінің физикалық мәнін түсіндіру |
Қолдану |
1 |
3 |
ЖТ |
2 |
3 |
9 |
|
8.2.1.2 Бір топтағы элементтердің сыртқы электрондық деңгейінде электрондар санының бірдей болатындығын түсіну; |
Білу және түсіну |
1 |
2 |
ТЖ |
3 |
2 |
||
|
8.2.1.3 Топтар мен
периодтарда |
Қолдану |
2 |
1, 4 |
ТЖ |
4 |
2 |
||
|
8.2.1.4 Химиялық элементтің периодтық кестеде орналасуына сай қасиеттерін болжау |
Жоғары деңгей дағдылары |
1 |
5 |
КТБ |
3 |
2 |
||
|
Химиялық |
8.1.4.1 Электртерістілік ұғымы негізінде атомдар арасындағы ковалентті байланыстың түзілуін түсіндіру |
Қолдану |
1 |
6 |
ТЖ |
5 |
2 |
5 |
|
8.1.4.2 Иондық байланыстың түзілу механизмін сипаттау және иондық қосылыстардың қасиеттерін болжау |
Қолдану |
2 |
7, 8 |
ТЖ |
4 |
3 |
||
|
Ерітінді-лер |
8.3.4.1 Заттарды судағы ерігіштігі бойынша жіктеу; |
Білу және түсіну |
3 |
10, 11 |
КТБ |
5 |
4 |
11 |
|
8.3.4.3 Заттың
ерігіштігіне |
Қолдану |
1 |
9 |
ЖТ |
3 |
2 |
||
|
8.3.4.5 Еріген заттың массалық үлесі мен ерітіндінің белгілі массасы бойынша еріген заттың массасын есептеу |
Қолдану |
2 |
12, 13 |
ТЖ |
6 |
3 |
||
|
8.3.4.6 Ерітіндідегі заттың молярлық концентрациясын есептеу |
Қолдану |
2 |
14, 15 |
|
4 |
2 |
||
|
Барлығы |
|
|
15 |
|
|
40 |
25 |
25 |
«Химия» пәнінен 3-тоқсанға арналған жиынтық бағалаудың тапсырмалары
1. Атом радиусының өсу реті бойынша орналасқан элементтер қатарын табыңыз.
А) Si P S
В) Be B C
С) Si Ge C
D) Ве Mg Ca
E) C N Li
[1]
2. а) Сыртқы электрондық деңгейінде электрондар саны бірдей элементтерді табыңыз: Be, Al, C, Mg, N, Ne, Cl, Ca
________________________________________________________________________
[1]
b) Элементтерді бір топқа біріктіруге негіз болатын қасиеттерді атаңдар.
________________________________________________________________________________________________________________________________________________
[1]
3. Топ, период, атом нөмірінің оның физикалық мағынасымен сәйкестендіріңіз.
-
Физикалық мағынасы
1
Топ нөмірі
А)
Атомның ядро зарядын
В)
Ядродағы протон санын
2
Период нөмірі
С)
Атомдағы электрон санын
D)
Энергетикалық деңгей санын
3
Атом нөмірі
Е)
Сыртқы деңгейдегі электрон санын
[3]
Химия қысқа мерзімді жоспарлар жиынтығы. 8 сынып. Д.Х.Аширова, Н.Б.Бақтыбаева.
4. Ве Мg Са К Аl Fe
а) Берілген металдарды металдық қасиеті артуы бойынша орналастырыңыз.
[1]
b) Металдық қасиетінің арту себебін түсіндіріңіз.
________________________________________________________________________
[1]
5. Көміртекке қатысты келесі тұжырымдардың дұрысын анықтаңыз.
А) екі энергетикалық деңгейі бар
В) қышқылдық та, негіздік те оксид түзеді
С) ұшқыш сутекті қосылысы СН4
D) ІІІ период, ІV топ, негізгі топшада орналасқан
Е) ІІ және ІІІ валенттілік көрсетеді
F) белсенді бейметалл
G) тотығу дәрежесі +4; -4; +2
H) жоғарғы оксиді СО2 , негіздік оксид
[1]
6. а) Сутек пен бром атомдарының арасында химиялық байланысты анықтаңыз.
___________________________________________________________________
[1]
b) Нүктелер және крестер диаграммасы арқылы сутек пен бром атомдарының арасында түзілуі мүмкін байланыстың схемасын құрыңыз.

[1]
7. Қаныққан ерітінді концентрлі ерітінді бола ала ма? Жауабыңызды түсіндіріңіз.
[1]
8. а) Литий және фтор атомдарының электрондарының энергетикалық деңгейлерге таралуын көрсетіңіз.
L![]()
![]() i ) )
F
) )
i ) )
F
) )
[1]
b) Литий және фтор атомдарының арасында иондық байланыстың түзілу сызбасын көрсетіңіз.

[1]
Химия қысқа мерзімді жоспарлар жиынтығы. 8 сынып. Д.Х.Аширова, Н.Б.Бақтыбаева.
9. Заттардың ерігіштігіне температураның әсерін түсіндіріңіз.
|
№ |
Тұжырымдар |
Себебі |
|
1 |
Қатты заттардың ерігіштігі температура жоғарылағанда артады. |
|
|
2 |
Газдардың ерігіштігі температура жоғарылағанда кемиді. |
|
[2]
10. Жақсы еритін затты анықтаңыз.
A) темір
B) калий гидроксиді
C) парафин
D) көміртек
Е) мұнай
[1]
11. Суда калий перманганатын (марганцовка) еріткенде байқалатын құбылыстарды түсіндіріңіз.
|
№ |
Құбылыстар |
Түсініктеме |
|
1 |
|
|
|
2 |
|
|
|
3 |
|
|
[3]
Химия. Жұмыс дәптері. 8 сынып. Н.Нұрахметов
12. Суреттегі екі затты араластыру арқылы алынған ерітіндінің пайыздық концентрациясы қанша?

 bilimland.kz
bilimland.kz
Ас тұзы 30 г су 75 г
А) 38 %
В) 35 %
С) 30 %
D) 29 %
Е)28 %
[1]
13. Мұғалім оқушыға 200 г 30 % -дық ерітінді дайындауды тапсырды. Ерітіндіні дайындау үшін оқушы қанша тұз және қанша су алуы керек.
А) 30 г тұз, 140 г су
В) 10 г тұз, 150 г су
С) 60 г тұз ,140 г су
D) 50 г тұз, 150 г су
Е) 20 г тұз , 180 г су
[2]
14. Молярлық концентрация дегеніміз не?
________________________________________________________________________
[1]
15 . 500 мл ерітіндіде 5 г NаОН бар ерітіндінің молярлық концентрациясын есептеңіз.
А) 1,01 моль/л
В) 1,05 моль/л
С) 0,50 моль/л
D) 0,35 моль/л
Е) 0,25 моль/л
[1]
http://xn--i1abbnckbmcl9fb.xn
Балл қою кестесі
|
№ |
Жауап |
Балл |
Қосымша ақпарат |
||||||||||||
|
1 |
D |
1 |
|
||||||||||||
|
2 |
a) Li, Na, K |
1 |
|
||||||||||||
|
b) Жоғарғы тотығу дәрежесі +1, валенттілігі І, белсенді сілтілік металдар, жоғарғы оксиді R2O |
1 |
|
|||||||||||||
|
3 |
1 - Е |
1 |
|
||||||||||||
|
2 - В |
1 |
|
|||||||||||||
|
3 – A, C, D |
1 |
|
|||||||||||||
|
4 |
a) Al, Fe, Mg, Ca, Na, K |
1 |
|
||||||||||||
|
|
b) Себебі, солдан оңға қарай сыртқы қабатындағы электрондар саны кемиді |
1 |
|
||||||||||||
|
5 |
A, C, G |
1 |
|
||||||||||||
|
6 |
а) Ковалентті полюсті |
1 |
|
||||||||||||
|
•• •• b) H• + •Br: → H(:)Br: •• ••
|
1 |
|
|||||||||||||
|
7 |
Қаныққан ерітінді концентрлі бола алмайды, себебі қаныққан ерітіндіде ары қарай зат ерімейді, ал концентрлі ерітіндіде ериді. |
1 |
Балама ұсыныстар қабылданады. |
||||||||||||
|
8 |
a) Li 2e1e F 2e 7e |
1 |
|
||||||||||||
|
b) •• + •• - b) Li• + •F: → Li [:F:] •• •• |
1 |
|
|||||||||||||
|
9 |
1. Қатты заттардың ерігіштігі температураны көтергенде артады, себебі температураның әсерінен диффузия тез жүреді. 2. Газдардың ерігіштігі температураны жоғарылатқанда кемиді, себебі газ бөлшектері арасындағы қашықтық үлкейеді. |
2 |
Балама ұсыныстар қабылданады. |
||||||||||||
|
10 |
В |
1 |
|
||||||||||||
|
11 |
|
3 |
Балама ұсыныстар қабылданады. |
||||||||||||
|
12 |
Е |
1 |
|
||||||||||||
|
13 |
С |
2 |
|
||||||||||||
|
14 |
Молярлы концентрация дегеніміз – 1 л көлемде еріген заттың мөлшері |
1 |
|
||||||||||||
|
15 |
Е |
1 |
|
||||||||||||
|
Барлығы |
25 |
|
|||||||||||||
4-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУ СПЕЦИФИКАЦИЯСЫ
4-тоқсанның жиынтық бағалауына шолу
Ұзақтығы - 40 минут
Балл саны - 25
Тапсырма түрі:
КТБ – көп тaңдауы бaр тапсырмалар;
ҚЖ – қысқа жауапты қажет ететін тапсырмалар;
ТЖ – толық жауапты қажет ететін тапсырмалар.
Жиынтық бағалаудың құрылымы
Берілген нұсқада әртүрлі тапсырмалар: көп таңдауы бар тапсырмалар, қысқа және толық жауапты қажет ететін тапсырмалар қамтылды.
Көп тaңдaуы бaр тaпсырмaлaрдa оқушылaр берілген жaуaп нұсқaлaрынaн дұрыс жaуaпты көрсетеді.
Қысқa жaуaпты қaжет ететін тaпсырмaлaрғa оқушылaр дәл жауапты, қысқa сөйлемдер түрінде жaуaп береді. Толық жaуaпты қaжет ететін тaпсырмaлaрдa оқушылар жоғары бaлл жинaу үшін тaпсырмaның әр қадамын орындау талап етіледі. Оқушы өз пікірін анық көрсетіп жазады және дәлелдейді. Тапсырмаларды орындау барысында оқушыларда жоғары деңгей дағдылары және өз бетінше іздену дағдылары қалыптасады. Тоқсандық жиынтық 11 тапсырмадан тұрады: бір дұрыс және бірнеше дұрыс жауапты таңдауға арналған, қысқа жауапты қажет ететін тапсырмалар. Сонымен қатар, толық жауапты қажет ететін тапсырмалар оқушылардың ойланып өз пікірлерін дәлелдерін толық жазуға арналған тапсырмалар.
4-тоқсaн бойыншa жиынтық бaғaлaу тaпсырмaлaрының сипaттaмaсы
|
Бөлім |
Тексерілетін мақсат |
Ойлау дағдыларының деңгейі |
Тап сыр ма саны* |
тапсыр ма* № |
Тапсырма түрі |
Орындау уақыты, мин* |
Балл* |
Бөлім бойынша балл |
|
Бейорганикалық қосылыстардың негізгі кластары. Генетикалық байланыс |
8.3.4.7 Оксидтердің жіктелуін және қасиеттерін білу, олардың химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрастыру |
Қолдану |
1 |
5 |
ТЖ |
5 |
2 |
10 |
|
8.3.4.8 Қышқылдардың жіктелуін, қасиеттерін білу және түсіну, олардың химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрастыру |
Қолдану |
1 |
6 |
ҚЖ |
3 |
3 |
||
|
8.3.4.9 Негіздердің жіктелуі мен қасиеттерін білу және түсіну, олардың химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрастыру |
Қолдану |
1 |
7 |
КТБ |
2 |
1 |
||
|
8.3.4.12 Бейорганикалық қосылыстардың негізгі кластары арасындағы генетикалық байланысты зерттеу |
Жоғары деңгей |
1 |
8 |
ТЖ |
6 |
4 |
||
|
Көміртек және оның қосылыстары |
8.4.3.1 Көміртек неліктен көптеген қосылыстарында төрт байланыс түзетінін түсіндіру; |
Қолдану |
1 |
9 |
ТЖ |
5 |
2 |
8 |
|
8.4.3.3 Көміртектің аллотропиялық түр өзгерістерінің құрылысын және қасиеттерін салыстыру; |
Білу және түсіну |
1 |
1 |
КТБ |
2 |
1 |
||
|
8.4.3.6 Көміртек жанған кезде көміртек диоксиді мен көміртек монооксидінің түзілу жағдайларын сипаттау және тірі ағзаларға иіс газының физиологиялық әсерін түсіндіру; |
Қолдану |
2 |
3,4 |
ТЖ |
8 |
3 |
||
|
8.4.3.7 Көмірқышқыл газын алу, оны анықтау және қасиеттерін зерттеу; |
Қолдану |
1 |
2 |
КТБ
|
2 |
2 |
||
|
Су |
8.4.2.8 Судың ластануының қауіптілігі мен себебін анықтау, суды тазарту әдістерін түсіндіру; |
Қолдану |
1 |
10 |
ҚЖ |
3 |
4 |
7 |
|
8.4.2.9 Судың «кермектігін» анықтау және оны жою тәсілдерін түсіндіру; |
Қолдану |
1 |
11 |
КТБ
|
4 |
3 |
||
|
Барлығы |
|
|
11 |
|
|
40 |
|
25 |
Химия пәнінен 4-тоқсанға арналған
жиынтық бағалаудың тапсырмалары
1. Зертханада көмір қышқыл газын алуға мүмкін болатын реакциясын таңдаңыз:
А) NaOH+HCl →
В) Ca(OH)2 +CO2 →
С) NaOH+HCl → D) Na 2СО3+HCl →
[1]
2. Ерімейтін негізді анықтаңыз:
А) NaOH
B) Ba(OH)2
C) Fe(OH)2
D) Ca(OH)2
Е) Cu(OH)2
F) LiOH
[2]
3.Берілген қышқылдардың ішінен оттекті қышқылдaрды бөліп жазыңыз: HNO3, HI, HBr, H3PO4, HCl, H2CO3
[1]
4. Көміртектің аллотропиялық түр өзгерісі мен олардың қасиеттері, құрылысы және қолдану аймағы арасындағы сәйкестікті анықтаңыз:
|
Көміртектің аллотропиялық түр өзгерісі |
Қасиеттері мен құрылысы |
Қолдану аймағы |
|
І.Графит |
1.Сызықтық құрылымды зат |
А.Жасанды қан тамырларын жасауда |
|
2.Қара түсті ұнтақ зат, жартылай өткізгіш |
||
|
ІІ. Карбин |
3. Сұр түсті, жұмсақ, ұстағанда май тәрізді зат |
B.Электродтар дайындауда |
|
4. Атомдық кристалдық торы бар |
І._________________ II.___________________
[2]
5 а) Көміртегі атомының қалыпты және қозған күйінің электрондық- графикалық формулаларын толықтырыз:


қалыпты күйі қозған күйі
[1]
b) Қалыпты және қозған күйлерінің ерекшеліктеріне сүйеніп көміртек атомының төрт байланыс түзу себебін түсіндіріңіз:
________________________________________________________________________________________________________________________________________
[1]
6 а) Сөйлемдерді толықтырыңыз:
Көміртек жанғанда оттектің мөлшері артық болса_________________________түзіледі. Көміртек оттек жеткіліксіз ортада жанғанда _______________________________ түзіледі.
[1]
b) Көміртек монооксиді иіс газы деп аталады. Ол иіссіз, түссіз және суда нашар еритін газ. Иіс газының адам ағзасына тигізетін әсерін 1 мысал келтіріп сипаттаңыз.
________________________________________________________________________________________________________________________________________
[2]
7. Сөзбен берілген реакция теңдеуін таңбалар мен формулалар арқылы жазып теңестіріңіз:
а) магний гидроксиді + тұз қышқылы → магний хлориді + су
____________________________________________________________________
[1]
8. a) Берілген оксидтердің ішінен қайсысы артық екендігін анықтаңыз.
|
Оксидтер |
«Артық» оксид |
Себебі |
|
Na2O CO2 MgO |
|
|
|
BeO SiO2 SO3 |
|
|
|
CO2 SO2 K2O |
|
|
[2]
b) Оксидтердің қасиеттерін сипаттаңдар. Жауаптарды тор көзге (+) және (-) белгісін қойыңыз.
-
Негіздік
Қышқылдық
Екі дайлы
-
Сумен әрекеттесуі
-
Қышқылдармен әрекеттесуі
-
Сілтілермен әрекеттесуі
-
[2]
9. Қышқыл мен негіз арасындағы бейтараптану реакциясына екі мысал жазып теңестіріңіз:
__________________________________________________________________________________________________________________________________
[2]
10. Су сапалы, тұщы, əртүрлі зиянды қоспалардан таза болуы шарт. Суды тазарту – адам денсаулығын сақтаудың бір жолы.
a) судың ластануының 1 себебін жазыңыз:
[1]




![]()
![]() b) Әрбір қадам үшін суды
тазартудың тиімді әдісін анықтаңыз.
b) Әрбір қадам үшін суды
тазартудың тиімді әдісін анықтаңыз.
![]()
А. лайланған су В. Тұнбасы бар су С. Тұнбасыз су D. Таза су
__________________ ________________ ___________________
[3]
11. а) Судың кермектілігі туралы тұжырымдардағы бос орындарды толтырыңыз:
Судың кермектілігінің үш түрі бар, олар _________________, ______________, _______ ________. Егер табиғи суда Ca2+ және HCO32- иондары бар болса, онда бұл _____________ кермектілік. Егер табиғи суда кальцийдің немесе магнийдің хлориді және нитраты бар болса, онда бұл____________________ кермектілік. Судың уақытша кермектілігін жою үшін _________________.
[2]
b) Өндірісте судың кермектілігін жою үшін оның түріне қарамастан, соданы қолдану тиімді. Сода қосу арқылы кермектілікті жою реакциясынының 1 теңдеуін жазыңыз:
____________________________________________________________________
[1]
Балл қою кестесі
|
№ |
Жауап |
Балл |
Қосымша ақпарат
|
|||||||||||||||||||||||||||||||||
|
1 |
D |
1 |
|
|||||||||||||||||||||||||||||||||
|
2 |
C, E |
2 |
|
|||||||||||||||||||||||||||||||||
|
3 |
HNO3 H3PO4, H2 CO3 |
1 |
Басқа жауап қабылданбайды |
|||||||||||||||||||||||||||||||||
|
4 |
І.Графит -3,4 ІІ. Карбин-1,2 |
2 |
үш жауап дұрыс болған жағдайда да бір балл беруге болады |
|||||||||||||||||||||||||||||||||
|
5 |
а) қалыпты күйі қозған күйі
b) Көміртек атомының қозған күйінде сыртқы энергетикалық деңгейінде 4 жұптаспаған электрон болғандықтан төрт химиялық байланыс түзеді
|
1
1 |
Басқа жауап қабылданбайды |
|||||||||||||||||||||||||||||||||
|
6 |
а) көміртек (IV) оксиді / СО2 Көміртек моноксиді/ СО b) Қан гемоглобинімен қосылып организімнің оттекпен қамтамасыз етілуін жояды |
1
2 |
Басқа жауап қабылданбайды Адам уланады жауабы қабылданады |
|||||||||||||||||||||||||||||||||
|
7 |
Mg(OH)2 + 2HCl= MgCl2+2H2O |
1 |
Басқа жауап қабылданбайды |
|||||||||||||||||||||||||||||||||
|
8 |
b)
|
2
2 |
Басқа жауап қабылданбайды |
|||||||||||||||||||||||||||||||||
|
9 |
HCl+NaOH=NaCl+H2O H2SO4+KOH=K2SO4+ H2O |
2 |
Нәтижесінде түз және су алынатын қышқылмен негіздің арасында жүретін кез-келген реакция |
|||||||||||||||||||||||||||||||||
|
10 |
а) жаза тайым оқиғалардан, тасталған қалдықтар, мұнай өнімдері төгілгенде минералды тыңайтқыштарды өте көп мөлшерде пайдалану микроорганизмдердің басым көпшілігін жою мақсатында улы химикаттарды қолдану b) тұндыру, сүзу, дистельдеу
|
1
3 |
Басқада ұсынған жауаптары дұрыс болса қабылданады
Басқа жауап қабылданбайды |
|||||||||||||||||||||||||||||||||
|
11 |
а) Уақытша/ карбонатты, тұрақты/ карбонатсыз, аралас
b |
2
1 |
|
|||||||||||||||||||||||||||||||||
1
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
бжб тжб химия 8 сынып
Жиынтық бағалауға арналған
әдістемелік ұсыныстар
Химия
8-сынып
«Жиынтық бағалау тапсырмаларының жинағы» әдістемелік құралы мұғалімге 8-сынып білім алушыларына «Химия» пәні бойынша жиынтық бағалауды жоспарлау, ұйымдастыру және өткізуге көмек құралы ретінде құрастырылған. Әдістемелік құрал 8-сынып «Химия» пәні бойынша ұзақ мерзімді оқу бағдарламасы негізінде дайындалған.
Бөлім бойынша жиынтық бағалаудың тапсырмалары мұғалімге білім алушылардың тоқсан бойынша жоспарланған оқу мақсаттарына жету деңгейін анықтауға мүмкіндік береді.
Әдістемелік құралда бөлім бойынша жиынтық бағалауды өткізуге арналған бағалау критерийлері мен дескрипторлары бар тапсырмалар ұсынылған. Дескрипторлары мен балдары бар тапсырмалар ұсыныс түрінде берілген.
Әдістемелік құрал жалпы орта білім беретін мектеп мұғалімдеріне, мектеп әкімшілігіне, білім беру бөлімінің әдіскерлеріне, критериалды бағалау бойынша мектеп, өңірлік үйлестірушілеріне және басқа да мүдделі тұлғаларға арналған.
Әдістемелік ұсыныстарды дайындау барысында ресми интернет-сайттағы қолжетімді ресурстар (суреттер, фотосуреттер, мәтіндер, аудио және бейнематериалдар) қолданылды.
1-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 4
8.1А «Атомдағы электрондардың қозғалысы» 4
8.1B «Заттардың формулалары және химиялық реакция теңдеулері» 8
8.1С «Металдар белсенділігін салыстыру» 12
2-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 15
8.2А, 8.2В «Зат мөлшері» және «Стехиометриялық есептеулер» 5
8.2C «Химиялық реакциядағы энергиямен танысу» 19
8.2D «Сутек. Оттек және озон» 23
3-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 27
8.3A «Химиялық элементтердің периодтық жүйесі» 27
8.3B «Химиялық байланыс түрлері» 31
8.3C «Ерітінділер және ерігіштік» 35
4-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 38
8.4A «Бейорганикалық қосылыстардың негізгі кластары. Генетикалық байланыс» .. 38
8.4B «Көміртек және оның қосылыстары» 42
1-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 48
2-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 57
3-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 64
4-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУҒА АРНАЛҒАН ТАПСЫРМАЛАР 69
«Атомдағы электрондардың қозғалысы» бөлімі бойынша
жиынтық бағалау
Оқу мақсаттары 8.1.3.1 Атомда электрондар ядродан
арақашықтығы артқан сайын біртіндеп
энергетикалық деңгейлер бойынша
таралатынын түсіну
8.1.3.4 Алғашқы 20 химиялық элементтердің
электрондық конфигурациясын және
электронды – графикалық формулаларын жаза
білу
8.1.3.5 Атомдар электрондарды қабылдай немесе
жоғалта алатынын және осының нәтижесінде
иондар түзілетінін түсіну
8.1.3.6 «Нөлдік қосынды» әдісімен
қосылыстардың формуласын құрастыру
Бағалау критерийлері Білім алушы:
• Атомдағы электрондардың энергетикалық
деңгейлерде орналасу ретін түсіндіреді.
• Алғашқы 20 химиялық элементтің электрондық және электронды - графикалық формулаларын
жазады.
• Қосып алатын немесе беретін электрондар саны
мен атом арасындағы байланысты анықтайды.
• «Нөлдік қосынды» әдісімен қосылыстардың
формуласын құрастырады.
Ойлау
дағдыларының
деңгейі Білу және түсіну,
қолдану
Орындалу уақыты 20 минут
Тапсырмалар
1. Келесі химиялық элементтер берілген: көміртек, натрий, фосфор, аргон.
Атом құрылысы және электрондардың энергетикалық деңгейлерде таралуы туралы тұжырымдар қай элементке қатысты айтылғанын анықтаңыз.
А) Сыртқы қабатында 1 электроны бар
В) Екі энергетикалық деңгейі бар
С) Сыртқы қабаты толық, аяқталған
D) 15 протоны, 15 электроны бар
|
С |
Na |
P |
Ar |
|
|
|
|
|
[2]
2. Химиялық элемент атомы мен электрондардың энергетикалық деңгейлерге таралуын сәйкестендіріңіз.
-
S А. 2е) 8е) 2е)
-
Al В. 2е) 8е) 8е) 1е)
-
K С. 2е) 8е ) 3е)
-
O D. 2е) 6е )
-
Mg Е. 2е) 8е )
-
Ne F. 2е) 8е) 6е)
[2]
Химия қысқы мерзімді жоспарлар жинағы. 8 сынып.
Д.Х Аширова, Н.Б. Бактыбаева.
3. Берілген химиялық элементтердің электрондық және графикалық формула-
ларын құрыңыз.
|
Химиялық элемент |
Электрондық формуласы |
Графикалық формуласы |
|
В |
|
|
|
Ne |
|
|
|
Si |
|
|
|
K |
|
|
[2]
4. (а) Натрий және күкірт атомдарындағы электрондардың таралуын сызбаға нүктемен көрсетіңіз.






![]()
![]()
Натрий атомы Күкірт атомы [1]
(b) Натрий және күкірт атомдарының иондарға айналуының сызбасын көрсетіңіз.






![]()
![]()
Натрий ионы Күкірт ионы
[1]
(с) Cыртқы энергетикалық деңгейдегі электрондар саны мен ион түзу (катион немесе анионға айналу) қасиеттерінің арасындағы байланысты түсіндіріңіз.
____________________________________________________________________________________________________________________________________________
[1]
Химия қысқы мерзімді жоспарлар жинағы. 8 сынып. Д.Х Аширова, Н.Б. Бактыбаева.
5. Химиялық қосылыстың молекула құрамы бойынша «нөлдік қосынды» әдісімен формуласын құрастырыңыз.
Азот (ІІІ) пен сутек
_____________________________________________________________________
[1]
Қалыптастырушы бағалауға арналған тапсырмалар жинағы. Химия 8-сынып
Балл қою кестесі
|
Бағалау критерийлері |
Тапсырма |
Дескрипторлар |
Балл |
|
Атомдағы электрондардың энергетикалық деңгейлерде орналасу ретін түсіндіреді
|
1 |
Берілген 4 тұжырымдарды химиялық элементке қатысты дұрыс анықтайды |
2 |
|
Атомдағы электрондардың энергетикалық деңгейлерде орналасу ретін түсіндіреді |
2 |
Берілген химиялық элементтердің электрондарының энергетикалық деңгейлерге таралуын анықтайды. |
1 |
|
Екінші бағанада берілген электрондардың энергетикалық деңгейлерге таралуымен сәйкестендіреді |
1 |
||
|
Химиялық элементтің электрондық конфигурациясын және электронды – графикалық формуларын жазады |
3 |
Берілген химиялық элементтердің электрондық формулаларын анықтайды |
1 |
|
Берілген химиялық элементтердің электронды-графикалық формулаларын анықтайды |
1 |
||
|
Қосып алатын немесе беретін электрондар саны мен атом арасындағы байланысты анықтайды
|
4 |
Натрий және күкірт атомдарының электрондарының энергетикалық деңгейлерге таралуын сызбада нүктемен көрсетеді |
1 |
|
Натрий және күкірт атомдарының иондарға айналуын сызбада нүктемен көрсетеді |
1 |
||
|
Сыртқы энергетикалық деңгейдегі электрондар саны мен ион түзу қасиеттерінің арасындағы байланысты анықтайды |
1 |
||
|
«Нөлдік қосынды» әдісімен қосылыстың формуласын құрастырады |
5 |
«Нөлдік қосынды» әдісімен берілген қосылыстардың формулаларын құрастырады |
1 |
|
Барлығы |
10 |
||
«Заттардың формулалары және химиялық реакция теңдеулері» бөлімі бойынша жиынтық бағалау
|
|
|
|
Оқу мақсаты |
8.2.3.1 Заттар құрамындағы элементтердің массалық үлесін табу, элементтердің массалық үлесі бойынша заттардың формуласын құрастыру; 8.2.3.3 Реакцияға қатысатын және түзілетін заттардың формулаларын жаза отырып, химиялық реакция теңдеуін құрастыру; 8.2.3.4 Заттар массасының сақталу заңын білу; 8.2.2.1 Бастапқы және түзілген заттардың саны мен құрамы бойынша химиялық реакцияларды жіктеу; 8.2.2.2 Табиғаттағы және тірі ағзалар мен адам тіршілігіндегі химиялық реакцияларды сипаттау. |
|
Бағалау критерийі |
Білім алушы: |
|
|
● Заттар құрамындағы элементтердің массалық үлесін табады, элементтердің массалық үлесі бойынша заттардың формуласын анықтайды ● Реагенттер мен өнімдерді жазу арқылы химиялық реакция теңдеуін жазады ● Зат массасының сақталу заңын тұжырымдайды ● Реакцияға қатысатын және реакция нәтижесінде түзілген заттардың саны мен құрамы бойынша химиялық реакцияларды жіктейді ● Табиғаттағы және тірі ағзалар мен адам тіршілігіндегі химиялық реакцияларды түсіндіреді |
|
|
|
|
Ойлау дағдыларының деңгейлері |
Қолдану, жоғары деңгей дағдылары |
|
|
|
|
Орындау уақыты |
20 минут |
Тапсырма
1. а) Химиялық элементтер жалпы молекуланың белгілі бір бөлігін құрайды. Фосфор (V) оксиді құрамындағы оттегінің массалық үлесін (%) анықтаңыз:
A) 11
B) 20
C) 34
D) 43
E) 56
Жауабы: _______________ [1]
b) Қосылыстардағы элементтердің мөлшерін білу оларды тиімді қолдану үшін қажет. Заттың құрамындағы натрийдің массалық үлесі - 54,5%, оттектің массалық үлесі - 40%, сутектің массалық үлесі – 5,5% көрсетеді. Қосылыстың формуласын анықтаңыз.
[1]
2. Химиялық реакция теңдеуі реагенттердің өнімдерге айналуын сипаттайды. Нүктелердің орнына тиісті формулаларды жазып, реакция теңдеуін құрастырыңыз.
Na + … → Na2S
H2CO3 → … + CO2
Са + O2 → …
Ag2O → Ag + … [4]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / Н.Нұрахметов, К.А.Сарманова, К.М.Жексембина - Алматы: «Мектеп», 2016
3. Төменде берілген суретте реакцияның жүру барысы көрсетілген. Реакция барысында зат массасының сақталу заңы сақталған ба, жауабыңызды түсіндіріңіз.

http://cubino.pl/2016/10/euro6-motorem-postepu/
[1]
4. Бастапқы заттар мен өнімдердің құрамы бойынша химиялық реакция теңдеуін жіктеңіз және әр типке мысал келтіріңіз.
![]()
Химиялық реакция типтері
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Алмасу
![]()
![]()
![]()
![]()
![]()
Айырылу
![]()
![]()
2NO + O2 → 2NO2
![]()
![]()
Mg + 2HCl → MgCl2 + Н2
[4]
5. Адам өміріндегі көптеген күнделікті қолданатын заттары және іс-әрекеттері химиялық процестерге негізделген. Мысалы жану және баяу тотығу процестері, әр процеске бір мысал келтіріңіз және жану мен баяу тотығу процесінің екі ұқсастығы мен айырмашылығын жазыңыз.
Мысалы:
Ұқсастығы:
Айырмашылығы:
[5]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
Ескерту |
|
Білім алушы |
||||
|
Заттар құрамындағы элементтердің массалық үлесін табады, элементтердің массалық үлесі бойынша заттардың формуласын анықтайды |
1(a) |
Қосылыс құрамындағы оттегінің массалық үлесінің мәнін анықтайды |
1 |
|
|
1(b) |
Массалық үлестің мәні бойынша қосылыстың формуласын анықтайды |
1 |
|
|
|
Реагенттер мен өнімдерді жазу арқылы химиялық реакция теңдеуін жазады |
2 |
Натрий сульфидінің түзілу реакция теңдеуін құрастырады |
1 |
|
|
Көмірқышқылының ыдырау реакция теңдеуін құрастырады |
1 |
|
||
|
Кальций мен оттегінің әрекеттесу реакция теңдеуін құрастырады |
1 |
|
||
|
Күміс оксидінің ыдырау реакция теңдеуін құрастырады |
1 |
|
||
|
Зат массасының сақталу заңын тұжырымдайды |
3 |
Зат массаның сақталу заңын тұжырымдайды |
1 |
|
|
Реакцияға қатысатын және реакция нәтижесінде түзілген заттардың саны мен құрамы бойынша химиялық реакцияларды жіктейді |
4 |
Қосылу реакциясын ажыратады |
1 |
|
|
Айырылу реакциясын ажыратады |
1 |
|
||
|
Орынбасу реакциясын ажыратады |
1 |
|
||
|
Алмасу реакциясын ажыратады |
1 |
|
||
|
Табиғаттағы және тірі ағзалар мен адам тіршілігіндегі химиялық реакцияларды түсіндіреді |
5 |
Жану реакциясына бір мысал жазады
|
1 |
|
|
Баяу тотығу процесіне бір мысал жазады |
1 |
|
||
|
Жану және баяу тотығу процестерінің өзара екі ұқсастығын жазады |
1 |
|
||
|
Жану процесінің баяу тотығу процесінен екі айырмашылығын жазады |
1 |
|
||
|
Баяу тотығу процесінің жану процесінен екі айырмашылығын жазады |
1 |
|
||
|
Барлығы |
16 |
|
||
«Металдар белсенділігін салыстыру» бөлімі бойынша жиынтық бағалау
|
|
|
|
Оқу мақсаты |
8.2.4.2 Белсенді металдардың салқын сумен, ыстық су немесе бумен әрекеттесуін сипаттау; 8.2.4.3 Металдар коррозиясын туындатуға әсер ететін жағдайларды зерттеу; 8.2.4.5 Металдардың қышқылдармен әрекеттесуінің реакция теңдеулерін құрастыру; 8.2.4.8 Металдардың белсенділік қатарын қолданып металдардың таныс емес орынбасу реакцияларының жүру мүмкіндігін болжау. |
|
Бағалау критерийі |
Білім алушы: |
|
|
● Белсенді металдардың салқын сумен, ыстық су немесе бумен әрекеттесуін сипаттайды; ● Металдар коррозиясын туындатуға әсер ететін жағдайларды зерттейді; ● Металдардың қышқылдармен әрекеттесуінің реакция теңдеулерін жазады; ● Металдардың белсенділік қатарын қолданып металдардың таныс емес орынбасу реакцияларының жүру мүмкіндігін болжайды. |
|
Ойлау дағдыларының деңгейлері |
Қолдану, жоғары деңгей дағдылары |
|
Орындау уақыты |
20 минут |
Тапсырма
1. Металдардың сумен әрекеттесуі берілген кестені қажетті сөздермен толықтырыңыз.
|
Металл |
Сумен әрекеттескендегі металдың белсенділігі |
Түзілген өнімдер |
|
Калий |
|
|
|
Мырыш |
|
|
|
Алтын |
|
|
[3]
2. а) Неліктен табиғатта алтынның бос күйінде кездесетінін, ал мырыштың бос күйінде кездеспейтінің түсіндіріңіз.
________________________________________________________________
__________________________________________________________________
[2]
b) Неліктен ертеректе темір ақша жасауда күмісті пайдаланды?
__________________________________________________________________
[1]
с) Металдар коррозиясының алдын алу үшін бір ұсыныс жазыңыз.
__________________________________________________________________
[1]
3. Металдардың қышқылдармен әрекеттесу белсенділігі әр түрлі. Төменде берілген реакция теңдеулерін жазыңыз.
1) Мырыштың сұйылтылған тұз қышқылымен әрекеттесуі
______________________________________________________________________
2) Магнийдің сұйылтылған күкірт қышқылымен әрекеттесуі
______________________________________________________________________
3) Күмістің сұйылтылған тұз қышқылымен әрекеттесуі
______________________________________________________________________
[3]
4. a) Оқушы химия зертханасында металдар мен тұздарды пайдалана отырып тәжірибе жасады. Металдар мен тұз ерітінділері арасында мүмкін болатын реакция теңдеулерін анықтаңыз (х-реакция жүрмейді, ˅ - реакция жүреді).
|
Тұз ерітінділері |
Мыс |
Қалайы |
Магний |
|
Мырыш сульфаты |
|
|
|
|
Темір хлориді |
|
|
|
|
Қорғасын (ІІ) нитраты |
|
|
|
Мүмкін болған реакция теңдеулерін жазыңыз:
___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
[4]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
Ескерту |
|
Білім алушы |
||||
|
Белсенді металдардың салқын сумен, ыстық су немесе бумен әрекеттесуін сипаттайды;
|
1 |
Калийдің сумен әрекеттесу белсенділін және реакция өнімін жазады Мырыштың сумен әрекеттесу белсенділін және реакция өнімін жазады Алтынның сумен әрекеттесу белсенділін және реакция өнімін жазады |
1 1 1 |
|
|
Металдар коррозиясын туындатуға әсер ететін жағдайларды зерттейді |
2 а) |
Табиғатта алтынның бос күйінде кездесу себебін жазады |
1 |
|
|
Табиғатта мырыштың қосылыс түрінде кездесу себебін жазады |
1 |
|
||
|
2 b) |
Күмістің темір ақша жасауда қолданылу себебін жазады |
1 |
|
|
|
2 с) |
Металдар коррозиясының алдын алудың бір ұсынысын жазады |
1 |
|
|
|
Металдардың қышқылдармен әрекеттесуінің реакция теңдеулерін жазады; |
3 |
Мырыштың сұйылтылған тұз қышқылымен әрекеттесу теңдеуін жазады |
1 |
|
|
Магийдің сұйылтылған тұз қышқылымен әрекеттесу теңдеуін жазады |
1 |
|
||
|
Күмістің сұйылтылған тұз қышқылымен әрекеттесу теңдеуін жазады |
1 |
|
||
|
Металдардың белсенділік қатарын қолданып металдардың таныс емес орынбасу реакцияларының жүру мүмкіндігін болжайды |
4 а) |
Мыстың тұз ертініділерімен мүмкін болатын реакция теңдеулерін жазады |
1 |
|
|
Қалайының тұз ертініділерімен мүмкін болатын реакция теңдеулерін жазады |
1 |
|
||
|
Магнийдің тұз ертініділерімен мүмкін болатын реакция теңдеулерін жазады |
1 |
|
||
|
b) |
Металдардың белсенділік қатарына байланысты орынбасу реакцияларның жүру мүмкіндігін жазады |
1 |
|
|
|
c) |
Берілген металдардың белсенділік қатарын жазады |
1 |
|
|
|
Барлығы |
15 |
|
||
«Зат мөлшері» және «Стехиометриялық есептеулер» бөлімдері
бойынша жиынтық бағалау
|
Оқу мақсаты |
8.1.1.3 Масса, зат мөлшері және құрылымдық санын есептеу; 8.2.3.5 Химиялық реакция теңдеулері бойынша заттың массасын, зат мөлшерін есептеу; 8.2.3.6 Авогадро заңын білу және стандартты жағдайлардағы газдар көлемін есептеуде молярлық көлемді қолдану; 8.2.3.7 Газдардың салыстырмалы тығыздығын және заттың молярлық массасын салыстырмалы тығыздық бойынша есептеу 8.2.3.8 Газдардың қатысуымен жүретін реакциялар бойынша есептер шығаруда газдардың көлемдік қатынас заңын қолдану |
|
Бағалау критерийі |
Білім алушы ● Зат массасы, мөлшері және құрылымдық бөлшектер санын есептеуде формуланы қолданып есептейді; ● Химиялық реакция теңдеуі бойынша зат массасын, зат мөлшерін анықтайды; ● Молярлық көлемді қолданып есептеулер жүргізеді; ● Салыстырмалы тығыздық бойынша газдың тығыздығын және заттың молярлық массасын есептейді; ● Есептер шығаруда газдардың көлемдік қатынас заңын қолданып есептеулер жүргізеді. |
|
Ойлау дағдыларының деңгейі |
Қолдану, жоғары деңгей дағдылары |
|
Орындалу уақыты |
20 минут |
Тапсырма
1. Молекулалар саны 12,04•1023 тең оттек газының зат мөлшері және массасын есептеңіз.
А) 3 моль және 96 г
В) 2 моль және 64 г
С) 1 моль және 32 г
D) 0,5 моль және 16 г
[2]
2. Массасы 26 г мырыш сұйылтылған тұз қышқылымен әрекеттесті. Түзілген мырыш хлоридінің массасын, зат мөлшерін табыңыз.
а) Мырыштың сұйылтылған тұз қышқылымен әрекеттесуінің реакция теңдеуін жазыңыз.
___________________________________________________________________
[1]
b) Мырыш хлоридінің массасын есептеңіз.
_________________________________________________________________________________________________________________________________________
[1]
c) Мырыш хлоридінің зат мөлшерін есептеңіз.
_________________________________________________________________________________________________________________________________________
[1]
3.Газдардың күйін сипаттайтын шамалар: қысым, көлем, температура. Газдарды сипаттағанда көбінесе қысым мен температураны тұрақты етіп алып, көлемнің өзгерістерін қарастырамыз, көлемнің өзгерісі газдар үшін деңгейлес болады, себебі олардың молекулааралық қашықтықтары шамамен бірдей.

Келесі тұжырымдардың шындық не жалған екендігін анықтап, кестеге шындық болса «+», жалған болса « -» белгісін қойыңыз.
|
Тұжырымдар |
Шындық |
Жалған |
|
5 моль азот молекуласының (қ.ж.) көлемі 112 л/моль болады |
|
|
|
1 моль сутек молекуласының (қ.ж.) көлемі 11,2 л/моль болады |
|
|
|
0,5 моль неон атомының көлемі 11,2 л/моль болады |
|
|
|
2 моль хлор молекуласының (қ.ж.) көлемі 22,4 л/моль болады |
|
|
[2]
4. Белгісіз газдың ауа бойынша салыстырмалы тығыздығы 1,103-ке тең. Осы газдың молярлық массасын табыңыз.
![]()
![]()
![]()
[1]
5. Табиғатта найзағай ойнағанда аудағы азот оттекпен қосылып, азот(II) оксидін түзеді.
-
Осы құбылыс кезінде жүретін реакцияның теңдеуін жазыңыз.
_______________________________________________________________________________________________________________________________________
[1]
-
Реакцияға түсетін газдардың көлемдік қатынасын анықтаңыз.
__________________________________________________________________________________________________________________________________________________________________________________________________________________
[1]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
|
Білім алушы |
|||
|
Зат массасы, мөлшері және құрылымдық бөлшектер санын есептеуде формуланы қолданып есептейді |
1 |
оттек газының зат мөлшерін есептейді; |
1 |
|
оттек газының массасын есептейді; |
1 |
||
|
Химиялық реакция теңдеуі бойыншазат массасын, зат мөлшерін анықтайды |
2 |
мырыштың сұйылтылған тұз қышқылымен әрекеттесуінің реакция теңдеуін жазады; |
1 |
|
мырыш хлоридінің массасын табады; |
1 |
||
|
мырыш хлоридінің зат мөлшерін табады; |
1 |
||
|
Молярлық көлемді қолданып есептеулер жүргізеді |
3 |
кестеге шындық болса «+» қояды; |
1 |
|
жалған болса « -» белгісін қояды; |
1 |
||
|
Салыстырмалы тығыздық бойынша газдың тығыздығын және заттың молярлық массасын есептейді |
4 |
ауамен салыстырғандағы тығыздығы бойынша белгісіз газдың молярлық массасын есептейді; |
1 |
|
Есептер шығаруда газдардың көлемдік қатынас заңын қолданып есептеулер жүргізеді |
5 |
азот(II) оксидін түзілунің реакция теңдеуін жазады; |
1 |
|
газдардың көлемдік қатынасын анықтайды. |
1 |
||
|
Барлығы |
10 |
||
«Химиялық реакциядағы энергиямен танысу» бөлімі бойынша
жиынтық бағалау
Оқу мақсаты 8.3.1.1 Заттың жану реакциясының өнімі көбінесе
оксид екенін және құрамында көміртегі бар
отын оттекте жанғанда, көмірқышқыл газы,
иіс газы немесе көміртек түзілетінін түсіну
-
8.3.1.2 Парниктік эффекттің себептерін түсіндіру және
-
шешу жолдарын ұсыну
-
8.3.1.3 Экзотермиялық реакциялар жылу бөле
-
жүретінін, ал эндотермиялық реакциялар
-
жылу сіңіре жүретінін білу
8.3.1.5 Энергия өзгерісін бөлшектердің кинетикалық
теориясы тұрғысынан түсіндіру
Бағалау критерийі Білім алушы
• Көміртекті отындар жанғанда түзілетін
оксидтерді және олардың қасиеттерін
анықтайды
• Парниктік эффектінің себептерін түсіндіреді
және шешу жолдарын ұсынады
• Экзотермиялық және эндотермиялық
реакцияларды ажыратады
• Энергия өзгерісін бөлшектердің кинетикалық
теориясы тұрғысынан сипаттайды
Ойлау дағдыларының деңгейі Білу және түсіну
Қолдану
Жоғары деңгей дағдылары
Орындалу уақыты 20 минут
Тапсырма
1(a) «Иіс газы» деп аталатын көміртек оксидінің формуласын белгілеңіз.
-
CO2
-
CH4
-
С3H8
-
SO2
-
СО
[1]
(b) Көміртек оксидтері жөніндегі тұжырымның шындық/жалғандығын «˅» белгісін қою арқылы анықтаңыз.
|
Тұжырымдар |
Шындық |
Жалған |
|
Көміртек(IV) оксиді жануды қолдамайды |
|
|
|
Көміртек(II) оксиді отын толық жанғанда түзіледі |
|
|
|
Көміртек(II) оксиді түссіз, иіссіз, өте улы газ |
|
|
|
Көміртек(II) оксидінің тотықтырғыш қасиеті бар |
|
|
|
Көміртек(IV) оксиді тұрмыстық пропан газы жанғанда түзіледі |
|
|
[5]
2. Атмосфераның құрамы мен жағдайы ғарышпен жер арасындағы сәуле, жылу алмасу процесіне әсер етеді. Күннен жерге немесе жерден ғарышқа қуат берілу процесі биосферадағы температураны белгілі бір деңгейде сақтайды. Мұнда биосферадағы температура жағдайын сақтап тұруда жерге жылу қуатын алып келетін күн радиациясының рөлі жоғары. Осы процесс бірі-бірімен тығыз байланыста болады. Сондықтан жердегі жылу балансының өзгеруі биосфераның орта температурасының ұлғаюына әкелуі мүмкін.
https://kk.wikipedia.org/wiki/ Парниктік эффект
(а) Парниктік эффектінің пайда болу себептеріне үш мысал келтіріп, түсіндіріңіз.
___________________________________________________________________________________________________________________________________________________________________________________________________________
[1]
(b) Парниктік эффектінің салдарларын азайтудың екі жолын ұсыныңыз.
1._____________________________________________________________________
2._____________________________________________________________________
[1]
3. Экзотермиялық, эндотермиялық, жылу эффектісі, термохимиялық теңдеу терминдерін сипаттайтын тұжырымдармен сәйкестендіріңіз.
|
Терминдер |
Тұжырымдар |
|
1. Экзотермиялық |
А) Химиялық реакцияның жылу эффектісі көрсетілген теңдеу |
|
2. Эндотермиялық |
В) Химиялық реакция кезінде бөлінетін немесе сіңірілетін жылу мөлшері |
|
3. Жылу эффектісі |
С) Жылу сіңіре жүретін реакция |
|
4. Термохимиялық теңдеу |
D) Жылу бөле жүретін реакция
|
1.______ 2._____ 3._____ 4._____
[4]
4. Фосфор оттекпен жарық шығара отырып, қарқынды жанады. Фосфор жанғанда, ақ түтін будақтап, оның оксиді түзіледі. Фосфордың жану реакциясының жылу эффектісі 3010 кДж тең.
https://surak.baribar.kz/648573/
(а) Осы реакцияның термохимиялық теңдеуін жазып көрсетіңіз.
__________________________________________________________________________________________________________________________________________________________________ [1]
(b) Азот пен оттектің аз мөлшерлері найзағай ойнаған кезде өзара әрекеттесіп, оксид түзеді. Осы құбылыс кезінде химиялық реакция энергиясы өзгереді. Энергия тұрғысынан реакция типін ажыратып жазыңыз.
_______________________________________________________________________________________________________________________________________________________________________________________________________________
[1]
Балл қою кестесі
|
Бағалау критерийі |
Тапсыр ма № |
Дескриптор |
Балл |
|
Білім алушы |
|||
|
Көміртекті отындар жанғанда түзілетін оксидтерді және олардың қасиеттерін анықтайды |
1 |
«Иіс газы» деп аталатын көміртек оксидінің формуласын анықтайды |
1 |
|
Көміртек (IV) оксиді жануды қолдамайды деген тұжырымның шындық екенін анықтайды |
1 |
||
|
Көміртек (II) оксиді отын толық жанғанда түзіледі деген тұжырымның жалған екенін анықтайды |
1 |
||
|
Көміртек (II) оксиді түссіз, иіссіз, өте улы газ деген тұжырымның шындық екенін анықтайды |
1 |
||
|
Көміртек (II) оксидінің тотықтырғыш қасиеті бар деген тұжырымның жалған екенін анықтайды |
1 |
||
|
Көміртек(IV) оксиді тұрмыстық пропан газы жанғанда түзіледі деген тұжырымның шындық екенін анықтайды |
1 |
||
|
Парниктік эффектінің себептерін түсіндіреді және шешу жолдарын ұсынады |
2 |
Парниктік эффектінің пайда болу себептеріне үш мысал келтіріп, түсіндіреді |
1 |
|
Парниктік эффектінің салдарларын азайтудың екі жолын ұсынады |
1 |
||
|
Экзотермиялық және эндотермиялық реакцияларды ажыратады |
3 |
Химиялық реакцияның жылу эффектісі көрсетілген теңдеудің термохимиялық теңдеу екенін сәйкестендіреді |
1 |
|
Жылу бөле жүретін реакциялар экзотермиялық екенін сәйкестендіреді |
1 |
||
|
Жылу сіңіре жүретін реакциялар эндотермиялық екенін сәйкестендіреді |
1 |
||
|
Химиялық реакция кезінде бөлінетін немесе сіңірілетін жылу мөлшерінің жылу эффектісі екенін сәйкестендіреді |
1 |
||
|
Энергия өзгерісін бөлшектердің кинетикалық теориясы тұрғысынан сипаттайды |
4 |
Фосфордың жану реакциясының термохимиялық теңдеуін жазады |
1 |
|
Энергия тұрғысынан реакция типін анықтайды. |
1 |
||
|
Барлығы |
14 |
||
«Сутек. Оттек және озон» бөлімі бойынша жиынтық бағалау
|
Оқу мақсаты |
8.4.2.1 Сутекті алу және оның қасиеттері мен қолданылуын зерттеу;
|
|
Бағалау критерийі |
Білім алушы ● Сутектің алыну жолын және оның қасиеттері мен қолданылуын сипаттайды; ● Оттекті алудың реакция теңдеуін және оттектің қасиеттері мен қолданылуын сипаттайды; ● Оттектің аллотропиялық түрөзгерістерінің құрамы мен қасиеттерін сәйкестендіреді; ● Озон қабатының маңызын түсіндіреді. |
|
Ойлау дағдыларының деңгейі |
Қолдану, жоғары деңгей дағдылары |
|
Орындалу уақыты |
20 минут |
Тапсырма
1. Зертханада сутекті алуға болатын заттардың қатарын көрсетіңіз
A) HNO3, Н2О,NaOH
B) СН4, С, Н2О
C) Н2О,Zn, НСl, Са
D) КMnO4, H2O, НCIO3
[]

(d) Жиналған газ сутегі газы екендігін дәлелдеңіз.
__________________________________________________________________________________________________________________________________________________________________________________________________________________
(e) Сутектің қолданылуына мысал келтіріңіз.
___________________________________________________________________________________________________________________________________________
[5]
3. Оттегі – химияның ең маңызды элементі және Жер бетіндегі көптеген тірі ағзалардың тыныс алуын қамтамасыз етеді.
а) Оттек туралы келесі тұжырымдардың шындық не жалған екендігін анықтап, кестеге шындық болса «+», жалған болса « -» белгісін қойыңыз.
|
Тұжырымдар |
Шындық |
Жалған |
|
1 Иіссіз, дәмсіз, түссіз газ |
|
|
|
2 Аудан жеңіл |
|
|
|
3 Суды ығыстыру арқылы жинауға болады |
|
|
|
4 -1830С сұйылады |
|
|
|
5 Суда жақсы ериді |
|
|
[2]
b) Өзгерістер тізбегі берілген: КМnO4 → А → Р2O5
c) А затын анықтаңыз __________________________________________________
[1]
d) КMnO4 -тен А затын алудың реакция теңдеуін жазыңыз
______________________________________________________________________
[1]
e) А затының алдына қойылатын коэффициентті анықтаңыз
4Р + А → 2Р2O5
______________________________________________________________________
[1]
4. Зат мөлшері 2 моль оттек(қ.ж.) қандай көлем алады?
![]()
[1]
5. Озон – химиялық формуласы О3 болып келетін оттегінің аллотропиялық түр өзгерісі. Түсі қою көк, өткір иісті газ,ал сұйық озон күлгін көк; балқу t – 192,7°С, қайнау t – 112°С. Суда ерігіштігі 0,394 г/л (0°С-та).
Төменде берілген сурет бойынша озонның қолданылу салаларын анықтаңыз.

[1]
6. Озон қабаты (озоносфера) бүкіл Жер шарын 10-50 км аралығында қоршап тұр, ал ең көп жинақталуы 20-25 км биіктікте болады. «Озон тесігі» деген атау алып, Антарктида үстіндегі кеңістікте озон мөлшерінің (50%) төмендеуіне байланысты ең бірінші озон қабатының жұқаруы 1985 жылы жүрт назарына ілікті. Содан бергі өлшеулер нәтижесі озон қабатының азаюын дәлелдеуде. Жердің озон қабатының бұзылуы адам, жануарлар, өсімдіктер мен микроағзалар тіршілігі үшін қатер болып табылады.
Озон қабатының бұзылуына себеп болатын жағдайларға екі мысал келтіріп жазыңыз.
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
[2]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
|
Білім алушы |
|||
|
Сутекті алу және оның қасиеттері мен қолданылуын сипаттайды |
1, 2 |
зертханада сутекті қандай заттардан алуға болатынын анықтайды; |
1 |
|
қай суретте сутек газын жинау әдісі көрсетілгенін дұрыс анықтайды; |
1 |
||
|
Өз таңдауын түсіндіреді; |
1 |
||
|
сутек газын зертханада алу үшін қолданылатын реактивтерді анықтайды; |
1 |
||
|
жиналған газдың сутек екенін дәлелдейді; |
1 |
||
|
сутектің қолданылуына мысал келтіреді; |
1 |
||
|
Оттекті алудың реакция теңдеуін және оттектің қасиеттері мен қолданылуын сипаттайды |
3,4 |
кестеге шындық болса «+» қояды; |
1 |
|
жалған болса « -» белгісін қояды; |
1 |
||
|
тізбектегі А затын анықтайды; |
1 |
||
|
калий перманганатын айырып А затын алудың реакция теңдеуін жазады; |
1 |
||
|
А затының алдына қойылатын коэффициентті анықта |
1 |
||
|
зат мөлшері белгілі газдың көлемін дұрыс есептейді; |
1 |
||
|
Оттектің аллотропиялық түрөзгерістерінің құрамы мен қасиеттерін сәйкестендіреді |
5 |
берілген сурет бойынша озонның қолданылу салаларын анықтайды; |
1 |
|
Озон қабатының маңызын түсіндіреді |
6 |
озон қабатының бұзылуына себеп болатын жағдайларға екі мысал келтіріп жазады; |
2 |
|
Барлығы |
15 |
||
«Химиялық элементтердің периодтық жүйесі» бөлімі бойынша жиынтық бағалау
|
|
|
|
Оқу мақсаты |
8.2.1.1 Топ, период, атом нөмірінің физикалық мәнін түсіндіру; 8.2.1.3 Топтар мен периодтарда элементтер қасиеттерінің заңдылықпен өзгеретінін түсіндіру; 8.2.1.4 Периодтық жүйедегі орны бойынша химиялық элементті сипаттау; 8.2.1.6 Химиялық элементтердің табиғи ұяластарын білу және сілтілік металдар, галогендер, инертті элементтердің ұяластарына мысалдар келтіру; 8.2.1.7 Химиялық элементтің периодтық кестеде орналасуына сай қасиеттерін болжау. |
|
Бағалау критерийі |
Білім алушы: |
|
|
● Топ, период, атом нөмірінің физикалық мәнін сипаттайды; ● Элементтер қасиеттерінің топтар мен периодтарда заңдылықпен өзгеретінін түсіндіреді; ● Химиялық элементтерді периодтық жүйедегі орны бойынша сипаттайды; ● Химиялық элементтердің табиғи ұяластарын атайды және олардың таңбасын жазады; ● Периодтық кестеде орналасуына байланысты химиялық элементтің қасиетін болжайды. |
|
Ойлау дағдыларының деңгейлері |
Қолдану, жоғары деңгей дағдылары |
|
Орындау уақыты |
20 минут |
Тапсырма
1. Элементтердің келесі қатары берілген. Берілген тұжырымдар мен химиялық элементтер арасындағы сәйкестікті анықтаңыз.
|
Тұжырымдар |
Химиялық элементтер |
|
1) элементтің 6 электроны бар |
A) Ag |
|
2) элементтің 7 нейтроны бар |
B) Al |
|
3) элементтің 5 энергетикалық деңгейі бар |
C) N |
|
4) элементтің протон санының мәні 3-ке тең |
D) Li |
|
5) элементтің соңғы энергетикалық деңгейінде 3 электрон бар |
E) C |
1) ___ 2)___ 3)___ 4)____ 5)___
[2]
2. a) Берілген кесте бойынша дұрыс жауаптарды анықтаңыз.
|
|
Период бойынша (солдан оңға қарай) |
Топ бойынша (жоғарыдан төмен қарай) |
|
1) Энергетикалық деңгей саны |
А) өзгермейді B) 1 энергетикалық деңгейге артады |
C) өзгермейді D) 1 энергетикалық деңгейге артады |
|
2) Сыртқы энергетикалық деңгейдегі электрон саны |
А) 1-ге артады B) тұрақты |
C) 1-ге артады D) тұрақты |
1) _______________
2) _______________
[2]
b) Берілген химиялық элементтердің қасиеттерінің периодты өзгеруіне байланысты тұжырымдардың бос орындарын қажетті сөздермен толықтырыңыз.

Период бойынша (солдан оңға қарай)
![]()
![]()


2. Атом радиусы ______________
1. Салыстырмалы атомдық масса _______________

Топ бойынша (жоғарыдан төмен қарай)
![]()
![]()


4. Оттекпен қосылысындағы валенттілігі ____________
3. Металдық қасиет ___________
[2]
3. Химиялық элементтің нейтрон санының мәні 12-ге тең. Бұл элемент ядролық реакторларда жылу тасымалдаушы ретінде, органикалық реакцияларда өршіткі, медицинада радиоактивті изотоп күйінде қолданылады. Периодтық жүйедегі орны және атом құрылысы тұрғысынан химиялық элементке сипаттама беріңіз.
1. Элементтің атомдық нөмірі __________________________________________
2. Периодтық жүйедегі орны ___________________________________________
3. Атом құрамы _____________________________________________________
4. Элементтен түзілген жай заттың қасиеті _______________________________
[4]
4. Берілген химиялық элементтерді табиғи ұялас топтарына топтастырыңыз және әр топты екі мысалмен толықтырыңыз.
Na, Cl, He, Li, Br, Ne, Rb, I, Kr
|
Табиғи топтар |
Ұялас элементтер |
Мысалдар |
|
Сілтілік металдар |
|
|
|
Галогендер |
|
|
|
Инертті газдар |
|
|
[3]
5. Кестеде бірінші топтың негізгі топша элементінің физикалық және химиялық қасиеттері берілген. Литий элементі үшін бос орындарды өз болжамыңызбен толықтырыңыз.
|
Химиялық элемент |
Валенттілігі |
Физикалық қасиеті |
Сумен әрекеттесуі |
|
Натрий |
І |
Ашық металдық жылтыры бар |
Шабытты |
|
|
|
|
|
[3]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
Ескерту |
|
Білім алушы |
||||
|
Топ, период, атом нөмірінің физикалық мәнін сипаттайды
|
1 |
Атом нөмірінің физикалық мәнін сипаттайды Периодтың физикалық мәнін сипаттайды |
1 1 |
|
|
Элементтер қасиеттерінің топтар мен периодтарда заңдылықпен өзгеретінін түсіндіреді |
2 а) |
Энергетикалық деңгей санының периодты өзгеруін анықтайды |
1 |
|
|
Сыртқы энергетикалық деңгейдегі электрон санының периодты өзгеруін анықтайды |
1 |
|
||
|
2 b) |
Химиялық элементтердің период бойынша өзгеретін қасиеттерін сипаттайды |
1 |
|
|
|
Химиялық элементтердің топ бойынша өзгеретін қасиеттерін сипаттайды |
1 |
|
||
|
Химиялық элементтерді периодтық жүйедегі орны бойынша сипаттайды |
3 |
Химиялық элементтің атомдық нөмірін анықтайды |
1 |
|
|
Периодтық жүйедегі орнын сипаттайды |
1 |
|
||
|
Атом құрамын анықтайды |
1 |
|
||
|
Элемент түзетін жай зат қасиетін сипаттайды |
1 |
|
||
|
Химиялық элементтердің табиғи ұяластарын атайды және олардың таңбасын жазады |
4 |
Сілтілік металдарды анықтайды, мысалдар келтіреді |
1 |
|
|
Галогендерді анықтайды, мысалдар келтіреді |
1 |
|
||
|
Инертті газдарды анықтайды, мысалдар келтіреді |
1 |
|
||
|
Периодтық кестеде орналасуына байланысты химиялық элементтің қасиетін болжайды |
5 |
Химиялық элементтің валенттілігін анықтайды |
1 |
|
|
Химиялық элементтің физикалық қасиетін сипаттайды |
1 |
|
||
|
Химиялық элементтің сумен әрекеттесуін сипаттайды |
1 |
|
||
|
Барлығы |
16 |
|
||
«Химиялық байланыс түрлері» бөлімі бойынша жиынтық бағалау
Оқу мақсаты 8.1.4.1 Электртерістілік ұғымы негізінде атомдар
арасындағы ковалентті байланыстың түзілуін
түсіндіру;
8.1.4.2 Иондық байланыстың түзілу механизмін
сипаттау және иондық қосылыстардың
қасиеттерін болжау;
8.1.4.3 Заттар қасиеттерінің кристалдық тор типтеріне
тәуелділігін түсіндіру.
Бағалау критерийі Білім алушы
-
Берілген формулалардағы электртерістігі үлкен элементті анықтайды
-
Атомдар арасындағы ковалентті байланыстың
түзілуін сипаттайды
-
Иондық байланыстың түзілу механизмін сипаттайды, иондық қосылыстардың қасиеттерін болжайды
-
Заттар қасиеттерінің кристалдық тор типтеріне тәуелділігін түсіндіреді
Ойлау дағдыларының Білу және түсіну деңгейі Қолдану
Жоғары деңгей дағдылары
Орындалу уақыты 20 минут
Тапсырма
1.Берілген формулалардағы электртерістілігі жоғары элементті анықтаңыз.
А) KCl
В) CuS
С) HF
D) CaO
Е) HI [1]
2. а) Атомдар арасында ковалентті байланыстың түзілуін электрондардың ортақ жұбы арқылы түзілуін көрсетіңіз.




![]()
![]()
![]()
сутегі сутегі
Ковалентті байланыстың бұл түрі электртерістілігі қандай атомдар арасында түзіледі ?
Ковалентті байланыстың бұл түрін қалай атайды?
______________________________________________________________________[2]



 b)
b)
![]()
![]()
![]() сутегі
йод
сутегі
йод
Ковалентті байланыстың бұл түрі электртерістілігі қандай атомдар арасында түзіледі ?
Ковалентті байланыстың бұл түрін қалай атайды?
______________________________________________________________________[1]
3. а) Берілген атомдар арасында иондық байланыстың түзілу механизмін көрсетіңіз.






![]()
калий хлор
[1]
b) Құрамында иондық байланысы бар, натрий хлоридінің кейбір физикалық қасиеттері туралы тұжырымдардың шындық не жалған екенін (˅) белгісімен анықтаңыз.
|
Тұжырым |
Шындық |
Жалған |
|
Натрий хлориді қатты, кристалл зат |
|
|
|
Қаттылығы және балқу температурасы төмен |
|
|
|
Суда жақсы ериді, органикалық еріткіште нашар ериді |
|
|
|
Ерітінділері мен балқымалары электр тогын мүлдем өткізбейді |
|
|
|
Балқу температурасы 801ºC |
|
|
[1]
Есептер мен жаттығулар жинағы, 8-сыныпқа арналған оқулық /Ә.Е.Темірбулатова, -Алматы: "Мектеп," 2004 жыл. 100-102 беттер/
4. Берілген заттардың формулалары бойынша кристалдық торын, балқу және қайнау температурасын анықтап, тор көзді толтырыңыз.
|
№ |
Формулалары |
Кристалдық торлардың түрі |
tºқайнау |
tºбалқу |
|
1 |
С |
|
|
|
|
2 |
СО2 |
|
|
|
|
3 |
NaCl |
|
|
|
[2]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / М.Қ.Оспанова, Қ.С.Ахуадиева, Т.Г.Белоусова, - Алматы:Мектеп,2018. 126-136 беттер.
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
|
Білім алушы |
|||
|
Берілген формулалардағы электртерістігі үлкен элементті анықтайды |
1 |
Электртерістігі үлкен элементті анықтайды |
1 |
|
Атомдар арасындағы ковалентті байланыстың түзілуін сипаттайды |
2 а) |
Ковалентті байланыс түрлерін ажыратады |
1 |
|
H2 -молекуласындағы ковалентті байланыстың түзілуі механизмін анықтайды |
1 |
||
|
2 b) |
HI- молекуласындағы ковалентті байланыстың түзілу механизмін құрастырады |
1 |
|
|
Иондық байланыстың түзілу механизмін сипаттайды, иондық қосылыстардың қасиеттерін болжайды |
3 а) |
Калий хлоридіндегі байланыстың түзілу механизмін құрастырады |
1 |
|
3 b) |
Натрий хлоридінің физикалық қасиетін болжап, анықтайды |
1 |
|
|
Заттар қасиеттерінің кристалдық тор типтеріне тәуелділігін түсіндіреді |
4 |
Кристалдық торлар түрін анықтайды |
1 |
|
Балқу және қайнау температурасын анықтайды |
1 |
||
|
Барлығы |
8 |
||
«Ерітінділер және ерігіштік» бөлімі бойынша жиынтық бағалау
Оқу мақсаты 8.3.4.1 Заттардың судағы ерігіштігі бойынша жіктеу;
8.3.4.5 Еріген заттың массалық үлесі мен ерітіндінің
белгілі массасы бойынша еріген заттың
массасын есептеу;
8.3.4.6 Ерітіндідегі заттың молярлық концентрациясын
есептеу.
Бағалау критерийлері Білім алушы:
-
Суда ерігіштігіне байланысты заттарды жіктейді;
-
Массалық үлесі мен ерітіндінің белгілі массасы
бойынша еріген заттың массасын анықтайды;
-
Ерітіндідегі заттың пайыздық және молярлық концентрациясын анықтайды.
Ойлау дағдыларының деңгейлері Білу және түсіну
Қолдану
Орындалу уақыты 20 минут
Тапсырма
1![]()
![]()
![]()

![]()
![]()
![]()
![]()
![]()

Заттар ддддддддддддддллРРРррржжжжжжжжжжжжжжжжЗзЗзвввхххххрррррррррььььтиммЗаттаЗаттарЗзатта
![]()
![]()
![]()
[2]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / М.Қ.Оспанова, Қ.С.Ахуадиева, Т.Г.Белоусова, - Алматы:Мектеп,2018.138-141 беттер.
2. Натрий хлоридінің массалық үлесі 10% -тік массасы 300 г ерітіндісін даярлау үшін қажетті тұз бен судың массаларын есептеңіз.
|
|
[3]
3. а) Айран ұйыту үшін 4 кг сүтке 40 г ұйытқы салынды. Айран ұйытқының массалық үлесін есептеңіз.
|
|
[2]
b) Калий гидроксидінің көлемі 1500 мл ерітіндісінде 16 г еріген зат болса, осы ерітіндінің молярлық концентрациясы қанша болатынын есептеңіз.
|
|
[2]
Есептер мен жаттығулар жинағы, 8-сыныпқа арналған оқулық /Ә.Е.Темірбулатова, -Алматы: "Мектеп," 2004 жыл. 56-63 беттер/
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
|
Білім алушы |
|||
|
Суда ерігіштігіне байланысты заттарды жіктейді |
1 |
заттарды суда ерігіштігіне байланысты жіктейді |
1 |
|
әр түріне бір-екі мысалдан келтіреді |
1 |
||
|
Массалық үлесі мен ерітіндінің белгілі массасы бойынша еріген заттың массасын анықтайды |
2 |
еріген заттың және еріткіштің массасын табуға арналған формуланы қолданады |
1 |
|
еріген затты анықтайды |
1 |
||
|
еріткіштің массасын анықтайды |
1 |
||
|
Ерітіндідегі заттың пайыздық және молярлық концентрациясын анықтайды |
3 а) |
массалық үлесті табуға арналған формуланы қолданады |
1 |
|
массалық үлесті анықтайды |
1 |
||
|
3 b) |
ерітіндегі заттың молярлық концентрациясын табуға арналған формуланы қолданады |
1 |
|
|
ерітіндінің молярлық концентрациясын анықтайды |
1 |
||
|
Барлығы |
9 |
||
«Бейорганикалық қосылыстардың негізгі кластары. Генетикалық байланыс» бөлімі бойынша жиынтық бағалау.
Оқу мақсаты 8.3.4.7 Оксидтердің жіктелуін және қасиеттерін сипаттайтын
реакция теңдеулерін құрастыру;
8.3.4.8 Қышқылдардың жіктелуін, қасиеттерін білу және түсіну,
олардың химиялық қасиеттерін сипаттайтын реакция теңдеулерін
құрастыру;
8.3.4.9 Негіздердің жіктелуі мен қасиеттерін білу және түсіну,
олардың химиялық қасиеттерін сипаттайтын реакция
теңдеулерін құрастыру;
8.3.4.12 Бейорганикалық қосылыстардың негізгі кластары
арасындағы генетикалық байланысты зерттеу.
Бағалау критерийлері Білім алушы:
● Оксидтердің, қышқылдардың және негіздердің
жіктелуін, қасиеттерін анықтайды, реакция
теңдеулерін құрастырады
●Бейорганикалық қосылыстардың негізгі кластары
арасындағы генетикалық байланысты анықтайды
Ойлау дағдыларының деңгейлері Білу және түсіну
Қолдану
Орындалу уақыты 25 минут
Тапсырма
1. Калий оксидіне ( K2O) қатысты тұжырымды (-дарды) анықтаңыз.
А) қышқылдық
В) екі дайлы
С) негіздік
D) тұз түзетін
Е) түз түзбейтін
[1]
2. Сызбанұсқасы берілген, нүктелердің орнына тиісті формулаларды жазып, реакция теңдеуін құрастырыңыз.
CaO + H2O → …
Li2O +…→ LiCl +H2O
SO2 + NaOH →… + …
N2O5 + ...→ HNO3
BeO + KOH→ … + H2O
ZnO + HCl → … + H2O
[3]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / М.Қ.Оспанова, Қ.С.Ахуадиева, Т.Г.Белоусова, - Алматы:Мектеп,2018.153-154 беттер.
3. а) Берілген қышқылды жіктелуі бойынша сипаттаңыз.

құрамы бойынша
_............................___________________________


негізділігі бойынша
...............................


![]()
![]()
H2SiO3
ерігіштігі бойынша
.................................
[3]
b) Күкірт қышқылын мырыш оксидімен әрекеттесу реакция теңдеуін құрастырыңыз.
______________________________________________________________________
[1]
4. а) Суда еритін және суда ерімейтін негіздерді сәйкестендіріңіз.
|
№ |
Түрлері |
Негіздердің формулалары |
|
1
|
суда еритін негіздер (сілтілер) |
А. Cu(OH)2 |
|
В. LiOH |
||
|
С. Fe(OH)3 |
||
|
D. NaOH |
||
|
2
|
суда ерімейтін негіздер |
Е. Zn(OH)2 |
|
F. Al(OH)3 |
||
|
G. Ca(OH)2 |
||
|
H. KOH |
1._____________________________________
2._____________________________________
[2]
ә) Негіздердің қышқылдармен бейтараптану реакциясына бір мысал келтіріңіз.
____________________________________________________________________
[1]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / М.Қ.Оспанова, Қ.С.Ахуадиева, Т.Г.Белоусова, - Алматы:Мектеп,2018. 167-169-беттер.
5. Берілген заттардың формулаларын қолданып, генетикалық қатар құрыңыз.
K2O , H3PO4, K2CO3, P, Ca3(PO4)2 , P2O5, Na, NaOH, K
______________________________________________________________________
[2]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
|
Білім алушы |
|||
|
Оксидтердің, қышқылдардың және негіздердің жіктелуін, қасиеттерін анықтайды, реакция теңдеулерін құрастырады |
1 |
Калий оксидіне қатысты тұжырымдарды анықтайды. |
1 |
|
2 |
Негіздік оксидтердің сумен және қышқылдар мен реакция теңдеуін құрастырады. |
1 |
|
|
Қышқылдық оксидтердің сумен және сілтілермен реакция теңдеуін құрастырады. |
1 |
||
|
Екідайлы оксидтердің сілтілермен және қышқылдармен реакция теңдеуін құрастырады. |
1 |
||
|
3 а) |
Қышқылдарды құрамы бойынша жіктейді. |
1 |
|
|
Қышқылдарды негізділігі бойынша жіктейді. |
1 |
||
|
Қышқылдарды ерігіштігі бойынша жіктейді. |
1 |
||
|
3 b) |
Күкірт қышқылымен мырыш оксидінің арасындағы реакция теңдеуін құрастырады. |
1 |
|
|
4 |
Суда еритін негіздерді сәйкестендіреді. |
1 |
|
|
Суда ерімейтін негіздерді сәйкестендіреді. |
1 |
||
|
Негіздердің бейтараптану реакциясына мысал келтіріп жазады. |
1 |
||
|
Бейорганикалық қосылыстардың негізгі кластары арасындағы гентикалық байланысты анықтайды |
5
|
Берілген заттардың формулаларын қолданып, генетикалық қатар құрыңыз. |
2 |
|
Барлығы |
13 |
||
8.4 В «Көміртек және оның қосылыстары» тарауы бойынша жиынтық бағалау
|
Оқу мақсаты |
8.4.3.1 Көміртек неліктен көптеген қосылыстарында төрт байланыс түзетінін түсіндіру; |
|
|
8.4.3.3 Көміртектің аллотропиялық түр өзгерістерінің құрылысын және қасиеттерін салыстыру; |
|
|
8.4.3.5 Көміртектің физикалық және химиялық қасиеттерін зерттеу; |
|
|
8.4.3.7 Көмірқышқыл газын ала алу, оны анықтау және қасиеттерін зерттеу. |
|
Бағалау критерийі |
Білім
алушы |
|
|
• Көміртектің аллотропиялық түр өзгерістерінің құрылысын және қасиеттерін салыстырады; |
|
|
• Көміртек минералдарының: мрамор мен магнезиттің формуласын анықтайды және олардың құрамындағы көміртектің массалық үлесін есептейді; |
|
|
• Көміртектің физикалық және химиялық қасиеттерін сипаттайтын химиялық реакцияларды құрады; |
|
|
• Зертханада көмірқышқыл газын алып, оны анықтайды, қасиеттерін сипаттайды. |
|
Ойлау дағдыларының деңгейі |
Қолдану, жоғарғы деңгей |
|
Орындау уақыты |
20 минут |
Тапсырмалар
1. Бос орындарға қажетті сөздерді қойыңыз.
Көміртек __________ периодта ________топта орналасқан, _____________ байланыс түзеді,_______ электрон қосып алады және___________электрон беріп жібере алады. Қосылыстарында_________ тотығу дәрежесін көрсетеді және ___________ валентті.
[1]
2. Көміртек мрамор және магнезит минералдарының құрамына кіреді. Қай минералдың құрамында көміртектің массалық үлесі көп екенін анықтаңыз.
|
|
[5]
3. Көміртектің аллотропиялық түр өзгерістері мен қолдану саласы арасындағы сәйкестікті бағдарша арқылы көрсетіңіз.
|
Аллотропиялық түр өзгерістері |
Қолданылуы |
|
Графит |
Лазер қондырғыларында, қымбат тастар. |
|
Карбин |
Микроэлектроникадағы нанотүтікшелер |
|
Алмаз |
Қарындаш, қара бояу, электродтар. |
|
Фуллерен |
Жасанды қан тамырлары. |
[4]
4. Реакция теңдеуін аяқтаңыз:
-
С + Ва→ ________________________________________________
-
C + Al2O3→_______________________________________________
-
C + O2(жеткіліксіз)→__________________________________________
[3]
5. «+» белгісі арқылы көмірқышқыл газының физикалық қасиеті мен алынуына байланысты шындық, жалған тұжырымдарды анықтаңыз.
|
Тұжырымдар |
Шындық |
Жалған |
|
1. Түссіз, иіссіз, дәмсіз газ |
|
|
|
2. Мрамор мен тұз қышқылының әрекеттесуі арқылы алынады. |
|
|
|
3. Ауадан жеңіл. |
|
|
|
4. Көмір жанғанда пештерді оттек жеткіліксіз жағдайларда түзіледі. |
|
|
[1]
Балл қою кестесі
|
Бағалау критерийі |
Тапсырма № |
Дескриптор |
Балл |
|
Көміртектің қосылыстарында көбінесе 4 байланыс түзетінін түсіндіреді. |
1 |
Периодтық жүйедегі орны бойынша көміртек атомының валенттік мүмкіндігін анықтайды. |
1 |
|
Минералдардың формуласы анықтап, құрамындағы көміртектің массалық үлесі қайсысында көбірек екенін есептейді. |
2 |
Мрамордың формуласын жазады. |
1 |
|
Магнезиттің формуласын жазады. |
1 |
||
|
Мрамордың құрамындағы көміртектің массалық үлесін есептейді. |
1 |
||
|
Магнезиттің құрамындағы көміртектің массалық үлесін есептейді. |
1 |
||
|
Мрамор мен магнезиттің құрамындағы көміртектің массалық үлестерін салыстырады. |
1 |
||
|
Көміртектің аллотропиялық түр өзгерістерінің қолданылу салаларын зерттейді. |
3 |
Графиттің қолданылу саласын анықтайды. |
1 |
|
Алмаздың қолданылу саласын анықтайды. |
1 |
||
|
Карбиннің қолданылу саласын анықтайды. |
1 |
||
|
Фуллереннің қолданылу саласын анықтайды. |
1 |
||
|
Көміртектің химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрады. |
4 |
Көміртек пен барийдің арасындағы химиялық реакция теңдеуін жазады. |
1 |
|
Көміртек пен алюминий оксидінің арасындағы химиялық реакция теңдеуін жазады. |
1 |
||
|
Көміртектің оттек жеткіліксіз жағдайындағы химиялық реакция теңдеуін жазады. |
1 |
||
|
Көмірқышқыл газының қасиетін және алыну жолдарын сипаттайды. |
5 |
Көмірқышқыл газын сипаттайтын дұрыс жауаптарды таңдайды. |
1 |
|
Жалпы балл |
14 |
||
8.4С «Су» бөлімі бойынша жиынтық бағалау
|
Оқу мақсаты:
|
8.4.2.6. Судың кең таралуын, ерекше қасиеттерін және адам өміріндегі маңызын түсіндіру; |
|
|
8.4.2.7 Табиғаттағы судың айналымын түсндіру; |
|
|
8.4.2.9 Судың кермектігін және оны жою жолдарын түсіндіру. |
|
Бағалау критерийлері:
|
Білім алушылар:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ойлау дағдыларының деңгейі: |
Білу, түсіну және қолдану. |
|
Орындау уақыты: |
20 минут |
Тапсырмалар:
1. Келесі сөйлемдерге қажетті сөздерді қойып, сөйлемдерді аяқтаңыз:
Су әмбебап ........................................................................................................................
Судың агрегаттық күйлері: ...................................................................................................
Судың қайнау температурасы...............................................................................................
Судың қату температурасы ..................................................................................................
Судың тығыздығы .................................................................................................................
Табиғи судың құрамында ....................................................................................................
[3]
2. Шындық пен жалған тұжырымдарды « + », « - » таңбаларымен анықтаңыз:
|
Тұжырымдамалар |
Шындық |
Жалған |
|
Судың молекуласының құрылысы сызықтық |
|
|
|
Адам организмі 70 % судан тұрады |
|
|
|
CuSO4* 5 H2O мыс купоросы көгілдір түсті |
|
|
|
Су белсенді металдармен және олардың оксидтерімен әрекеттеспейді |
|
|
|
Сүйектегі судың мөлшері 31% |
|
|
[2]
3. «Судың кермектігінің түрлері» кестесін толтырыңыз:
|
Кермектік түрлері |
Кермектікті жою жолдары (реакция теңдеулері) |
|
Уақытша (карбонатты) кермектік судың құрамында
__________________________ болуына байланысты. |
_________________________________________ |
|
Тұрақты кермектік судың құрамында
__________________________ болуына байланысты. |
_________________________________________________ |
[4]
4![]() . а ) Суды тазалау этаптарын
көрсетіңіз:
. а ) Суды тазалау этаптарын
көрсетіңіз:
![]()
![]()
![]()
![]()
b) Суды дезинфекциялайтын зат формуласын анықтаңыз:
А) Cl2
Б) I2
В) F2
С) P
[2]
5. Судың табиғаттағы айналымы схемасындағы бос жерлерді толтырыңыз:
![]()
![]()

https://infourok.ru/prezentaciya-k-otkritomu-uroku-krugovorot-vodi-v-prirode-1721776.html
[2]
Балл қою кестесі
|
Бағалау критерийлері |
№ |
Дескрипторлар |
Балл |
|
Оқушылар |
|
|
|
|
Судың физикалық қасиеттерін сипаттайды; |
1 |
Судың агрегаттық күйлерін дұрыс анықтайды. |
1 |
|
Судың қайнау және балқу температурасын дұрыс жазады. |
1 |
||
|
Судың ерекшелігін сипаттайды. |
1 |
||
|
Су молекуласының құрылысын және қасиеттерін анықтайды; |
1 |
Судың қасиеттерін сипаттайтын шындық, жалған тұжырымдарды дұрыс анықтайды. |
2 |
|
Судың кермектігін және оны жою жолдарын сипаттайды; |
1 |
Суды қайнату арқылы гидрокарбонаттарды ыдырату теңдеуін жазады. |
1 |
|
Соданың гидрокарбонатқа әсерін сипаттайтын реакция теңдеуін жазады. |
1 |
||
|
Ізбес суының судың кермектігін жою теңдеуін жазады. |
1 |
||
|
Соданың сульфаттарды жою теңдеуін жазады. |
1 |
||
|
Суды тазалау процесін сипаттайды; |
2 |
Суды тазалау этаптарын дұрыс жазады. Суды дезинфекциялауға арналған заттың формуласын табады. |
1 1 |
|
Табиғаттағы судың айналымын сипаттайды. |
1 |
Судың булануын жазады. Бұлттың түзілуін жазады. |
1 1 |
|
Барлығы |
13 |
||
I ТОҚСАННЫҢ ЖИЫНТЫҚ БАҒАЛАУ СПЕЦИФИКАЦИЯСЫ
I тоқсанның жиынтық бағалауына шолу
Жиынтық бағалаудың өткізілу уақыты - 40 минут
Балл саны - 25
Тапсырмалар түрлері:
КТБ- Көп таңдауды бар тапсырмалар;
ҚЖ- Қысқа жауапты қажет ететін тапсырмалар;
ТЖ -Толық жауапты қажет ететін тапсырмалар.
Жиынтық бағалаудың құрылымы
Берілген нұсқа көп таңдауы бар тапсырмаларды, қысқа және толық жауапты қажет ететін сұрақтарды қамтитын 12 тапсырмадан тұрады. Көп таңдауы бар тапсырмаларға оқушылар ұсынылған жауап нұсқаларынан дұрыс жауабын таңдау арқылы жауап береді.
Қысқа жауапты қажет ететін сұрақтарға сөздер немесе қысқа сөйлемдер түрінде жауап береді. Толық жауапты қажет ететін сұрақтарда оқушыдан жоғары балл жинау үшін тапсырманың шешімін табудың әр қадамын анық көрсетуі талап етіледі. Оқушының тапсырмаларды орындауда тиімді тәсілдерді таңдай білуі және оны қолдана алу қабілеті бағаланады. Тапсырмалардың ішінде бірнеше құрылымдық бөліктерден/сұрақтардан тұратын түрлеріде кездеседі.
I тоқсан бойынша жиынтық бағалау тапсырмаларының сипаттамасы
|
Бөлім |
Тексерілетін мақсат |
Ойлау дағдыларының деңгейі |
Тапсы рма саны* |
№ тапсыр ма* |
Тапсыр ма түрі* |
Орын дау уақыты, мин* |
Балл* |
Бөлім бойынша балл |
|
Атомдағы электрондарды ң қозғалысы |
8.1.3.1 Атомда электрондар ядродан арақашықтығы артқан сайын біртіндеп энергетикалық деңгейлер бойынша таралатынын түсіну |
Білу және түсіну |
1 |
2 |
КТБ |
2 |
1 |
8 |
|
8.1.3.4 Алғашқы 20 химиялық элементтің электрондық конфигурациясын және электронды- графикалық формуларын жаза білу |
Қолдану |
1 |
6 |
ТЖ |
6 |
2 |
||
|
8.1.3.5 Атомдар электрондарды қабылдай немесе жоғалта алатынын және осының нәтижесінде иондар түзілетінін түсіну |
Білу және түсіну |
2 |
1,5 |
КТБ |
5 |
3 |
||
|
8.1.3.6 «Нольдік қосынды» әдісімен қосылыстардың формуласын құрастыру |
Қолдану |
1 |
3 |
ҚЖ |
3 |
2 |
||
|
Заттардың формулалары және химиялық реакция теңдеулері |
8.2.3.1 Заттар құрамындағы элементтердің массалық үлесін табу, элементтердің массалық үлесі бойынша заттардың формуласын шығару |
Қолдану |
2 |
9 |
ТЖ |
6 |
3 |
8 |
|
8.2.3.3 Реакцияға қатысатын және түзілетін заттардың формуласын жаза отырып, химиялық реакциялар теңдеулерін құру; |
Қолдану |
1 |
4 |
КЖ |
2 |
2 |
||
|
8.2.2.1 Бастапқы және түзілген заттардың саны мен құрамы бойынша химиялық реакцияларды жіктеу |
Білу және түсіну |
2 |
7,8 |
ҚЖ |
2 |
3 |
||
|
Металдар белсенділігін салыстыру |
8.2.4.3 Металдар коррозиясын туындатуға әсер ететін жағдайларды зерттеу |
Жоғарғы деңгей дағдылары |
1 |
10 |
ТЖ |
4 |
4 |
9 |
|
8.2.2.5 Металдардың қышқылдармен әрекеттесуінің реакция теңдеулерін құрастыру |
Қолдану |
1 |
11 |
ҚЖ |
5 |
2 |
||
|
8.2.4.8 Металдардың белсенділік қатарын қолданып металдардың таныс емес орынбасу реакцияларының жүру мүмкіндігін болжау |
Жоғарғы деңгей дағдылары |
1 |
12 |
ТЖ |
5 |
3 |
||
|
Барлығы |
|
|
|
|
|
|
25 |
|
«Химия» пəнінен I тоқсанға арналған жиынтық бағалаудың тапсырмалары
1. Натрий атомы үшін дұрыс тұжырымдарды анықтаңыз.
1) Натрийдің сыртқы электрондық қабатында 1 электрон бар
2) Натрий сыртқы қабатындағы 1 электронды беріп жібере алады
3) Натрий сыртқы қабатына 2 электрон қосып алады
4) Na+ ионын түзе алады
5) Na1 ионын түзе алады
A) 3,5
B) 2,4
C) 1,2,4
D) 3,4,5
[1]
2. 1, 2, 3 және 4 - энергетикалық деңгейлердегі электрондардың
максимал санының өсу ретімен орналасқанын белгілеңіз.
A) 2е; 4е; 8е; 18е B) 2е;8е; 32е; 18е C) 2е; 8е; 18е; 32е D) 8е; 18е; 32е; 2е
[1]
3. Төменде берілген қосылыстардың формуласын «нольдік қосынды»
әдісі бойынша құрастырыңыз:
-
Fe3+ және S2-
-
Cl7+ және O2-
[2]
4. Фосфор оттекпен жарық шығара отырып, қарқынды жанып, фосфор(V) оксидін түзеді. Фосфор(V) оксиді суда ерігенде фосфор қышқылы түзіледі. Осы өзгерістерді сипаттайтын реакция теңдеулерін жазып көрсетіңіз.
1) Фосфордың жануы
2) Фосфор(V) оксидінің сумен әрекеттесуі
[2]
5. Кестеде берілген атомдар мен иондарды электрондық формуласымен cәйкестендіріңіз.
-
Атомдар мен иондар
Электрондық формуласы
А. Al3+
1. 1s22s22p63s23p64s2
В. Са
2. 1s22s22p63s23p6
С. Сl1-
3. 1s22s22p63s2
D. Mg
4. 1s22s22p6
A.____ B._____ C._____ D._____
[2]
6. Алюминий – күміс түсті ақ металл, жылуды және электр тогын жақсы өткізеді. Жер қыртысында таралуы бойынша элементтер арасында 4-, металдар арасында 1- орында. Табиғатта оның жүздеген минералдары кездеседі.
https://kk.wikipedia.org/wiki
Алюминийдің периодтық жүйедегі орнын ескере отырып оның электрондық конфигурациясы мен электронды-графикалық формуласын жазып кестені толтырыңыз.
|
Электрондық конфигурациясы |
Электронды-графикалық формуласы |
|
|
|
[2]
7. Кестеде берілген химиялық реакциялардың типтерін анықтаңыз.
|
№ |
Химиялық реакция теңдеулері |
Реакция типі |
|
1 |
MgO + SO2 → MgSO3 |
|
|
2 |
Cu + HgCI2 → Hg + CuCI2 |
|
|
3 |
Cu(OH)2 → CuO + H2O |
|
|
4 |
3NaOH + FeCI3 → Fe(OH)3↓ + 3NaCI |
|
[2]
8. Сөйлемді мұқият оқып, бос орындарды толтырыңыз:
Бір күрделі зат айырылып, нәтижесінде бірнеше жай немесе күрделі заттар түзілетін реакция _________________________ реакциясы деп аталады.
[1]
9. Ас содасы ақ түсті, кристалды ұнтақ. Улы емес, өртенбейді, жарылмайды. Медицинада, химиялық өнеркәсібінде, тамақ өнеркәсібінде т.б. қолданылады.
Ас содасының құрамы 27,38% натрий, 1,19% сутек, 14,29% көміртек, 57,14% оттектен тұратындығы белгілі болса ас содасының формуласын жазыңыз.
[3]
https://kk.wikipedia.org/wiki/
_________________________________________________________________________________
10. Металдар мен құймалар әр түрлі заттармен жанасқанда, олармен әрекеттесіп, химиялық қосылыстар түзеді. Әсіресе жаңбыр, топырақ ылғалы, ауа әсерінен қоршаған ортадағы металдар бүлініп желінеді. Бұл кезде металдан жасалған бұйымның қасиеті мүлдем өзгеріп, ол біртіндеп бүліне бастайды. Бұл өте зиянды әрі қауіпті процесс жемірілу деп аталады (коррозия — лат. korrosio — желіну деген сөз).
(a) Алюминийден жасалған бұйымдармен салыстырғанда, темірден жасалған бұйымдардың жылдам жемірілуге ұшырауының себебін түсіндіріңіз.
______________________________________________________________________________________________________________________________________________
__________________________________________________________________
[2]
(b) Коррозиядан қорғаудың кез-келген екі жолын ұсыныңыз:
![]()
______________________________________________________________________
[2]
 11(a) Суретте металдардың
қышқылдармен
11(a) Суретте металдардың
қышқылдармен
әрекеттесуі көрсетілген:
№1 сынауықта – реакция шабытты жүріп, көп
мөлшерде газ бөлінеді;
№2 сынауықта – реакция белсенді жүріп, газ бөлінеді;
№3 сынауықта – реакция белгілері байқалмайды.
https://www.google.kz/search
Тапсырма:
№1 және №2 сынауықтардағы металдарды
анықтаңыз:
№1 сынауық
№2 сынауық
[2]
(b) Анықталған №1 және №2 сынауықтардағы металдардың қышқылмен әрекеттесу реакция теңдеуін жазып теңестіріңіз.
_________________________________________________________________________________________________________________________________________
12. Арман кобальт металының белсенділігін тексеріп көру үшін оны ішінде әртүрлі ерітінділер бар стаканға салып, тәжірибе жасады.
а) Төменде берілген кестеге «+» немесе «-» белгісін қою арқылы кобальт металының қайсыларымен әрекеттескенін анықтаңыз.
-
-
-
-
AgNO3
HCl
ZnSO4
CaCl2
Со
-
-
-
b) Кобальт металының осындай қасиет көрсетуінің себебін түсіндіріңіз.
![]()
[3]
|
Балл қою кестесі |
||||||||||||||
|
№ |
Жауап |
Балл |
Қосымша ақпарат |
|||||||||||
|
1 |
C |
1 |
|
|||||||||||
|
2 |
C |
1 |
|
|||||||||||
|
3 |
Fe2S3 |
1 |
|
|||||||||||
|
Cl2O7 |
1 |
|||||||||||||
|
4 |
4P + 5O2→ 2P2O5 |
1 |
|
|||||||||||
|
P2O5+3H2O→2 H3 PO4 |
1 |
|||||||||||||
|
5 |
А.4 В.1 |
1 |
Кез келген екі дұрыс жауап үшін 1 балл |
|||||||||||
|
С.2 Д.3 |
1 |
|||||||||||||
|
6 |
1s 22s22p63s23p1 |
1 |
|
|||||||||||
|
|
1 |
|||||||||||||
|
7 |
1 |
Қосылу |
1 |
Кез келген екі дұрыс жауап үшін 1 балл |
||||||||||
|
2 |
Орынбасу |
|||||||||||||
|
3 |
Айырылу |
1 |
||||||||||||
|
4 |
Алмасу |
|||||||||||||
|
8 |
Алмасу |
1 |
Басқа жауап Қабылданбайды. |
|||||||||||
|
9 |
NaxHyCzOn= ω /Ar: ω/Ar: ω /Ar |
1 |
|
|||||||||||
|
ω(Na): ω (H): ω(C) : ω (O) =27,38/23: 1,19/1: 14,29/12: 57,14/16 =1:1:1:4 |
1 |
|
||||||||||||
|
NaHCO3 |
1 |
|
||||||||||||
|
10 |
Алюминий металының бетінде оксидтен тұратын өте жұқа қабықша пайда болып, металды қоршаған ортамен жанасудан сақтап тұрады. |
1 |
|
|||||||||||
|
Темір металында ондай оксидтен тұратын қабықша жоқ. Темірдің таттануы оттектің әсерінен болады. |
1 |
Басқаша тұжырымдалған дұрыс жауаптарда қабылданады. |
||||||||||||
|
Металл бетін жемірілуге қарсы тұрақты қабатпен қаптау. |
1 |
Мысалы: лакпен, бояумен т.с.с жауаптарда қабылданады |
||||||||||||
|
Жемірілуді баяулататын тежегіш(ингибитор) заттарды енгізу. |
1 |
|
||||||||||||
|
11 |
№1 сынауықтағы магний Mg +2HCl = MgCl2+H2 |
1 |
||||||||||||
|
№2 сынауықтағы мырыш Zn +2HCl = ZnCl2+H2 |
1 |
|||||||||||||
|
12 |
|
1
|
Zn, Ca металдары активтік қатарда Со алдында тұр. Сондықтан оларды ығыстыра алмайды деген жауап қабылданады. |
|||||||||||
|
Кобальт металы активтік қатарда өзінен кейінгілерін тұздар ерітіндісінен ығыстырып шығарады. |
1 |
|||||||||||||
|
Активтік қатарда сутекке дейін орналасқан металдар сутекті қышқылдардан ығыстыра алады. |
1 |
|||||||||||||
|
|
Барлығы |
25 |
|
|||||||||||
2-ТОҚСАННЫҢ ЖИЫНТЫҚ БАҒАЛАУ СПЕЦИФИКАЦИЯСЫ
2-тоқсанның жиынтық бағалауына шолу
Жиынтық бағалаудың өткізілу уақыты – 40 минут
Балл саны - 25
Тапсырмалар түрлері:
КТБ – Көп таңдауы бар тапсырмалар;
ҚЖ – Қысқа жауапты қажет ететін тапсырмалар;
ТЖ – Толық жауапты қажет ететін тапсырмалар.
Жиынтық бағалаудың құрылымы
Ұсынылған нұсқада көп жауапты таңдауы бар сұрақтар, қысқа және толық жауапты қажет ететін құрылымдастырылған сұрақтардан тұратын тапсырмалар қолданылады. Нұсқада 11 тапсырма бар.
Көп таңдауы бар тапсырмаларға оқушылар бір немесе бірнеше дұрыс жауабын таңдау және сәйкестендіру арқылы жауап береді.
Қысқа жауапты қажет ететін сұрақтарға оқушылар қажетті сөздерді бос орындарға толтыру және сұрақтарға қысқа жауап беру арқылы жауап береді.
Толық жауапты қажет ететін сұрақтар оқушылардың формулаларды қолданып, химиялық есептерді шығару дағдысын, заттардың химиялық қасиеттеріне сәйкес химиялық реакция теңдеулерін жазу дағдысын, химиялық реакциялардың жүру процестерін түсіндіру және салдарларын көрсететін логикалық ойлау дағдысын, стехиометриялық есептер шығару дағдысын, химиялық реакция теңдеуін құру дағдысын көрсетеді.
2-тоқсан бойынша тапсырмаларының сипаттамасы
|
Бөлім |
Тексерілетін мақсат |
Ойлау дағдылары-ның деңгейі |
Тапсырма саны * |
№ тапсырма * |
Тапсыр-ма түрі * |
Орындау уақыты * |
Балл * |
Бөлім бойынша балл |
|
Зат мөлшері |
8.1.1.3 Масса, зат мөлшері және құрылымдық бөлшектер санын анықтау |
Қолдану |
2 |
1, 2 |
КТБ |
4 |
3 |
3 |
|
Сехио-метрия-лық есептеу-лер |
8.2.3.5 Химиялық реакция теңдеулері бойынша заттың массасын, зат мөлшерін есептеу |
Қолдану |
1 |
6 |
ТЖ |
4 |
2 |
6 |
|
8.2.3.6 Авогадро заңын білу және қалыпты және стандартты жағдайдардағы газдар көлемін есептеуде молярлық көлемді қолдану |
Қолдану |
2 |
3, 4 |
КТБ |
6 |
4 |
||
|
Химия-лық реакциядағы энергиямен танысу |
8.3.1.1 Заттың жану реакциясының өнімі көбінесе оксид екенін және құрамында көміртегі бар отын оттекте жанғанда, көмірқышқыл газы, иіс газы немесе көміртек түсілетінін түсіну |
Білу және түсіну |
1 |
5 |
ҚЖ |
3 |
2 |
6 |
|
8.3.1.3 Экзотермиялық реакциялар жылу бөле жүретінін, ал эндотермиялық реакциялар жылу сіңіре жүретінін білу |
Білу және түсіну |
1 |
7 |
ҚЖ |
2 |
2 |
||
|
8.3.1.5 Энергия өзгерісін бөлшектердің кинетикалық теориясы тұрғысынан түсіндіру |
Жоғары деңгей дағдылары |
1 |
11 |
ТЖ |
6 |
2 |
||
|
Сутек. Оттек және озон |
8.4.2.1 Сутекті алу және оның қасиеттері мен қолданылуын зерттеу |
Қолдану |
1 |
8 |
ТЖ |
5 |
4 |
10 |
|
8.4.2.3 Оттекті алу және оның қасиеттері мен қолданылуын зерттеу |
Қолдану |
1 |
9 |
ҚЖ/ТЖ |
5 |
4 |
||
|
8.4.2.5 Жер бетіндегі озон қабатының маңызын түсіндіру |
Білу және түсіну |
1 |
10 |
ТЖ |
5 |
2 |
||
|
|
Барлығы |
|
11 |
|
|
40 |
25 |
25 |
«Химия» пәнінен 2-тоқсанға арналған
жиынтық бағалаудың тапсырмалары
1. Молекула саны 128 г көмірқышқыл газында қанша атом оттек бар екенін анықтаңыз.
A) 6,023*1023
B) 17,52*1023
C) 24,10*1023
D) 27,53*1023
E) 48,18*1023 [1]
2. 0,5 моль алюминий сульфидінің (Al2S3) массасы мен молекула санын анықтаңыз.
A) 29,5 г
B) 43 г
C) 61,5 г
D) 75 г
E) 3,01*1023
F) 6,02*1023
G) 12,04*1023 [2]
3. Төменде берілген газдарға арналған Авогадро заңы туралы тұжырымдардың шындық не жалған екенін (˅) белгісімен анықтаңыз.
|
Тұжырым |
Шындық |
Жалған |
|
Мольдік көлемнің мәні тұрақсыз шама. |
|
|
|
Мольдік көлем арқылы газдардың көлемін есептеуге болады. |
|
|
|
Қалыпты жағдайда кез келген заттың көлемдері бірдей болады. |
|
|
|
Кез келген жағдайда көлемдері бірдей газдардың массалары тең болады. |
|
|
|
Қалыпты жағдайда 1 моль оттектің көлемі 1 моль көмірқышқыл газының көлеміне тең. |
|
|
[1]
4. Төменде берілген заттардың мәндері мен көлемдері арасындағы сәйкестікті анықтаңыз.
|
Заттардың мәні |
Көлем |
|
1) 0,5 моль азот |
A) 11,2 л |
|
2) 32 г метан (СН4) |
B) 33,6 л |
|
3) 1,5 моль аммиак (NH3) |
C) 44,8 л |
1)________ 2) _____________ 3) __________ [3]
5. Күнделікті тұрмыста әртүрлі заттардың жануын байқайсыңдар. Төменде берілген жану реакциялары тұжырымдарының бос орындарын қажетті сөздермен толықтырыңыз.
Жану ________ реакция болып табылады, себебі реакция нәтижесінде жылу мен жарық бөлінеді. Жану реакциясының негізгі белгісі – реагент ретінде жануды қолдайтын ____________ болуы және реакция нәтижесінде _____________ _______, су және жылудың бөлінуі. Жану реакциясының өнімі ___________ деп аталады. Отын толық жанғанда ___________ _____ бөлінеді, шала жану кезінде ___ _____ және ______ бөлінеді, олар улы газдар.
Қажетті сөздер: көмірқышқыл газы, оттегі, иіс газы, оксид, күйе, химиялық, көмірқышқыл газы
[2]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / М.Қ.Оспанова, Қ.С.Аухадиева, Т.Г.Белоуосова. – Алматы: Мектеп, 2018
6. Сутегі – ХХІ ғасырдың отыны. Оны суды айыру арқылы зертханада алуға болады. 4 г сутегін алу үшін қажет судың массасы мен зат мөлшерін анықтаңыз.
[2]
7. Берілген эндотермиялық және экзотермиялық реакцияға байланысты тұжырымдардың бос орындарын қажетті сөздермен толықтырыңыз.
Найзағай кезінде озонның түзілуінде энергия __________. Табиғи газ жанғанда энергия ________. Жылу бөле жүретін реакцияларда кинетикалық энергия ________. _____________ рeaкцияда температура төмендейді. Экзотермиялық реакцияда зат бөлшектері ______ жылдамдықпен қозғалады.
Қажетті сөздер: эндотермиялық, жоғарылайды, жоғары, бөлінеді, сіңіріледі
[2]
Химия. Жалпы білім беретін мектептің 8-сыныбына арналған оқулық / М.Қ.Оспанова, Қ.С.Аухадиева, Т.Г.Белоуосова. – Алматы: Мектеп, 2018
8. Сутегі – ең кең тараған элемент, тіпті Күн массасының 75%-н құрайды.
a) Сутектің қолданылу салаларына екі мысал келтіріңіз:
1)____________________________________________________________
2)____________________________________________________________
[1]
b) Төменде берілген айналымдарды іске асыруға мүмкін реакция теңдеулерін жазыңыз.
1 2
С → H2 → NH3
↓ 3
NaH
1)_________________________________________________________________2)_________________________________________________________________3)________________________________________________________________
[3]
9. Оттегі адамдардың есте сақтау, назар аудару және физикалық қасиеттерін арттырады. Организмге түскен оттектің 20%-ы мидың жұмысына жұмсалады. Оттегінің химиялық белсенділігі де жоғары.
а) Оттектің берілген заттармен әрекеттесуінің реакция теңдеулерін жазыңыз:
1) Al
2) Са
_________________________________________________________________________________________________________________________________
[2]
b) Оттектің қолданылатын салаларын анықтаңыз.
A) метил спиртін алуда
B) тұз қышқылын алуда
C) су астында тыныс алуға
D) мұнай өнімдерін өңдеуде
E) қатты майларды алуда
[1]
с) Оттекті күрделі заттарды қыздырып, айыру арқылы алады. Өршіткі марганец (ІV) оксидінің қатысында сутек пероксиді (Н2О2) шабытты реакцияға түсіп, оттек газын түзеді. Реакция теңдеуін жазыңыз.
[1]
10. Адам тіршілігінің нәтижесінде озон қабаты жұқарады. Озон қабатының жұқаруына суретте көрсетілген факторлар әсер етеді.

https://www.syl.ru/article/188050/new_chto-takoe-ozonovyiy-sloy-zemli-problemyi-ozonovogo-sloya
а) Осы факторлардың біреуінің озон қабатына қалай әсер ететінін жазыңыз.
_______________________________________________________________
[1]
b) Озон қабатының жұқаруының бір салдарын көрсетіңіз.
_____________________________________________________________
[1]
11. CaCO3 → CaO + CO2 реакциясында энергия өзгереді.
а) Жылудың бөлінуі немесе сіңірілуіне байланысты реакцияның типін анықтаңыз.
______________________________________________________________[1]
b) Энергия өзгерісін бөлшектердің кинетикалық теориясы тұрғысынан түсіндіріңіз.
_______________________________________________________________
_______________________________________________________________
________________________________________________________________
[1]
Балл қою кестесі
|
№ |
Жауап |
Балл |
Қосымша ақпарат |
|
1 |
B |
1 |
|
|
2 |
D |
1 |
|
|
E |
1 |
|
|
|
3 |
Мольдік көлем арқылы газдардың көлемін есептеуге болады. Қалыпты жағдайда 1 моль оттектің көлемі 1 моль көмірқышқыл газының көлеміне тең. |
1 |
2 дұрыс жауап үшін 1 балл |
|
4 |
1) A |
1 |
|
|
2) C |
1 |
|
|
|
3) B |
1 |
|
|
|
5 |
Химиялық, оттегі, көмірқышқыл газы |
1 |
Екі сөйлемдегі барлық дұрыс жауап үшін 1 балл беріледі. |
|
Оксид, көмірқышқыл газы, иіс газы, күйе |
1 |
Екі сөйлемдегі барлық дұрыс жауап үшін 1 балл беріледі. |
|
|
6 |
2 моль, 36 г |
2 |
Әр дұрыс жауап үшін 1 балл |
|
7 |
Сіңіріледі, бөлінеді, жоғарылайды |
1 |
Үш сөйлемдегі барлық дұрыс жауап үшін 1 балл беріледі. |
|
Эндотермиялық, жоғары |
1 |
Екі сөйлемдегі барлық дұрыс жауап үшін 1 балл беріледі. |
|
|
8 |
а) Отын ретінде, металдарды дәнекерлеу |
1 |
Кез келген екі дұрыс саланы атап жазса 1 балл беріледі. |
|
b) 1. C + H2O → CO + H2↑ |
1 |
|
|
|
2. N2 + 3H2 → 2NH3 |
1 |
|
|
|
3. 2Na + H2 → 2NaH |
1 |
|
|
|
9 |
a) 4Al + 3O2 → 2Al2O3 |
1 |
|
|
2Са + О2 → 2СаО |
1 |
|
|
|
b) C |
1 |
|
|
|
c) 2H2O2 → 2H2O + O2 |
1 |
|
|
|
10 |
a) Хлор қосылыстары күн радиациясы әсерінен хлор атомдарына ыдырап, озонның молекулаларымен реакцияға түседі. |
1 |
Хлор атомы озон молекулаларымен әрекеттесіп, озон молекуласын бұзады. |
|
b) Климаттың өзгеруі |
1 |
Кез келген дұрыс салдарды жазса 1 балл беріледі. |
|
|
11 |
а) Эндотермиялық реакция |
1 |
|
|
b) Молекулалар баяу/жай қозғалғандықтан, кинетикалық энергия кемиді. Бөлшектер арасында қашықтық/кеңістік кішірейеді/азаяды. |
1 |
Бөлшектер арасындағы байланыс күшейеді деген жауап қабылданады. |
|
|
|
Барлығы |
25 |
|
3-ТОҚСАННЫҢ ЖИЫНТЫҚ БАҒАЛАУ СПЕЦИФИКАЦИЯСЫ
3-тоқсанның жиынтық бағалауына шолу
Жиынтық бағалаудың өткізілу уақыты – 40 минут
Балл саны – 25
Тапсырма түрлері:
КТБ – Көп таңдауы бар тапсырмалар;
ҚЖ – Қысқа жауапты қажет ететін тапсырмалар;
ТЖ – Толық жауапты қажет ететін тапсырмалар.
Жиынтық бағалаудың құрылымы
Берілген нұсқада әртүрлі тапсырмалар: көп жауапты таңдауы бар сұрақтар, қысқа және толық жауапты қажет ететін сұрақтар қолданылады.
Көп таңдауы бар тапсырмаларда оқушылар бір және бірнеше дұрыс жауапты таңдайды. Қысқа жауапты қажет ететін сұрақтарға сөздер немесе қысқа сөйлемдер түрінде жауап береді. Толық жауапты қажет ететін сұрақтарда білім алушылар логикалық ойлау және шығармашылық дағдыларын көрсетеді. Толық жауапты қажет ететін тапсырмаларды орындау барысында оқушылар өздерінің түсініктерін, ойлау деңгейін көрсетеді.
Нұсқада 15 тапсырма берілген.
3-тоқсан бойынша жиынтық бағалау тапсырмаларының сипаттамасы
|
Бөлім |
Тексерілетін мақсат |
Ойлау |
Тап-сыр-ма |
№ сырма |
Тап-сыр |
Орындау |
Балл* |
Бөлім ша балл |
|
Химиялық |
8.2.1.1 Топ, период, атом нөмірінің физикалық мәнін түсіндіру |
Қолдану |
1 |
3 |
ЖТ |
2 |
3 |
9 |
|
8.2.1.2 Бір топтағы элементтердің сыртқы электрондық деңгейінде электрондар санының бірдей болатындығын түсіну; |
Білу және түсіну |
1 |
2 |
ТЖ |
3 |
2 |
||
|
8.2.1.3 Топтар мен
периодтарда |
Қолдану |
2 |
1, 4 |
ТЖ |
4 |
2 |
||
|
8.2.1.4 Химиялық элементтің периодтық кестеде орналасуына сай қасиеттерін болжау |
Жоғары деңгей дағдылары |
1 |
5 |
КТБ |
3 |
2 |
||
|
Химиялық |
8.1.4.1 Электртерістілік ұғымы негізінде атомдар арасындағы ковалентті байланыстың түзілуін түсіндіру |
Қолдану |
1 |
6 |
ТЖ |
5 |
2 |
5 |
|
8.1.4.2 Иондық байланыстың түзілу механизмін сипаттау және иондық қосылыстардың қасиеттерін болжау |
Қолдану |
2 |
7, 8 |
ТЖ |
4 |
3 |
||
|
Ерітінді-лер |
8.3.4.1 Заттарды судағы ерігіштігі бойынша жіктеу; |
Білу және түсіну |
3 |
10, 11 |
КТБ |
5 |
4 |
11 |
|
8.3.4.3 Заттың
ерігіштігіне |
Қолдану |
1 |
9 |
ЖТ |
3 |
2 |
||
|
8.3.4.5 Еріген заттың массалық үлесі мен ерітіндінің белгілі массасы бойынша еріген заттың массасын есептеу |
Қолдану |
2 |
12, 13 |
ТЖ |
6 |
3 |
||
|
8.3.4.6 Ерітіндідегі заттың молярлық концентрациясын есептеу |
Қолдану |
2 |
14, 15 |
|
4 |
2 |
||
|
Барлығы |
|
|
15 |
|
|
40 |
25 |
25 |
«Химия» пәнінен 3-тоқсанға арналған жиынтық бағалаудың тапсырмалары
1. Атом радиусының өсу реті бойынша орналасқан элементтер қатарын табыңыз.
А) Si P S
В) Be B C
С) Si Ge C
D) Ве Mg Ca
E) C N Li
[1]
2. а) Сыртқы электрондық деңгейінде электрондар саны бірдей элементтерді табыңыз: Be, Al, C, Mg, N, Ne, Cl, Ca
________________________________________________________________________
[1]
b) Элементтерді бір топқа біріктіруге негіз болатын қасиеттерді атаңдар.
________________________________________________________________________________________________________________________________________________
[1]
3. Топ, период, атом нөмірінің оның физикалық мағынасымен сәйкестендіріңіз.
-
Физикалық мағынасы
1
Топ нөмірі
А)
Атомның ядро зарядын
В)
Ядродағы протон санын
2
Период нөмірі
С)
Атомдағы электрон санын
D)
Энергетикалық деңгей санын
3
Атом нөмірі
Е)
Сыртқы деңгейдегі электрон санын
[3]
Химия қысқа мерзімді жоспарлар жиынтығы. 8 сынып. Д.Х.Аширова, Н.Б.Бақтыбаева.
4. Ве Мg Са К Аl Fe
а) Берілген металдарды металдық қасиеті артуы бойынша орналастырыңыз.
[1]
b) Металдық қасиетінің арту себебін түсіндіріңіз.
________________________________________________________________________
[1]
5. Көміртекке қатысты келесі тұжырымдардың дұрысын анықтаңыз.
А) екі энергетикалық деңгейі бар
В) қышқылдық та, негіздік те оксид түзеді
С) ұшқыш сутекті қосылысы СН4
D) ІІІ период, ІV топ, негізгі топшада орналасқан
Е) ІІ және ІІІ валенттілік көрсетеді
F) белсенді бейметалл
G) тотығу дәрежесі +4; -4; +2
H) жоғарғы оксиді СО2 , негіздік оксид
[1]
6. а) Сутек пен бром атомдарының арасында химиялық байланысты анықтаңыз.
___________________________________________________________________
[1]
b) Нүктелер және крестер диаграммасы арқылы сутек пен бром атомдарының арасында түзілуі мүмкін байланыстың схемасын құрыңыз.

[1]
7. Қаныққан ерітінді концентрлі ерітінді бола ала ма? Жауабыңызды түсіндіріңіз.
[1]
8. а) Литий және фтор атомдарының электрондарының энергетикалық деңгейлерге таралуын көрсетіңіз.
L![]()
![]() i ) )
F
) )
i ) )
F
) )
[1]
b) Литий және фтор атомдарының арасында иондық байланыстың түзілу сызбасын көрсетіңіз.

[1]
Химия қысқа мерзімді жоспарлар жиынтығы. 8 сынып. Д.Х.Аширова, Н.Б.Бақтыбаева.
9. Заттардың ерігіштігіне температураның әсерін түсіндіріңіз.
|
№ |
Тұжырымдар |
Себебі |
|
1 |
Қатты заттардың ерігіштігі температура жоғарылағанда артады. |
|
|
2 |
Газдардың ерігіштігі температура жоғарылағанда кемиді. |
|
[2]
10. Жақсы еритін затты анықтаңыз.
A) темір
B) калий гидроксиді
C) парафин
D) көміртек
Е) мұнай
[1]
11. Суда калий перманганатын (марганцовка) еріткенде байқалатын құбылыстарды түсіндіріңіз.
|
№ |
Құбылыстар |
Түсініктеме |
|
1 |
|
|
|
2 |
|
|
|
3 |
|
|
[3]
Химия. Жұмыс дәптері. 8 сынып. Н.Нұрахметов
12. Суреттегі екі затты араластыру арқылы алынған ерітіндінің пайыздық концентрациясы қанша?

 bilimland.kz
bilimland.kz
Ас тұзы 30 г су 75 г
А) 38 %
В) 35 %
С) 30 %
D) 29 %
Е)28 %
[1]
13. Мұғалім оқушыға 200 г 30 % -дық ерітінді дайындауды тапсырды. Ерітіндіні дайындау үшін оқушы қанша тұз және қанша су алуы керек.
А) 30 г тұз, 140 г су
В) 10 г тұз, 150 г су
С) 60 г тұз ,140 г су
D) 50 г тұз, 150 г су
Е) 20 г тұз , 180 г су
[2]
14. Молярлық концентрация дегеніміз не?
________________________________________________________________________
[1]
15 . 500 мл ерітіндіде 5 г NаОН бар ерітіндінің молярлық концентрациясын есептеңіз.
А) 1,01 моль/л
В) 1,05 моль/л
С) 0,50 моль/л
D) 0,35 моль/л
Е) 0,25 моль/л
[1]
http://xn--i1abbnckbmcl9fb.xn
Балл қою кестесі
|
№ |
Жауап |
Балл |
Қосымша ақпарат |
||||||||||||
|
1 |
D |
1 |
|
||||||||||||
|
2 |
a) Li, Na, K |
1 |
|
||||||||||||
|
b) Жоғарғы тотығу дәрежесі +1, валенттілігі І, белсенді сілтілік металдар, жоғарғы оксиді R2O |
1 |
|
|||||||||||||
|
3 |
1 - Е |
1 |
|
||||||||||||
|
2 - В |
1 |
|
|||||||||||||
|
3 – A, C, D |
1 |
|
|||||||||||||
|
4 |
a) Al, Fe, Mg, Ca, Na, K |
1 |
|
||||||||||||
|
|
b) Себебі, солдан оңға қарай сыртқы қабатындағы электрондар саны кемиді |
1 |
|
||||||||||||
|
5 |
A, C, G |
1 |
|
||||||||||||
|
6 |
а) Ковалентті полюсті |
1 |
|
||||||||||||
|
•• •• b) H• + •Br: → H(:)Br: •• ••
|
1 |
|
|||||||||||||
|
7 |
Қаныққан ерітінді концентрлі бола алмайды, себебі қаныққан ерітіндіде ары қарай зат ерімейді, ал концентрлі ерітіндіде ериді. |
1 |
Балама ұсыныстар қабылданады. |
||||||||||||
|
8 |
a) Li 2e1e F 2e 7e |
1 |
|
||||||||||||
|
b) •• + •• - b) Li• + •F: → Li [:F:] •• •• |
1 |
|
|||||||||||||
|
9 |
1. Қатты заттардың ерігіштігі температураны көтергенде артады, себебі температураның әсерінен диффузия тез жүреді. 2. Газдардың ерігіштігі температураны жоғарылатқанда кемиді, себебі газ бөлшектері арасындағы қашықтық үлкейеді. |
2 |
Балама ұсыныстар қабылданады. |
||||||||||||
|
10 |
В |
1 |
|
||||||||||||
|
11 |
|
3 |
Балама ұсыныстар қабылданады. |
||||||||||||
|
12 |
Е |
1 |
|
||||||||||||
|
13 |
С |
2 |
|
||||||||||||
|
14 |
Молярлы концентрация дегеніміз – 1 л көлемде еріген заттың мөлшері |
1 |
|
||||||||||||
|
15 |
Е |
1 |
|
||||||||||||
|
Барлығы |
25 |
|
|||||||||||||
4-ТОҚСАН БОЙЫНША ЖИЫНТЫҚ БАҒАЛАУ СПЕЦИФИКАЦИЯСЫ
4-тоқсанның жиынтық бағалауына шолу
Ұзақтығы - 40 минут
Балл саны - 25
Тапсырма түрі:
КТБ – көп тaңдауы бaр тапсырмалар;
ҚЖ – қысқа жауапты қажет ететін тапсырмалар;
ТЖ – толық жауапты қажет ететін тапсырмалар.
Жиынтық бағалаудың құрылымы
Берілген нұсқада әртүрлі тапсырмалар: көп таңдауы бар тапсырмалар, қысқа және толық жауапты қажет ететін тапсырмалар қамтылды.
Көп тaңдaуы бaр тaпсырмaлaрдa оқушылaр берілген жaуaп нұсқaлaрынaн дұрыс жaуaпты көрсетеді.
Қысқa жaуaпты қaжет ететін тaпсырмaлaрғa оқушылaр дәл жауапты, қысқa сөйлемдер түрінде жaуaп береді. Толық жaуaпты қaжет ететін тaпсырмaлaрдa оқушылар жоғары бaлл жинaу үшін тaпсырмaның әр қадамын орындау талап етіледі. Оқушы өз пікірін анық көрсетіп жазады және дәлелдейді. Тапсырмаларды орындау барысында оқушыларда жоғары деңгей дағдылары және өз бетінше іздену дағдылары қалыптасады. Тоқсандық жиынтық 11 тапсырмадан тұрады: бір дұрыс және бірнеше дұрыс жауапты таңдауға арналған, қысқа жауапты қажет ететін тапсырмалар. Сонымен қатар, толық жауапты қажет ететін тапсырмалар оқушылардың ойланып өз пікірлерін дәлелдерін толық жазуға арналған тапсырмалар.
4-тоқсaн бойыншa жиынтық бaғaлaу тaпсырмaлaрының сипaттaмaсы
|
Бөлім |
Тексерілетін мақсат |
Ойлау дағдыларының деңгейі |
Тап сыр ма саны* |
тапсыр ма* № |
Тапсырма түрі |
Орындау уақыты, мин* |
Балл* |
Бөлім бойынша балл |
|
Бейорганикалық қосылыстардың негізгі кластары. Генетикалық байланыс |
8.3.4.7 Оксидтердің жіктелуін және қасиеттерін білу, олардың химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрастыру |
Қолдану |
1 |
5 |
ТЖ |
5 |
2 |
10 |
|
8.3.4.8 Қышқылдардың жіктелуін, қасиеттерін білу және түсіну, олардың химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрастыру |
Қолдану |
1 |
6 |
ҚЖ |
3 |
3 |
||
|
8.3.4.9 Негіздердің жіктелуі мен қасиеттерін білу және түсіну, олардың химиялық қасиеттерін сипаттайтын реакция теңдеулерін құрастыру |
Қолдану |
1 |
7 |
КТБ |
2 |
1 |
||
|
8.3.4.12 Бейорганикалық қосылыстардың негізгі кластары арасындағы генетикалық байланысты зерттеу |
Жоғары деңгей |
1 |
8 |
ТЖ |
6 |
4 |
||
|
Көміртек және оның қосылыстары |
8.4.3.1 Көміртек неліктен көптеген қосылыстарында төрт байланыс түзетінін түсіндіру; |
Қолдану |
1 |
9 |
ТЖ |
5 |
2 |
8 |
|
8.4.3.3 Көміртектің аллотропиялық түр өзгерістерінің құрылысын және қасиеттерін салыстыру; |
Білу және түсіну |
1 |
1 |
КТБ |
2 |
1 |
||
|
8.4.3.6 Көміртек жанған кезде көміртек диоксиді мен көміртек монооксидінің түзілу жағдайларын сипаттау және тірі ағзаларға иіс газының физиологиялық әсерін түсіндіру; |
Қолдану |
2 |
3,4 |
ТЖ |
8 |
3 |
||
|
8.4.3.7 Көмірқышқыл газын алу, оны анықтау және қасиеттерін зерттеу; |
Қолдану |
1 |
2 |
КТБ
|
2 |
2 |
||
|
Су |
8.4.2.8 Судың ластануының қауіптілігі мен себебін анықтау, суды тазарту әдістерін түсіндіру; |
Қолдану |
1 |
10 |
ҚЖ |
3 |
4 |
7 |
|
8.4.2.9 Судың «кермектігін» анықтау және оны жою тәсілдерін түсіндіру; |
Қолдану |
1 |
11 |
КТБ
|
4 |
3 |
||
|
Барлығы |
|
|
11 |
|
|
40 |
|
25 |
Химия пәнінен 4-тоқсанға арналған
жиынтық бағалаудың тапсырмалары
1. Зертханада көмір қышқыл газын алуға мүмкін болатын реакциясын таңдаңыз:
А) NaOH+HCl →
В) Ca(OH)2 +CO2 →
С) NaOH+HCl → D) Na 2СО3+HCl →
[1]
2. Ерімейтін негізді анықтаңыз:
А) NaOH
B) Ba(OH)2
C) Fe(OH)2
D) Ca(OH)2
Е) Cu(OH)2
F) LiOH
[2]
3.Берілген қышқылдардың ішінен оттекті қышқылдaрды бөліп жазыңыз: HNO3, HI, HBr, H3PO4, HCl, H2CO3
[1]
4. Көміртектің аллотропиялық түр өзгерісі мен олардың қасиеттері, құрылысы және қолдану аймағы арасындағы сәйкестікті анықтаңыз:
|
Көміртектің аллотропиялық түр өзгерісі |
Қасиеттері мен құрылысы |
Қолдану аймағы |
|
І.Графит |
1.Сызықтық құрылымды зат |
А.Жасанды қан тамырларын жасауда |
|
2.Қара түсті ұнтақ зат, жартылай өткізгіш |
||
|
ІІ. Карбин |
3. Сұр түсті, жұмсақ, ұстағанда май тәрізді зат |
B.Электродтар дайындауда |
|
4. Атомдық кристалдық торы бар |
І._________________ II.___________________
[2]
5 а) Көміртегі атомының қалыпты және қозған күйінің электрондық- графикалық формулаларын толықтырыз:


қалыпты күйі қозған күйі
[1]
b) Қалыпты және қозған күйлерінің ерекшеліктеріне сүйеніп көміртек атомының төрт байланыс түзу себебін түсіндіріңіз:
________________________________________________________________________________________________________________________________________
[1]
6 а) Сөйлемдерді толықтырыңыз:
Көміртек жанғанда оттектің мөлшері артық болса_________________________түзіледі. Көміртек оттек жеткіліксіз ортада жанғанда _______________________________ түзіледі.
[1]
b) Көміртек монооксиді иіс газы деп аталады. Ол иіссіз, түссіз және суда нашар еритін газ. Иіс газының адам ағзасына тигізетін әсерін 1 мысал келтіріп сипаттаңыз.
________________________________________________________________________________________________________________________________________
[2]
7. Сөзбен берілген реакция теңдеуін таңбалар мен формулалар арқылы жазып теңестіріңіз:
а) магний гидроксиді + тұз қышқылы → магний хлориді + су
____________________________________________________________________
[1]
8. a) Берілген оксидтердің ішінен қайсысы артық екендігін анықтаңыз.
|
Оксидтер |
«Артық» оксид |
Себебі |
|
Na2O CO2 MgO |
|
|
|
BeO SiO2 SO3 |
|
|
|
CO2 SO2 K2O |
|
|
[2]
b) Оксидтердің қасиеттерін сипаттаңдар. Жауаптарды тор көзге (+) және (-) белгісін қойыңыз.
-
Негіздік
Қышқылдық
Екі дайлы
-
Сумен әрекеттесуі
-
Қышқылдармен әрекеттесуі
-
Сілтілермен әрекеттесуі
-
[2]
9. Қышқыл мен негіз арасындағы бейтараптану реакциясына екі мысал жазып теңестіріңіз:
__________________________________________________________________________________________________________________________________
[2]
10. Су сапалы, тұщы, əртүрлі зиянды қоспалардан таза болуы шарт. Суды тазарту – адам денсаулығын сақтаудың бір жолы.
a) судың ластануының 1 себебін жазыңыз:
[1]




![]()
![]() b) Әрбір қадам үшін суды
тазартудың тиімді әдісін анықтаңыз.
b) Әрбір қадам үшін суды
тазартудың тиімді әдісін анықтаңыз.
![]()
А. лайланған су В. Тұнбасы бар су С. Тұнбасыз су D. Таза су
__________________ ________________ ___________________
[3]
11. а) Судың кермектілігі туралы тұжырымдардағы бос орындарды толтырыңыз:
Судың кермектілігінің үш түрі бар, олар _________________, ______________, _______ ________. Егер табиғи суда Ca2+ және HCO32- иондары бар болса, онда бұл _____________ кермектілік. Егер табиғи суда кальцийдің немесе магнийдің хлориді және нитраты бар болса, онда бұл____________________ кермектілік. Судың уақытша кермектілігін жою үшін _________________.
[2]
b) Өндірісте судың кермектілігін жою үшін оның түріне қарамастан, соданы қолдану тиімді. Сода қосу арқылы кермектілікті жою реакциясынының 1 теңдеуін жазыңыз:
____________________________________________________________________
[1]
Балл қою кестесі
|
№ |
Жауап |
Балл |
Қосымша ақпарат
|
|||||||||||||||||||||||||||||||||
|
1 |
D |
1 |
|
|||||||||||||||||||||||||||||||||
|
2 |
C, E |
2 |
|
|||||||||||||||||||||||||||||||||
|
3 |
HNO3 H3PO4, H2 CO3 |
1 |
Басқа жауап қабылданбайды |
|||||||||||||||||||||||||||||||||
|
4 |
І.Графит -3,4 ІІ. Карбин-1,2 |
2 |
үш жауап дұрыс болған жағдайда да бір балл беруге болады |
|||||||||||||||||||||||||||||||||
|
5 |
а) қалыпты күйі қозған күйі
b) Көміртек атомының қозған күйінде сыртқы энергетикалық деңгейінде 4 жұптаспаған электрон болғандықтан төрт химиялық байланыс түзеді
|
1
1 |
Басқа жауап қабылданбайды |
|||||||||||||||||||||||||||||||||
|
6 |
а) көміртек (IV) оксиді / СО2 Көміртек моноксиді/ СО b) Қан гемоглобинімен қосылып организімнің оттекпен қамтамасыз етілуін жояды |
1
2 |
Басқа жауап қабылданбайды Адам уланады жауабы қабылданады |
|||||||||||||||||||||||||||||||||
|
7 |
Mg(OH)2 + 2HCl= MgCl2+2H2O |
1 |
Басқа жауап қабылданбайды |
|||||||||||||||||||||||||||||||||
|
8 |
b)
|
2
2 |
Басқа жауап қабылданбайды |
|||||||||||||||||||||||||||||||||
|
9 |
HCl+NaOH=NaCl+H2O H2SO4+KOH=K2SO4+ H2O |
2 |
Нәтижесінде түз және су алынатын қышқылмен негіздің арасында жүретін кез-келген реакция |
|||||||||||||||||||||||||||||||||
|
10 |
а) жаза тайым оқиғалардан, тасталған қалдықтар, мұнай өнімдері төгілгенде минералды тыңайтқыштарды өте көп мөлшерде пайдалану микроорганизмдердің басым көпшілігін жою мақсатында улы химикаттарды қолдану b) тұндыру, сүзу, дистельдеу
|
1
3 |
Басқада ұсынған жауаптары дұрыс болса қабылданады
Басқа жауап қабылданбайды |
|||||||||||||||||||||||||||||||||
|
11 |
а) Уақытша/ карбонатты, тұрақты/ карбонатсыз, аралас
b |
2
1 |
|
|||||||||||||||||||||||||||||||||
1

шағым қалдыра аласыз







 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
