
Қостанай облысы әкімдігі білім басқармасының
«Бейімбет Майлин ауданы білім бөлімінің
Сапар Ерғалиев атындағы жалпы білім беретін мектебі» КММ
«Химия пәнінен олимпиадаға дайындық жолдары» шебер-сыныбының
ӘЗІРЛЕМЕСІ
Дайындыған: химия пәнінің мұғалімі Ильясова С.А. педагог-сарапшы
Әйет ауылы,
2023-2024 оқу жылы
Мақсаты: Педагогтардың химиядан олимпиада есептерін шығару қабілеттерін жетілдіре отырып, сандық және сапалық есептерді шығару арқылы топта әрекет ету қабілеттерін дамыту, педагогтермен өзара тәжірибе алмасу. Көрнекіліктері : интерактивті тақта, презентация, үлестірмелі материалдар
Өткізілу түрі: шебер-сынып
Барысы:
Ұйымдастыру: Қайырлы күн, Әріптестер! Бүгінгі шебер сыныпқа қош келдіңіздер!
«Жағымды психологиялық ахуал» педагогтарды ортаға шақырамын.
Әріптестер, барлығымыз ортаға шығып «Молекула» ойынын ойнайық, молекула-3, молекула-5, молекула-6 деп 2-топқа бөлінеміз.
Тапсырма: «Миға шабуыл» Сіздермен Қазақстан Республикасының Білім және ғылым министрінің 07.12.2011 жылғы №514 бұйрығына сәйкес Химиялық олимпиадалар тізімін кластер түрінде жазып көрсек, алдарыңызға берілген А4 параққа жазып толтырамыз.
Бағалау: «Керемет!», «Жарайсыздар!» қошемет сөздермен шабыт беремін.
Шебер сынып химия пәнінен олимпиада есептерін шығару жолдарын үйрету болғандықтан, алдымен химия пәнінен есептердің түрлері мен олимпиадаға дайындау жолдарымен таныссақ.
Есеп шығару– оқушылардың химиялық ой-өрісін дамытудың негізгі құралдарының бірі, теориялық білім мен тәжірибе арасындағы байланысты жүзеге асырудың ажырамас жолы. Сабақ барысында есептер шығару химияны оқытудың ажырамас бөлігі деп қарау керек, өйткені есеп шығару арқылы теориялық ұғымдар, заңдар, теориялар тереңдей түседі, оқушылардың химиялық қисынды ойлауын өрістетуге, білімдерін іс жүзінде қолдануға мүмкіндік жасалады. Химиялық есептер екі топқа бөлінеді: сандық есептер мен сапалық есептер. Сандық есептерді шығару арқылы жаңа білім беріледі, алынған білім нығайтылады, жетілдіріледі. Есептеулер арқылы химиялық теориялардың, заңдардың мәні ашылады.
Тапсырма: 1-топ сандық есептер типтеріне мысалдар келтіреді.
Сандық есептердің типтері:
І. Химиялық формулалар арқылы есептеу.
ІІ. Химиялық теңдеулер арқылы есептеу.
ІІІ. Ерітіндіге арналған есептер.
2-топ сапалық есептер типтеріне мысалдар келтіреді.
Сапалық есептер– эксперимент есептері, химиялық тәжірибелер жасау арқылы шығарылады.
Бағалау: «Бас бармақ» әдісімен бағалайды.
Топпен жұмыс: Олимпиадаға дайындау жолдары алгоритмдері 2-топқа қағаз кесінділері арқылы беріледі, топтағы педагогтар орын ауыстырады (1-топ 2-топ орнына, 2-топ 1-топ орнына) педагогтар ретімен орналастырып құрастырады, әр топ өз орнына барып бірін бірі «Шапалақ» әдісімен бағалайды.
Олимпиадаға дайындау жолдары дұрыс алгоритмі:
1. Химияның негізгі түсініктері мен заңдарды, химиялық терминдерді
қайталау;
2. Бейорганикалық және органикалық заттардың жіктелуі мен олардың
арасындағы генетикалық байланыстарды өзгерістер арқылы іске асыру
теңдеулерін жазып дәлелдеуге үйрету;
3. Заттардың алыну тәсілдері мен химиялық қасиеттерін реакция теңдеулері арқылы өрнектеуге үйрету;
4. Есептердің шығару алгоритмдерін меңгерту;
5. Есеп шартын дұрыс жазу дағдысын қалыптастыру;
6. Есептердегі физикалық шамаларды анықтауға арналған формулаларды
есте сақтауға арналған жаттығулар арқылы орындату;
7. Химиялық реакциялар теңдеулерін жазу және коэффиценттер қою
әдістерін үйрету;
8. Күрделілігі жоғары есептерді шығаруға дағдыландыру.
9. Тәжірибелік тур есептерін шығаруға үйрету.
Қазіргі жаңа технология мен АКТ құзыреттілігі дамыған кезеңде пәндер олимпиадасына дайындық көптеген сайттар арқылы жүзеге асырылады. Солардың ішінде көп қолданыста жүрген сайттардың бірі-
https://olympiads.bc-pf.org сайты арқылы химия пәнінен олимпиада тапсырмаларын шешу жолдарын қарастырамыз.
1-топ тапсырмасы:
№1 Есеп. Бақалшақ химиясы.
Жағажайда серуендеп жүрген жас химик бақалшақ тауып алды. Теңіз моллюскаларының қабықшалары негізінен арагониттен (кальций карбонатынан) тұратынын білетін жас химик шағын тәжірибе жүргізуді ұйғарды. Массасы 15,57 г болатын бақалшақ концентрлі тұз қышқылында толығымен ерітілді. Реакция кезінде бөлінген газды колбаға жинап, оған жас химик қыздырылған магний жоңқаларын салды. Жарқылдан реакциядан кейін ыдыстың қабырғаларында массасы 1,76 г қара тұнба пайда болды.
1. Барлық сипатталған реакциялардың теңдеулерін жазыңыз.
2. Бақалшақтағы арагониттің массалық үлесін есептеңіз.
Жауабы, есептің шығарылу жолдары:
1.1 (5 ұпай)
Теңіз моллюскаларының бақалшақтары (қабықшалары) негізінен
арагониттен CaCO3 және органикалық бөліктен тұрады. Бақалшақтар
қышқылда көмірқышқыл газының бөлінуімен тез ериді:
CaCO3 + 2HCl = CaCl2 + CO2 + H2O
Магний белсенді металл, сондықтан ол CO2 атмосферасында жанады:
2 Mg + CO2 = 2MgO + C
Қара тұнба - түзілген көмір болып табылады. Әр дұрыс реакция теңдеуі үшін
1.2 (5 ұпай)
Түзілген көмірдің мөлшерін анықтаймыз (1 ұпай):
ν(C) = m(C)/M(C) = 1,76 г/ 12,01 г моль−1 = 0,15 моль
Бастапқы кальций карбонатының зат мөлшері көмірдің зат мөлшеріне тең (1
ұпай):
ν(CaCO3) = ν(C) = 0,15 моль
Арагониттің массасын және оның бақалшақтағы құрамын есептейміз
(әрқайсы үшін 1,5 ұпай, барлығы үшін 3 ұпай):
m(CaCO3) = ν(CaCO3) · M(CaCO3) = 0,15 · 100,09 = 15,01 г
w(CaCO3) =
m(CaCO3)/ m(бақалшақ)=15,01 г/ 15,57
г · 100% = 96,40%
2 топ тапсырмасы:
№2 Есеп. Белгісіз заттар
Қатты күйдегі А жай заты B және C екі атомды газдарымен әрекеттесіп (1 және 2 реакциялары), сәйкес келетін D және E өнімдерін түзеді. Бір қызығы, түзілген газдардың әрқайсысы суда ерігенде қышқылдар қоспалары түзіледі (3 және 4 реакциялары). Алынған ерітінділердің екеуінде де кездесетін F қышқылын G оксидінің (құрамында оттегінің массалық үлесі 68.95%) (5 реакция) гидролизі арқылы алуға болады. A-G заттарын анықтап, 1-5 реакция теңдеулерін жазыңыз. D және E заттары - әрқайсысында 4 атомнан бар бинарлы заттар. D затының молярлық массасы E затынан молярлық массасынан 1,727 есе артық және 49,36 г моль−1 ға көп. Ескерту: бұл тапсырмада титулдық бетте берілген периодтық кестедегі атомдық массалардың нақты мәндерін қолданыңыз.
Жауабы, есептің шығарылу жолдары:
2.1 (14 ұпай)
Есепті G оксидінен бастап шешкен жөн. Өйткені оттегінің массалық үлесі туралы біле отырып, қай элементтің оксиді екенін анықтауға болады. Барлық ықтимал нұсқаларды қарастырайық. Жалпы алғанда, оксид формуласы келесідей көрінеді - E2Ox. Осыған сүйене отырып теңдеу құрайық:
16x / 16x + 2E/ = 0,6895 (1)
16x = 0,6895(16x + 2E) (2)
E = 3,5968x (3)
Мынадай мәндер алуға болады:
-
x
E (г/моль)
1
3,59
2
7,19 (≈Li)
3
10,79 (B)
4
14,38 (≈N)
5
17,98
6
21,58
7
25,17
Көріп отырғаныңыздай, x = 3 мәнінде элементтің молярлық массасы
бордың молярлық массасына дәл сәйкес келеді. Сонда G оксиді B2O3 сәйкес келеді. Бұл оксидтің гидролизі нәтижесінде алынған қышқылдың бор
қышқылы екенін болжау оңай. Осылайша, F - H3BO3.
1- және 2-реакцияларын жалпы түрде жазайық: A + B −−→ D және
A + C −−→ E. Егер D заты бинарлы қосылыс болса, онда A немесе B немесе екеуінің де құрамында бор бар деген сөз. Бірақ құрамында бор бар екі
атомды газ жоқ, одан A заты бор деген қорытынды жасауға болады. Онда B
заты да жай зат.
Енді молярлық масса бойынша есептейік. Сандық мәліметтер бойынша
теңдеулерді құрастырайық:
MD − ME = 49,36 (1)
MD / ME = 1,727 (2)
0,727ME = 49,36 (3)
ME = 67,9 г моль−1 (4)
E қосылысы бордан және тағы бір элементтен құралған, және оның құрамында 4 атом бар. Белгісіз элементті X деп белгілей отырып, 3 түрлі формуланы жазуға болады: BX3, B2X2, B3X. Барлық 3 жағдайда да X үшін қандай молярлық масса болатынын тексерейік.
Практикалық кезең тапсырмалары:
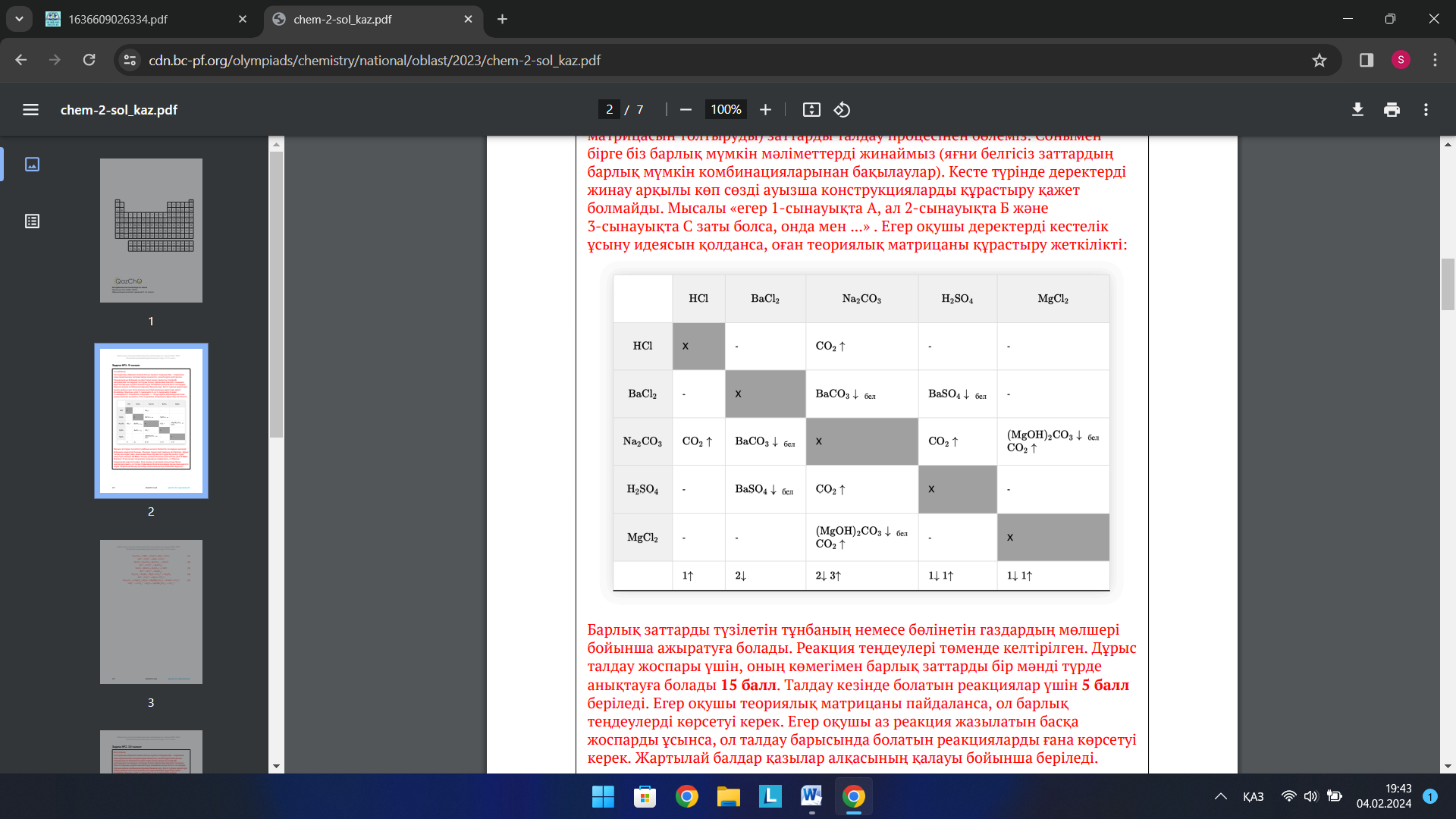
1-топ: №1 Есеп. 9-сынып Бес нөмірленген сынауықтарда мына заттардың сулы ерітінділері бар: тұз қышқылы, барий хлориді, натрий карбонаты, күкірт қышқылы және магний хлориді. Тек жоғарыда аталған ерітінділерді реактив ретінде пайдаланып, қай сынауықта қай зат бар екенін анықтауыңыз қажет. Бұл тапсырманы орындау үшін сізге шынайы экспериментті өткуздің қажеті жоқ. Тек қана талдау жоспарын ұсынып, бүкіл реакция теңдеулерін (молекулалық және қысқартылған иондық) жазу жеткілікті болады.
Жауабы: теориялық матрицаны құрастырамыз, жүретін реакция теңдеулерін (молекулалық және қысқартылған иондық) жазамыз.
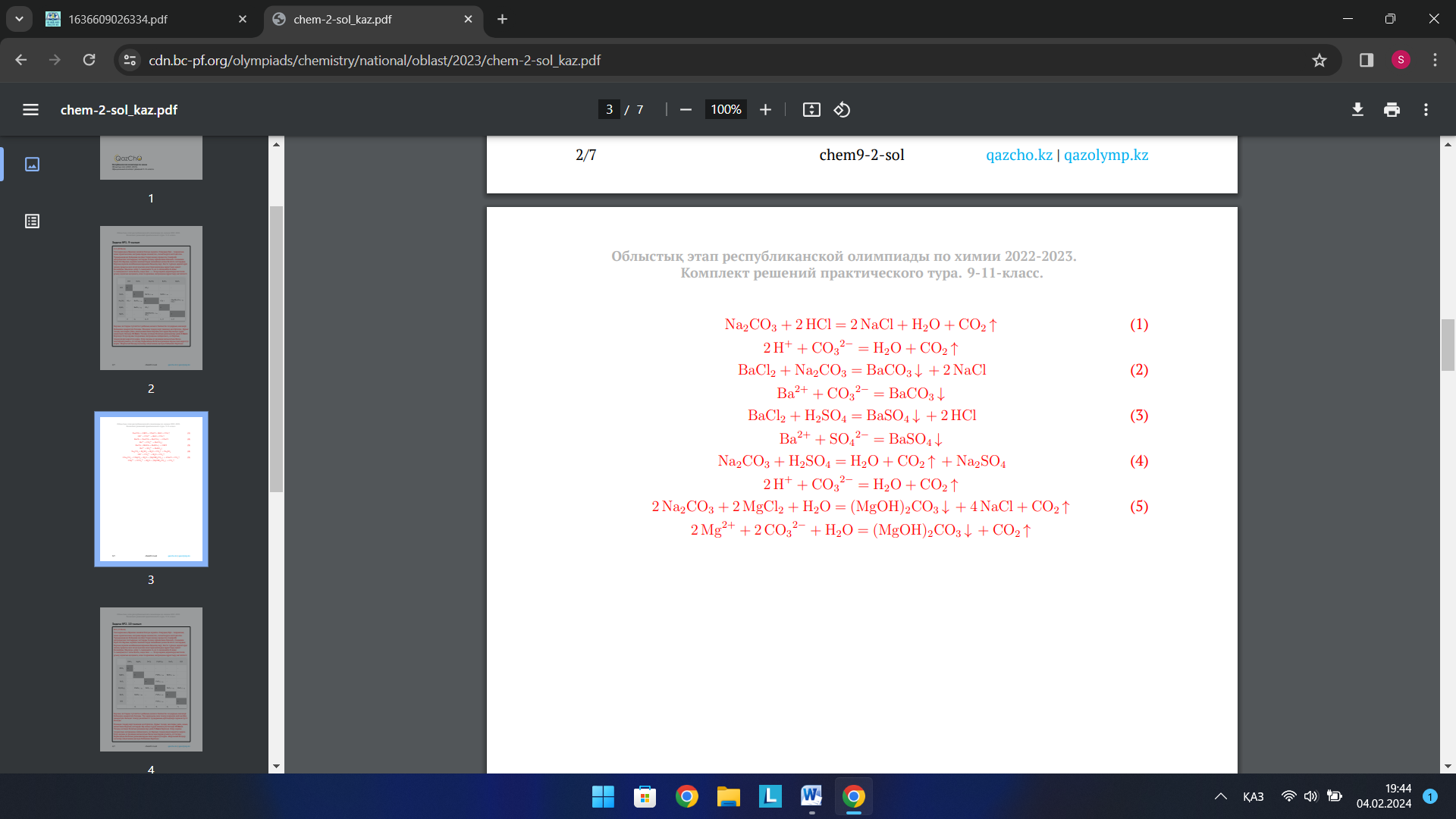
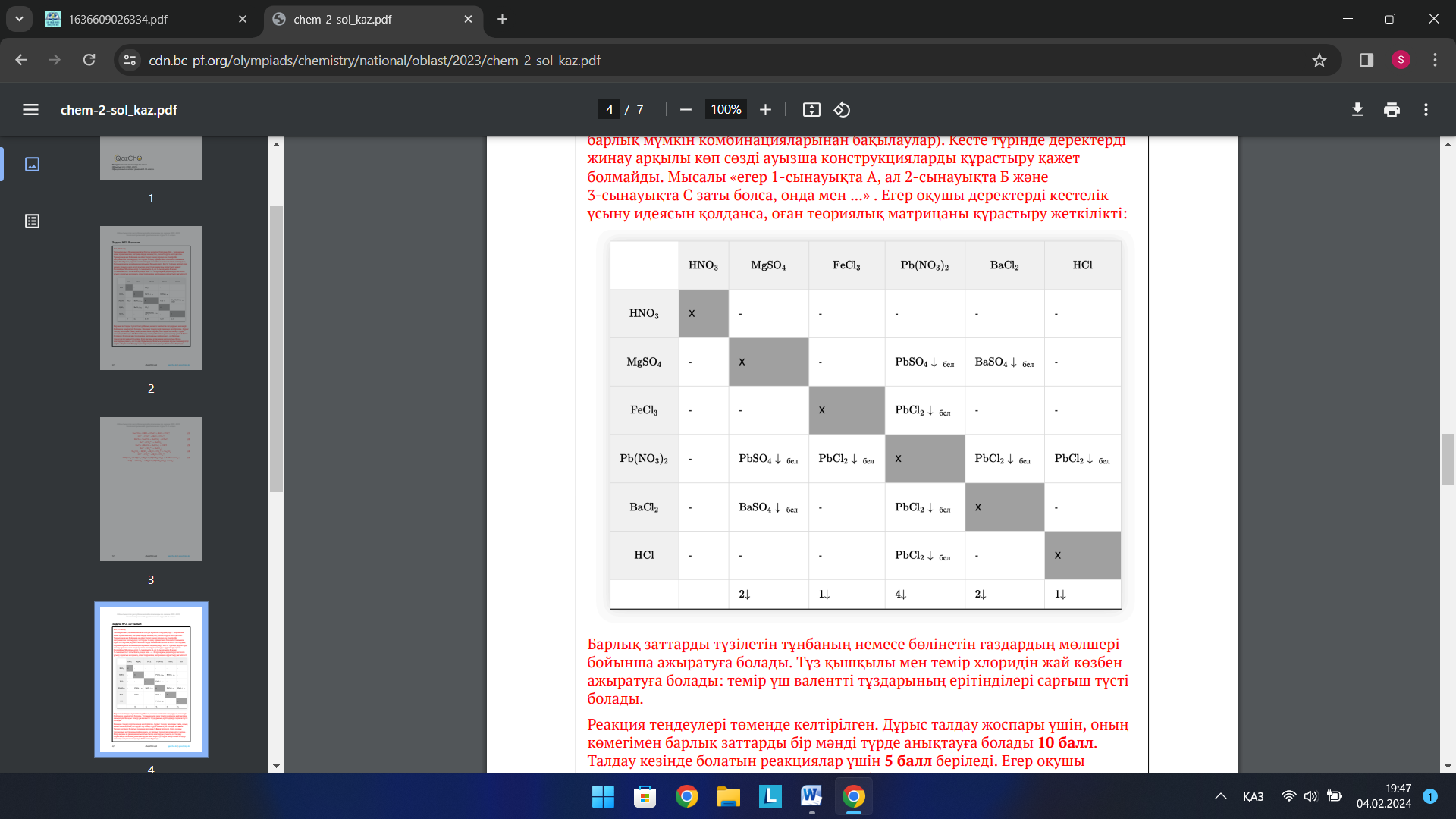
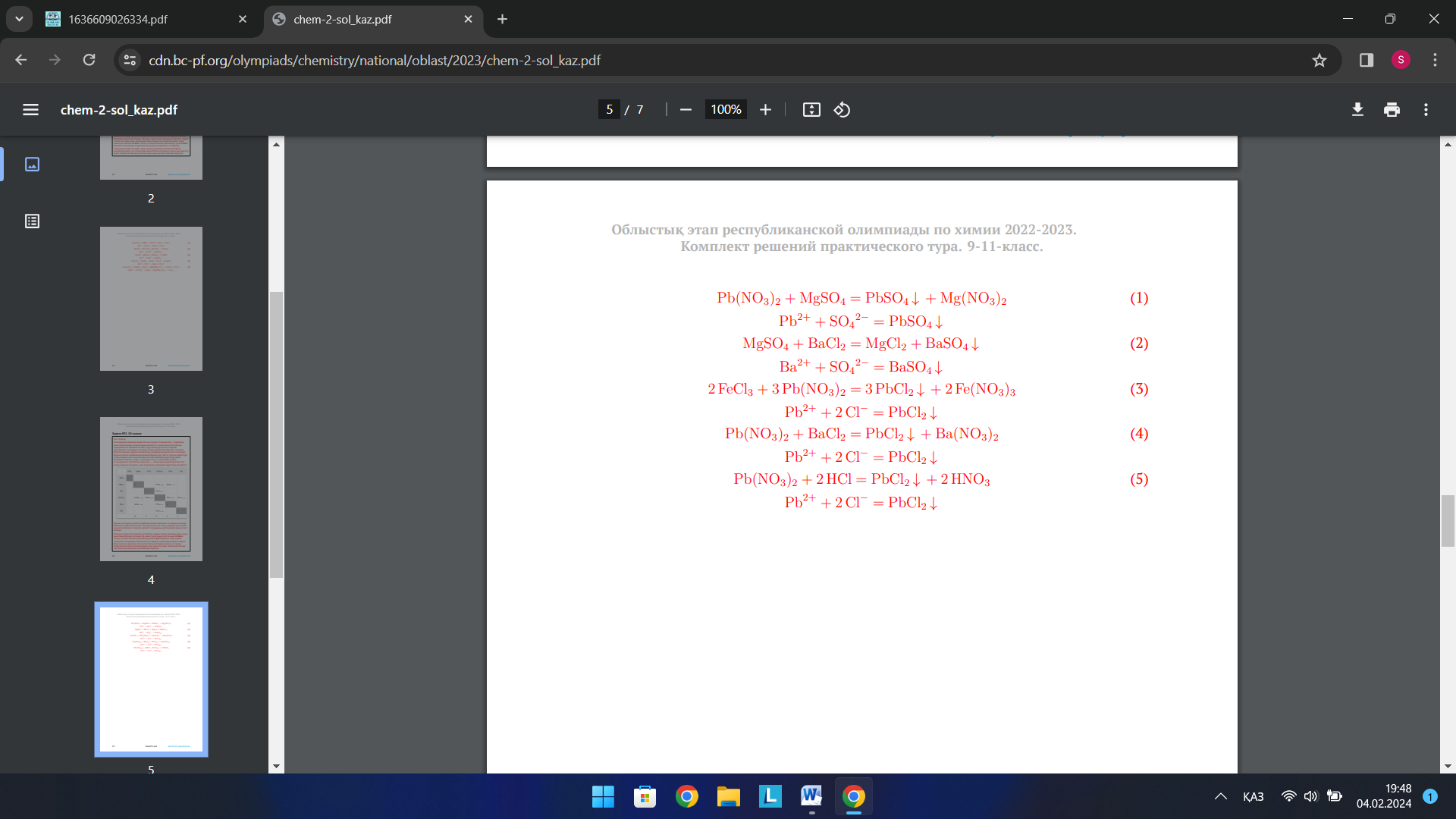
2-топ: №2 Есеп. 10-сынып Алты нөмірленген сынауықтарда мына заттардың сулы ерітінділері бар: азот қышқылы, магний сульфаты, темір (III) хлориді, қорғасын нитраты, барий хлориді және тұз қышқылы. Тек жоғарыда аталған ерітінділерді реактив ретінде пайдаланып, қай сынауықта қай зат бар екенін анықтауыңыз қажет. Бұл тапсырманы орындау үшін сізге шынайы экспериментті өткуздің қажеті жоқ. Тек қана талдау жоспарын ұсынып, бүкіл реакция теңдеулерін (молекулалық және қысқартылған иондық) жазу жеткілікті болады.
Кері байланыс: бүгінгі шебер сыныптан өздеріңізге алған мәліметтер бойынша кері байланыс берулеріңізді сұраймын.

Құрметті әріптестер, шебер сыныпқа қатысып, белсенділік танытқандарыңыз үшін көп рахмет!
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
«Химия пәнінен олимпиадаға дайындық жолдары» шебер сынып
Қостанай облысы әкімдігі білім басқармасының
«Бейімбет Майлин ауданы білім бөлімінің
Сапар Ерғалиев атындағы жалпы білім беретін мектебі» КММ
«Химия пәнінен олимпиадаға дайындық жолдары» шебер-сыныбының
ӘЗІРЛЕМЕСІ
Дайындыған: химия пәнінің мұғалімі Ильясова С.А. педагог-сарапшы
Әйет ауылы,
2023-2024 оқу жылы
Мақсаты: Педагогтардың химиядан олимпиада есептерін шығару қабілеттерін жетілдіре отырып, сандық және сапалық есептерді шығару арқылы топта әрекет ету қабілеттерін дамыту, педагогтермен өзара тәжірибе алмасу. Көрнекіліктері : интерактивті тақта, презентация, үлестірмелі материалдар
Өткізілу түрі: шебер-сынып
Барысы:
Ұйымдастыру: Қайырлы күн, Әріптестер! Бүгінгі шебер сыныпқа қош келдіңіздер!
«Жағымды психологиялық ахуал» педагогтарды ортаға шақырамын.
Әріптестер, барлығымыз ортаға шығып «Молекула» ойынын ойнайық, молекула-3, молекула-5, молекула-6 деп 2-топқа бөлінеміз.
Тапсырма: «Миға шабуыл» Сіздермен Қазақстан Республикасының Білім және ғылым министрінің 07.12.2011 жылғы №514 бұйрығына сәйкес Химиялық олимпиадалар тізімін кластер түрінде жазып көрсек, алдарыңызға берілген А4 параққа жазып толтырамыз.

Бағалау: «Керемет!», «Жарайсыздар!» қошемет сөздермен шабыт беремін.
Шебер сынып химия пәнінен олимпиада есептерін шығару жолдарын үйрету болғандықтан, алдымен химия пәнінен есептердің түрлері мен олимпиадаға дайындау жолдарымен таныссақ.
Есеп шығару– оқушылардың химиялық ой-өрісін дамытудың негізгі құралдарының бірі, теориялық білім мен тәжірибе арасындағы байланысты жүзеге асырудың ажырамас жолы. Сабақ барысында есептер шығару химияны оқытудың ажырамас бөлігі деп қарау керек, өйткені есеп шығару арқылы теориялық ұғымдар, заңдар, теориялар тереңдей түседі, оқушылардың химиялық қисынды ойлауын өрістетуге, білімдерін іс жүзінде қолдануға мүмкіндік жасалады. Химиялық есептер екі топқа бөлінеді: сандық есептер мен сапалық есептер. Сандық есептерді шығару арқылы жаңа білім беріледі, алынған білім нығайтылады, жетілдіріледі. Есептеулер арқылы химиялық теориялардың, заңдардың мәні ашылады.
Тапсырма: 1-топ сандық есептер типтеріне мысалдар келтіреді.
Сандық есептердің типтері:
І. Химиялық формулалар арқылы есептеу.
ІІ. Химиялық теңдеулер арқылы есептеу.
ІІІ. Ерітіндіге арналған есептер.
2-топ сапалық есептер типтеріне мысалдар келтіреді.
Сапалық есептер– эксперимент есептері, химиялық тәжірибелер жасау арқылы шығарылады.
Бағалау: «Бас бармақ» әдісімен бағалайды.
Топпен жұмыс: Олимпиадаға дайындау жолдары алгоритмдері 2-топқа қағаз кесінділері арқылы беріледі, топтағы педагогтар орын ауыстырады (1-топ 2-топ орнына, 2-топ 1-топ орнына) педагогтар ретімен орналастырып құрастырады, әр топ өз орнына барып бірін бірі «Шапалақ» әдісімен бағалайды.
Олимпиадаға дайындау жолдары дұрыс алгоритмі:
1. Химияның негізгі түсініктері мен заңдарды, химиялық терминдерді
қайталау;
2. Бейорганикалық және органикалық заттардың жіктелуі мен олардың
арасындағы генетикалық байланыстарды өзгерістер арқылы іске асыру
теңдеулерін жазып дәлелдеуге үйрету;
3. Заттардың алыну тәсілдері мен химиялық қасиеттерін реакция теңдеулері арқылы өрнектеуге үйрету;
4. Есептердің шығару алгоритмдерін меңгерту;
5. Есеп шартын дұрыс жазу дағдысын қалыптастыру;
6. Есептердегі физикалық шамаларды анықтауға арналған формулаларды
есте сақтауға арналған жаттығулар арқылы орындату;
7. Химиялық реакциялар теңдеулерін жазу және коэффиценттер қою
әдістерін үйрету;
8. Күрделілігі жоғары есептерді шығаруға дағдыландыру.
9. Тәжірибелік тур есептерін шығаруға үйрету.
Қазіргі жаңа технология мен АКТ құзыреттілігі дамыған кезеңде пәндер олимпиадасына дайындық көптеген сайттар арқылы жүзеге асырылады. Солардың ішінде көп қолданыста жүрген сайттардың бірі-
https://olympiads.bc-pf.org сайты арқылы химия пәнінен олимпиада тапсырмаларын шешу жолдарын қарастырамыз.
1-топ тапсырмасы:
№1 Есеп. Бақалшақ химиясы.
Жағажайда серуендеп жүрген жас химик бақалшақ тауып алды. Теңіз моллюскаларының қабықшалары негізінен арагониттен (кальций карбонатынан) тұратынын білетін жас химик шағын тәжірибе жүргізуді ұйғарды. Массасы 15,57 г болатын бақалшақ концентрлі тұз қышқылында толығымен ерітілді. Реакция кезінде бөлінген газды колбаға жинап, оған жас химик қыздырылған магний жоңқаларын салды. Жарқылдан реакциядан кейін ыдыстың қабырғаларында массасы 1,76 г қара тұнба пайда болды.
1. Барлық сипатталған реакциялардың теңдеулерін жазыңыз.
2. Бақалшақтағы арагониттің массалық үлесін есептеңіз.
Жауабы, есептің шығарылу жолдары:
1.1 (5 ұпай)
Теңіз моллюскаларының бақалшақтары (қабықшалары) негізінен
арагониттен CaCO3 және органикалық бөліктен тұрады. Бақалшақтар
қышқылда көмірқышқыл газының бөлінуімен тез ериді:
CaCO3 + 2HCl = CaCl2 + CO2 + H2O
Магний белсенді металл, сондықтан ол CO2 атмосферасында жанады:
2 Mg + CO2 = 2MgO + C
Қара тұнба - түзілген көмір болып табылады. Әр дұрыс реакция теңдеуі үшін
1.2 (5 ұпай)
Түзілген көмірдің мөлшерін анықтаймыз (1 ұпай):
ν(C) = m(C)/M(C) = 1,76 г/ 12,01 г моль−1 = 0,15 моль
Бастапқы кальций карбонатының зат мөлшері көмірдің зат мөлшеріне тең (1
ұпай):
ν(CaCO3) = ν(C) = 0,15 моль
Арагониттің массасын және оның бақалшақтағы құрамын есептейміз
(әрқайсы үшін 1,5 ұпай, барлығы үшін 3 ұпай):
m(CaCO3) = ν(CaCO3) · M(CaCO3) = 0,15 · 100,09 = 15,01 г
w(CaCO3) =
m(CaCO3)/ m(бақалшақ)=15,01 г/ 15,57
г · 100% = 96,40%
2 топ тапсырмасы:
№2 Есеп. Белгісіз заттар
Қатты күйдегі А жай заты B және C екі атомды газдарымен әрекеттесіп (1 және 2 реакциялары), сәйкес келетін D және E өнімдерін түзеді. Бір қызығы, түзілген газдардың әрқайсысы суда ерігенде қышқылдар қоспалары түзіледі (3 және 4 реакциялары). Алынған ерітінділердің екеуінде де кездесетін F қышқылын G оксидінің (құрамында оттегінің массалық үлесі 68.95%) (5 реакция) гидролизі арқылы алуға болады. A-G заттарын анықтап, 1-5 реакция теңдеулерін жазыңыз. D және E заттары - әрқайсысында 4 атомнан бар бинарлы заттар. D затының молярлық массасы E затынан молярлық массасынан 1,727 есе артық және 49,36 г моль−1 ға көп. Ескерту: бұл тапсырмада титулдық бетте берілген периодтық кестедегі атомдық массалардың нақты мәндерін қолданыңыз.
Жауабы, есептің шығарылу жолдары:
2.1 (14 ұпай)
Есепті G оксидінен бастап шешкен жөн. Өйткені оттегінің массалық үлесі туралы біле отырып, қай элементтің оксиді екенін анықтауға болады. Барлық ықтимал нұсқаларды қарастырайық. Жалпы алғанда, оксид формуласы келесідей көрінеді - E2Ox. Осыған сүйене отырып теңдеу құрайық:
16x / 16x + 2E/ = 0,6895 (1)
16x = 0,6895(16x + 2E) (2)
E = 3,5968x (3)
Мынадай мәндер алуға болады:
-
x
E (г/моль)
1
3,59
2
7,19 (≈Li)
3
10,79 (B)
4
14,38 (≈N)
5
17,98
6
21,58
7
25,17
Көріп отырғаныңыздай, x = 3 мәнінде элементтің молярлық массасы
бордың молярлық массасына дәл сәйкес келеді. Сонда G оксиді B2O3 сәйкес келеді. Бұл оксидтің гидролизі нәтижесінде алынған қышқылдың бор
қышқылы екенін болжау оңай. Осылайша, F - H3BO3.
1- және 2-реакцияларын жалпы түрде жазайық: A + B −−→ D және
A + C −−→ E. Егер D заты бинарлы қосылыс болса, онда A немесе B немесе екеуінің де құрамында бор бар деген сөз. Бірақ құрамында бор бар екі
атомды газ жоқ, одан A заты бор деген қорытынды жасауға болады. Онда B
заты да жай зат.
Енді молярлық масса бойынша есептейік. Сандық мәліметтер бойынша
теңдеулерді құрастырайық:
MD − ME = 49,36 (1)
MD / ME = 1,727 (2)
0,727ME = 49,36 (3)
ME = 67,9 г моль−1 (4)
E қосылысы бордан және тағы бір элементтен құралған, және оның құрамында 4 атом бар. Белгісіз элементті X деп белгілей отырып, 3 түрлі формуланы жазуға болады: BX3, B2X2, B3X. Барлық 3 жағдайда да X үшін қандай молярлық масса болатынын тексерейік.
Практикалық кезең тапсырмалары:
1-топ: №1 Есеп. 9-сынып Бес нөмірленген сынауықтарда мына заттардың сулы ерітінділері бар: тұз қышқылы, барий хлориді, натрий карбонаты, күкірт қышқылы және магний хлориді. Тек жоғарыда аталған ерітінділерді реактив ретінде пайдаланып, қай сынауықта қай зат бар екенін анықтауыңыз қажет. Бұл тапсырманы орындау үшін сізге шынайы экспериментті өткуздің қажеті жоқ. Тек қана талдау жоспарын ұсынып, бүкіл реакция теңдеулерін (молекулалық және қысқартылған иондық) жазу жеткілікті болады.
Жауабы: теориялық матрицаны құрастырамыз, жүретін реакция теңдеулерін (молекулалық және қысқартылған иондық) жазамыз.


2-топ: №2 Есеп. 10-сынып Алты нөмірленген сынауықтарда мына заттардың сулы ерітінділері бар: азот қышқылы, магний сульфаты, темір (III) хлориді, қорғасын нитраты, барий хлориді және тұз қышқылы. Тек жоғарыда аталған ерітінділерді реактив ретінде пайдаланып, қай сынауықта қай зат бар екенін анықтауыңыз қажет. Бұл тапсырманы орындау үшін сізге шынайы экспериментті өткуздің қажеті жоқ. Тек қана талдау жоспарын ұсынып, бүкіл реакция теңдеулерін (молекулалық және қысқартылған иондық) жазу жеткілікті болады.


Кері байланыс: бүгінгі шебер сыныптан өздеріңізге алған мәліметтер бойынша кері байланыс берулеріңізді сұраймын.

Құрметті әріптестер, шебер сыныпқа қатысып, белсенділік танытқандарыңыз үшін көп рахмет!

шағым қалдыра аласыз





 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
