
|
школа |
|
|||||
|
Предмет |
физика |
|||||
|
Раздел |
Строение атома. Атомные явления |
|||||
|
ФИО педагога |
|
|||||
|
Дата |
|
|||||
|
Класс 9б |
Количество присутствующих: |
отсутствующих: |
||||
|
Тема урока |
Опыт Резерфорда, строение атома |
|||||
|
Цели обучения, которые достигаются на данном уроке (ссылка на учебную программу) |
9.6.1.7 - описывать опыт Резерфорда по рассеянию альфа-частиц. |
|||||
|
Цель урока |
Ознакомление учащихся с опытом Резерфорда, планетарной моделью атома и атомного ядра. ознакомить учащихся строением атома, расширить представление учащихся о физической картине мира. |
|||||
|
Критерии успеха |
Изучать планетарную модель атома. Познакомиться с гипотезой Томсона и фундаментальным опытом Резерфорда. Знает как описывать опыт Резерфорда по рассеянию альфа-ча ; |
|||||
|
Ход урока |
||||||
|
Этапы урока |
Деятельность учителя |
Деятельность обучающихся |
Оценивание |
Ресурсы |
||
|
|
Приветствует учащихся, проверяет готовность к уроку, желает успеха. Для создания психологической атмосферы проводит игру «Расскажи мне обо мне», а также делятся на группы. Проверка домашней работы. «Мозговой штурм»
- Каковы были
взгляды о строении вещества в
древности?
Изучение нового материала Группа 1. После
открытия в 1897 году электрона, входящего в состав атома, был
сделан вывод о сложном строении атома. Первая достаточно
разработанная модель атома была предложена Томсоном. Согласно этой
модели вещество в атоме несет положительный заряд и равномерно
заполняет весь объем атома. Электроны “вкраплены” в атом, словно
изюм в булку. Но она требовала
доказательств. |
Учащиеся рассаживаются по местам. Проверяют наличие принадлежностей. |
|
видеоролик |
||
|
Изучение нового материала |
Для проверки
гипотезы Дж. Дж. Томсона необходимо было провести эксперимент, что
и сделал Э. Резерфорд. Он решил проникнуть внутрь атома с помощью
α- частиц, которые
имели положительный заряд, массу почти в 7300 раз большую чем масса
электрона и очень большую скорость (около 20000км/c). С точки
зрения Резерфорда α-частицы должны
были легко "пробить" атом и тем самым доказать справедливость
модели атома Томсона.
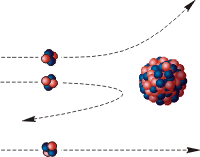
Ресурс 1 Изучение нового материала Группа 2. Схему экспериментальной установки Резерфорда
В
цилиндрическом сосуде с небольшим отверстием находился
радиоактивный препарат, испускавший поток -частиц. Они
попадали на золотую фольгу и, проходя через нее, ударялись о
люминесцирующий экран. В местах удара частиц на экране возникали
вспышки света . При столкновениях с отдельными электронами -частицы испытывают отклонения на очень небольшие углы, так как масса электрона мала. Однако в тех редких случаях, когда она пролетает на близком расстоянии от одного из атомных ядер, под действием сильного электрического поля ядра может произойти отклонение на большой угол. Итак, Резерфорд предложил планетарную модель атома. Согласно этой модели, в центре атома располагается положительно заряженное ядро, в котором сосредоточена почти вся масса атома. Атом в целом нейтрален. Вокруг ядра, подобно планетам, вращаются под действием кулоновских сил со стороны ядра электроны. Находиться в состоянии покоя электроны не могут, так как они упали бы на ядро.
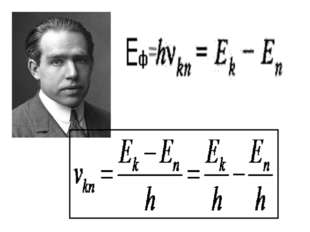
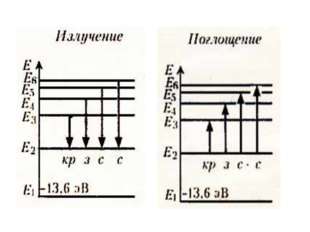
(E n) в
стационарное состояние с большей энергией (E k).
Работа в паре Задание 1 – Найдите ошибки в следующем тексте Учитель раздает заранее подготовленный текст “Французский физик Э. Резерфорд, проведя исследования состава и строения атомов, сделал выводы, что каждый атом состоит из электронов, которые находятся в его центре; протонов, движущихся вокруг электронов, и нейтронов, располагающихся снаружи атома. Поскольку заряженные частицы сосредоточены внутри атома, а на его поверхности расположены, не имеющие заряды, атом в целом нейтрален”. Задание 2 1) Используя Периодическую систему химических элементов Д.И. Менделеева, определите, к атому какого элемента принадлежат следующие ядра 2Х4; 79Х197; 26Х56; 47Х108; 13Х27 2) Какие частицы или ядра химических элементов представлены в следующих символах: 1р1; 2Не4; 0n1; -1е0; 1Н2? Задание 3 Написать синквейн на тему атом
Синквейн (в переводе с франц.– пять строк):
Первая строка – название темы одним словом; Вторая строка – описание темы в двух словах (двумя прилагательными); Третья строка – описание действия в рамках темы тремя словами; Четвертая строка – фраза из четырех слов, показывающая отношение к теме; Пятая строка – синоним из одного слова, который повторяет суть темы. Индвидуальное работа
2. Ядро состоит из 92 протонов. Записать количество электронов и определить, какой это химический элемент.
3.
Атом перешел с первого уровня на второй. Какова порция поглощенной энергии? Ф взаимооценивание через вопросы учащихся и по критериям. |
Устно отвечают на вопросы, с объяснением. Находит ошибки в примерах Каждая группа читает свой параграф, выбирает и предоставляет ключевую информацию из изученного материала. |
Стратегия «Верно - не верно» Словесная оценка учителя. Взаимооценивание Стратегия «Стикер» |
|
||
|
Подведение итогов урока (5 мин)
|
Беседа. Рефлексия. «Рефлексивный ринг» Сегодня я узнал… Я научился… Меня удивило… У меня получилось… Было трудно… Я смог … Я понял, что… Я теперь могу… Меня удивило… Мне захотелось… Домашнее задание §36, стр 211 |
Ученики показывают умение обосновывать свое понимание Записывают д.з. в дневники |
Самооценивание |
Рефлексивный лист, стикеры |
||
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Опыт Резерфорда, строение атома 9 класс
|
школа |
|
|||||
|
Предмет |
физика |
|||||
|
Раздел |
Строение атома. Атомные явления |
|||||
|
ФИО педагога |
|
|||||
|
Дата |
|
|||||
|
Класс 9б |
Количество присутствующих: |
отсутствующих: |
||||
|
Тема урока |
Опыт Резерфорда, строение атома |
|||||
|
Цели обучения, которые достигаются на данном уроке (ссылка на учебную программу) |
9.6.1.7 - описывать опыт Резерфорда по рассеянию альфа-частиц. |
|||||
|
Цель урока |
Ознакомление учащихся с опытом Резерфорда, планетарной моделью атома и атомного ядра. ознакомить учащихся строением атома, расширить представление учащихся о физической картине мира. |
|||||
|
Критерии успеха |
Изучать планетарную модель атома. Познакомиться с гипотезой Томсона и фундаментальным опытом Резерфорда. Знает как описывать опыт Резерфорда по рассеянию альфа-ча ; |
|||||
|
Ход урока |
||||||
|
Этапы урока |
Деятельность учителя |
Деятельность обучающихся |
Оценивание |
Ресурсы |
||
|
|
Приветствует учащихся, проверяет готовность к уроку, желает успеха. Для создания психологической атмосферы проводит игру «Расскажи мне обо мне», а также делятся на группы. Проверка домашней работы. «Мозговой штурм»
- Каковы были
взгляды о строении вещества в
древности?
Изучение нового материала Группа 1. После
открытия в 1897 году электрона, входящего в состав атома, был
сделан вывод о сложном строении атома. Первая достаточно
разработанная модель атома была предложена Томсоном. Согласно этой
модели вещество в атоме несет положительный заряд и равномерно
заполняет весь объем атома. Электроны “вкраплены” в атом, словно
изюм в булку. Но она требовала
доказательств. |
Учащиеся рассаживаются по местам. Проверяют наличие принадлежностей. |
|
видеоролик |
||
|
Изучение нового материала |
Для проверки
гипотезы Дж. Дж. Томсона необходимо было провести эксперимент, что
и сделал Э. Резерфорд. Он решил проникнуть внутрь атома с помощью
α- частиц, которые
имели положительный заряд, массу почти в 7300 раз большую чем масса
электрона и очень большую скорость (около 20000км/c). С точки
зрения Резерфорда α-частицы должны
были легко "пробить" атом и тем самым доказать справедливость
модели атома Томсона.
Ресурс 1 Изучение нового материала Группа 2. Схему экспериментальной установки Резерфорда
В
цилиндрическом сосуде с небольшим отверстием находился
радиоактивный препарат, испускавший поток -частиц. Они
попадали на золотую фольгу и, проходя через нее, ударялись о
люминесцирующий экран. В местах удара частиц на экране возникали
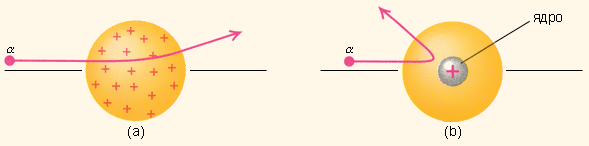
вспышки света . При столкновениях с отдельными электронами -частицы испытывают отклонения на очень небольшие углы, так как масса электрона мала. Однако в тех редких случаях, когда она пролетает на близком расстоянии от одного из атомных ядер, под действием сильного электрического поля ядра может произойти отклонение на большой угол. Итак, Резерфорд предложил планетарную модель атома. Согласно этой модели, в центре атома располагается положительно заряженное ядро, в котором сосредоточена почти вся масса атома. Атом в целом нейтрален. Вокруг ядра, подобно планетам, вращаются под действием кулоновских сил со стороны ядра электроны. Находиться в состоянии покоя электроны не могут, так как они упали бы на ядро.
(E n) в
стационарное состояние с большей энергией (E k).
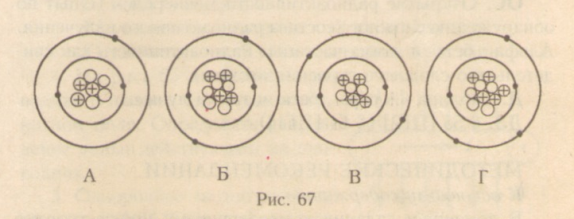
Работа в паре Задание 1 – Найдите ошибки в следующем тексте Учитель раздает заранее подготовленный текст “Французский физик Э. Резерфорд, проведя исследования состава и строения атомов, сделал выводы, что каждый атом состоит из электронов, которые находятся в его центре; протонов, движущихся вокруг электронов, и нейтронов, располагающихся снаружи атома. Поскольку заряженные частицы сосредоточены внутри атома, а на его поверхности расположены, не имеющие заряды, атом в целом нейтрален”. Задание 2 1) Используя Периодическую систему химических элементов Д.И. Менделеева, определите, к атому какого элемента принадлежат следующие ядра 2Х4; 79Х197; 26Х56; 47Х108; 13Х27 2) Какие частицы или ядра химических элементов представлены в следующих символах: 1р1; 2Не4; 0n1; -1е0; 1Н2? Задание 3 Написать синквейн на тему атом
Синквейн (в переводе с франц.– пять строк):
Первая строка – название темы одним словом; Вторая строка – описание темы в двух словах (двумя прилагательными); Третья строка – описание действия в рамках темы тремя словами; Четвертая строка – фраза из четырех слов, показывающая отношение к теме; Пятая строка – синоним из одного слова, который повторяет суть темы. Индвидуальное работа
2. Ядро состоит из 92 протонов. Записать количество электронов и определить, какой это химический элемент.
3.
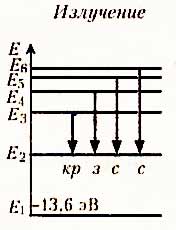
Атом перешел с первого уровня на второй. Какова порция поглощенной энергии? Ф взаимооценивание через вопросы учащихся и по критериям. |
Устно отвечают на вопросы, с объяснением. Находит ошибки в примерах Каждая группа читает свой параграф, выбирает и предоставляет ключевую информацию из изученного материала. |
Стратегия «Верно - не верно» Словесная оценка учителя. Взаимооценивание Стратегия «Стикер» |
|
||
|
Подведение итогов урока (5 мин)
|
Беседа. Рефлексия. «Рефлексивный ринг» Сегодня я узнал… Я научился… Меня удивило… У меня получилось… Было трудно… Я смог … Я понял, что… Я теперь могу… Меня удивило… Мне захотелось… Домашнее задание §36, стр 211 |
Ученики показывают умение обосновывать свое понимание Записывают д.з. в дневники |
Самооценивание |
Рефлексивный лист, стикеры |
||

шағым қалдыра аласыз


 ролетают сквозь него.
ролетают сквозь него.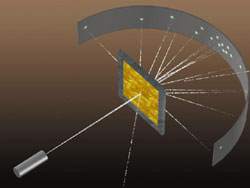
 ....
....
 ?
?




 Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
Бұл курс Қазақстан Республикасы Оқу-ағарту министрлігімен келісілген
