
УТВЕРЖДАЮ
заместитель директора по НМР
________З.М.Жакупова
«____» _________ 20__ж/г.
ПОУРОЧНЫЙ ПЛАН № 1
Тема занятия Современная теория строения атома. Состояние и движение электронов в атоме
Наименование модуля /дисциплины __Химия_
«__»____________ 2025 года
-
Общие сведения
Курс, группы
Тип занятия _ Теория
2.Цель: знать современную теорию строения атома и важнейшие характеристики частиц вещества и атома; различать формы s, p, d, f-орбиталей;
Задачи:
Способствовать формированию представлений о сложности строения атома, составе атомных ядер, физическом смысле атомного номера; формированию умений давать характеристику элементарных частиц (протонов, нейтронов и электронов), определять число протонов в ядре атома химического элемента.
Развивать умение анализировать, сравнивать, делать выводы, сопоставлять, выделять главное.
Формировать навыки самостоятельной работы с текстом учебника,
способствовать формированию познавательного интереса к изучаемой теме и предмету в целом.
3. Ожидаемые результаты (профессиональных умений, которыми овладеют обучающиеся в процессе учебного занятия) перечисляет основные положения современной теории строения атома; объясняет физический смысл протонов, нейтронов, электронов, нуклонов и нуклидов; раскрывает содержание понятий изотопы.
4. Необходимые ресурсы
4.1 Учебно-методическое оснащение, справочная литература, лекционные материалы (Приложение) Учебник: Химия 10 класс Оспанова М., Белоусова Т., Аухадиева К.
4.2 Техническое оснащение, материалы. Пройдите по ссылке и ознакомьтесь с материалом https://chemege.ru/stroenie-atoma-2/ https://www.yaklass.ru/materiali?themeid=145&mode=lsntheme
https://www.youtube.com/watch?v=kqHYbT9rv6A
5. Ход занятия
5.1. Орг.момент. Актуализация знаний. Определение целей урока с обуч-ся и тд.
-
Организационный момент. Приветствие. Проверка отсутствующих.
-
Актуализация новых знаний
Фронтальный опрос по теме «Периодическая система химических элементов».
1. Дайте определение понятий: группа, период, А-группа, В-группа.
2. Укажите атомный номер, номер периода и номер группы, в которых находятся химические элементы: фтор, магний, железо.
3. Укажите химический элемент, простое вещество которого имеет более выраженные металлические свойства: натрий или алюминий. Ответ поясните.
4. Укажите химические элементы, которые образуют высший оксид состава Э2O5.
5.2. Изучение нового учебного материала
-
Атом – неделимая микрочастица, имеющая форму шара.
-
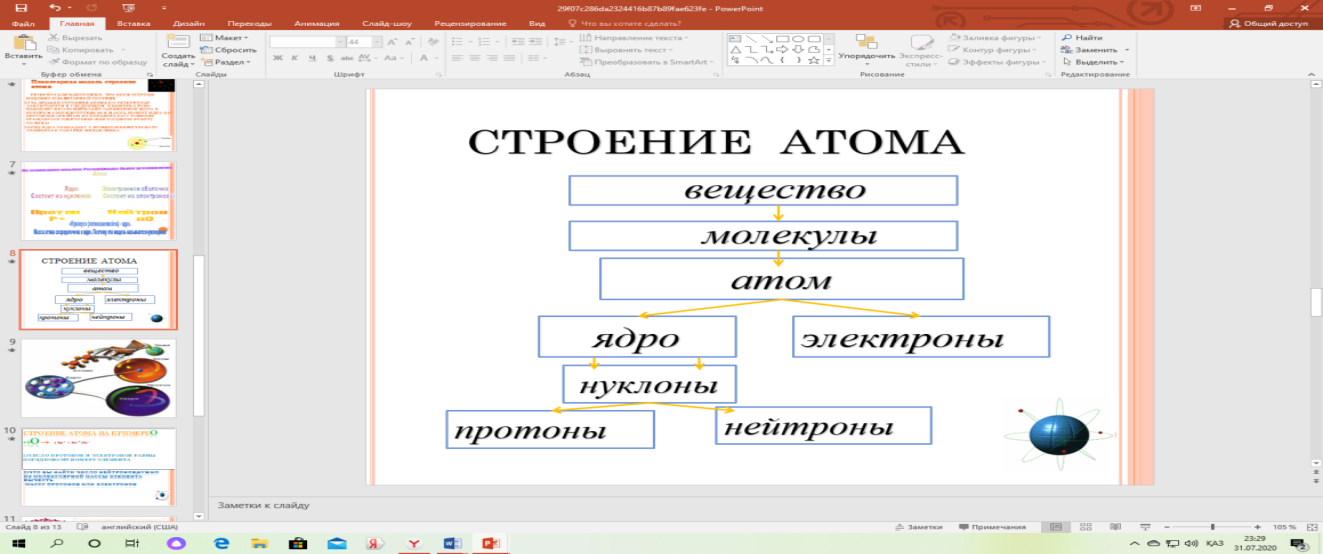
Атом состоит из ядра и электронов.
-
Ядро имеет очень маленький размер и положительный заряд.
-
Атом – электронейтрален, так как число протонов и электронов одинаково.
-
Электроны обладают отрицательным зарядом и движутся вокруг ядра.
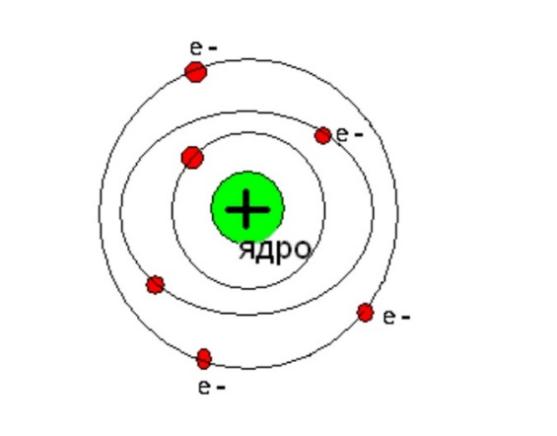
Планетарная модель Резерфорда.
Суть планетарной модели строения атома можно свести к следующим утверждениям:
1. В центре атома находится положительно заряженное ядро, занимающее ничтожную часть пространства внутри атома.
2. Весь положительный заряд и почти вся масса атома сосредоточены в его ядре.
3. Вокруг ядра вращаются электроны. Их число равно положительному заряду ядра.
Эта модель оказалась очень наглядной и полезной для объяснения многих экспериментальных данных, но обнаружила и свои недостатки.
Теория Бора. В 1913 г. Н. Бор предложил свою теорию строения атома, в основу положено два необычных постулата:
1. Электрон может вращаться вокруг ядра не по произвольным, а только по строго определенным (стационарным) круговым орбитам.
2. При движении по стационарным орбитам электрон не излучает и не поглощает энергии.
Строение всех атомов зашифровано в периодической системе химических элементов Д. И. Менделеева. Вы, знаете, что каждому химическому элементу присвоен порядковый номер и для каждого элемента подсчитана атомная масса. Но это не просто числа, они имеют физический смысл. В чем он заключается, мы сейчас узнаем.
Введем следующие обозначения
Z – порядковый номер химического элемента
М – массовое число, М =Ar
N – число нейтронов
Z – указывает на заряд ядра, а следовательно на число протонов, а так как атом нейтрален, то число протонов равно числу электронов.
М – сумма протонов и нейтронов в ядре атома
М = Z + N
Введем обозначение химического элемента:
Х 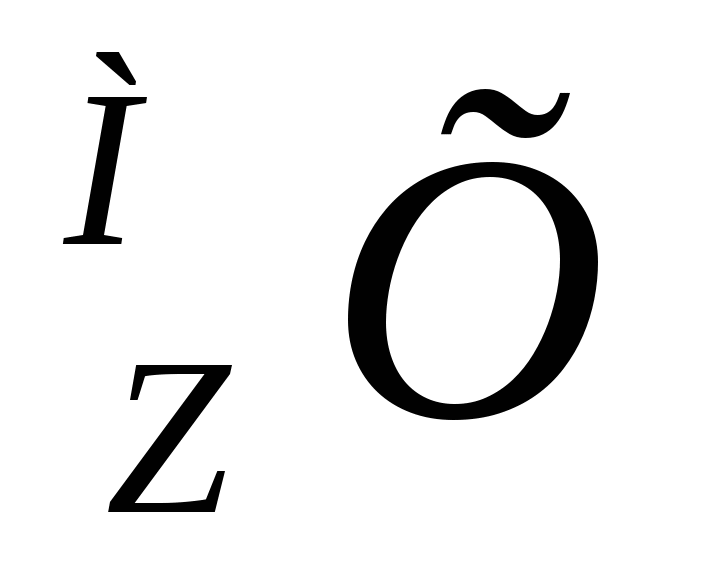 - символ химического
элемента
- символ химического
элемента
Z - заряд ядра
М – массовое число
Например: формула состава
атома кислорода: ![]() (8р;
8е;8N)
(8р;
8е;8N)
Интернет источники: Пройдите по ссылке и ознакомьтесь с материалом https://chemege.ru/stroenie-atoma-2/ https://www.yaklass.ru/materiali?themeid=145&mode=lsntheme
Просмотрите видео материал: https://www.youtube.com/watch?v=kqHYbT9rv6A
5.3. Закрепление нового УМ.
-
Заполни таблицу «Периодическая система и строение атома»:
-
Представьте электронные структуры Zn2+; S6+
|
Частица |
Заряд |
Массовое число |
Ca |
Fe |
Cu |
C l |
|
е– - |
|
|
|
|
|
|
|
р+ - |
|
|
|
|
|
|
|
n0 - |
|
|
|
|
|
|
Я знаю
Я знал
Я узнал
5.5 Домашнее задание 10кл.-§1 стр. 5 читать
Лекция № 1
Предмет: Химия
Тема: Современная теория строения атома. Состояние и движение электронов в атоме
Цели урока: Способствовать формированию представлений о сложности строения атома, составе атомных ядер, физическом смысле атомного номера; формированию умений давать характеристику элементарных частиц (протонов, нейтронов и электронов), определять число протонов в ядре атома химического элемента.
Ход урока
Актуализация знаний:
Фронтальный опрос по теме «Периодическая система химических элементов».
1. Дайте определение понятий: группа, период, А-группа, В-группа.
2. Укажите атомный номер, номер периода и номер группы, в которых находятся химические элементы: фтор, магний, железо.
3. Укажите химический элемент, простое вещество которого имеет более выраженные металлические свойства: натрий или алюминий. Ответ поясните.
4. Укажите химические элементы, которые образуют высший оксид состава Э2O5.
3. Лекционный материал
До конца XIX в. атом считали неделимой частицей, но последовавшие позже открытия (радиоактивность, фотоэффект) поколебали это убеждение. Сейчас известно, что атом состоит из элементарных частиц, основные из которых – протон, нейтрон, электрон.
Прямым доказательством сложности строения атома явилось и открытие самопроизвольного распада атомов некоторых элементов с испусканием невидимых глазу лучей. Это явление, открытое в 1896 г. французским ученым Анри Беккерелем, получило название радиоактивности. В 1897 г. английский физик Дж. Дж. Томсон установил существование в атоме электронов — отрицательно заряженных частиц. Эти открытия свидетельствовали о том, что атом имеет сложное строение.
После открытия основных элементарных частиц, входящих в состав атома, встал вопрос об их местонахождении, т.е. о строении атома. В 1911 г. Томсон предложил свою модель строения атома, которая получила условное название «пудинг с изюмом». Согласно этой модели атом представляет собой некую субстанцию, в которой равномерно распределены протоны, нейтроны и электроны. Число протонов равно числу электронов, поэтому атом в целом электронейтрален.
В 1913 г. Резерфорд ставит опыт, результаты которого модель Томсона объяснить не может. Это заставляет Резерфорда предложить свою модель строения атома, получившую название планетарной. Согласно этой модели атом состоит из ядра, в котором сконцентрирована основная масса атома, поскольку ядро содержит протоны и нейтроны; вокруг ядра на огромной скорости вращаются электроны. Поскольку модель Резерфорда содержала ряд противоречий, Н.Бором были введены постулаты, устраняющие эти противоречия.
1-й постулат. Электроны вращаются вокруг ядра не по произвольным, а по строго определенным, стационарным орбитам.
2-й постулат. При движении по стационарной орбите электрон не излучает и не поглощает энергию. Изменение энергии происходит при переходе электрона с одной стационарной орбиты на другую.
Но теория Резерфорда–Бора дает удовлетворительные результаты только для атома водорода. Современные представления о строении атома подчиняются квантовой модели строения атома.
Из курса химии вы уже знаете одно определение атома как мельчайшей, химически неделимой частицы. Теперь можно дать еще одно, физическое, определение этого понятия. Давайте запишем его в конспект:
Атом — электронейтральная частица, состоящая из положительно за-
ряженного ядра и отрицательно заряженных электронов.
Позже было установлено, что ядро атома также имеет сложное строение.
Оно состоит из частиц двух типов: протонов и нейтронов.
Протон и нейтрон имеют практически одинаковую массу, равную примерно 1 u, т. е. одной атомной единице массы. Протон (его символ р) имеет относительный заряд 1+, а нейтрон (символ n) электронейтрален.
Относительный заряд электрона (его символическое обозначение е) равен 1−, а масса примерно в 1840 раз меньше массы протона, т. е. равна 1/1840u.
В начале XX века была принята планетарная модель строения атома, предложенная Резерфордом, согласно которой вокруг очень малого по размерам положительно заряженного ядра движутся электроны, как планеты вокруг Солнца. Следовательно, в атоме есть траектории, по которым движется электрон. Однако дальнейшие исследования показали, что в атоме не существует траекторий движения электронов. Движение без траектории означает, что мы не знаем, как электрон движется в атоме, но можем установить область, где чаще всего встречается электрон. Это уже не орбита, а орбиталь. Двигаясь вокруг атома, электроны образуют в совокупности его электронную оболочку.
Давайте выясним, как движутся электроны вокруг ядра?
Беспорядочно или в определенном порядке?
Исследования Нильса Бора – основоположника современной атомной физики, а также ряда других ученых позволили сделать вывод: электроны в атомах располагаются определенными слоями – оболочками и в определенном порядке.
Строение электронных оболочек атомов имеют важную роль для химии, так как именно электроны обуславливают химические свойства веществ. Важнейшей характеристикой движения электрона на определенной орбитали является энергия его связи с ядром. Электроны в атоме различаются определенной энергией, и, как показывают опыты, одни притягиваются к ядру сильнее, другие слабее. Объясняется это удаленностью электронов от ядра. Чем ближе электроны к ядру, тем больше связь их с ядром, но меньше запас энергии. По мере удаления от ядра атома сила притяжения электрона к ядру уменьшается, а запас энергии увеличивается. Так образуются электронные слои в электронной оболочке атома. Электроны, обладающие близкими значениями энергии образуют единый электронный слой, или энергетический уровень. Энергия электронов в атоме и энергетический уровень определяется главным квантовым числом n и принимает целочисленные значения 1, 2, 3, 4, 5, 6 и 7 иногда их обозначают буквами K.L.M.N.O.P.Q. Чем больше значение n, тем больше энергия электрона в атоме. Максимальное число электронов, которое может находиться на том или ином энергетическом уровне, определяется по формуле:
N = 2n2
Где N – максимальное число электронов на уровне;
n – номер энергетического уровня на котором расположен электрон, характеризующее энергию электронов, называется главным квантовым числом.
Установлено, что на первой оболочке располагается не более двух электронов, на второй – не более восьми, на третьей – не более 18, на четвертой – не более 32. Заполнение более далеких оболочек мы рассматривать не будем. Известно, что на внешнем энергетическом уровне может находиться не более восьми электронов, его называют завершенным. Электронные слои, не содержащие максимального числа электронов, называют незавершенными.
Число электронов на внешнем энергетическом уровне электронной оболочки атома равно номеру группы для химических элементов главных подгрупп.
Массовое число А – сумма чисел протонов и нейтронов атома.
Заряд ядра Z – число протонов, определяется по порядковому номеру элемента в таблице Д.И.Менделеева. В 1913 г. английским физиком Г.Мозли было установлено, что положительный заряд ядра атома (в условных единицах) равен порядковому номеру элемента в периодической системе Д.И.Менделеева.
Число нейтронов N определяется как разность между массовым числом и зарядом ядра (учитывая, что массой электрона можно пренебречь).
Изотопы – атомы одного элемента, имеющие одинаковый заряд ядра (следовательно, и количество электронов), но различное число нейтронов (следовательно, различные массовые числа). Например, элемент водород имеет три изотопа: протий, дейтерий и тритий. Первые два существуют в природе, тритий получен искусственным путем. Подавляющее большинство химических элементов имеет разное число природных изотопов с разным процентным содержанием каждого из них. Относительная атомная масса элемента, которая приводится в периодической системе, – это средняя величина массовых чисел природных изотопов данного элемента с учетом процентного содержания каждого из этих изотопов. Химические свойства всех изотопов одного химического элемента одинаковы. Следовательно, химические свойства элемента зависят не от атомной массы, а от заряда ядра.
В 1913—1916 гг. рядом теоретических и экспериментальных исследований было установлено, что атомный (порядковый) номер элемента в периодической системе равен заряду ядра его атомов. Именно в этом заключается физический смысл атомного номера элемента.(Запишем в конспект)
Заряд ядра определяется числом протонов, и, поскольку атом в целом электронейтрален, очевидно, что число протонов в его ядре равно числу электронов.
Увеличение атомного номера элемента связано с возрастанием числа про-
тонов в ядре, т. е. с увеличением положительного заряда ядра.
Таким образом, можно заключить, что заряд ядра является главной характеристикой элемента, определяя его положение в периодической системе, а следовательно, все свойства этого элемента и его соединений.
Поэтому современная формулировка периодического закона звучит так:
свойства атомов химических элементов, а также состав и свойства образуемых ими веществ находятся в периодической зависимости от зарядов атомных ядер.
Периодический закон дал импульс к изучению внутреннего строения веществ, в том числе и строения атома. В свою очередь, теория строения атома способствовала пониманию сущности периодического закона и периодической системы химических элементов, наполнила их современным содержанием и определила пути дальнейшего развития.
Вопросы для контроля знаний:
-
Кому принадлежит теория ядерной модели атома? Какое она имеет название?
теория ядерной модели атома принадлежит Резерфорду, она называется планетарной.
-
Каково строения атома? (модель простейшего атома водорода из электрона, протона, нейтрона ).
-
Что является главной характеристикой данного химического элемента?
главной характеристикой химического элемента является число протонов в ядре атома.
-
Определите число электронов в атомах химических элементов магния и алюминия.
у магния 12 электронов, у алюминия – 13.
-
Определите число протонов в атомах химических элементов фосфора и хлора.
у фосфора 15 протонов, у хлора – 17, что равно порядковому номеру химического элемента.
-
Как образуется отрицательный ион? атом приобретает электрон – отрицательно заряженную частицу.
7. Найдите ряд, в котором правильно указано количество электронов в нейтральных атомах химических элементов Ве, В, С: а) 3,4,5; б) 4,5,6; в) 9,10,12.
Предполагаемый ответ: вариант б – 4,5,6.
-
Найдите ряд, в котором верно указаны число протонов в атомах химических элементов Аl, Si, P и заряды ядра: а) 27, 28, 31; б) +13, +14, +15; в) 13, 14,15.
Предполагаемый ответ: вариант б - +13, +14, +15.
Рефлексия.
Составить синквейн к термину «атом».
1. Название синквейна.
2. 2 глагола.
3. 3 прилагательных.
4. Обобщающая фраза.
5. Существительное.
жүктеу мүмкіндігіне ие боласыз
Бұл материал сайт қолданушысы жариялаған. Материалдың ішінде жазылған барлық ақпаратқа жауапкершілікті жариялаған қолданушы жауап береді. Ұстаз тілегі тек ақпаратты таратуға қолдау көрсетеді. Егер материал сіздің авторлық құқығыңызды бұзған болса немесе басқа да себептермен сайттан өшіру керек деп ойласаңыз осында жазыңыз
Тема занятия Современная теория строения атома. Состояние и движение электронов в атоме
УТВЕРЖДАЮ
заместитель директора по НМР
________З.М.Жакупова
«____» _________ 20__ж/г.
ПОУРОЧНЫЙ ПЛАН № 1
Тема занятия Современная теория строения атома. Состояние и движение электронов в атоме
Наименование модуля /дисциплины __Химия_
«__»____________ 2025 года
-
Общие сведения
Курс, группы
Тип занятия _ Теория
2.Цель: знать современную теорию строения атома и важнейшие характеристики частиц вещества и атома; различать формы s, p, d, f-орбиталей;
Задачи:
Способствовать формированию представлений о сложности строения атома, составе атомных ядер, физическом смысле атомного номера; формированию умений давать характеристику элементарных частиц (протонов, нейтронов и электронов), определять число протонов в ядре атома химического элемента.
Развивать умение анализировать, сравнивать, делать выводы, сопоставлять, выделять главное.
Формировать навыки самостоятельной работы с текстом учебника,
способствовать формированию познавательного интереса к изучаемой теме и предмету в целом.
3. Ожидаемые результаты (профессиональных умений, которыми овладеют обучающиеся в процессе учебного занятия) перечисляет основные положения современной теории строения атома; объясняет физический смысл протонов, нейтронов, электронов, нуклонов и нуклидов; раскрывает содержание понятий изотопы.
4. Необходимые ресурсы
4.1 Учебно-методическое оснащение, справочная литература, лекционные материалы (Приложение) Учебник: Химия 10 класс Оспанова М., Белоусова Т., Аухадиева К.
4.2 Техническое оснащение, материалы. Пройдите по ссылке и ознакомьтесь с материалом https://chemege.ru/stroenie-atoma-2/ https://www.yaklass.ru/materiali?themeid=145&mode=lsntheme
https://www.youtube.com/watch?v=kqHYbT9rv6A
5. Ход занятия
5.1. Орг.момент. Актуализация знаний. Определение целей урока с обуч-ся и тд.
-
Организационный момент. Приветствие. Проверка отсутствующих.
-
Актуализация новых знаний
Фронтальный опрос по теме «Периодическая система химических элементов».
1. Дайте определение понятий: группа, период, А-группа, В-группа.
2. Укажите атомный номер, номер периода и номер группы, в которых находятся химические элементы: фтор, магний, железо.
3. Укажите химический элемент, простое вещество которого имеет более выраженные металлические свойства: натрий или алюминий. Ответ поясните.
4. Укажите химические элементы, которые образуют высший оксид состава Э2O5.
5.2. Изучение нового учебного материала
-
Атом – неделимая микрочастица, имеющая форму шара.
-
Атом состоит из ядра и электронов.
-
Ядро имеет очень маленький размер и положительный заряд.
-
Атом – электронейтрален, так как число протонов и электронов одинаково.
-
Электроны обладают отрицательным зарядом и движутся вокруг ядра.
Планетарная модель Резерфорда.
Суть планетарной модели строения атома можно свести к следующим утверждениям:
1. В центре атома находится положительно заряженное ядро, занимающее ничтожную часть пространства внутри атома.
2. Весь положительный заряд и почти вся масса атома сосредоточены в его ядре.
3. Вокруг ядра вращаются электроны. Их число равно положительному заряду ядра.
Эта модель оказалась очень наглядной и полезной для объяснения многих экспериментальных данных, но обнаружила и свои недостатки.


Теория Бора. В 1913 г. Н. Бор предложил свою теорию строения атома, в основу положено два необычных постулата:
1. Электрон может вращаться вокруг ядра не по произвольным, а только по строго определенным (стационарным) круговым орбитам.
2. При движении по стационарным орбитам электрон не излучает и не поглощает энергии.
Строение всех атомов зашифровано в периодической системе химических элементов Д. И. Менделеева. Вы, знаете, что каждому химическому элементу присвоен порядковый номер и для каждого элемента подсчитана атомная масса. Но это не просто числа, они имеют физический смысл. В чем он заключается, мы сейчас узнаем.
Введем следующие обозначения
Z – порядковый номер химического элемента
М – массовое число, М =Ar
N – число нейтронов
Z – указывает на заряд ядра, а следовательно на число протонов, а так как атом нейтрален, то число протонов равно числу электронов.
М – сумма протонов и нейтронов в ядре атома
М = Z + N
Введем обозначение химического элемента:
Х 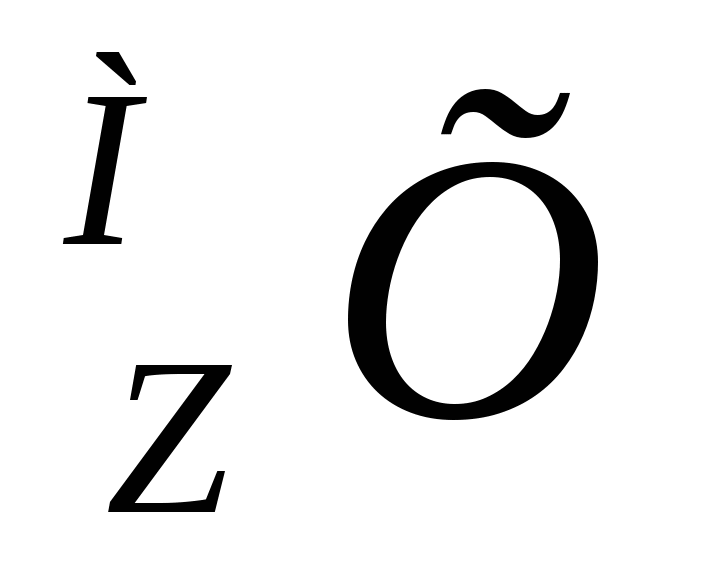 - символ химического
элемента
- символ химического
элемента
Z - заряд ядра
М – массовое число
Например: формула состава
атома кислорода: ![]() (8р;
8е;8N)
(8р;
8е;8N)
Интернет источники: Пройдите по ссылке и ознакомьтесь с материалом https://chemege.ru/stroenie-atoma-2/ https://www.yaklass.ru/materiali?themeid=145&mode=lsntheme
Просмотрите видео материал: https://www.youtube.com/watch?v=kqHYbT9rv6A
5.3. Закрепление нового УМ.
-
Заполни таблицу «Периодическая система и строение атома»:
-
Представьте электронные структуры Zn2+; S6+
|
Частица |
Заряд |
Массовое число |
Ca |
Fe |
Cu |
C l |
|
е– - |
|
|
|
|
|
|
|
р+ - |
|
|
|
|
|
|
|
n0 - |
|
|
|
|
|
|
Я знаю
Я знал
Я узнал
5.5 Домашнее задание 10кл.-§1 стр. 5 читать
Лекция № 1
Предмет: Химия
Тема: Современная теория строения атома. Состояние и движение электронов в атоме
Цели урока: Способствовать формированию представлений о сложности строения атома, составе атомных ядер, физическом смысле атомного номера; формированию умений давать характеристику элементарных частиц (протонов, нейтронов и электронов), определять число протонов в ядре атома химического элемента.
Ход урока
Актуализация знаний:
Фронтальный опрос по теме «Периодическая система химических элементов».
1. Дайте определение понятий: группа, период, А-группа, В-группа.
2. Укажите атомный номер, номер периода и номер группы, в которых находятся химические элементы: фтор, магний, железо.
3. Укажите химический элемент, простое вещество которого имеет более выраженные металлические свойства: натрий или алюминий. Ответ поясните.
4. Укажите химические элементы, которые образуют высший оксид состава Э2O5.
3. Лекционный материал
До конца XIX в. атом считали неделимой частицей, но последовавшие позже открытия (радиоактивность, фотоэффект) поколебали это убеждение. Сейчас известно, что атом состоит из элементарных частиц, основные из которых – протон, нейтрон, электрон.
Прямым доказательством сложности строения атома явилось и открытие самопроизвольного распада атомов некоторых элементов с испусканием невидимых глазу лучей. Это явление, открытое в 1896 г. французским ученым Анри Беккерелем, получило название радиоактивности. В 1897 г. английский физик Дж. Дж. Томсон установил существование в атоме электронов — отрицательно заряженных частиц. Эти открытия свидетельствовали о том, что атом имеет сложное строение.
После открытия основных элементарных частиц, входящих в состав атома, встал вопрос об их местонахождении, т.е. о строении атома. В 1911 г. Томсон предложил свою модель строения атома, которая получила условное название «пудинг с изюмом». Согласно этой модели атом представляет собой некую субстанцию, в которой равномерно распределены протоны, нейтроны и электроны. Число протонов равно числу электронов, поэтому атом в целом электронейтрален.
В 1913 г. Резерфорд ставит опыт, результаты которого модель Томсона объяснить не может. Это заставляет Резерфорда предложить свою модель строения атома, получившую название планетарной. Согласно этой модели атом состоит из ядра, в котором сконцентрирована основная масса атома, поскольку ядро содержит протоны и нейтроны; вокруг ядра на огромной скорости вращаются электроны. Поскольку модель Резерфорда содержала ряд противоречий, Н.Бором были введены постулаты, устраняющие эти противоречия.
1-й постулат. Электроны вращаются вокруг ядра не по произвольным, а по строго определенным, стационарным орбитам.
2-й постулат. При движении по стационарной орбите электрон не излучает и не поглощает энергию. Изменение энергии происходит при переходе электрона с одной стационарной орбиты на другую.
Но теория Резерфорда–Бора дает удовлетворительные результаты только для атома водорода. Современные представления о строении атома подчиняются квантовой модели строения атома.
Из курса химии вы уже знаете одно определение атома как мельчайшей, химически неделимой частицы. Теперь можно дать еще одно, физическое, определение этого понятия. Давайте запишем его в конспект:
Атом — электронейтральная частица, состоящая из положительно за-
ряженного ядра и отрицательно заряженных электронов.
Позже было установлено, что ядро атома также имеет сложное строение.
Оно состоит из частиц двух типов: протонов и нейтронов.
Протон и нейтрон имеют практически одинаковую массу, равную примерно 1 u, т. е. одной атомной единице массы. Протон (его символ р) имеет относительный заряд 1+, а нейтрон (символ n) электронейтрален.
Относительный заряд электрона (его символическое обозначение е) равен 1−, а масса примерно в 1840 раз меньше массы протона, т. е. равна 1/1840u.
В начале XX века была принята планетарная модель строения атома, предложенная Резерфордом, согласно которой вокруг очень малого по размерам положительно заряженного ядра движутся электроны, как планеты вокруг Солнца. Следовательно, в атоме есть траектории, по которым движется электрон. Однако дальнейшие исследования показали, что в атоме не существует траекторий движения электронов. Движение без траектории означает, что мы не знаем, как электрон движется в атоме, но можем установить область, где чаще всего встречается электрон. Это уже не орбита, а орбиталь. Двигаясь вокруг атома, электроны образуют в совокупности его электронную оболочку.
Давайте выясним, как движутся электроны вокруг ядра?
Беспорядочно или в определенном порядке?
Исследования Нильса Бора – основоположника современной атомной физики, а также ряда других ученых позволили сделать вывод: электроны в атомах располагаются определенными слоями – оболочками и в определенном порядке.
Строение электронных оболочек атомов имеют важную роль для химии, так как именно электроны обуславливают химические свойства веществ. Важнейшей характеристикой движения электрона на определенной орбитали является энергия его связи с ядром. Электроны в атоме различаются определенной энергией, и, как показывают опыты, одни притягиваются к ядру сильнее, другие слабее. Объясняется это удаленностью электронов от ядра. Чем ближе электроны к ядру, тем больше связь их с ядром, но меньше запас энергии. По мере удаления от ядра атома сила притяжения электрона к ядру уменьшается, а запас энергии увеличивается. Так образуются электронные слои в электронной оболочке атома. Электроны, обладающие близкими значениями энергии образуют единый электронный слой, или энергетический уровень. Энергия электронов в атоме и энергетический уровень определяется главным квантовым числом n и принимает целочисленные значения 1, 2, 3, 4, 5, 6 и 7 иногда их обозначают буквами K.L.M.N.O.P.Q. Чем больше значение n, тем больше энергия электрона в атоме. Максимальное число электронов, которое может находиться на том или ином энергетическом уровне, определяется по формуле:
N = 2n2
Где N – максимальное число электронов на уровне;
n – номер энергетического уровня на котором расположен электрон, характеризующее энергию электронов, называется главным квантовым числом.
Установлено, что на первой оболочке располагается не более двух электронов, на второй – не более восьми, на третьей – не более 18, на четвертой – не более 32. Заполнение более далеких оболочек мы рассматривать не будем. Известно, что на внешнем энергетическом уровне может находиться не более восьми электронов, его называют завершенным. Электронные слои, не содержащие максимального числа электронов, называют незавершенными.
Число электронов на внешнем энергетическом уровне электронной оболочки атома равно номеру группы для химических элементов главных подгрупп.
Массовое число А – сумма чисел протонов и нейтронов атома.
Заряд ядра Z – число протонов, определяется по порядковому номеру элемента в таблице Д.И.Менделеева. В 1913 г. английским физиком Г.Мозли было установлено, что положительный заряд ядра атома (в условных единицах) равен порядковому номеру элемента в периодической системе Д.И.Менделеева.
Число нейтронов N определяется как разность между массовым числом и зарядом ядра (учитывая, что массой электрона можно пренебречь).
Изотопы – атомы одного элемента, имеющие одинаковый заряд ядра (следовательно, и количество электронов), но различное число нейтронов (следовательно, различные массовые числа). Например, элемент водород имеет три изотопа: протий, дейтерий и тритий. Первые два существуют в природе, тритий получен искусственным путем. Подавляющее большинство химических элементов имеет разное число природных изотопов с разным процентным содержанием каждого из них. Относительная атомная масса элемента, которая приводится в периодической системе, – это средняя величина массовых чисел природных изотопов данного элемента с учетом процентного содержания каждого из этих изотопов. Химические свойства всех изотопов одного химического элемента одинаковы. Следовательно, химические свойства элемента зависят не от атомной массы, а от заряда ядра.
В 1913—1916 гг. рядом теоретических и экспериментальных исследований было установлено, что атомный (порядковый) номер элемента в периодической системе равен заряду ядра его атомов. Именно в этом заключается физический смысл атомного номера элемента.(Запишем в конспект)
Заряд ядра определяется числом протонов, и, поскольку атом в целом электронейтрален, очевидно, что число протонов в его ядре равно числу электронов.
Увеличение атомного номера элемента связано с возрастанием числа про-
тонов в ядре, т. е. с увеличением положительного заряда ядра.
Таким образом, можно заключить, что заряд ядра является главной характеристикой элемента, определяя его положение в периодической системе, а следовательно, все свойства этого элемента и его соединений.
Поэтому современная формулировка периодического закона звучит так:
свойства атомов химических элементов, а также состав и свойства образуемых ими веществ находятся в периодической зависимости от зарядов атомных ядер.
Периодический закон дал импульс к изучению внутреннего строения веществ, в том числе и строения атома. В свою очередь, теория строения атома способствовала пониманию сущности периодического закона и периодической системы химических элементов, наполнила их современным содержанием и определила пути дальнейшего развития.
Вопросы для контроля знаний:
-
Кому принадлежит теория ядерной модели атома? Какое она имеет название?
теория ядерной модели атома принадлежит Резерфорду, она называется планетарной.
-
Каково строения атома? (модель простейшего атома водорода из электрона, протона, нейтрона ).
-
Что является главной характеристикой данного химического элемента?
главной характеристикой химического элемента является число протонов в ядре атома.
-
Определите число электронов в атомах химических элементов магния и алюминия.
у магния 12 электронов, у алюминия – 13.
-
Определите число протонов в атомах химических элементов фосфора и хлора.
у фосфора 15 протонов, у хлора – 17, что равно порядковому номеру химического элемента.
-
Как образуется отрицательный ион? атом приобретает электрон – отрицательно заряженную частицу.
7. Найдите ряд, в котором правильно указано количество электронов в нейтральных атомах химических элементов Ве, В, С: а) 3,4,5; б) 4,5,6; в) 9,10,12.
Предполагаемый ответ: вариант б – 4,5,6.
-
Найдите ряд, в котором верно указаны число протонов в атомах химических элементов Аl, Si, P и заряды ядра: а) 27, 28, 31; б) +13, +14, +15; в) 13, 14,15.
Предполагаемый ответ: вариант б - +13, +14, +15.
Рефлексия.
Составить синквейн к термину «атом».
1. Название синквейна.
2. 2 глагола.
3. 3 прилагательных.
4. Обобщающая фраза.
5. Существительное.

шағым қалдыра аласыз















