Коваленттік полюсті, полюссіз байланыс 8-сынып химия
Коваленттік полюсті, полюссіз байланыс 8-сынып химия


#1 слайд
Зат жойылмайды, жоқтан пайда
болмайды. М.С. Ломоносов
Шаттық шеңбері
Топқа біріктіру .
Атомдар мен
молекулалар ойыны
1 слайд
Зат жойылмайды, жоқтан пайда болмайды. М.С. Ломоносов Шаттық шеңбері Топқа біріктіру . Атомдар мен молекулалар ойыны
#2 слайд
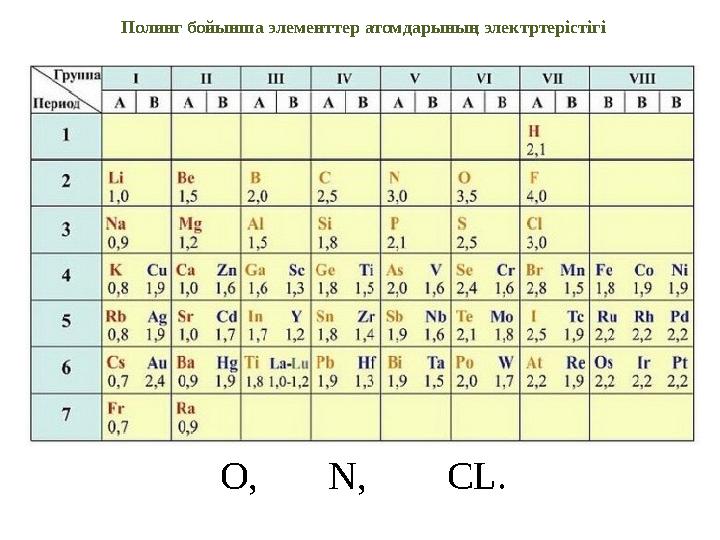
Полинг бойынша элементтер атомдарының электртерістігі
Топ
О , N, CL.
2 слайд
Полинг бойынша элементтер атомдарының электртерістігі Топ О , N, CL.
#3 слайд
3 слайд

#4 слайд
Сабақ тақырыбы
Коваленттік полюсті, полюссіз
байланыс
Оқу мақсаттары
8.1.4.1 электртерістік негізінде
атомдар арасындағы коваленттік
байланыстың түзілуін түсіндіру
4 слайд
Сабақ тақырыбы Коваленттік полюсті, полюссіз байланыс Оқу мақсаттары 8.1.4.1 электртерістік негізінде атомдар арасындағы коваленттік байланыстың түзілуін түсіндіру

#5 слайд
Сабақ мақсаттары
коваленттік полюсті, полюссіз
байланыстың түзілу механизмін
қарастыру
коваленттік полюсті, полюссіз
байланысы бар заттарды анықтау
5 слайд
Сабақ мақсаттары коваленттік полюсті, полюссіз байланыстың түзілу механизмін қарастыру коваленттік полюсті, полюссіз байланысы бар заттарды анықтау

#6 слайд
Бағалау критерийлері және
дикрипторлары
коваленттік полюсті, полюссіз
байланыстың түзілуін түсіндіреді;
коваленттік полюссіз және коваленттік
полюсті байланыстарының ұқсастығы мен
айырмашылығын көрсетеді;
формула бойынша коваленттік полюсті
байланысы бар заттарды коваленттік
полюссіз байланысы бар заттардан
ажырата алады;
«айқыш-нүктелер» диаграммасын салады
6 слайд
Бағалау критерийлері және дикрипторлары коваленттік полюсті, полюссіз байланыстың түзілуін түсіндіреді; коваленттік полюссіз және коваленттік полюсті байланыстарының ұқсастығы мен айырмашылығын көрсетеді; формула бойынша коваленттік полюсті байланысы бар заттарды коваленттік полюссіз байланысы бар заттардан ажырата алады; «айқыш-нүктелер» диаграммасын салады
#7 слайд
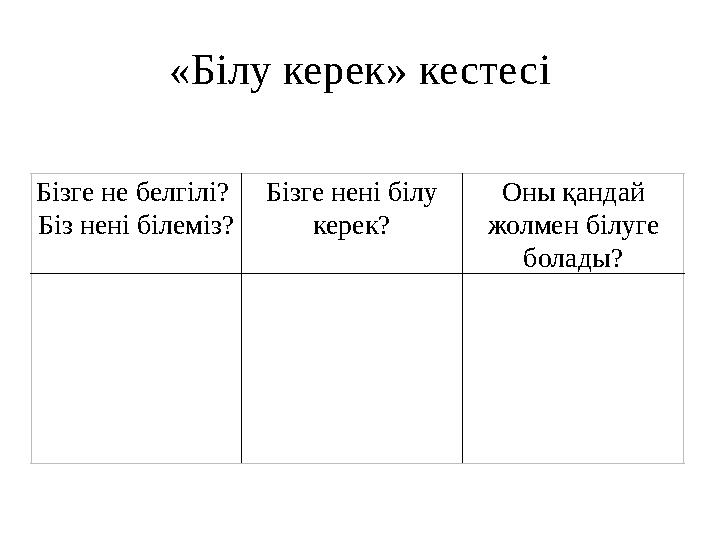
«Білу керек» кестесі
Бізге не белгілі?
Біз нені білеміз? Бізге нені білу
керек? Оны қандай
жолмен білуге
болады?
7 слайд
«Білу керек» кестесі Бізге не белгілі? Біз нені білеміз? Бізге нені білу керек? Оны қандай жолмен білуге болады?
#8 слайд
8 слайд
#9 слайд
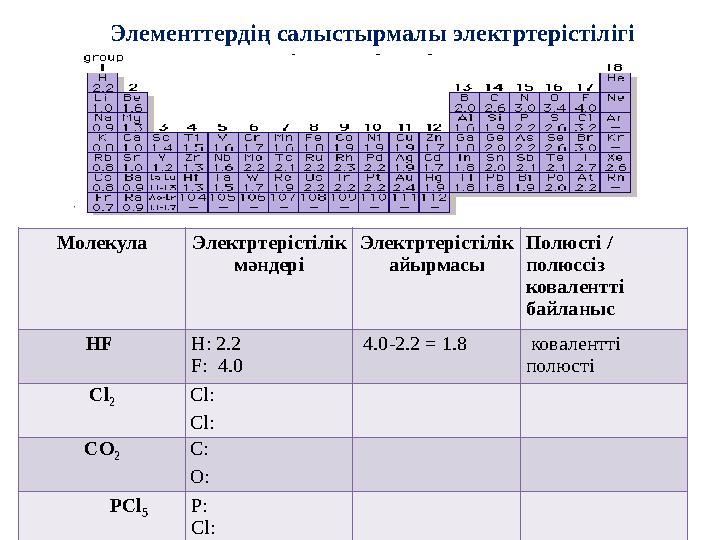
Элементтердің салыстырмалы электртерістілігі
Молекула Электртерістілік
мәндері Электртерістілік
айырмасы Полюсті /
полюссіз
ковалентті
байланыс
HF H: 2.2
F: 4.0 4.0-2.2 = 1.8 ковалентті
полюсті
Cl
2 Cl:
Cl:
CO
2 C:
O:
PCl
5 P:
Cl:
9 слайд
Элементтердің салыстырмалы электртерістілігі Молекула Электртерістілік мәндері Электртерістілік айырмасы Полюсті / полюссіз ковалентті байланыс HF H: 2.2 F: 4.0 4.0-2.2 = 1.8 ковалентті полюсті Cl 2 Cl: Cl: CO 2 C: O: PCl 5 P: Cl:
#10 слайд
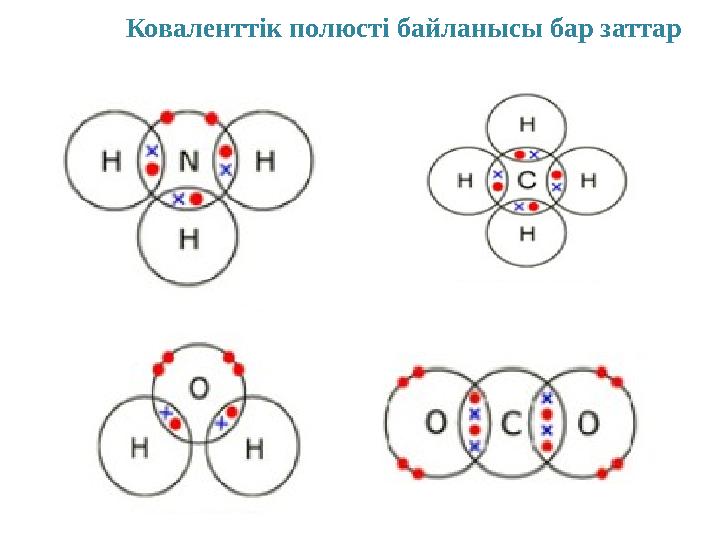
Коваленттік полюсті байланысы бар заттар
10 слайд
Коваленттік полюсті байланысы бар заттар
#11 слайд
ХИМИЯЛЫҚ БАЙЛАНЫС
КОВАЛЕНТТІ БАЙЛАНЫС.
11 слайд
ХИМИЯЛЫҚ БАЙЛАНЫС КОВАЛЕНТТІ БАЙЛАНЫС.
#12 слайд
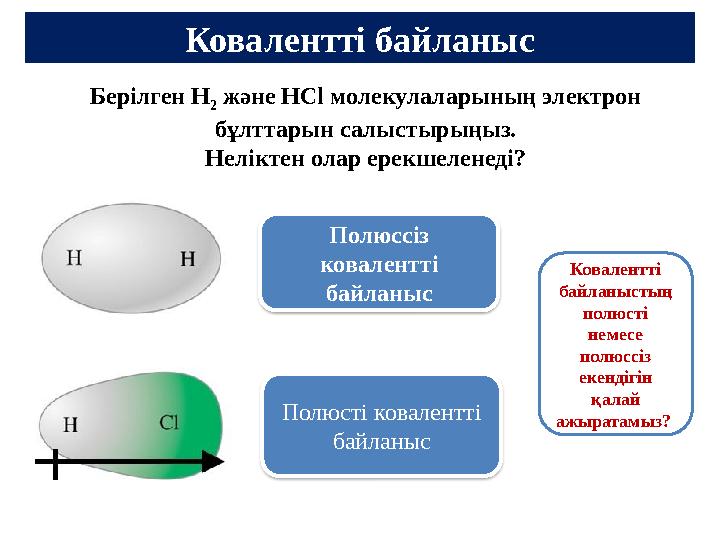
Ковалентті байланыс
Берілген Н
2 және НС l молекулаларының электрон
бұлттарын салыстырыңыз.
Неліктен олар ерекшеленеді?
Н
2 молекуласында
электрон тығыздығы
теңдей таралады Полюссіз
ковалентті
байланыс
Н Cl молекуласында
электрон тығыздығы хлор
атомына қарай ығысады Полюсті ковалентті
байланыс Ковалентті
байланыстың
полюсті
немесе
полюссіз
екендігін
қалай
ажыратамыз?
12 слайд
Ковалентті байланыс Берілген Н 2 және НС l молекулаларының электрон бұлттарын салыстырыңыз. Неліктен олар ерекшеленеді? Н 2 молекуласында электрон тығыздығы теңдей таралады Полюссіз ковалентті байланыс Н Cl молекуласында электрон тығыздығы хлор атомына қарай ығысады Полюсті ковалентті байланыс Ковалентті байланыстың полюсті немесе полюссіз екендігін қалай ажыратамыз?
#13 слайд
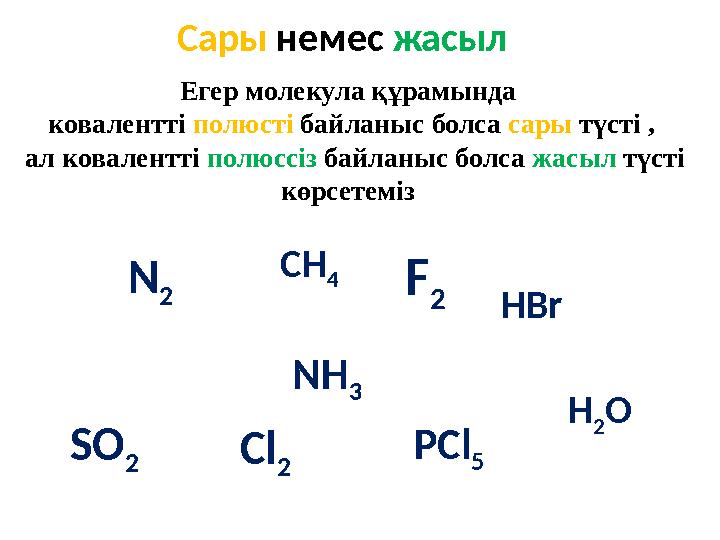
Сары немес жасыл
Егер молекула құрамында
ковалентті полюсті байланыс болса сары түсті ,
ал ковалентті полюссіз байланыс болса жасыл түсті
көрсетеміз
N
2 CH
4
HBr
Cl
2 NH
3
H
2 OF
2
SO
2 PCl
5
13 слайд
Сары немес жасыл Егер молекула құрамында ковалентті полюсті байланыс болса сары түсті , ал ковалентті полюссіз байланыс болса жасыл түсті көрсетеміз N 2 CH 4 HBr Cl 2 NH 3 H 2 OF 2 SO 2 PCl 5
#14 слайд
Тұжырымдар Н-Н Н- Br
1
Екі атом арасындағы коваленттік байланыс
полюсті (полярлы )емес
2
Екі атом арасындағы коваленттік байланыс
полюсті (полярлы)
3
Атомдарды байланыстыратын электрондық
жұп атомдар арасында бірдей бөлінеді
4
Молекула полюсті (полярлы)
5
Молекула полюсті (полярлы) емес
6
Ортақ электрондық жұп байланысқан
атомдардың біреуіне қарай ығысқан •
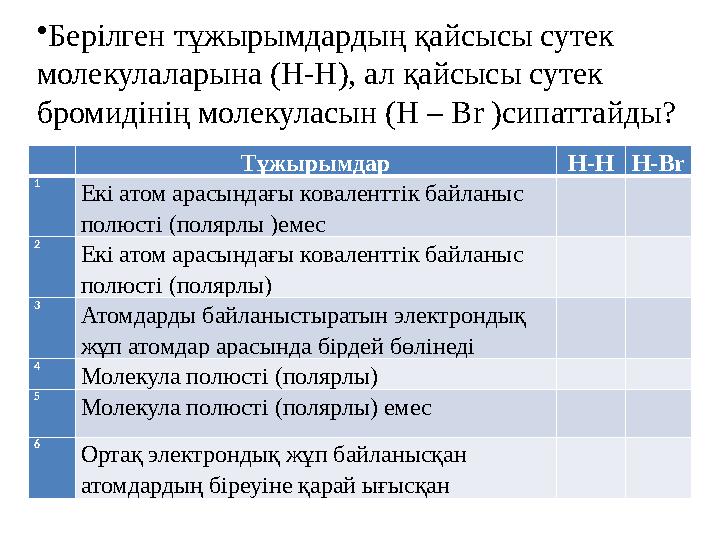
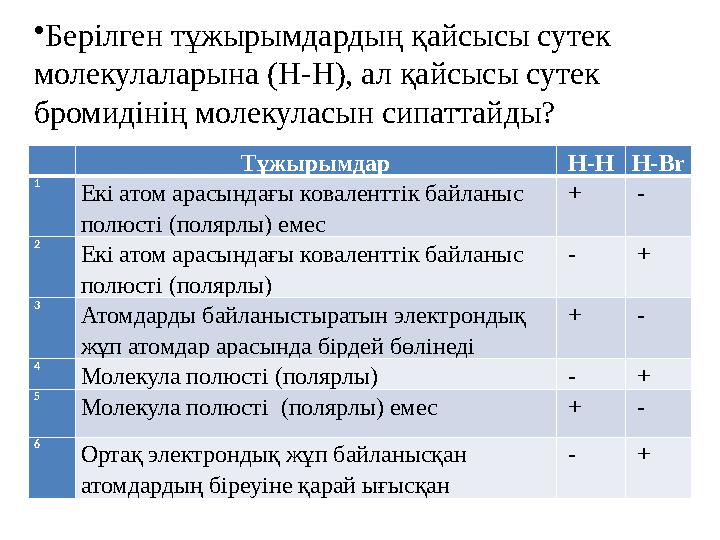
Берілген тұжырымдардың қайсысы сутек
молекулаларына (Н-Н), ал қайсысы сутек
бромидінің молекуласын (H – Br ) сипаттайды?
14 слайд
Тұжырымдар Н-Н Н- Br 1 Екі атом арасындағы коваленттік байланыс полюсті (полярлы )емес 2 Екі атом арасындағы коваленттік байланыс полюсті (полярлы) 3 Атомдарды байланыстыратын электрондық жұп атомдар арасында бірдей бөлінеді 4 Молекула полюсті (полярлы) 5 Молекула полюсті (полярлы) емес 6 Ортақ электрондық жұп байланысқан атомдардың біреуіне қарай ығысқан • Берілген тұжырымдардың қайсысы сутек молекулаларына (Н-Н), ал қайсысы сутек бромидінің молекуласын (H – Br ) сипаттайды?
#15 слайд
Тұжырымдар Н-Н Н- Br
1
Екі атом арасындағы коваленттік байланыс
полюсті (полярлы) емес + -
2
Екі атом арасындағы коваленттік байланыс
полюсті (полярлы) - +
3
Атомдарды байланыстыратын электрондық
жұп атомдар арасында бірдей бөлінеді + -
4
Молекула полюсті (полярлы) - +
5
Молекула полюсті (полярлы) емес + -
6
Ортақ электрондық жұп байланысқан
атомдардың біреуіне қарай ығысқан - +•
Берілген тұжырымдардың қайсысы сутек
молекулаларына (Н-Н), ал қайсысы сутек
бромидінің молекуласын сипаттайды?
15 слайд
Тұжырымдар Н-Н Н- Br 1 Екі атом арасындағы коваленттік байланыс полюсті (полярлы) емес + - 2 Екі атом арасындағы коваленттік байланыс полюсті (полярлы) - + 3 Атомдарды байланыстыратын электрондық жұп атомдар арасында бірдей бөлінеді + - 4 Молекула полюсті (полярлы) - + 5 Молекула полюсті (полярлы) емес + - 6 Ортақ электрондық жұп байланысқан атомдардың біреуіне қарай ығысқан - +• Берілген тұжырымдардың қайсысы сутек молекулаларына (Н-Н), ал қайсысы сутек бромидінің молекуласын сипаттайды?
#16 слайд
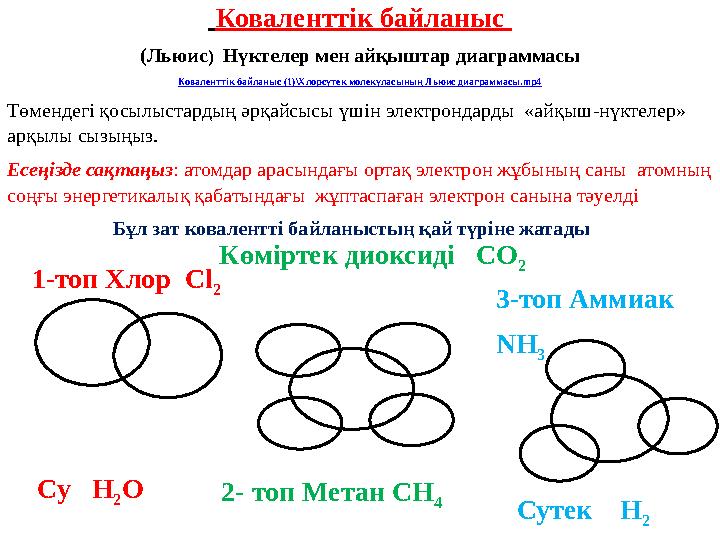
Коваленттік байланыс
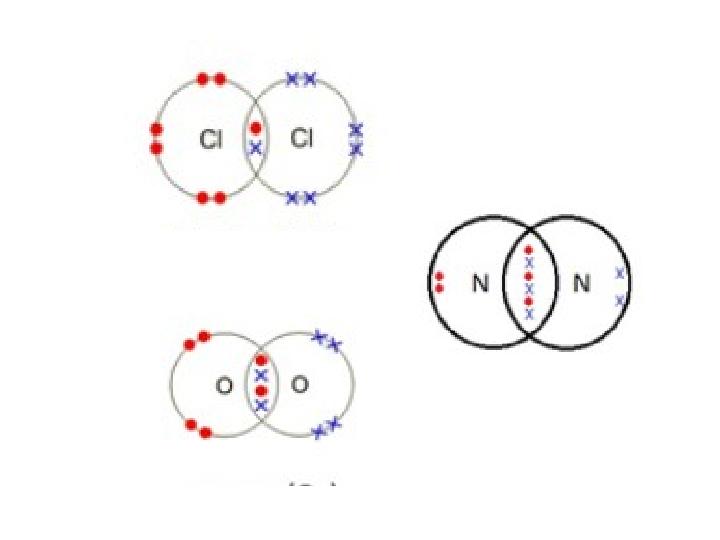
(Льюис ) Нүктелер мен айқыштар диаграммасы
Коваленттік байланыс (1)\ Хлорсутек молекуласының Льюис диаграммасы.mp4
Төмендегі қосылыстардың әрқайсысы үшін электрондарды «айқыш-нүктелер»
арқылы сызыңыз.
Есеңізде сақтаңыз : атомдар арасындағы ортақ электрон жұбының саны атомның
соңғы энергетикалық қабатындағы жұптаспаған электрон санына тәуелді
Бұл зат ковалентті байланыстың қай түріне жатады
1-топ Хлор Cl
2
2- топ Метан CH
4 3-топ Аммиак
NH
3
Су H
2 O Көміртек диоксиді CO
2
Сутек H
2
16 слайд
Коваленттік байланыс (Льюис ) Нүктелер мен айқыштар диаграммасы Коваленттік байланыс (1)\ Хлорсутек молекуласының Льюис диаграммасы.mp4 Төмендегі қосылыстардың әрқайсысы үшін электрондарды «айқыш-нүктелер» арқылы сызыңыз. Есеңізде сақтаңыз : атомдар арасындағы ортақ электрон жұбының саны атомның соңғы энергетикалық қабатындағы жұптаспаған электрон санына тәуелді Бұл зат ковалентті байланыстың қай түріне жатады 1-топ Хлор Cl 2 2- топ Метан CH 4 3-топ Аммиак NH 3 Су H 2 O Көміртек диоксиді CO 2 Сутек H 2

#17 слайд
Берілген заттардың ішінен
1- топ ковалентт і полюсті
2- топ ковалентті полюссіз
3- топ ковалентті байланысқа жатпайтын заттар
Na
2 O, Mg, CsF, CaCl
2 , Cu,
HCl, Al
2 O
3 , Br
2 , MgI
2 , PH
3 ,
H
2 O, Fe, I
2 , SiO
2 , Ca, F
2 , LiH,
CO
2
Mg, Cu, Fe , Ca -бұлар металдар.
Металдарда болатын химиялық байланыс -
металдық байланыс деп аталады.
17 слайд
Берілген заттардың ішінен 1- топ ковалентт і полюсті 2- топ ковалентті полюссіз 3- топ ковалентті байланысқа жатпайтын заттар Na 2 O, Mg, CsF, CaCl 2 , Cu, HCl, Al 2 O 3 , Br 2 , MgI 2 , PH 3 , H 2 O, Fe, I 2 , SiO 2 , Ca, F 2 , LiH, CO 2 Mg, Cu, Fe , Ca -бұлар металдар. Металдарда болатын химиялық байланыс - металдық байланыс деп аталады.
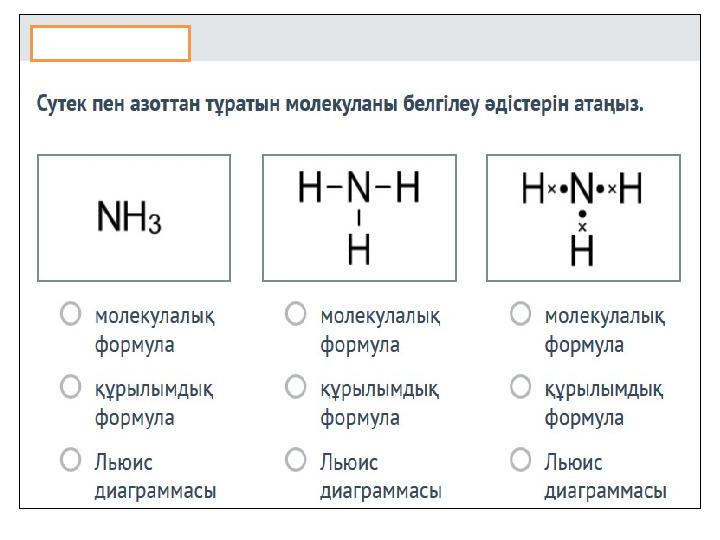
#18 слайд
18 слайд

#19 слайд
Кері байланыс
«Білу керек» кестесі
Бізге не белгілі?
Біз нені білеміз? Бізге нені білу
керек? Оны қандай
жолмен білуге
болады?
19 слайд
Кері байланыс «Білу керек» кестесі Бізге не белгілі? Біз нені білеміз? Бізге нені білу керек? Оны қандай жолмен білуге болады?
#20 слайд
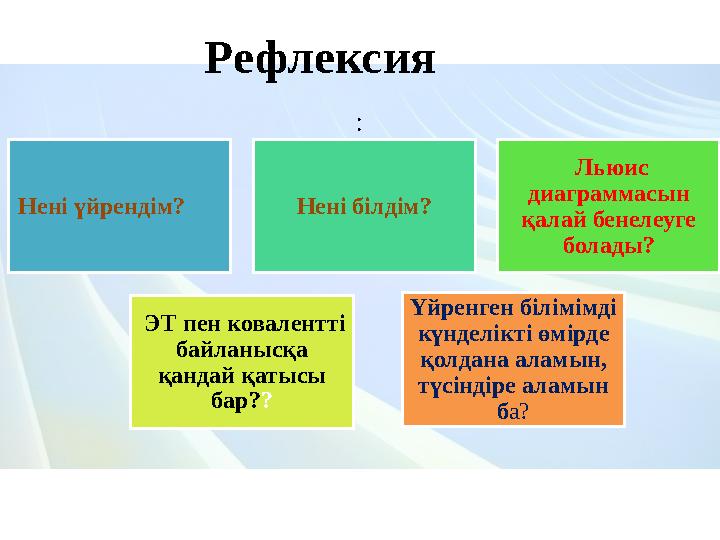
:
Нені үйрендім? Нені білдім? Льюис
диаграммасын
қалай бенелеуге
болады?
ЭТ пен ковалентті
байланысқа
қандай қатысы
бар? ? Үйренген білімімді
күнделікті өмірде
қолдана аламын,
түсіндіре аламын
б а?Рефлексия
20 слайд
: Нені үйрендім? Нені білдім? Льюис диаграммасын қалай бенелеуге болады? ЭТ пен ковалентті байланысқа қандай қатысы бар? ? Үйренген білімімді күнделікті өмірде қолдана аламын, түсіндіре аламын б а?Рефлексия
#21 слайд
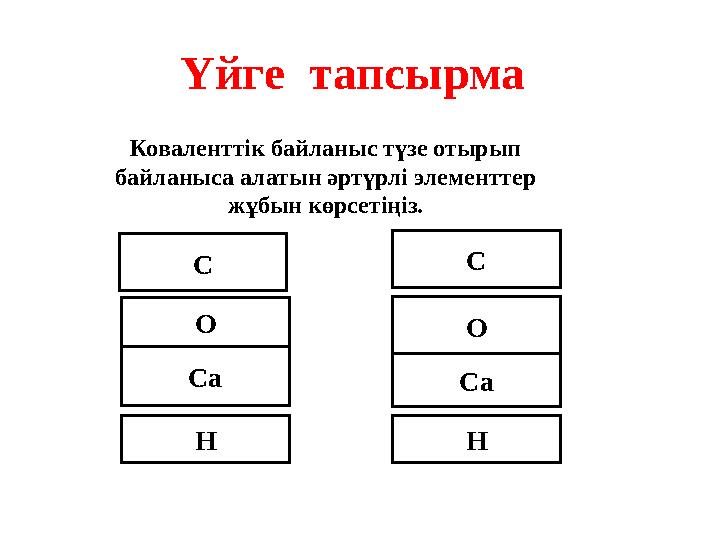
Үйге тапсырма
Коваленттік байланыс түзе отырып
байланыса алатын әртүрлі элементтер
жұбын көрсетіңіз.
С
О
Са
Н С
О
Са
Н
21 слайд
Үйге тапсырма Коваленттік байланыс түзе отырып байланыса алатын әртүрлі элементтер жұбын көрсетіңіз. С О Са Н С О Са Н

шағым қалдыра аласыз
















