Қанның құрамы қызметі
Қанның құрамы қызметі


#1 слайд
Тақырыбы: « Зат мөлшері. Моль. Авогадро саны. Молдік масса»
8 сыныпНұр - Сұлтан қаласы № 38 мектеп-лицейі
Химия пәні мұғалімі: Макет а ва Ақтоты Турсынгазиевна
1 слайд
Тақырыбы: « Зат мөлшері. Моль. Авогадро саны. Молдік масса» 8 сыныпНұр - Сұлтан қаласы № 38 мектеп-лицейі Химия пәні мұғалімі: Макет а ва Ақтоты Турсынгазиевна

#2 слайд
2Оқу мақсаты
Ба ғалау критерийлері•
8.1.1.1 зат мөлшерінің өлшем бірлігі ретінде –мольді білу және Авогадро санын білу
•
8.1.1.2 қосылыстың молярлық массасын есептей алу
•
8.1.1.3 масса, зат мөлшері және құрылымдық бөлшектер санын есептеу
•
зат мөлшерінің өлшем бірлігі ретінде –мольді және Авогадро санын біледі
•
масса, зат мөлшері және құрылымдық бөлшектер санын есептей алады
•
қосылыстың молярлық массасын есептей алады
2 слайд
2Оқу мақсаты Ба ғалау критерийлері• 8.1.1.1 зат мөлшерінің өлшем бірлігі ретінде –мольді білу және Авогадро санын білу • 8.1.1.2 қосылыстың молярлық массасын есептей алу • 8.1.1.3 масса, зат мөлшері және құрылымдық бөлшектер санын есептеу • зат мөлшерінің өлшем бірлігі ретінде –мольді және Авогадро санын біледі • масса, зат мөлшері және құрылымдық бөлшектер санын есептей алады • қосылыстың молярлық массасын есептей алады

#3 слайд
3•
Зат мөлшері
•
Моль
•
Авогадро саны
•
Құрылымдық бөлшектер саны
•
Мольдік масса Тірек ұғымдар:
3 слайд
3• Зат мөлшері • Моль • Авогадро саны • Құрылымдық бөлшектер саны • Мольдік масса Тірек ұғымдар:

#4 слайд
4 ф
1000 г – 1 кг
30 күн – 1 ай
100 тиын – 1 теңге
100 жыл – 1 ғасыр
Химияда заттың өлшемі ретінде ерекше физикалық шама –
зат мөлшері алынады. Зат мөлшері
4 слайд
4 ф 1000 г – 1 кг 30 күн – 1 ай 100 тиын – 1 теңге 100 жыл – 1 ғасыр Химияда заттың өлшемі ретінде ерекше физикалық шама – зат мөлшері алынады. Зат мөлшері

#5 слайд
5
Зат мөлшері мольмен өрнектеледі .
Моль – бұл құрамында 0,012 кг (12 г) көміртекте болатын
атомдар санына тең құрылымдық бөлшектер (атомдар,
молекулалар, т.б.) болатын заттың мөлшері.
Көміртектің әрбір атомының массасын (19,93∙10 -27
кг) біле
отырып көміртектің 0,012 кг массасында қанша атом (N)
болатынын есептеуге болады.
N= 0,012 кг / 19,93∙10 -27
кг = 6,02∙10 23
(атом )
602 000 000 000 000 000 000 000 (немесе 6,02∙10 23
) құрылымдық бөлшектерді атом, молекула
және т.б біріктіріп 1 моль деп атайды.
5 слайд
5 Зат мөлшері мольмен өрнектеледі . Моль – бұл құрамында 0,012 кг (12 г) көміртекте болатын атомдар санына тең құрылымдық бөлшектер (атомдар, молекулалар, т.б.) болатын заттың мөлшері. Көміртектің әрбір атомының массасын (19,93∙10 -27 кг) біле отырып көміртектің 0,012 кг массасында қанша атом (N) болатынын есептеуге болады. N= 0,012 кг / 19,93∙10 -27 кг = 6,02∙10 23 (атом ) 602 000 000 000 000 000 000 000 (немесе 6,02∙10 23 ) құрылымдық бөлшектерді атом, молекула және т.б біріктіріп 1 моль деп атайды.

#6 слайд
6
Авогадро саны
6,02∙10 23
саны итальяндық ғалым Амадео Авогадроның құрметіне
Авогадро саны деп аталады.
Белгісі N
А , өлшем бірлігі моль -1
.
N
А = 6,02∙10 23
моль -1
.
Ол кез келген заттың 1 молінде 6,02∙10 23
бөлшектер болатынын
көрсетеді.
Мысалы : 1 моль суда да, 1 моль темірде де бөлшектер саны бірдей, тек судың
1 молінде 6,02∙10 23
молекула болса, темірдің 1 молінде 6,02∙10 23
атом бар.
Авогадро санын заттың молекуласын табу үшін қолданады.
6 слайд
6 Авогадро саны 6,02∙10 23 саны итальяндық ғалым Амадео Авогадроның құрметіне Авогадро саны деп аталады. Белгісі N А , өлшем бірлігі моль -1 . N А = 6,02∙10 23 моль -1 . Ол кез келген заттың 1 молінде 6,02∙10 23 бөлшектер болатынын көрсетеді. Мысалы : 1 моль суда да, 1 моль темірде де бөлшектер саны бірдей, тек судың 1 молінде 6,02∙10 23 молекула болса, темірдің 1 молінде 6,02∙10 23 атом бар. Авогадро санын заттың молекуласын табу үшін қолданады.

#7 слайд
7Зат мөлшерінің формуласы: n = N / N
А
Зат мөлшері белгілі болса бөлшектер санын анықтауға болады.
Молекуланы (N) әрпімен белгілейді.
Ол Авогадро санын зат мөлшеріне көбейткенге тең.
N = n ∙N
А
мұндағы : n - зат мөлшері
N - молекула немесе атом саны
N
А - Авогадро саны
Зат мөлшері мен Авогадро саны арасындағы байланыс
7 слайд
7Зат мөлшерінің формуласы: n = N / N А Зат мөлшері белгілі болса бөлшектер санын анықтауға болады. Молекуланы (N) әрпімен белгілейді. Ол Авогадро санын зат мөлшеріне көбейткенге тең. N = n ∙N А мұндағы : n - зат мөлшері N - молекула немесе атом саны N А - Авогадро саны Зат мөлшері мен Авогадро саны арасындағы байланыс

#8 слайд
8
Мольдік масса - заттың бір молінің массасы.
М әрпімен белгілейді және өлшем бірлігі г/ моль
Мольдік масса мен салыстырмалы молекулалық массаның
(немесе атомдық) сандық мәндері бір - біріне сәйкес болады.
Метанның CH
4 мольдік массасын анықтайық:
Mr( CH
4 ) = Ar ( C ) + Ar ( H ) ∙ 4 = 12 + 1 ∙ 4 = 16
M ( CH
4 ) = 16 г / моль Мольдік масса
8 слайд
8 Мольдік масса - заттың бір молінің массасы. М әрпімен белгілейді және өлшем бірлігі г/ моль Мольдік масса мен салыстырмалы молекулалық массаның (немесе атомдық) сандық мәндері бір - біріне сәйкес болады. Метанның CH 4 мольдік массасын анықтайық: Mr( CH 4 ) = Ar ( C ) + Ar ( H ) ∙ 4 = 12 + 1 ∙ 4 = 16 M ( CH 4 ) = 16 г / моль Мольдік масса

#9 слайд
9Мольдік масса
Мольдік масса зат массасының оның мөлшеріне қатынасымен өрнектеледі.
M = m / n
б ұдан моль санын есептеуге болады:
n = m / M
немесе мол саны мен мольдік массалары бойынша заттың массасын
есептеуге болады:
m = n ∙ M
мұндағы : n - зат мөлшері
M – мольдік масса
m
– заттың массасы
9 слайд
9Мольдік масса Мольдік масса зат массасының оның мөлшеріне қатынасымен өрнектеледі. M = m / n б ұдан моль санын есептеуге болады: n = m / M немесе мол саны мен мольдік массалары бойынша заттың массасын есептеуге болады: m = n ∙ M мұндағы : n - зат мөлшері M – мольдік масса m – заттың массасы

#10 слайд
10 Мольдік масса
Заттың мольдік массасының мәні оның сапалық және сандық құрамымен
анықталады, яғни Mr және Ar - ге тәуелді. Сондықтан әртүрлі заттардың
моль саны бірдей болса да , массалары түрліше болады.
Графит 12 г
Күкірт 23 г
Темір 56 г
Мыс 64 г 1 моль
атом
6,02∙10 23
10 слайд
10 Мольдік масса Заттың мольдік массасының мәні оның сапалық және сандық құрамымен анықталады, яғни Mr және Ar - ге тәуелді. Сондықтан әртүрлі заттардың моль саны бірдей болса да , массалары түрліше болады. Графит 12 г Күкірт 23 г Темір 56 г Мыс 64 г 1 моль атом 6,02∙10 23

#11 слайд
11Бекіту тапсырмасы
1-тапсырма. Төменде хлорсутектің, азот, күкірт және фосфор қышқылдарының
молекулаларының модельдері берілген. Олардың формулаларын жазып , мольдік
массаларын есептеңдер.
Дескриптор:
Білім алушы
- қосылыстардың молекулалық формулаларын жазады
- қосылыстардың мольдік массаларын есептейді
11 слайд
11Бекіту тапсырмасы 1-тапсырма. Төменде хлорсутектің, азот, күкірт және фосфор қышқылдарының молекулаларының модельдері берілген. Олардың формулаларын жазып , мольдік массаларын есептеңдер. Дескриптор: Білім алушы - қосылыстардың молекулалық формулаларын жазады - қосылыстардың мольдік массаларын есептейді

#12 слайд
12Дұрыс жауабы
Хлорсутек HCl
M(HCl) = Ar(H) + Ar ∙(Cl ) = 1 + 35,5 =36,5 г / моль
Азот қышқылы HNO
3
M(H NO
3 ) = Ar( H ) + Ar ∙( N ) + Ar ∙( O ) ∙ 3 = 1 + 14 +48 = 63 г / моль
Күкірт қышқылы H
2 SO
4
M(H
2 SO
4 ) = Ar( H ) ∙ 2 + Ar ∙( S ) + Ar ∙( O ) ∙ 4 = 2 + 32 +64 = 98 г / моль
Фосфор қышқылы H
3 PO
4
M(H
3 PO
4 ) = Ar( H ) 3 + Ar ∙( P ) + Ar ∙( O ) ∙ 4 = 3 + 31 +64 = 98 г / моль
12 слайд
12Дұрыс жауабы Хлорсутек HCl M(HCl) = Ar(H) + Ar ∙(Cl ) = 1 + 35,5 =36,5 г / моль Азот қышқылы HNO 3 M(H NO 3 ) = Ar( H ) + Ar ∙( N ) + Ar ∙( O ) ∙ 3 = 1 + 14 +48 = 63 г / моль Күкірт қышқылы H 2 SO 4 M(H 2 SO 4 ) = Ar( H ) ∙ 2 + Ar ∙( S ) + Ar ∙( O ) ∙ 4 = 2 + 32 +64 = 98 г / моль Фосфор қышқылы H 3 PO 4 M(H 3 PO 4 ) = Ar( H ) 3 + Ar ∙( P ) + Ar ∙( O ) ∙ 4 = 3 + 31 +64 = 98 г / моль
#13 слайд
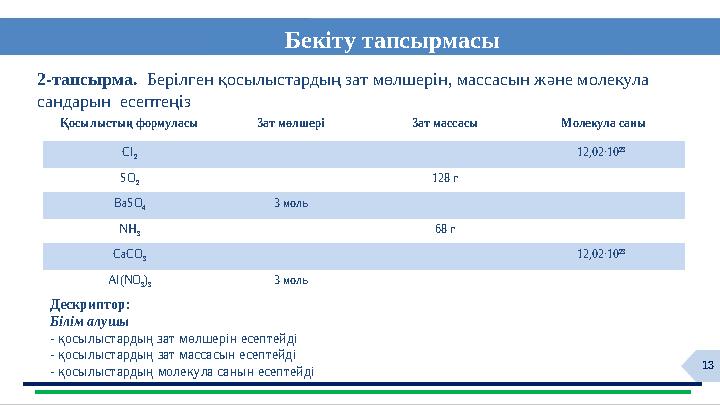
13Бекіту тапсырмасы
2-тапсырма. Берілген қосылыстардың зат мөлшерін, массасын және молекула
сандарын есептеңіз
Дескриптор:
Білім алушы
- қосылыстардың зат мөлшерін есептейді
- қосылыстардың зат массасын есептейді
- қосылыстардың молекула санын есептейді Қосылыстың формуласы Зат мөлшері Зат массасы Молекула саны
Сl
2 12 ,02∙10 23
SO
2 1 28 г
BaSO
4 3 моль
N H
3 68 г
CaCO
3 12 ,02∙10 23
Al(NO
3 )
3 3 моль
13 слайд
13Бекіту тапсырмасы 2-тапсырма. Берілген қосылыстардың зат мөлшерін, массасын және молекула сандарын есептеңіз Дескриптор: Білім алушы - қосылыстардың зат мөлшерін есептейді - қосылыстардың зат массасын есептейді - қосылыстардың молекула санын есептейді Қосылыстың формуласы Зат мөлшері Зат массасы Молекула саны Сl 2 12 ,02∙10 23 SO 2 1 28 г BaSO 4 3 моль N H 3 68 г CaCO 3 12 ,02∙10 23 Al(NO 3 ) 3 3 моль
#14 слайд
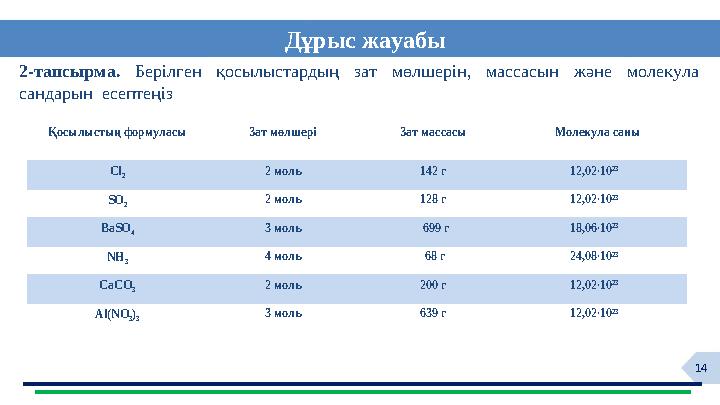
14Дұрыс жауабы
Қосылыстың формуласы Зат мөлшері Зат массасы Молекула саны
Сl
2 2 моль 142 г 12,02∙10 23
SO
2 2 моль 128 г 12,02∙10 23
BaSO
4 3 моль 699 г 18,06∙10 23
NH
3 4 моль 68 г 24,08∙10 23
CaCO
3 2 моль 200 г 12,02∙10 23
Al(NO
3 )
3 3 моль 639 г 12,02∙10 23
2-тапсырма. Берілген қосылыстардың зат мөлшерін, массасын және молекула
сандарын есептеңіз
14 слайд
14Дұрыс жауабы Қосылыстың формуласы Зат мөлшері Зат массасы Молекула саны Сl 2 2 моль 142 г 12,02∙10 23 SO 2 2 моль 128 г 12,02∙10 23 BaSO 4 3 моль 699 г 18,06∙10 23 NH 3 4 моль 68 г 24,08∙10 23 CaCO 3 2 моль 200 г 12,02∙10 23 Al(NO 3 ) 3 3 моль 639 г 12,02∙10 23 2-тапсырма. Берілген қосылыстардың зат мөлшерін, массасын және молекула сандарын есептеңіз

#15 слайд
15Қорытынды
Бүгінгі сабақта:
•
зат мөлшерінің өлшем бірлігі ретінде –мольді және Авогадро санын
білдім
•
қосылыстың мольдік массасын есептей аламын
•
масса, зат мөлшері және құрылымдық бөлшектер санын есептей аламын
15 слайд
15Қорытынды Бүгінгі сабақта: • зат мөлшерінің өлшем бірлігі ретінде –мольді және Авогадро санын білдім • қосылыстың мольдік массасын есептей аламын • масса, зат мөлшері және құрылымдық бөлшектер санын есептей аламын

#16 слайд
16Қосымша р есурстар
Химия оқулығы 8 сынып
Оспанова М.Қ., Белоусова Т.Г. Аухадиева.Қ.С
https://bilimland.kz/kk/subject/ximiya/ 8 -synyp/
16 слайд
16Қосымша р есурстар Химия оқулығы 8 сынып Оспанова М.Қ., Белоусова Т.Г. Аухадиева.Қ.С https://bilimland.kz/kk/subject/ximiya/ 8 -synyp/

шағым қалдыра аласыз
















